
En este artículo, volveré al tema de la radiación planteada en mi publicación en el mostrador Geiger.
... A finales de los años ochenta y principios de los noventa, las personas a menudo iban al mercado con un dosímetro, eligiendo con él "limpio", como pensaban, verduras y frutas. A veces y ahora en foros y lugares públicos temáticos surge la pregunta: qué dosímetro comprar para ir al mercado de alimentos. Y si hay personas competentes en la comunidad, darán la respuesta correcta: ninguna. Y explicarán que la radioactividad de los productos alimenticios es detectada por el dosímetro solo a niveles muchas veces más altos que el límite, el dosímetro no distinguirá la actividad inofensiva de potasio 40 del equivalente en las lecturas del dosímetro, sino que matará con el consumo regular de actividad de estroncio 90, y el plutonio alfa-activo y muy radiotóxico con Estados Unidos no verá nada, y para evaluar la idoneidad del producto para su uso, es necesaria la investigación en un laboratorio especial.
En este momento estoy trabajando en un laboratorio así. No hacemos medidas de higiene. Nuestra tarea es estudiar la radiactividad del entorno natural, principalmente agua de mar, precipitación. Lo que nos interesa no es el hecho de exceder los estándares, sino los niveles de radionucleidos en los propios objetos naturales, las formas en que están presentes, su distribución y migración. Afortunadamente, aunque el contenido de radionúclidos en el medio ambiente en la mayoría de los casos es muy pequeño. Y me gustaría contar cómo encontramos estos niveles bajos y, al mismo tiempo, disipar algunos mitos comunes.
En KDPV - Novaya Zemlya, donde visité el año anterior como parte de una expedición al buque de investigación del buque Ártico Mstislav Keldysh.
Alfa, Beta, Gamma, Cribble, Cangrejo, Plumas
Una propiedad única de la desintegración radiactiva como fuente de una señal analítica es que registramos fácilmente un solo evento de desintegración, es decir, lo que le sucedió a un átomo. Por lo tanto, la medición de la radiactividad es a menudo superior en sensibilidad a cualquier otro método analítico. Solo los elementos de vida muy larga (uranio 238 y 235, torio, a veces neptunio) son más sensibles a la determinación química.
Como probablemente todos sepan, durante la desintegración radiactiva, se emiten partículas alfa - núcleos de helio-4, partículas beta - electrones y, a veces, positrones, rayos gamma y, en casos raros, se emiten neutrones, núcleos y protones de "fragmentación". A veces, sin embargo, sucede que parece que no se emite nada: por el contrario, el núcleo captura un electrón. Pero en este caso, no puede prescindir de la radiación: la capa de electrones de un átomo, al reconstruirse, emite radiación característica de rayos X.
La forma más fácil es si el isótopo que nos interesa es un emisor gamma. La radiación gamma rara vez existe por separado de todas las demás, solo después de la transición de los isómeros nucleares de larga vida al estado fundamental del núcleo. Como regla, ocurre durante la desintegración alfa y beta, debido al hecho de que después de la desintegración, el nuevo núcleo necesita perder el exceso de energía. Debido a la penetración, la radiación gamma generalmente deja fácilmente los límites de una muestra
muy gruesa , lo cual es imposible en el caso de la radiación alfa y no siempre es posible cuando se trata de beta. Y la radiación gamma tiene una buena característica: su espectro es lineal e identifica de forma única el nucleido emitido.
Por desgracia, lejos de todos los radionucleidos son fuentes efectivas de radiación gamma. Para algunos, se emite un rayo gamma en el 0,0001% de todas las desintegraciones, para alguien, una desintegración tiene lugar inmediatamente en el estado fundamental del núcleo hijo y no se puede obtener ningún gamma de él. Por lo tanto, debe observar la radiación alfa y beta.
Desde la escuela, sabemos que un trozo de papel retrasa la radiación alfa. Diré más: se retrasa un par de centímetros de aire y, lo más importante, se retrasa por el colapso mismo. Y si tratamos de detectar la radiación alfa al llevar el sensor hacia afuera, entonces solo las partículas alfa emitidas por la capa superior de materia, un espesor de una micra o unas pocas micras, caerán en ella. Un problema similar es con el registro de la radiación beta. Si es rígido (como el estroncio 90), puede superar varios milímetros de muestra. Y los rayos beta de tritio "penetran" incluso menos que las partículas alfa, y no pueden cruzar ninguna ventana. Incluso las partículas beta de carbono 14 o níquel-63 apenas pasan a través de una mica delgada de un contador Geiger o una lámina opaca que cubre el detector de centelleo.
Luego te diré qué hacen con esta impenetrabilidad y cómo enfrentarla.
Pero primero, sobre la espectrometría gamma
Sobre la espectrometría de rayos gamma probablemente se menciona en cualquier discusión sobre el tema de "controlar los hongos con un dosímetro". Esto es comprensible: el método para resolver el problema de "determinar el cesio-137 en el nivel de MPC" es relativamente simple en hardware (hasta opciones "hasta la rodilla" en el hogar) y bastante expresivo (es decir, da un resultado rápido).
La espectrometría gamma se basa en el hecho de que la radiación gamma resultante de la desintegración radiactiva de este isótopo en particular es una corriente de rayos gamma casi monoenergéticos. Es decir, en el espectro de radiación vemos una línea estrecha, o varias líneas. Y este espectro es característico, puede usarse para identificar de manera confiable un radionúclido.
Si la radiación óptica o incluso los rayos X pueden descomponerse en el espectro utilizando algún elemento dispersante: un prisma o una rejilla de difracción (para rayos X, una rejilla de cristal, por ejemplo, el grafito sirve como este último), entonces la única forma de obtener un espectro de radiación gamma es medir la energía de cada uno de los grabados. es quanta Hay muchos métodos para tal medición, por ejemplo, hay varios métodos en los que un "cuántico gamma" se convierte en un electrón con casi la misma energía, y luego el flujo de electrones se expande en el espectro de acuerdo con las energías en el campo magnético. Pero tales métodos son aplicables en física nuclear experimental, pero no en mediciones de rutina. Por lo general, se usa un detector de radiación ionizante
proporcional para medir la energía de los rayos gamma.
Un contador Geiger-Muller, por ejemplo, no es un detector de este tipo. Habiendo absorbido el cuántico de rayos gamma americio-241, generará un pulso que no será diferente del mismo pulso que emitirá un contador Geiger en respuesta al cuántico de rayos gamma de cobalto-60, a pesar de que las energías de estos dos cuantos difieren en 23 tiempos Pero el contador de centelleo, por el contrario, tiene la propiedad de proporcionalidad: la intensidad del destello de luz y, por lo tanto, la amplitud del pulso en el ánodo del multiplicador de fotoelectrones está determinada por la cantidad de energía absorbida en el cristal.
Un espectrómetro de centelleo gamma, por lo tanto, es simplemente un detector de centelleo: un cristal de centelleador, por ejemplo, yoduro de sodio activado con talio, al que se une un PMT. Los pulsos PMT se alimentan a un dispositivo especial llamado
analizador multicanal (a menudo se encuentra la abreviatura inglesa MCA). De hecho, este es un ADC, pero con una serie de requisitos específicos (en particular, una no linealidad diferencial extremadamente pequeña, que en las aplicaciones ordinarias es de poca preocupación para nadie). El principio de su acción es que mide la magnitud (su amplitud, o la integral bajo este impulso) de cada impulso y "descompone" estos impulsos en "montones" de acuerdo con su magnitud. Estos "montones" - canales - generalmente de 256 a 4096 o más. En esencia, el MCA funciona como una función llamada con cada nuevo pulso:
unsigned int spectrum[4096] = {0};
Y luego, cuando se recopilan suficientes pulsos, puede construir un gráfico, que se convierte en una visualización del espectro gamma. Algo como esto:
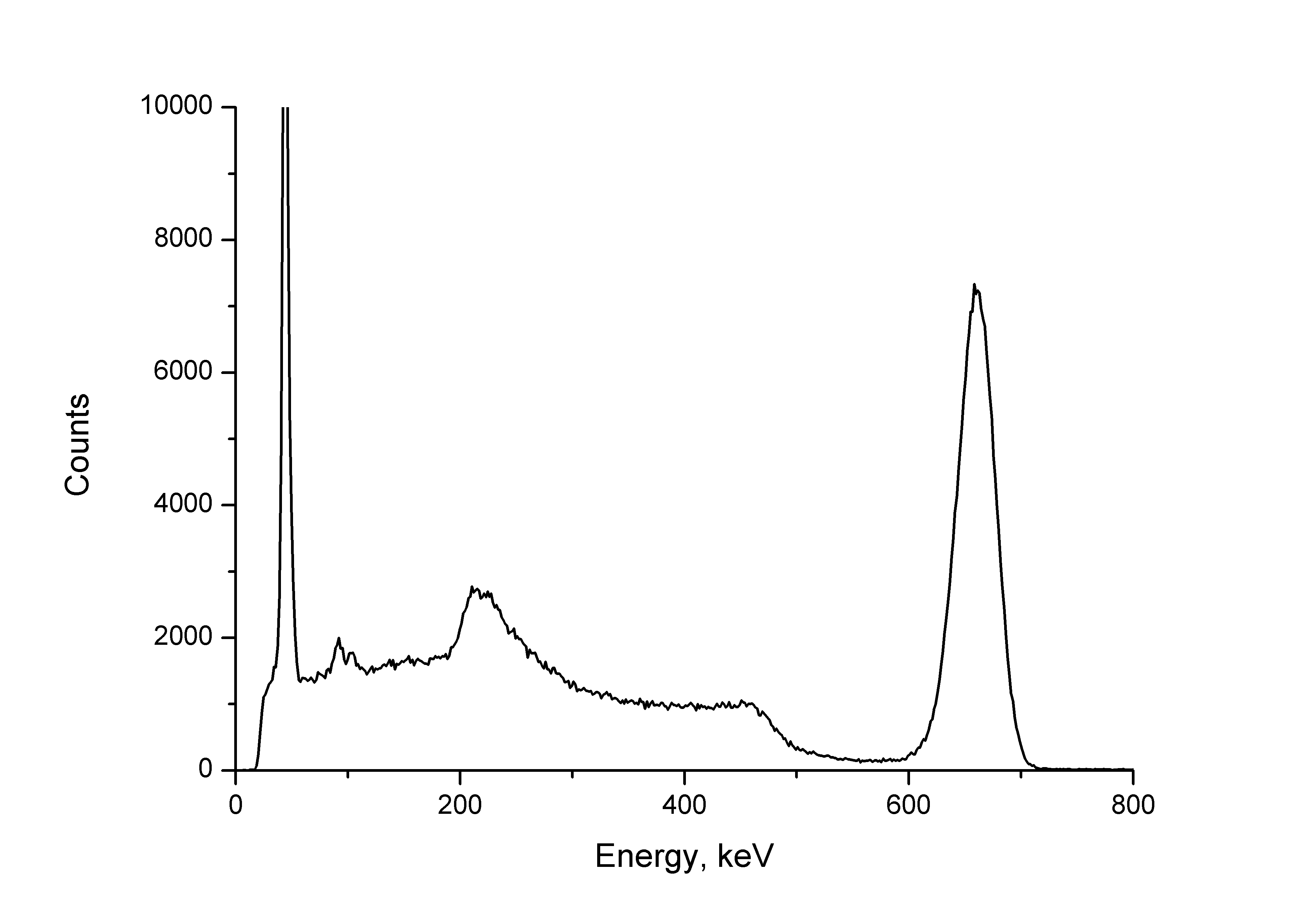
Esto les traje una imagen muy reveladora, que demuestra que todo parece ser simple, pero al mismo tiempo, no muy. El hecho es que este es un espectro registrado a partir de una fuente de radiación monoenergética. Pero de ninguna manera es el único "palo" a 662 keV. No solo eso, en lugar de un palo, tenemos una "campana" bastante vaga. A su izquierda tenemos algo que en realidad no existe (a excepción del pico más a la izquierda, existe en realidad). Por desgracia, el espectro de
hardware no es igual al real.
¿De dónde vienen estas diferencias? De la física del proceso de registro de radiación gamma.
El gamma cuántico puede ser absorbido en todo el cristal centelleador, dándole toda la energía, que se convertirá en la energía cinética de los fotoelectrones, que finalmente excitan un destello de luminiscencia en el centelleo cristalino. De tales cuantos tenemos un pico a la derecha, lo llamamos el
pico de la
foto , porque se refiere a la absorción a través del efecto fotoeléctrico. Y otro cuanto puede "pasar directamente", dándole solo una parte de la energía. Y, cualquiera: desde casi cero hasta una cierta fracción límite, dependiendo del ángulo en el que el electrón que interactúa con el cuanto se alejará. Este es el efecto Compton. Y de él, esta amplia meseta a la izquierda del pico, el
continuo de Compton . A altas energías, también veremos un efecto como la formación de pares de electrones-positrones, debido a los picos de emisión simple y doble que aparecen en el espectro, que están a 511 y 1022 keV lejos del fotopico, y el pico de 511 keV en sí mismo de la radiación gamma aniquilación En el contexto del continuo Compton, es visible un pico de retrodispersión: esta es la radiación gamma reflejada de los objetos que rodean el detector, que perdió parte de la energía debido al efecto Compton, y aún más abajo vemos líneas de rayos X características de la protección contra el plomo. Bueno, la línea extrema izquierda también es una línea característica de rayos X, solo desde ese bario, en el que se convirtió el cesio, que se rompió. Sí, este es el espectro de cesio-137. Y casi todo lo que vemos en este espectro es una visualización de una
sola línea espectral . Habrá dos líneas: cada una tendrá la misma forma y veremos su suma. Y sí, la apariencia de cada una de estas líneas depende de su energía: al aumentarla, la fracción del componente Compton primero aumenta y el fotopico cae, luego aparecen y crecen los efectos de la creación de pares electrón-positrón (picos de emisión, picos de aniquilación). A partir de aquí obtenemos una complejidad decente de procesamiento de los espectros.
Un espectrómetro de centelleo gamma es un dispositivo, como ya he dicho, relativamente simple. Hasta el punto de que cualquier ama de casa puede conseguirlo. Con toda seriedad: los dispositivos se fabrican y venden por menos de mil dólares, todo lo que necesita para trabajar es una computadora con un puerto USB y protección contra el plomo. Dentro del cuerpo cilíndrico, todo, y el cristal, y PMT, y su fuente de energía, y el ADC. Para aquellos interesados - google sobre Atom Spectra. Y para aquellos que pueden sostener un soldador en sus manos, es bastante posible fabricar dicho dispositivo por sí mismos: el papel de un analizador multicanal se jugará con éxito con una tarjeta de sonido de computadora y un programa especial, por ejemplo,
BeckMoni , o puede basarse en un microcontrolador, un integrador con un reinicio y un ADC externo (el incorporado parámetros muy pobres) hacen un MCA que no es inferior a lo que hace Greenstar. Sí, y los dispositivos de laboratorio a veces se ajustan a la etiqueta de precio "hasta un millón de rublos" y (aparte de la protección con plomo) casi no ocupan espacio en el banco de laboratorio (por ejemplo, Kolibri de
Green Star mide 8 x 13 x 3 cm y también funciona desde un puerto USB). Tienen un inconveniente: baja resolución.
Los mejores cristales de NaI (Tl) dan una resolución espectral a lo largo de la línea de cesio-137 de aproximadamente 6%. Un centelleador nuevo y muy costoso, el bromuro de lantano, es del 3,2%. Y estos números conducen al hecho de que el espectro
real se parece a esto:
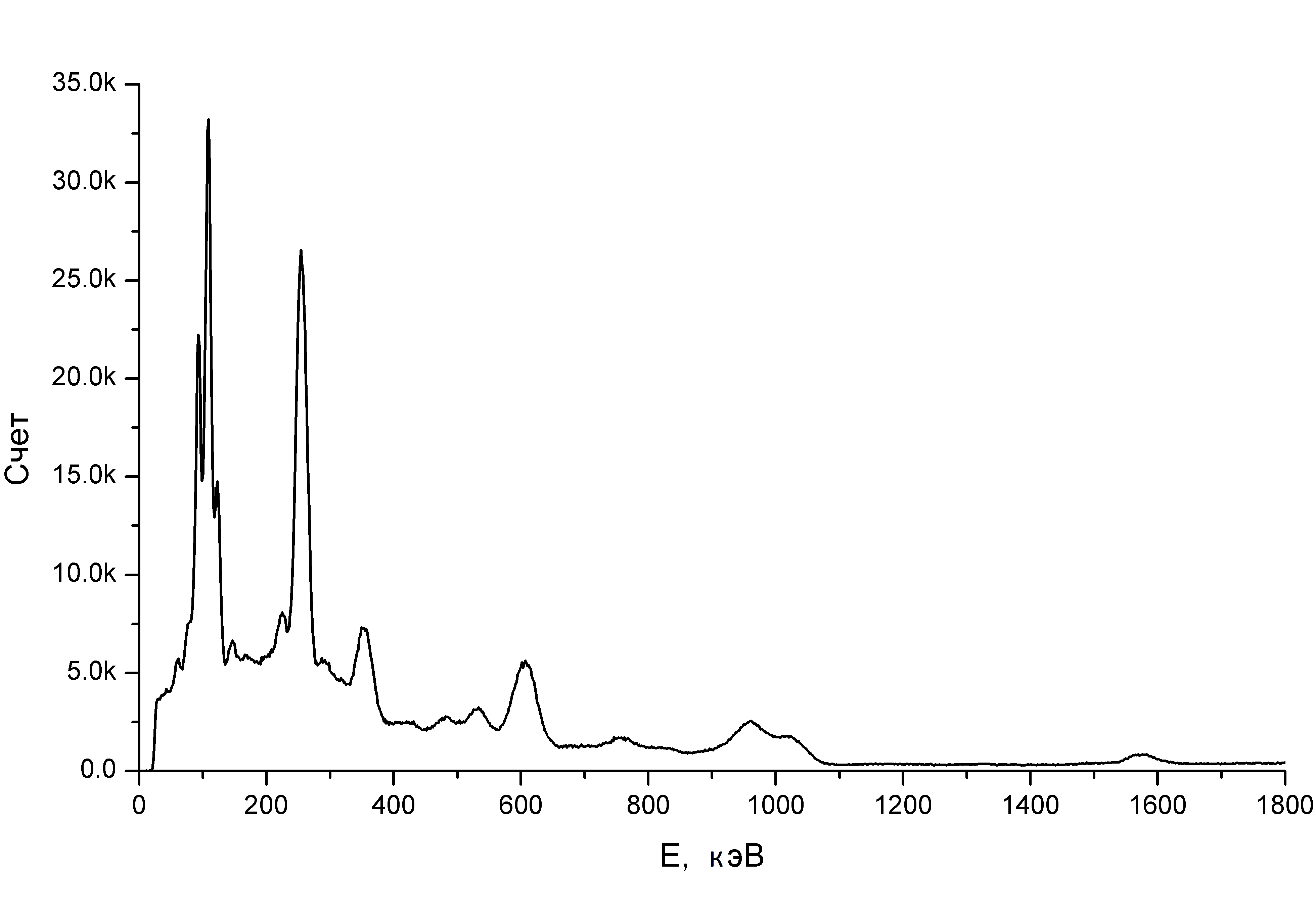
Y en el peor de los casos, será una colina tan inexpresiva, en cuya pendiente los tubérculos individuales son apenas visibles, por los cuales los isótopos aún se pueden identificar, pero no se trata de cuantificarlos. Y nuestras muestras naturales en un espectrómetro de centelleo gamma se ven así. Y el espectro "en el mejor de los casos", por cierto, es de un guijarro, desde el cual Terra-P se inundó y mostró miliregenes por hora (el granito daría casi la misma imagen, solo tomaría todo un día obtener el espectro, y este espectro escrito en un minuto).
Por lo tanto, en la mayoría de los casos, trabajamos en un espectrómetro con un detector de semiconductores. Por diseño, se asemeja a un fotodiodo pin de germanio, oculto de la luz, pero accesible a los rayos gamma. Pero, de hecho, es solo una cámara de ionización. Solo se llena no con gas, sino con germanio sin dopar, al que se hacen contactos en forma de una región p por un lado y una región n por el otro. Un fotón que vuela a través del detector (o más bien, a través de la región, genera pares de electrones en su camino, que se extienden por el campo eléctrico desde el voltaje aplicado al cristal semiconductor a los electrodos de esta cámara de ionización, lo que conduce a la aparición de un pulso de corriente corto y muy débil, nuevamente proporcional a la energía, Debido a la muy baja energía requerida para formar un par, y por varias otras razones, la resolución espectral de un detector OCH o HPGE es de décimas de ciente y la línea espectral en el espectro de verdad -. de línea (aunque sus compañeros como picos de salida continuo Compton, retrodispersión, y otras cosas - no va a desaparecer).
Para ilustrar, este no es un espectro de mi trabajo y
lo he tomado de Internet . Este es el espectro total de 89 muestras de salmón capturado en la costa de Columbia Británica, lo que demuestra que el eco de Fukushima no llegó allí: se detectaron trazas de cesio-137, pero no hubo cesio-134 "fresco" con una vida media corta.
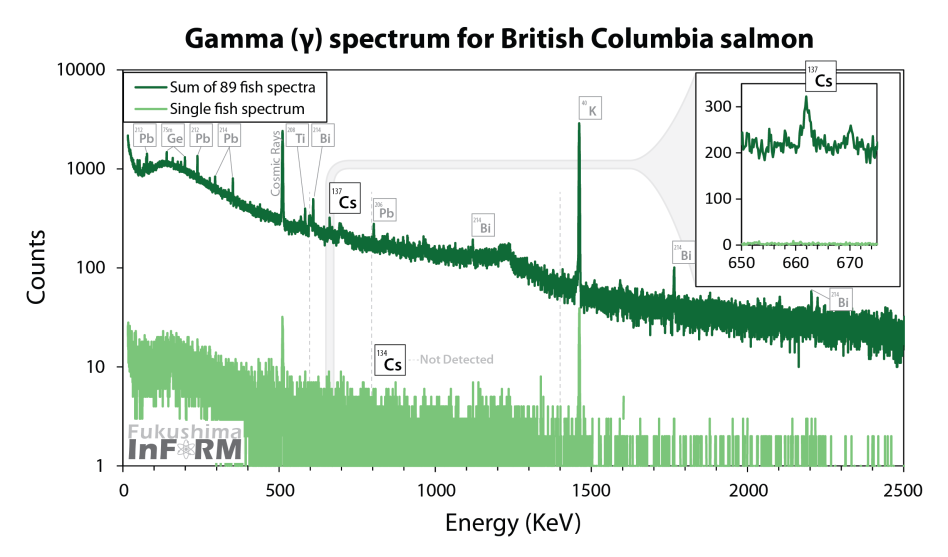
¿Ves cuántos tipos de líneas débiles y pequeñas aparecieron en el espectro? El espectro de centelleo de rayos gamma no daría absolutamente nada aquí. En primer lugar, porque la línea de cesio-137 se superpondría con la línea 609 keV relacionada con el bismuto-214, y la línea de cesio-134 ni siquiera intentaría separarse de la línea de plomo-214.
Pero el PPD no funciona a temperatura ambiente y requiere enfriamiento con nitrógeno líquido, y en general es un dispositivo muy costoso que no todos los laboratorios tienen. Tuvimos suerte: tenemos nuestro propio Canberra, pero aún medimos algunas de las muestras en el Departamento de Radioquímica, Departamento de Química de la Universidad Estatal de Moscú.
Pero un espectrómetro de centelleo se puede llevar con usted en un vuelo a un barco. E incluso póngalo en una bolsa y lleve a cabo un conjunto de espectros de rayos gamma en Novaya Zemlya durante el aterrizaje.
Espectrometría alfa y un poco sobre los rayos beta
La radiación alfa de los isótopos radiactivos también es monoenergética y su espectro es característico. Por lo tanto, la espectrometría alfa es una fuente muy valiosa de información sobre la composición de radionúclidos. Y de alguna manera, es un método más simple que la espectrometría gamma: una partícula alfa siempre se absorbe completamente en el detector, por lo tanto, el espectro instrumental de la radiación alfa coincide con el real teniendo en cuenta la resolución espectral limitada. Y el detector es tan simple como tres centavos: es un centelleador delgado o el mismo detector de semiconductores, que, en el caso de la radiación alfa, es muy similar en estructura a un fotodiodo pin estándar, con la única diferencia de que el grosor de la capa "muerta" es Las superficies que incluyen el metal y la región p + tienen el grosor más pequeño posible (recuerde la capacidad de penetración de las partículas alfa). No necesita enfriamiento, y dado que las partículas alfa tienen energías de varios MeV, muchos de los agujeros de electrones salen de cada uno de ellos y el nivel de señal no es tan bajo como con HPGE, donde debe usar un preamplificador de muy bajo ruido, enfriado junto con el detector.
Las dificultades surgen solo por la misma pequeña capacidad de penetración. El detector y la muestra se colocan en una pequeña cámara de vacío, que se bombea a varios milímetros de mercurio, y la muestra se hace muy delgada. Uno de los métodos es la electrodeposición: se coloca una solución de ácido nítrico que contiene isótopos alfa activos en la celda de electrólisis, el ánodo es un alambre de platino y el cátodo es un disco de acero inoxidable. Anteriormente, la solución se limpia al máximo de todo lo innecesario utilizando una columna con una resina de intercambio iónico. Una hora y media, y 10 mililitros de la solución se convirtieron en una película con un espesor de no más de una décima parte de un micrón.
En cuanto a los rayos beta, su espectro no es tan brillante e impresionante. Debido al hecho de que con cada desintegración beta, el antineutrino se lleva parte de la energía (y qué parte será necesaria), el espectro de radiación beta es continuo y tiene la forma de grandes jorobas. Por lo tanto, a menudo se limitan a su puntaje, ya que previamente han seleccionado el elemento de interés por medios químicos.
Aquí, si la radiación es lo suficientemente dura, se puede detectar con un detector de centelleo y un semiconductor (similar al de la radiación alfa, pero más grueso, y hay detectores universales, como en el "caballo de batalla" del laboratorio radioquímico), un radiómetro de escritorio alfa-beta UMF-2000). Y si, por ejemplo, obtuvimos tritio, entonces no hay mejor opción que tomar y mezclar la muestra con un centelleador líquido. Este método se llama recuento de centelleo líquido. Por cierto, es adecuado para alfa, y en general es un método bastante universal. Sin embargo, los dispositivos vuelven a ser caros y complejos, no tenemos ese dispositivo, damos muestras al Laboratorio Radioquímico del Instituto de Geoquímica de la Academia de Ciencias de Rusia, o al Departamento de Radioquímica de la Facultad de Química. La razón es, en primer lugar, que la energía de desintegración es a menudo muy pequeña, por lo que en el caso del tritio es necesario capturar pulsos de luz que componen solo una docena o dos fotones. Utiliza el método favorito de los físicos nucleares: el método de las coincidencias. Un tubo fotomultiplicador, incluso en ausencia de luz, genera constantemente pulsos correspondientes en amplitud a uno o incluso varios fotoelectrones. Pero la probabilidad de que los pulsos que exceden un electrón coincidan inmediatamente en tres PMT en un instante es muy pequeña. Pero una verdadera llamarada de centelleo, incluso si solo hubiera entre 10 y 15 fotones, dará una respuesta coincidente de inmediato en los tres canales y se grabará.
Algunas palabras sobre protección
Cuando se trata de radiación, no pasa sin hablar de protección radiológica. También tenemos que pensar en esto, pero no para protegernos: los niveles de radiación de nuestras muestras son muy pequeños. Nuestros dispositivos deben estar protegidos, de lo contrario, el fondo de radiación externa anulará todos los intentos de ver flujos de radiación débiles. Cuanto más pequeño es el fondo en defensa, más sensible es la definición.
La forma más fácil es con radiación alfa. Por sí mismo no atraviesa nada, y la energía de las partículas alfa difiere notablemente de la radiación gamma de fondo, por lo que no se requiere protección particular para un espectrómetro alfa. Los espectrómetros gamma y los contadores beta se colocan en un escudo masivo, generalmente de plomo. Por cierto, el plomo se toma para su especial. Canberra, por ejemplo, utiliza plomo levantado del fondo del mar a partir de naufragios de barcos antiguos. En primer lugar, en este plomo no hay absolutamente ningún radionúclido de origen antropogénico, y en segundo lugar, el plomo 210 ya se ha descompuesto en él. Este isótopo es especialmente importante para nosotros como un "reloj radiactivo", que permite determinar la tasa de acumulación de sedimentos en el fondo de los mares.
Para reducir aún más el fondo, incluidos los asociados con la radiación cósmica, el interior de la protección está revestido con cobre, cadmio y plástico. Esto se hace para eliminar la fluorescencia de rayos X del plomo, así como los electrones secundarios.
Y para mediciones de fondo especialmente bajas, el equipo se coloca en un sótano profundo o incluso en una mina cortada en rocas de baja actividad. Esta es a veces la única forma de reducir repetidamente el nivel de rayos cósmicos, que vuelan sin demora a través de decenas de centímetros de plomo.
¿Qué es la radioquímica?
La situación habitual es cuando el radionúclido de interés es tan pequeño que dicho volumen de muestra, que contiene su actividad mínima detectable, no puede introducirse en el dispositivo. A veces debido a las dimensiones del dispositivo, y a veces, por razones fundamentales (como en el caso de los isótopos alfa-activos: debe convertir el cubo de muestra en una película de una fracción de un micrón de espesor). Esta es la tarea de los métodos de concentración.
Por ejemplo, tenemos cesio-137 en el aire. No hubo guerra nuclear, Chernobyl fue hace mucho tiempo, por lo que hay poco cesio-137.
y menos becquerel por metro cúbico. Es decir, en su habitación, la descomposición de un átomo de cesio-137 ocurre varias veces por hora. Para la espectrometría gamma, se debe escribir al menos becquerel. Que hacer Tomamos una aspiradora, le conectamos un filtro especial. El cesio será parte del polvo y se asentará en este filtro. Condujeron diez mil metros cúbicos de aire a través de él, y el polvo resultante puede ser empujado a un espectrómetro de rayos gamma.
O otra opción: para aislar el mismo cesio-137 del agua de mar, conduzca mil litros de agua de mar a través de una toallita empapada en ferrocianuro de cobalto, que tiende a separar eficientemente el cesio del agua.
¿Recuerdas cómo los cónyuges de Curie extraían radio? Se coprecipitó con sulfato de bario, repitiendo este proceso muchas veces y aumentando la concentración de radio en cada etapa. Aproximadamente de la misma manera: mediante coprecipitación, sorción en resinas de intercambio iónico y otros sorbentes, electrólisis y otros métodos, concentramos el elemento cuyo isótopo nos interesa, eliminando los que interfieren (incluida su radiactividad) y, a veces, reduciendo el volumen de la muestra en millones tiempos
Ya hablé de uno de los métodos de concentración cuando hablé de la espectrometría alfa: de unos pocos mililitros de una solución de ácido nítrico obtuvimos la película más delgada. Y antes de eso, recogimos un barril de agua de mar por la borda, agregamos cloruro férrico y luego lo precipitamos con amoníaco. La mayor parte del plutonio contenido en el agua resultó estar en sedimento (la coprecipitación generalmente se usa en radioquímica; por ejemplo, se usa para separar el estroncio 90). Todo este sedimento, junto con una pequeña cantidad de agua, se colocó en una botella de litro, que llevaremos a tierra. Y luego primero eliminamos el exceso de agua, luego disolvemos el precipitado y eliminamos el hierro de allí usando una resina de intercambio iónico, y luego eliminamos todo lo demás usando una columna cromatográfica con otra resina de intercambio iónico, de donde saldrá el plutonio en el momento adecuado. Y así aparecen estos pocos mililitros, a partir de los cuales el electrolisis precipita el plutonio.
¿Hubo una guerra nuclear en el siglo XVII?
Sí, imagínense: existe una "teoría" tal que hace 200-300 años se produjo una guerra nuclear y la civilización altamente desarrollada de los terrícolas fue arrojada a una sociedad capitalista tardía feudal-temprana. Y no fue el único: se encuentran rastros de un conflicto nuclear en la antigua India (Mohenjo-Daro), y la radioactividad de muchos huesos antiguos también es bien conocida, lo que también es evidencia de que las explosiones nucleares tronaron sobre las civilizaciones antiguas.
Supongamos que lo fuera. ¿Qué buscar como evidencia? Dirá "infección radioactiva" y se equivocará. Más bien, solo tienen razón en parte.
La radiactividad fue y es sin guerra nuclear. Pero la radioactividad de la bomba atómica es especial, tiene algo que permite distinguirla de la natural sin error. Esta es una composición especial de radionúclidos.
La radiactividad natural se debe a isótopos bien definidos. Estos son potasio-40, rubidio-87, uranio y torio (con productos radiactivos de su descomposición), en general, isótopos que tienen enormes semividas que les permitieron sobrevivir incluso desde el momento en que no había ni la Tierra ni el Sol. Se les agregan algunos de los llamados isótopos cosmogénicos: carbono 14, berilio 7, sodio 22 y tritio. Se forman bajo la influencia de los rayos cósmicos y se reproducen constantemente.
Pero los radionucleidos característicos de una explosión nuclear son completamente diferentes. En la era pre-nuclear en la Tierra (sin contar los reactores nucleares naturales de Okloo), no había un átomo de cesio-137, ni cobalto-60, ni rutenio-106. Si surgieron una vez, durante el estallido de la Supernova, que generó la sustancia a partir de la cual el Sol y los planetas se formaron con el tiempo, entonces, en nuestra era, habían desaparecido sin dejar rastro. Y después de 200 años, los más longevos habrían sobrevivido. Y los encontraríamos, en forma de picos de actividad distintos en las capas de sedimentos del fondo, que vemos ahora en las capas de los años 1950-60 del siglo pasado, así como en la capa de 1986.
Los habríamos encontrado en Mohenjo-Daro y en esos mismos huesos radiactivos de la Edad de Piedra. Pero allí encontramos solo torio y uranio. Y los productos de su descomposición son el mismo radio.
Otro mito: el fondo de radiación se ha multiplicado por diez desde el descubrimiento de la radiactividad. Una variante del mito con elementos de la teoría de la conspiración: para ocultar esto, en los años sesenta, los dispositivos radiométricos fueron retirados de los laboratorios y devueltos después de la recalibración.
Este mito es refutado de manera muy simple. Desde entonces, es sorprendente cómo, pero en los depósitos de laboratorio los viejos mostradores Geiger se conservaron en sus cajas nativas con pasaportes. Tipos MS-6, BC-6, etc. Y en ellos estaba la figura escrita a mano del "fondo natural". «» , , .
, — , — - , , -137 . , - . 8-12 / , , — . 0,5-1 / .
- . . , -90, , , -137. -137 50-100 /, — . -239
.
— , . -, -137 - , «» - .
::: , ,