
Uno de los superhéroes más famosos de Marvel siempre ha sido y será considerado Logan, también conocido como Wolverine. ¿Y qué característica de su cuerpo viene a la mente primero, además de, por supuesto, la regeneración con la velocidad de Flash? En una palabra: adamantium. Este metal raro tiene propiedades únicas, es casi imposible destruirlo y el procesamiento requiere mucho esfuerzo. Esta sustancia ficticia tiene varios equivalentes en nuestra realidad, que también tienen propiedades muy específicas. Entre ellos, el iridio merecía especial atención de los científicos. Este metal difícilmente puede hacer un súper héroe de una persona simple, pero él sabe cómo destruir las células cancerosas (Deadpool no rechazaría tal cosa). ¿Cómo llegaron los científicos a esta conclusión: qué tan efectivo es el iridio en la lucha contra el cáncer y cuál es su futuro en oncología? Sumérgete en el informe del grupo de estudio para obtener respuestas. Vamos
Ciencia del metalEl iridio (Ir) es un metal de transición extremadamente sólido del grupo del platino. Al igual que el adamantium ficticio, el iridio es muy resistente a la corrosión incluso a temperaturas de 2000 ° C. Otra similitud de estos dos metales en su origen extraterrestre. Más precisamente, el iridio en nuestro planeta es muy pequeño, por lo tanto, en alta concentración se encuentra en lugares donde caen meteoritos.
 Iridium (Ir)
Iridium (Ir)El iridio es un metal bastante joven en el mundo científico, ya que fue descubierto en 1803 por el químico Smithson Tennant. Trabajó en platino con una mezcla de ácidos nítrico e clorhídrico, que tiene un nombre muy inusual: aqua regia. Y como queda claro por la composición de esta solución, después de usarla no se convertirá en un "maestro borracho", como Jackie Chan en la película del mismo nombre, sino más bien un maestro muerto. Porque la palabra "vodka" originalmente significaba agua corriente y solo después del siglo XIV comenzó a usarse para significar una bebida alcohólica.
Con la ayuda del vodka real, el Sr. Tennant pudo obtener en forma pura las impurezas que estaban en platino, a saber, osmio e iridio.
Como se mencionó anteriormente, hay muy poco iridio: se extraen alrededor de 3 toneladas de este metal por año. A modo de comparación, la extracción de plata, según algunas fuentes, supera la marca de 27,000 toneladas por año.
Base de estudioEl estudio se basa en el método ya aplicado de tratamiento del cáncer (y algunos otros también): la terapia fotodinámica (PDT). Los personajes principales de este método son los fotosensibilizadores y la luz.
Fotosensibilizadores * : sustancias que aumentan la sensibilidad a la exposición a la luz en los tejidos biológicos.
Los sensibilizadores son bastante exigentes, es decir, se acumulan solo en aquellos tejidos que deben cambiarse para el procedimiento adicional de irradiación con luz.
Cuando la luz ingresa al tejido objetivo, se produce una reacción fotoquímica: el oxígeno del triplete molecular (
3 O
2 ) se convierte en oxígeno singlete. Además, se forman radicales altamente activos. Juntos, esto conduce a la muerte de las células cancerosas.
Los científicos citan la fotofrina y el ácido aminolevulínico como los fotosensibilizadores más comunes en la terapia PDT. Sin embargo, en los últimos años, se ha prestado cada vez más atención a los metales con un alto coeficiente de luminiscencia, ya que tienen propiedades fotoquímicas y fotofísicas inusuales y útiles. Por ejemplo, TLD1433 (rutenio) para el tratamiento de PDT para la vejiga y WST11 (paladio) para el tratamiento de los vasos sanguíneos.
Resultados de la investigaciónEntonces, ¿por qué no usar iridio, pensaron los científicos? Pero primero necesita un mecanismo que permita utilizar este metal. El paciente no tomará iridio por vía oral, como las tabletas normales. Y aquí la albúmina sérica humana (
HSA ) está conectada al trabajo, que, debido a sus propiedades y cantidad (aproximadamente el 55% de todas las proteínas de la sangre), es un excelente portador de diversas sustancias (en nuestro caso, medicinales). En pocas palabras, el CSA se puede usar para administrar medicamentos contra el cáncer en el área deseada del cuerpo del paciente, lo cual ya se ha demostrado en estudios anteriores con osmio, rutenio y paladio.
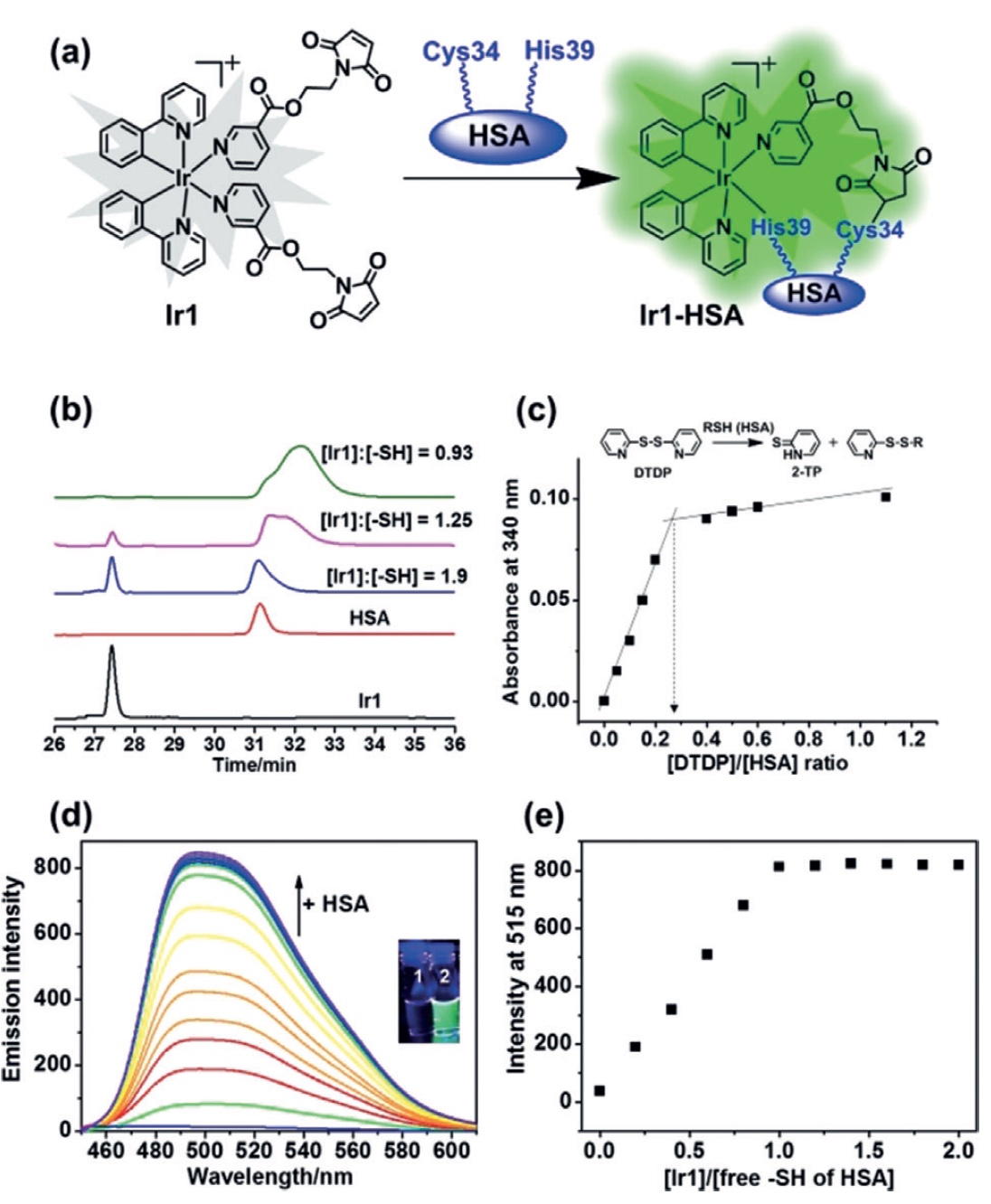 Imagen No. 1
Imagen No. 1En nuestro estudio, los científicos crearon un complejo de organoiridio octaédrico funcionalizado con maleimida (III) Ir1 (
1a ) en combinación con HSA. Este complejo (Ir1-HSA) resultó ser mucho más efectivo para aumentar la fosforescencia en comparación con Ir1 "puro", es decir, sin HSA.
En la oscuridad, Ir1-HSA es en gran medida no tóxico para las células ordinarias, pero exhibe una fuerte fototoxicidad hacia las células cancerosas y sus esferoides (formaciones celulares).
El Ir1 sintetizado fue estable durante 12 horas en la oscuridad y después de 1 hora de exposición a la luz azul. Fue necesario verificar el enlace carbono-carbono (C = C). Para esto, se hizo reaccionar un complejo de Ir1 y cisteína (Cys) en una relación molar de Cys: Ir1 - 2: 1 en [D6] DMSO / D2O a una temperatura de 298 K durante 30 minutos. Como resultado de la resonancia magnética de protones, los científicos encontraron que el valor máximo de los protones de vinilo de los grupos maleimida es de alrededor de 6.62 ppm (millonésimas de una parte). Con la adición de cisteína, los picos desaparecieron, pero luego reaparecieron ya en el rango de 2.9 ... 3.9 ppm. Los científicos atribuyen esto a la conjugación de cisteína.
Luego, los científicos verificaron si el tiol libre Cys34 de HSA puede reaccionar con C = C. Para esto, se incubaron 30 μM (micromol) Ir1 con HSA (0-120 μM) durante 1 hora. Además, los productos de reacción resultantes se separaron usando cromatografía líquida de alto rendimiento en fase inversa (RP-HPLC).
Cuando la HSA alcanzó 120 μM, el pico de Ir1 desapareció por completo (relación de HSA: Ir1 = 4: 1). Por lo tanto, el contenido de tiol (SH) fue de 0.27 ± 0.1 mol de SH por 1 mol de HSA (
1 s ). En consecuencia, la concentración de grupos SH libres de HSA 120 μM es 32.4 ± 1.2 μM. Con este indicador, se produce una reacción con 30 μM de Ir1, lo que lleva a la aparición de un aducto (conexión directa de moléculas) Ir1 y HSA en una proporción 1: 1.
El Ir1 puro no exhibió radiación fuerte en solución acuosa, en contraste con el complejo Ir1-HSA (
1d ). Cuanto mayor es la concentración de HSA, más fuerte se vuelve la fosforescencia de Ir1 (
1e ).
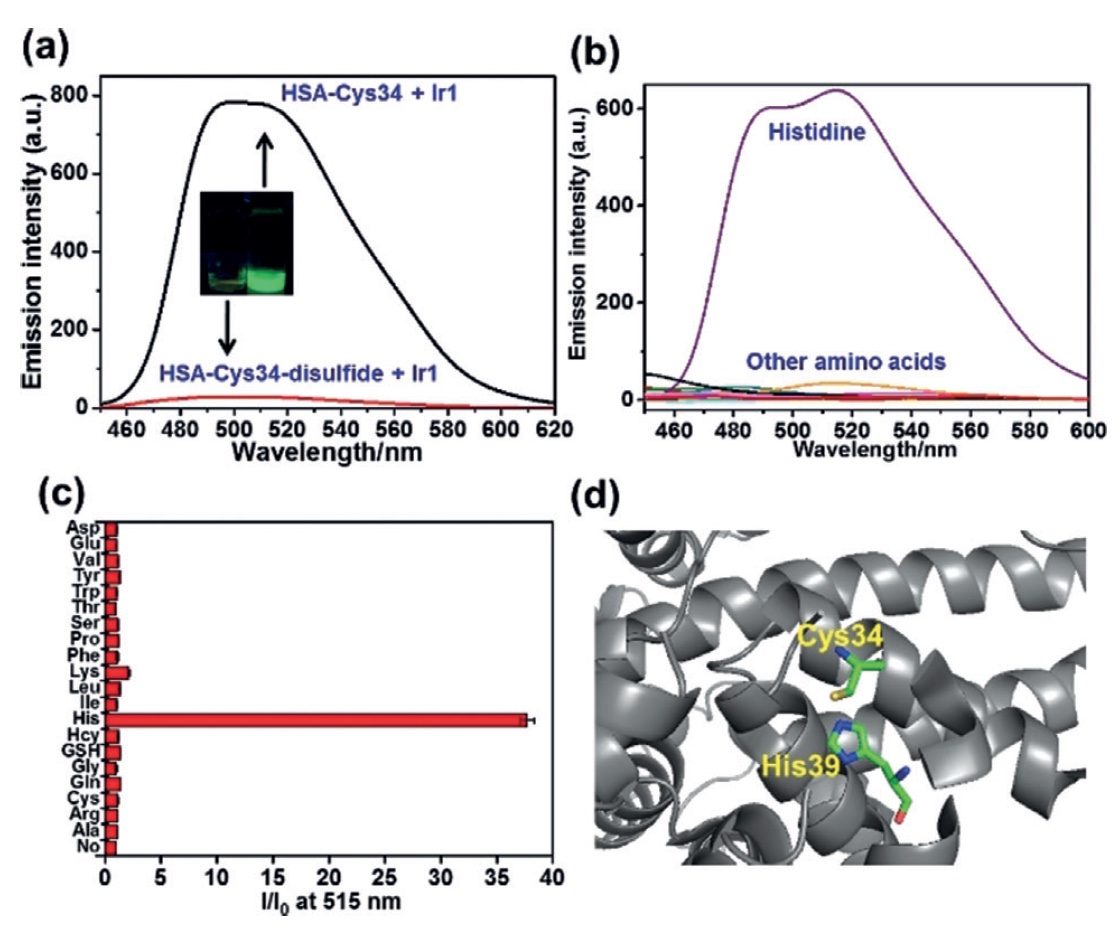 Imagen No. 2
Imagen No. 2Para eliminar los grupos tiol libres de HSA, se añadió cistina 100 μM por día a la solución a una temperatura de 277 K. El producto resultante se combinó con Ir1 durante 30 minutos. Las observaciones mostraron una disminución significativa en la fosforescencia. En el caso del conjugado HSA-Cys34 e Ir1 (
2a ), la situación era opuesta, y esto sugiere que el Thysol Cys34 libre es el enlace de conexión (más precisamente, el dominio de unión) para Ir1.
Ahora era necesario estudiar el CSA con más detalle, analizándolo en sus componentes. La albúmina sérica humana tiene una cadena de 585 residuos de aminoácidos, entre los cuales los científicos necesitan encontrar exactamente aquellos que mejoren la luminiscencia de Ir1. Para esto, se realizó un análisis luminiscente de la interacción de Ir1 con varios aminoácidos (
2b y
2c ). Y como podemos ver en el gráfico
2b , el líder entre los aminoácidos con un margen enorme es la histidina (His), que aumenta la luminiscencia de Ir1 en 37 veces.
Al comprender un poco qué y cómo funciona dentro de los componentes constitutivos del complejo Ir1-HSA, los científicos cambiaron a la aplicación práctica, es decir, a los experimentos.
Primero, se diluyeron 0,4 milimoles de Ir1 en 20 ml de MeOH: H2O, se añadieron 0,4 milimoles de HSA y se agitó durante 1 hora. Luego se usó microscopía confocal para investigar la distribución de Ir1-HSA en células vivas de cáncer de pulmón (A549).
Ya después de 30 minutos, Ir1-HSA se concentró principalmente en el citoplasma de las células cancerosas. A los 60-120 minutos del inicio de la incubación, el complejo penetró en los núcleos de las células cancerosas.
 Imagen 3: Microscopía confocal de células de cáncer de pulmón A549.
Imagen 3: Microscopía confocal de células de cáncer de pulmón A549.Sin embargo, vale la pena señalar que no todo el complejo penetró en los núcleos de las células cancerosas, sino solo Ir1. Una prueba de inmunofluorescencia mostró que HSA simplemente estaba ausente en los núcleos de las células expuestas a Ir1.
 Imagen No. 4: análisis de inmunofluorescencia de la presencia de HSA en células de cáncer de pulmón.
Imagen No. 4: análisis de inmunofluorescencia de la presencia de HSA en células de cáncer de pulmón.Pero la HSA no desaparece sin dejar rastro, simplemente permanece en el citoplasma y en la membrana del núcleo de la célula cancerosa. Resulta que el HSA cumple plenamente su función: entregó Ir al núcleo de la célula y se quedó afuera.
 Imagen No. 5: rendimiento cuántico y vida útil de la fosforescencia Ir1 y el complejo Ir1-HSA.
Imagen No. 5: rendimiento cuántico y vida útil de la fosforescencia Ir1 y el complejo Ir1-HSA.Los científicos también verificaron el rendimiento cuántico (exagerado, fuerza) y la vida útil de la fosforescencia Ir1 (por sí misma) y el complejo Ir1-HSA.
El rendimiento cuántico de Ir1 fue muy pequeño (solo 0.001), y la vida útil a una temperatura de 298 K fue de 182.7 nanosegundos (
5a ). Pero el rendimiento cuántico de Ir1-CSA ya era 0.036, y la vida útil fue de 871.8 ns. Esta duración de la fosforescencia contribuye a la generación de oxígeno singlete (
1 O
2 ).
La espectroscopía de resonancia paramagnética de electrones usando 2,2,6,6-tetrametilpiperidina como trampa de rotación ayudó a detectar la generación de 1O2 en Ir1 puro y en el complejo Ir1-HSA tras la irradiación a 465 nm durante 20 minutos (
5b ). Como se esperaba, el rendimiento cuántico de 1O2 de Ir1-HSA fue significativamente mayor (0.83) que el de Ir1 (0.06).
También fue necesario verificar el grado de efecto de Ir1-HSA e Ir1 en las células cancerosas y en las sanas. Se utilizaron tres opciones como células cancerosas: cáncer de pulmón A549, hepatoma Hep-G2 y cáncer de pulmón resistente a cisplatino A549R. Como células sanas, se utilizaron MRC-5 (pulmones) y LO2 (hígado). El experimento se llevó a cabo en dos variaciones de iluminación: oscuridad completa durante todo el experimento y luz azul.
Las células se incubaron con Ir1 o Ir1-HSA durante 2 horas, se lavaron con perborato de sodio y se irradiaron con luz azul durante 20 minutos, o se dejaron en la oscuridad (segunda versión del experimento). Después de esto, las células se restauraron en 46 horas.
El efecto de Ir1 sobre las células A549 en la oscuridad (89,6 μM) y bajo iluminación (53,3 μM) estaba prácticamente ausente.
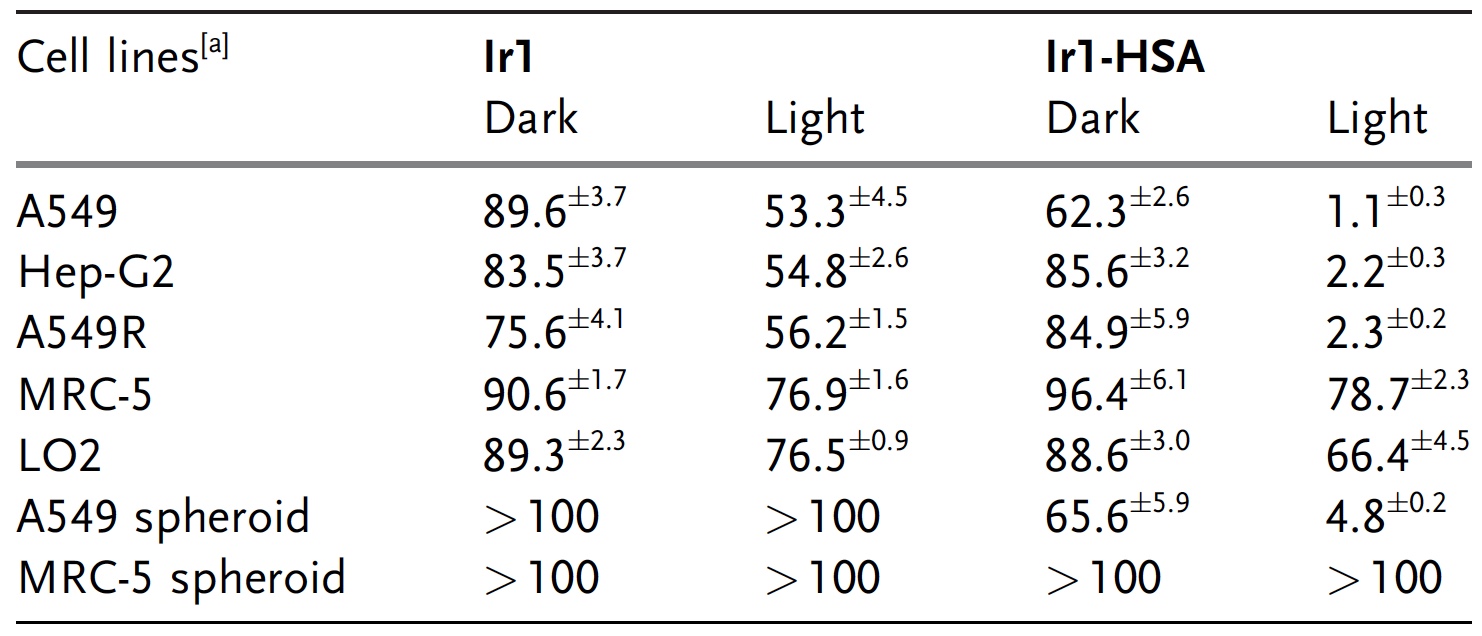 Tabla de los efectos de Ir1 e Ir1-HSA en las células cancerosas: cuanto mayor es el número, menor es la exposición (es decir, más células cancerosas permanecen ilesas).
Tabla de los efectos de Ir1 e Ir1-HSA en las células cancerosas: cuanto mayor es el número, menor es la exposición (es decir, más células cancerosas permanecen ilesas).Pero Ir1-CSA mostró resultados muy diferentes. En la oscuridad, el complejo de prueba no afectó a las células cancerosas de ninguna manera, pero cuando se iluminó, su citotoxicidad aumentó significativamente. Resultados similares, como vemos en la tabla anterior, Ir1 e Ir1-HSA mostraron en relación con otras células cancerosas. Al mismo tiempo, las células sanas en la oscuridad y bajo iluminación no se vieron afectadas por Ir1 e Ir1-HSA.
Finalmente, los científicos realizaron un análisis de especies reactivas de oxígeno (ROS) dentro de las células después de la exposición a la luz. En la oscuridad, como se esperaba, no se detectaron ROS. Pero en las células que se sometieron a irradiación de luz después de la aplicación de Ir1-HSA, se detectaron ROS (
5c ).
Para un conocimiento más detallado del estudio, le recomiendo que consulte el
informe de los científicos y los
materiales adicionales .
EpílogoCon este estudio, los científicos no intentaron inventar una bicicleta en forma de metales raros en la terapia fotodinámica, porque ya se había hecho antes con osmio y paladio. Sin embargo, nadie ha intentado usar iridio, que los investigadores decidieron arreglar. Su trabajo no fue inútil, ya que el iridio mostró excelentes resultados en la lucha contra las células cancerosas de varios tipos, sin afectar las saludables.
Las enfermedades oncológicas son una de las más comunes y se cobran millones de vidas cada año. La invención de nuevos métodos para combatir esta dolencia y la mejora de los existentes deberían y continuarán. Por supuesto, todavía estamos lejos de una victoria total sobre el cáncer, pero los científicos de todo el mundo continúan luchando en los laboratorios, como millones de pacientes en las salas.
No olvide también los factores que conducen a la aparición de cáncer. Algunos de ellos (ecología, malos hábitos, etc.) pueden ser completamente eliminados por una persona.
Viernes fuera del tema:
Nadie en su sano juicio se regocijará en oncología. Tales diagnósticos hacen que te rindas y te olvides de todo. Pero nunca debes rendirte. Si no peleas, el diagnóstico definitivamente prevalecerá. Pero si luchas contra la enfermedad, siempre existe la posibilidad de vencerla. Entonces, ¿por qué no aprovechar esta oportunidad?
Gracias por mirar, mantén la curiosidad y que tengan un gran fin de semana, muchachos.
Gracias por quedarte con nosotros. ¿Te gustan nuestros artículos? ¿Quieres ver más materiales interesantes?
Apóyenos haciendo un pedido o recomendándolo a sus amigos, un
descuento del 30% para los usuarios de Habr en un análogo único de servidores de nivel de entrada que inventamos para usted: toda la verdad sobre VPS (KVM) E5-2650 v4 (6 núcleos) 10GB DDR4 240GB SSD 1Gbps de $ 20 o cómo dividir el servidor? (las opciones están disponibles con RAID1 y RAID10, hasta 24 núcleos y hasta 40GB DDR4).
VPS (KVM) E5-2650 v4 (6 núcleos) 10GB DDR4 240GB SSD 1Gbps hasta la primavera sin cargo al pagar por un período de seis meses, puede ordenar
aquí .
Dell R730xd 2 veces más barato? ¡Solo tenemos
2 x Intel Dodeca-Core Xeon E5-2650v4 128GB DDR4 6x480GB SSD 1Gbps 100 TV desde $ 249 en los Países Bajos y los Estados Unidos! Lea sobre
Cómo construir un edificio de infraestructura. clase utilizando servidores Dell R730xd E5-2650 v4 que cuestan 9,000 euros por un centavo?