
Con casi todas las conversaciones sobre la radiactividad con un laico, resulta que el interlocutor tiene, en un grado u otro, una vaga idea de unidades de medida. Entonces, cuando publiqué un artículo sobre el laboratorio radioquímico, uno de los lectores se quejó conmigo en la tarde de que tenía muchas unidades encontradas en libros y artículos sobre radioactividad: rayos X, rems, rems, alegres, grises, sievert, curie, becquerel e incluso equivalentes de gramo de radio: mi cabeza da vueltas y me pide que escriba al respecto. Cumplo su pedido.
Sí, en KDPV - cónyuges Maria Sklodovskaya-Curie y Pierre Curie.
Un poco de historia
En 1895, Wilhelm Konrad Roentgen descubrió la radiación que tenía propiedades sorprendentes: actuando como la luz en las placas fotográficas y excitando el brillo de las pantallas luminiscentes, penetraba fácilmente a través de obstáculos opacos. No pasó mucho tiempo, resultó que la fuente de dicha radiación no es solo un tubo de Crookes que funciona, como en los experimentos de rayos X, sino también sustancias que contienen uranio, que, además, emiten esta radiación de forma continua, invariable y sin ningún suministro de energía. desde el exterior Esto fue seguido literalmente por una avalancha de descubrimientos. El descubrimiento de radio, polonio y luego un montón de nuevos elementos radiactivos, estableciendo la conexión de la desintegración radiactiva con la conversión de un elemento a otro, las primeras reacciones nucleares llevadas a cabo ... En general, el experimento sorprendentemente simple de Becquerel con sal de uranio en una placa fotográfica envuelta en papel negro literalmente imprimió un "pote- no cocine ”nuevo conocimiento. La conversación sobre estos descubrimientos es el tema de otro artículo (y no uno), y ahora solo diré que ya en los primeros meses y años de este "auge del radio", las mediciones no pudieron prescindirse.
El primer dispositivo de medición para determinar la intensidad de la radiación ionizante fue un electroscopio o electrómetro ordinario, que se descargó bajo la influencia de la radiación, y la velocidad de esta descarga fue proporcional a su intensidad. Y el primer estándar fue ...
Miligramo de ampolla de radio como medida de radiactividad
Esta ampolla no solo fue el primer estándar para la calibración de electrómetros y cámaras de ionización, sino que fue una medida de la cantidad de radiactividad. Una propiedad sorprendente del radio era la constancia excepcional de su radiación: su intensidad dependía solo de la cantidad de radio. Por lo tanto, una vez que tomó una muestra de 1 mg de radio y la selló en una ampolla de platino, fue posible no pesar nunca más el radio. Al comparar la intensidad de la radiación gamma de una ampolla de referencia y una muestra colocada en una ampolla con el mismo grosor de pared, fue posible determinar la cantidad de radio con alta precisión. Por lo tanto, las ampollas con radio tomaron su lugar legítimo en las cámaras de pesas y medidas junto a los estándares de metros, kilogramos
y caballos esféricos .
Estrictamente hablando, la fuente de radiación gamma no es el radio. Y es precisamente con esto que la
ampolla sellada era el estándar. El hecho es que el radio-226 no emite rayos gamma durante la descomposición. Emite una partícula alfa, convirtiéndose en radón-222, que luego se llamaba la
emanación de radio . Este último, que también es alfa-activo, sufre una serie de desintegraciones con la emisión de partículas alfa y beta, algunas de las cuales están acompañadas por radiación gamma. El radón no tiene a dónde ir desde una ampolla sellada, y
se establece un
equilibrio secular entre el radio y sus productos de desintegración radiactiva: cuánto radón (y cada miembro posterior de la serie radiactiva) se ha formado, tanta desintegración.
Al comparar la radiactividad de otros elementos descubiertos posteriormente con la radiación, comenzaron a utilizar una unidad como el
equivalente en miligramos de radio , igual a la cantidad de sustancia radiactiva que proporciona la misma intensidad de radiación gamma que miligramos de radio a la misma distancia.
El equivalente en miligramos de radio, como unidad de radioactividad, tiene el inconveniente obvio de que la radiación gamma, en general, es un tipo de efecto secundario de la desintegración radiactiva. En muchos casos, está ausente o no en cada acto de descomposición. Por lo tanto, pasamos de comparar las intensidades de radiación gamma al concepto de
actividad como una medida del número de eventos de descomposición en una preparación por unidad de tiempo . El estándar permaneció en la misma ampolla con radio, y a partir de aquí apareció una unidad
curie , definida como la actividad de una sustancia radiactiva en la que se descomponen tantos átomos por unidad de tiempo (es decir,
piezas), cuántos átomos de radio-226 se descomponen en un gramo.
La unidad curie ahora se considera obsoleta, como todas las unidades que no son del sistema. En el sistema SI, el
becquerel lo reemplaza: esta es la actividad de la droga, en la cual ocurre en promedio una descomposición por segundo. Por lo tanto, 1 Ki =
Bq.
Electrómetro y dosis de exposición
El primer dispositivo para medir la intensidad de la radiación radiactiva, como dije, fue un electrómetro, que se descargó bajo la influencia de los rayos de radio. Se convirtió en el precursor de la cámara de ionización, una cámara con dos electrodos con carga opuesta, lo que permitió determinar la cantidad de iones formados en el aire que llena la cámara. Estos iones en un campo eléctrico dentro de la cámara de ionización comienzan a moverse hacia los electrodos y, una vez que los alcanzan, los descargan. La magnitud de la disminución en la carga de los electrodos puede determinar el número de pares de iones que se forman en el aire bajo la influencia de la radiación. Y midiendo la corriente que fluye a través de la cámara en el circuito de una fuente de voltaje externa, puede determinar el número de pares de iones generados en la cámara por unidad de tiempo, proporcional a la intensidad de la radiación.
El valor así medido se llamó
dosis de exposición de la radiación. Y la unidad de medida era
la radiografía . A una dosis de exposición de 1 radiografía en un centímetro cúbico de aire seco, se forma una unidad de HSE (
C) carga de cada uno de los iones, que corresponde a
pares de iones Por cierto, nuestra referencia de 1 mg de radio en una ampolla de platino a una distancia de 1 cm durante una hora crea una dosis de exposición de 8.4 rayos X (generalmente en este caso dicen que la
tasa de dosis de exposición es 8.4 R / h).
No hay una unidad especial de dosis de exposición en el sistema SI y la unidad es colgante por kilogramo.
1 C / kg = 3875.97 R. Sin embargo, en la actualidad esta unidad se usa muy raramente debido al rechazo del concepto mismo de dosis de exposición. La razón de esta falla es que esta cantidad fácilmente medible es de poca utilidad para la aplicación práctica. Por lo general, no estamos interesados en cuántos iones se formaron en el aire, sino en la acción que irradiaba la sustancia o el tejido vivo.
Dosis absorbida
La idea de considerar la energía absorbida en esta sustancia como una medida del efecto de la radiación radiactiva en una sustancia es bastante obvia. Esta es la
dosis absorbida , cuya medida es la energía de radiación absorbida por una unidad de masa de la sustancia. La unidad de medida de la dosis absorbida en SI es
gris : 1 Gy = 1 J / kg. Anteriormente, se utilizaba otra unidad,
me alegro . 1 rad = 100 erg / g = 0.01 Gy. A una dosis de exposición de 1 P, la dosis absorbida en el aire es de 0,88 rad. En la mayoría de los casos, estos 0.88 se redondean a la unidad, lo que equivale a rad a rayos X (aunque en realidad son cantidades físicas diferentes), y gris (y sievert, que se describe a continuación) a 100 rayos X.
Pero la dosis en varias sustancias a la misma dosis de exposición será diferente según el tipo y la energía de la radiación y las propiedades del absorbente. Es por esta razón que ahora se ha abandonado el concepto de dosis de exposición. En la práctica, es mucho más correcto medir no la dosis de exposición, sino tomar un detector cuyo número atómico promedio es igual al número atómico promedio de tejido biológico (en este caso hablamos de un
detector equivalente de tejido ) y medir la dosis absorbida en él. Luego, con cierto grado de precisión, se puede suponer que la dosis absorbida en el detector será igual a la dosis absorbida en el tejido biológico.
Todo tipo de dosis diferentes.
Pero resulta que diferentes tipos de radiación radioactiva actúan de manera diferente en el tejido vivo. La radiación alfa, los protones y los neutrones a la misma dosis absorbida le causan mucho más daño que la radiación gamma y las partículas beta. En este sentido, junto con la dosis absorbida, surge otro tipo de dosis: la
dosis equivalente . Es igual a la dosis de radiación gamma, que causa
el mismo efecto biológico que la dosis de esta radiación.
La unidad de dosis equivalente es
sievert . La unidad anterior de la dosis equivalente es el
equivalente biológico de rayos X o
rem , en inglés
REM (a veces en la literatura y los radiólogos traducidos puede encontrar la unidad "rem", este es el mismo rem). 1 Sv = 100 rem.
Para traducir la dosis absorbida en el equivalente, debe multiplicar la dosis absorbida por el llamado
factor de calidad . Este coeficiente para fotones, electrones y muones es igual a la unidad, para partículas alfa se supone que es igual a 20, para protones según diversas fuentes es de 2 a 5, y para neutrones depende mucho de la energía, llegando a 20 en el rango de energía de 100 keV a 2 MeV ( ver foto).
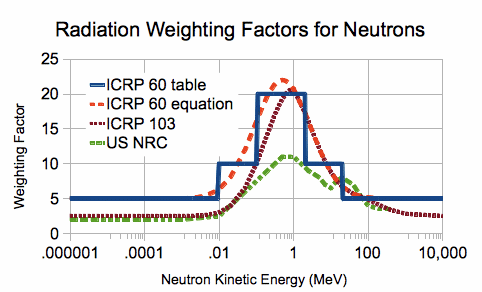
Además del equivalente, también se considera una dosis efectiva. Tiene en cuenta no solo un grado diferente de daño de la radiación, sino también un grado diferente de daño de la irradiación de una u otra parte del cuerpo u órgano cuando se irradia no solo todo el cuerpo, sino también su parte. Los factores de pesaje se atribuyen a cada tejido y órgano de tal manera que la suma es igual a uno. Con una exposición uniforme a todo el cuerpo, la dosis efectiva es equivalente. Se mide en las mismas unidades que el equivalente.
Me detendré aquí: no te confundiré y te diré qué es kerma, la dosis equivalente ambiental y muchas cosas más.
¿Y cómo se mide todo?
Para medir la dosis de exposición, como dije, debe tomar una cierta cantidad de aire, recolectar los iones formados en ella y determinar su cantidad, que puede resolverse con éxito usando una cámara de ionización. Es sobre la base de las cámaras de ionización que se hizo la mayor parte de los dosímetros acumulativos del tipo "lápiz".
Y para medir la dosis absorbida, debe medir la cantidad de energía liberada en la sustancia. Y aquí radica la principal dificultad. La medición directa de esta energía es muy difícil, ya que en la mayoría de los casos es muy pequeña. Un gris (y esta es una dosis grave, que ya causa enfermedad por radiación) es solo un julio por kilogramo. Si intentamos medir esta dosis, por ejemplo, calorimétricamente, por cambio de temperatura, entonces, por ejemplo, el aluminio se calentará un poco más de una milésima de grado.
Por lo tanto, todos los métodos para medir la dosis absorbida o su potencia son indirectos. Consisten en el hecho de que observamos un cierto proceso causado por la irradiación y que requiere gastos de energía, y suponemos que la "salida" de este proceso dependerá linealmente de la contribución de energía de la radiación absorbida.
El acto primario de interacción de la radiación ionizante con la materia es casi siempre la ionización misma. Un cuántico de rayos gamma u otra partícula emitida por una sustancia radiactiva generalmente tiene una energía que es mucho más alta que la energía necesaria para arrancar un electrón de un átomo. Por lo tanto, no termina con un solo acto de ionización. A lo largo de toda la trayectoria de la partícula, se generan electrones libres e iones cargados positivamente en la sustancia, cuyas energías generalmente exceden la energía de ionización, lo que lleva al desarrollo de una cascada completa de procesos para la formación de electrones e iones libres, hasta que su energía sea comparable con la energía del enlace químico , con las primeras energías de ionización, etc. Y estos electrones e iones ya llevan a cabo directamente el efecto sobre la sustancia característica de los rayos ionizantes: excitan la luminiscencia, inician reacciones químicas, destruyen estructuras biológicas y se convierten en portadores de corriente eléctrica. Tanto su cantidad como su energía total son proporcionales a la dosis absorbida (estrictamente hablando, menos la energía de los electrones que salen de la sustancia), y ya "no saben nada" sobre lo que les dio origen.
Históricamente, uno de los primeros dosímetros fue una película ordinaria envuelta en un material resistente a la luz. El grado de ennegrecimiento después de la manifestación depende aproximadamente de la dosis absorbida, así como de la exposición a la luz visible ordinaria: hay una región de dependencia lineal limitada por la flexión en la región de dosis baja y por saturación (con posterior solarización - disminución de la densidad) en la región de dosis alta. La película es un dosímetro barato y bastante sensible, pero no muy confiable, ya que pequeñas desviaciones en los regímenes de tratamiento pueden dar errores notables en la determinación de la dosis. La película fotográfica es uno de los primeros representantes de la familia de dosímetros químicos en los que el valor de la dosis está determinado por la cantidad de una sustancia formada o consumida durante la reacción: coloreada, paramagnética o que posee otra propiedad fácilmente medible. Puede ser una solución en una ampolla que se oscurece o se mancha bajo la influencia de la radiación (por ejemplo, debido a la oxidación del hierro (II) a hierro (III) con la posterior formación de tiocianato rojo de colores brillantes), vidrio o un cristal en el que la llamada radiación Defectos que absorben la luz. Los dosímetros químicos permiten determinar la dosis de radiación con alta precisión y dentro de un rango muy amplio, desde aquellos que no causan daño especial a una persona hasta aquellos que lo matan en un minuto. Pero, como regla, no permiten medir la tasa de dosis.
La luminiscencia permite detectar incluso el acto de absorción de una sola partícula o rayo gamma, lo que provoca la aparición de un breve destello de luz en el material del detector: centelleo. Este principio se basa en la acción de los detectores de centelleo, que permiten medir incluso flujos de radiación muy débiles, que son decenas y cientos de veces más débiles que el fondo de radiación natural. El sensor de radiación de centelleo, a diferencia de los detectores químicos, le permite determinar la potencia de la dosis absorbida por el detector en tiempo real. Por supuesto, para obtener el valor de dosis, o la tasa de dosis, es necesario no solo contar el número de pulsos, sino resumir e integrar la luz emitida por el centelleador.
Un tipo especial de tales detectores son los llamados detectores termoluminiscentes. Utilizan material luminiscente que, en lugar de emitir cada partícula con un destello de luz, retiene las cargas libres formadas por este en forma de defectos reticulados cargados de larga duración. Cuando se calientan, estos defectos "sanan", y los electrones y agujeros liberados se recombinan, transfiriendo energía a los centros de luminiscencia. E integrando el pulso de luz que ocurre cuando se calienta el termoluminóforo, determinaremos la dosis acumulada por él.
Finalmente, podemos "captar" no los efectos secundarios causados por la ionización, sino los iones mismos, al igual que en la cámara de ionización, solo esta cámara no está llena de gas, sino de un semiconductor: germanio, silicio, telururo de cadmio y, finalmente, diamante. La corriente promedio a través del detector será proporcional a la potencia de la dosis absorbida por él.
Pero, ¿qué pasa con el conocido contador Geiger? Pero él no mide la dosis. Solo puede reaccionar con impulso al paso de partículas a través de él, sin comprender qué voló hacia él, ni qué tipo de energía tenía. Es decir, puede medir una característica del flujo de partículas como la
fluencia : cuántas partículas volaron a través de un área determinada. Un detector de centelleo o semiconductor funcionará exactamente de la misma manera si solo registramos el hecho de la aparición de un pulso, ignorando su amplitud.
Dosis en diferentes materiales y trazo con rigidez
En el párrafo sobre la dosis absorbida, mencioné de pasada que la dosis absorbida por diferentes materiales en el mismo flujo de radiación será diferente y dependerá de la energía de los cuantos y las propiedades de la sustancia. En el caso de la radiación gamma, su absorción está determinada por la única característica del material: el número atómico promedio (o efectivo)
. La radiación gamma se transfiere a sustancias con el mismo
la misma energía cuando pasa a través de una capa con la misma masa por unidad de área. Por lo tanto, un material que tenga la misma composición atómica bruta que el tejido vivo absorberá los rayos gamma a cualquier energía de la misma manera que el tejido vivo, y por lo tanto la dosis absorbida en un detector hecho de este material será igual a la dosis absorbida en el cuerpo humano . Y si hacemos un detector con yoduro de cesio (uno de los centelleadores más utilizados), entonces podemos calibrarlo para cualquier energía, y en otras energías yacerá. Tal cambio en las lecturas de un dispositivo dosimétrico que depende de la energía de radiación se denomina "accidente cerebrovascular con rigidez" o la
dependencia energética de la sensibilidad a la dosis del detector .

La figura (del New Handbook of a Chemist and Technologist, vol. 11, p. 111) muestra las dependencias energéticas de la sensibilidad a la dosis de los detectores fabricados en base a diferentes centelleadores.
A la izquierda, se compara el antraceno (más ligero en peso atómico promedio que el tejido vivo) y el yoduro de sodio (significativamente más "pesado" que el anterior). ¡Se puede ver que en un cierto rango de energía, el detector a base de yoduro de sodio sobreestima la dosis en 10 veces! Y en el gráfico de la derecha se muestra que tomando una mezcla de centelleadores orgánicos, más "ligero" y más "pesado" que el tejido vivo, puede eliminar casi por completo el "movimiento con rigidez".Otra forma de eliminar el "golpe con rigidez" es seleccionar filtros que absorban la radiación en el área donde la sensibilidad del detector es excesiva.Conclusión
En conclusión, daré un plato pequeño, que resume las principales cantidades consideradas en el artículo. Y para una familiarización más completa con el tema, recomiendo las conferencias del profesor Igor Nikolaevich Bekman , Universidad Estatal de Moscú.
Y para una familiarización más completa con el tema, recomiendo las conferencias del profesor Igor Nikolaevich Bekman , Universidad Estatal de Moscú.Todos los artículos de la serie.
Radiación: vida cotidiana del laboratorio radioquímicoRadiación: fuentesRadiación: riesgos, seguridad, protección