
Tenemos alrededor de 205 de ellos, en total pesan alrededor de 5-6 kg y cada 10 años se actualizan por completo a nivel celular. Y hay una expresión idiomática que indica que todos la tienen en el armario. Esto, por supuesto, se trata del esqueleto y de los huesos que lo componen. La lesión ósea es una de las lesiones más comunes en el mundo. A veces, tales lesiones no requieren tratamiento óseo, sino su reemplazo. El trasplante de hueso está asociado con una serie de peligros para el paciente, que incluyen dolor posterior, infección, sangrado, daño a los tejidos conjugados, etc.
Algunos científicos creen que la clave para un trasplante óseo exitoso radica en el uso de huesos impresos, que serán ideales para un paciente en particular y estarán libres de defectos. ¿Cómo imprimieron los huesos los científicos, qué se aplicó para esto y qué resultados mostró la operación de implantación en una rata? Aprendemos sobre esto del informe del grupo de investigación. Vamos
Base de estudio
Los métodos para tratar las lesiones óseas no han cambiado mucho desde la antigüedad. Los científicos incluso analizaron 36 esqueletos de neandertales que mostraban signos de fracturas. De estos, solo 11 tratamientos de estas lesiones pueden considerarse infructuosos.
Sin embargo, el éxito del tratamiento en todo momento no se aplica a todos los tipos de fracturas. Algunas lesiones han sido tratadas con éxito y sin consecuencias, incluso con suficientes equipos médicos modernos, conocimientos y técnicas.
Por el momento, los aloinjertos o materiales aloplásticos a menudo se usan en trasplante óseo.
Alotrasplante * : un trasplante de órgano de persona a persona (de un individuo de una especie de un individuo de la misma especie).
Estos métodos son bastante avanzados, pero no omnipotentes. Los defectos craneomaxilofaciales (origen congénito, oncológico o traumático) son bastante complejos. En tales casos, se necesitan implantes específicos para un paciente en particular. Por lo tanto, no se pueden tomar del donante, sino que se deben fabricar. En tales casos, se usa una craneoplastia, pero el implante no tendrá regeneración y no crecerá junto con otros huesos del paciente. También se utilizan huesos óseos, matriz ósea desmineralizada, astillas de hueso sintético o masillas óseas, que llenan el área del defecto. Pero estos materiales no son porosos y tienen una porosidad limitada limitada. Debido a esto, se reduce la migración y la vascularización de las células de la superficie (vascularización) de las células, lo que puede conducir a la
encapsulación * en lugar de la integración del tejido. Como resultado, el riesgo de infección aumenta considerablemente.
Encapsulación * : la formación de una cápsula alrededor de un cuerpo extraño en el cuerpo.
Los investigadores sugieren utilizar la impresión tridimensional, porque este método le permite hacer un implante económico que se adaptará idealmente a un defecto específico en un paciente en particular.
Los investigadores también señalan que, hasta ahora, en la impresión biomédica tridimensional hay una falta de materiales de alto rendimiento que combinen la facilidad de fabricación, el uso en la impresión y la funcionalidad biológica. Y esto significa que necesita crear su propio material, naturalmente.
 Hueso hiperelástico
Hueso hiperelásticoY el nombre de este nuevo material es "hueso hiperelástico" (material óseo hiperelástico). Este material osteoregenerativo se fabrica por extrusión a temperatura ambiente de hidroxiapatita (sólido, 90% de la masa total) y poli (ácido glicólico láctico) (líquido, 10% de la masa total) en formas tridimensionales sin la necesidad de
sinterizar * ,
curar * o Otras formas de estabilización física y química.
La sinterización * es el proceso de fabricación de materiales sólidos y porosos a partir de una base de polvo fino a temperaturas elevadas y / o alta presión.
El curado * es un proceso irreversible de conversión de oligómeros y (o) monómeros reactivos líquidos en polímeros reticulados sólidos, no fundibles e insolubles.
El marco impreso tridimensional resultante tiene buena elasticidad y alta absorción. Además, el marco induce la
diferenciación osteogénica
* de la médula ósea derivada de células madre mesenquimales humanas sin la adición de catalizadores osteoinductores.
Diferenciación celular * : el proceso de formar un fenotipo especializado de una célula que muestra sus funciones. Exagerado, el empleo de células, que anteriormente no tenían la profesión exacta.
Al mismo tiempo, el hueso hiperelástico no causó una respuesta inmune negativa, se vascularizó e integró con los tejidos circundantes, apoyando el crecimiento del nuevo hueso. Otro logro es la capacidad de transferir células madre grasas transducidas a través de un implante impreso.
A continuación, veremos más de cerca los resultados de la prueba práctica. Los científicos realizaron un análisis comparativo de la capacidad osteorregenerativa del hueso hiperelástico y una variante comercial (hueso autólogo) con defectos de tamaño crítico en ratas. Pero primero, un poco sobre la preparación para el experimento y cómo se hicieron el material de prueba y el implante.
Fabricación de hueso hiperelástico.
Como ya sabemos, el marco óseo hiperelástico estaba hecho de hidroxiapatita y poli (ácido glicólico láctico).
 Impresora BioPlotter
Impresora BioPlotterTodas las muestras se imprimieron con la impresora BioPlotter Manufacturing de EnvisionTEC. El grosor de las láminas (5x5 cm), que consta de 5 capas de 120 μm cada una, ascendió a un total de 0.6 mm. A continuación, se sacaron piezas en bruto redondas (8 mm de diámetro) de las hojas usando un estilete de biopsia. Los blancos resultantes se lavaron y esterilizaron.
 Imagen # 1: proceso de fabricación de implantes.
Imagen # 1: proceso de fabricación de implantes.Operación de implantación
Se utilizaron ratas Sprague-Dawley de laboratorio, machos que pesaban aproximadamente 500 gramos cada una, como sujetos experimentales.
Durante la operación, los sujetos estaban bajo anestesia general (2% de isoflurano / 100% de oxígeno). Se realizó una incisión sagital (1,5 cm) entre las suturas lambdoide y coronal para exponer el cráneo. Usando un taladro manual con una trefina (una aguja con un molino o un taladro para formar agujeros en tejidos densos), se creó un defecto artificial del cráneo de 8 mm de diámetro.
Los sujetos se dividieron en 4 grupos:
- 7 individuos - grupo de control negativo (sin implante en el defecto);
- 6 individuos - grupo de control positivo (con hueso autólogo como implante);
- 6 individuos: grupo de estudio nº 1 (con un marco de poli (ácido glicólico de leche) como implante);
- 10 individuos - grupo de estudio No. 2 (con hueso hiperelástico como implante).
Este spoiler contiene una foto del experimento durante la operación (no busque el corazón débil, el proceso se describió anteriormente en forma de texto). Después de la implantación (con o sin ella), el periostio y la piel se cerraron usando una sutura móvil absorbible, y se administraron analgésicos a los sujetos experimentales. Los sujetos se mantuvieron en celdas en dos. El acceso al agua y la comida era ilimitado.
Las muestras de cráneo se analizaron mediante tomografía computarizada con haz cónico. Se extirparon áreas de interés de los huesos del cráneo, se colocaron en etanol al 70% y se escanearon utilizando un tomógrafo de microordenador. Luego, utilizando el software de análisis de imágenes médicas (Mimics Medical 19.0), los científicos examinaron con más detalle las áreas del cráneo donde se implantaron los implantes.
Después de la tomografía microcomputada, las muestras se cortaron por la mitad para el análisis histológico y se visualizaron mediante microscopía electrónica de barrido. También se realizó una evaluación del grado de regeneración después de 8 y 12 semanas.
Y ahora procedemos directamente a los resultados de las observaciones.
Resultados de la investigación
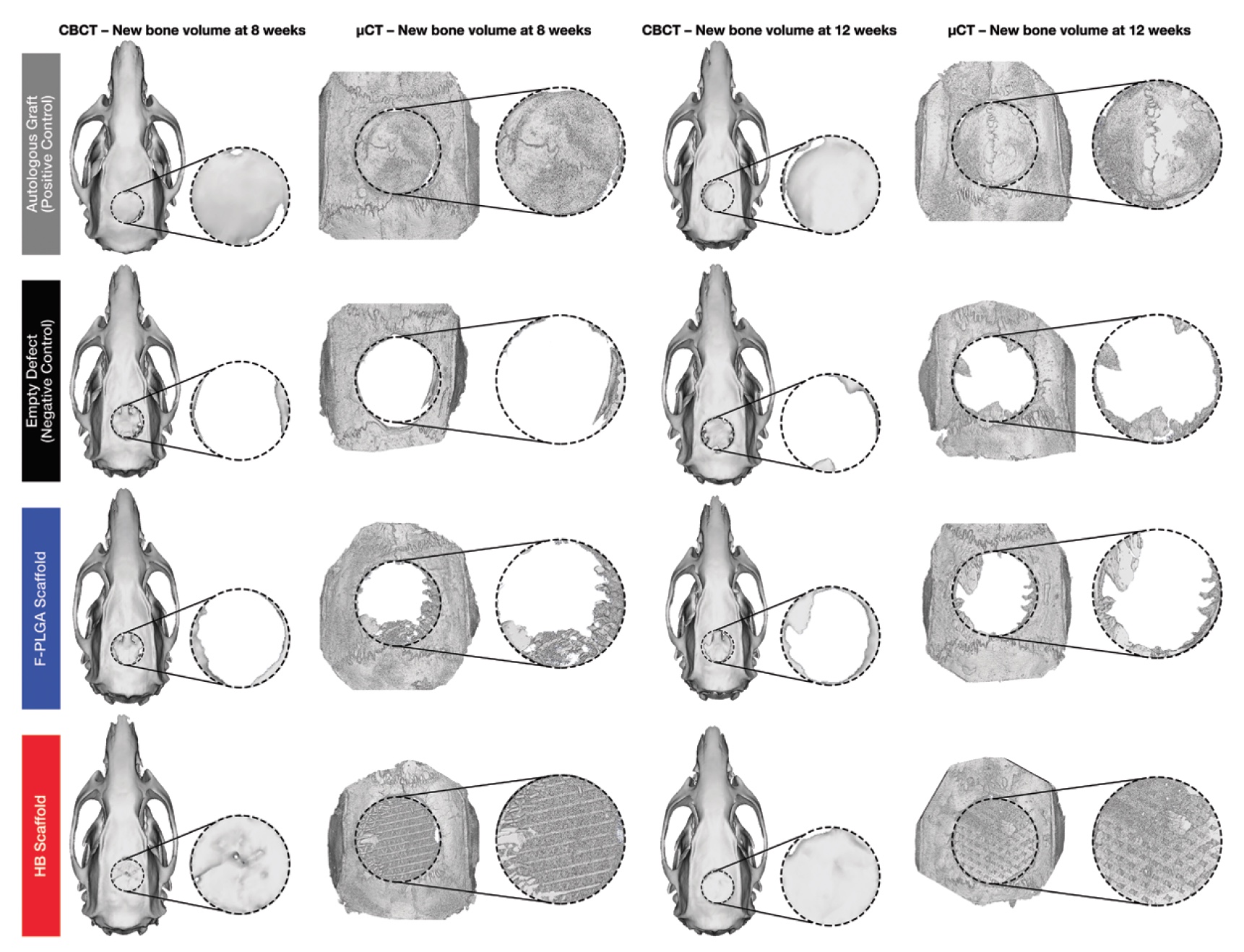 Imagen No. 3a: gris - con un hueso autólogo; negro - sin implante; azul - con un implante hecho de poli (ácido glicólico de leche); rojo - con hueso hiperelástico.
Imagen No. 3a: gris - con un hueso autólogo; negro - sin implante; azul - con un implante hecho de poli (ácido glicólico de leche); rojo - con hueso hiperelástico.La imagen de arriba (
3a ) muestra reconstrucciones tridimensionales de haz cónico y tomografía computarizada. La cantidad de tejido óseo regenerado se determinó por la cantidad de hueso mineralizado como una fracción del volumen total de tejido de interés. El volumen óseo por fracción del volumen total para hueso hiperelástico, poli (ácido láctico-glicólico) y para el grupo de control negativo se normalizó en relación con el volumen óseo por fracción del volumen total para el grupo de control positivo (con hueso autólogo). Por lo tanto, se realizó un análisis comparativo de los indicadores de rendimiento de todas las opciones de implantes.
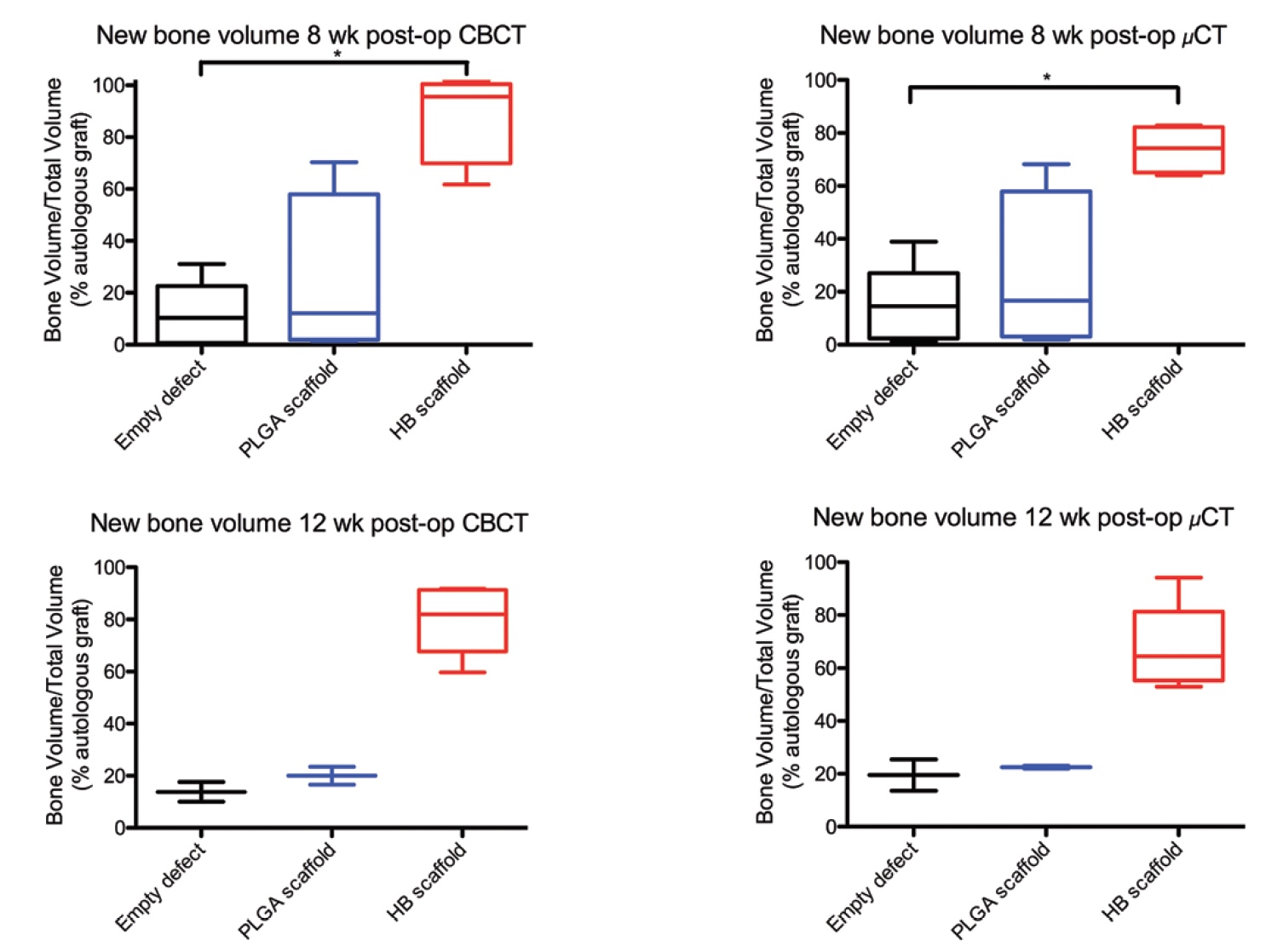 Imagen # 3b
Imagen # 3bEl haz cónico y la tomografía computarizada micro mostraron un aumento en la cantidad de matriz ósea mineralizada en defectos tratados con implantes óseos hiperelásticos (
3b ).
Según la tomografía de haz cónico, el volumen de hueso mineralizado en el caso de utilizar un implante óseo hiperelástico fue del 55,7% a las 8 semanas y del 57,0% a las 12 semanas de observación. Según la tomografía microcomputada, 36.1% en la semana 8 y 37.1% en la semana 12 de observaciones. Estos son datos antes de la normalización.
Después de eso, se llevó a cabo la normalización de los indicadores del volumen de hueso mineralizado en el caso de trasplantes autólogos. Ahora quedó claro que el volumen de regeneración con hueso hiperelástico fue del 95,6% y el 82,0% (8 y 12 semanas de observación) del volumen del grupo de control positivo (con hueso autólogo). Y la tomografía microcomputada arrojó los siguientes resultados: 74.2% y 64.5% (8 y 12 semanas de observaciones).
El uso exclusivo de poli (ácido láctico-glicólico) como material para la implantación resultó bastante ineficaz: 16.6% y 22.5% (8 y 12 semanas de observación) del grupo de control positivo. La ineficiencia de este método también se confirma por el hecho de que sus resultados no difieren significativamente de los resultados del grupo de control negativo, que no tenía implantes: 10.3% y 13.8% en la tomografía de haz cónico y 14.5% y 19.5% en la tomografía micro computada.
La comparación de los resultados del nuevo material probado (hueso hiperelástico) con los resultados del grupo de control negativo mostró una diferencia en el volumen de hueso mineralizado en 7.81 veces a las 8 semanas y 5.75 veces a las 12 semanas a favor del hueso hiperelástico.
Por lo tanto, en términos del volumen de regeneración, el uso de hueso hiperelástico es prácticamente comparable al uso de variantes comerciales de implantes con hueso autólogo.
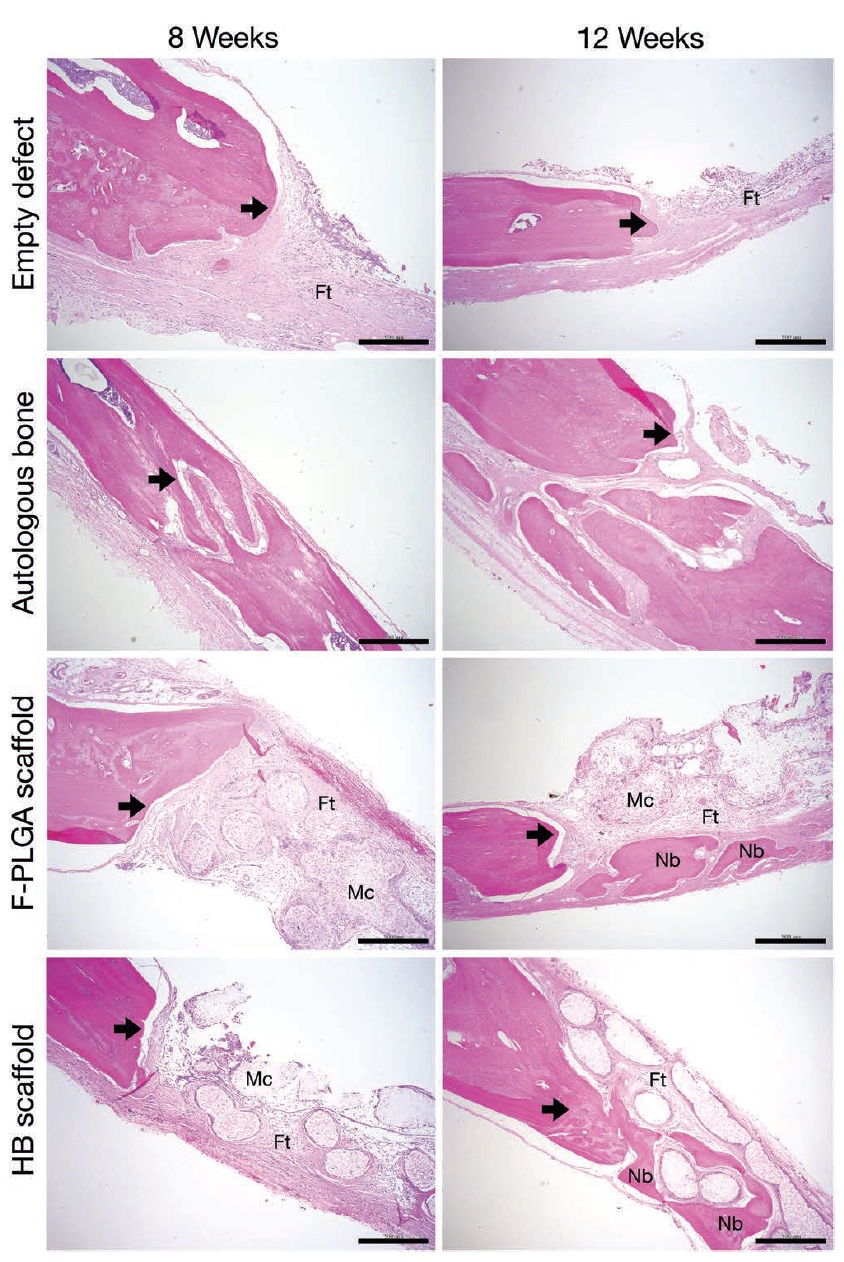 Imagen No. 4: flechas - borde defectuoso; Ft - tejido fibroso (fibroso); Mc es un componente de membrana celular; Nb es el hueso nuevo.
Imagen No. 4: flechas - borde defectuoso; Ft - tejido fibroso (fibroso); Mc es un componente de membrana celular; Nb es el hueso nuevo.El análisis histológico realizado solo confirmó los datos del haz cónico y la tomografía microcomputada. Los científicos identificaron los bordes de los defectos y la formación de un hueso nuevo se tiñó especialmente con eosina para una mejor visualización.
En el caso del grupo de control negativo, se observó tejido fibroso, pero la formación de un nuevo hueso fue mínima (fila superior en la imagen No. 4). Las muestras con poli (ácido glicólico láctico) tampoco podían presumir de un gran volumen de hueso recién formado (tercera fila).
Pero las muestras donde se aplicó hueso hiperelástico, por el contrario, mostraron la formación de tejido óseo mineralizado en la superficie de los bordes de los defectos (cuarta fila). En la octava semana de observaciones, en los lugares de defectos, aparecen tejidos fibrosos y componentes de células de membrana dentro del implante, y en la semana 12, comienza la formación de un nuevo hueso alrededor de los elementos del marco del implante.
 Imagen No. 5
Imagen No. 5Y finalmente, el análisis de imágenes SEM (microscopio electrónico de barrido) de muestras con hueso hiperelástico a las 12 semanas de observación mostró la formación de un contacto celular cercano de los tejidos con el material dentro del implante.
Para un conocimiento más detallado de los matices del estudio, le recomiendo que consulte el
informe de los científicos .
Epílogo
En este trabajo, los científicos han demostrado un nuevo tipo de biomateriales osteogénicos que permiten la creación de implantes para el tratamiento de defectos óseos. Los científicos llaman a las características más importantes de su creación: facilidad de implantación, facilidad de fabricación, alta eficiencia, bajo costo de producción y personalización del implante para un paciente en particular.
El hueso hiperelástico es realmente muy flexible y puede tomar la forma necesaria tanto durante el proceso de fabricación como en el momento de la implantación, lo que facilita enormemente este proceso. Los implantes de cerámica y polímero-cerámica no pueden presumir de esto.
Pero incluso esta no es la ventaja más importante. Un alto grado de regeneración ósea y supervivencia del implante es mucho más importante. 4 semanas después de la implantación, comienza un proceso activo de mineralización ósea.
Los científicos también señalan que dicha velocidad y eficiencia son extremadamente importantes en el caso de defectos suficientemente grandes (como se demostró durante los experimentos prácticos).
El uso de dicha tecnología puede simplificar enormemente la vida de médicos y pacientes. La individualidad del tratamiento, la velocidad de producción, la implantación y una recuperación rápida sin efectos secundarios: este es un excelente anuncio de la nueva tecnología. En el futuro, los científicos tienen la intención de realizar varios experimentos más, estudiar con más detalle el proceso de regeneración y mejorar su invención.
Sin embargo, vale la pena señalar que la presencia de tales innovaciones no significa que pueda romper huesos de izquierda a derecha. Entonces nadie ha cancelado las reglas de seguridad.
Fuera de la red fuera de la parte superior:
Sí, hoy no es viernes y no es el momento para el off-top, pero no pude resistirme. :)
El cadáver de la novia (2005, dirigida por Tim Burton)
Gracias por su atención, sigan curiosos y tengan una buena semana laboral, muchachos. :)
Gracias por quedarte con nosotros. ¿Te gustan nuestros artículos? ¿Quieres ver más materiales interesantes?
Apóyenos haciendo un pedido o recomendándolo a sus amigos, un
descuento del 30% para los usuarios de Habr en un análogo único de servidores de nivel de entrada que inventamos para usted: toda la verdad sobre VPS (KVM) E5-2650 v4 (6 núcleos) 10GB DDR4 240GB SSD 1Gbps de $ 20 o cómo dividir el servidor? (las opciones están disponibles con RAID1 y RAID10, hasta 24 núcleos y hasta 40GB DDR4).
VPS (KVM) E5-2650 v4 (6 núcleos) 10GB DDR4 240GB SSD 1Gbps hasta el verano de forma gratuita al pagar por un período de seis meses, puede ordenar
aquí .
Dell R730xd 2 veces más barato? ¡Solo tenemos
2 x Intel TetraDeca-Core Xeon 2x E5-2697v3 2.6GHz 14C 64GB DDR4 4x960GB SSD 1Gbps 100 TV desde $ 199 en los Países Bajos! Dell R420 - 2x E5-2430 2.2Ghz 6C 128GB DDR3 2x960GB SSD 1Gbps 100TB - ¡desde $ 99! Lea sobre
Cómo construir un edificio de infraestructura. clase utilizando servidores Dell R730xd E5-2650 v4 que cuestan 9,000 euros por un centavo?