
Antes de comenzar a leer, calcule cuántos dispositivos con baterías están a su lado en un radio de varios metros. ¿Seguramente verá un teléfono inteligente, tableta, reloj inteligente, rastreador de ejercicios, computadora portátil, mouse inalámbrico? Todos estos dispositivos están equipados con baterías de iones de litio; su invención puede considerarse uno de los eventos más importantes en el campo de la energía.
Las baterías de iones de litio livianas, espaciosas y compactas contribuyeron al auge de la electrónica portátil, cuya existencia era anteriormente imposible. Solo los dispositivos en los últimos 30 años han dado un salto tecnológico fantástico, y las baterías modernas de iones de litio casi no son diferentes de los primeros modelos de producción de principios de la década de 1990. ¿Quién y cómo inventó las baterías recargables de iones de litio, qué composiciones se utilizan en ellas y existe una conspiración mundial contra las baterías "eternas"? Estamos contando
La leyenda de la primera batería.
Entre el primer intento de producir electricidad químicamente y la creación de baterías de iones de litio, tal vez hayan pasado dos milenios. Hay un presentimiento no confirmado de que el primer elemento galvánico hecho por el hombre en la historia de la humanidad fue la "batería de Bagdad", encontrada en 1936 cerca de Bagdad por el arqueólogo Wilhelm Koenig. El hallazgo, fechado en el siglo II-IV antes de Cristo. e., es un recipiente de arcilla en el que hay un cilindro de cobre y una varilla de hierro, el espacio entre el cual podría llenarse con "electrolito" - ácido o álcali. La reconstrucción moderna del hallazgo ha demostrado que cuando el recipiente se llena con jugo de limón, es posible alcanzar un voltaje de hasta 0.4 voltios.
 La batería de Bagdad es bastante similar a una batería portátil. ¿O una caja de papiro? Fuente: Ironie / Wikimedia
La batería de Bagdad es bastante similar a una batería portátil. ¿O una caja de papiro? Fuente: Ironie / Wikimedia
¿Por qué podría usarse la "batería de Bagdad" si quedan un par de miles de años antes del descubrimiento de la electricidad? Tal vez se utilizó para el depósito preciso de oro en figurillas por el método de galvanización: la corriente y el voltaje de la "batería" son suficientes para esto. Sin embargo, esto es solo una teoría, porque los pueblos antiguos no obtuvieron ninguna evidencia del uso de electricidad y esta misma "batería": el dorado se aplicó por amalgamación en ese momento, y el recipiente inusual en sí mismo podría ser un contenedor protegido para rollos.
La teoría de Little Bang
El proverbio ruso "No habría felicidad, pero la desgracia ayudó" ilustra el curso del trabajo con baterías de iones de litio de la mejor manera posible. Sin un incidente inesperado y desagradable, la creación de nuevas baterías podría retrasarse durante varios años.
En la década de 1970, el británico Stanley Whittingham, que trabajaba en Exxon Energy Company, utilizó un ánodo de sulfuro de titanio y un cátodo de litio para crear una batería de litio recargable. La primera batería de litio recargable mostró indicadores de corriente y voltaje tolerables, solo explotó periódicamente y envenenó a las personas que la rodeaban con gas: el disulfuro de titanio liberaba sulfuro de hidrógeno al entrar en contacto con el aire, que es al menos desagradable para respirar, pero lo más peligroso. Además, el titanio siempre ha sido muy costoso en todo momento, y en la década de 1970 el precio del disulfuro de titanio era de aproximadamente $ 1,000 por kilogramo (el equivalente a $ 5,000 en la actualidad). Sin mencionar el hecho de que el litio metálico se quema en el aire. Entonces Exxon apartó el proyecto de Whittingham del pecado.
En 1978, Koichi Mizushima, que defendió su doctorado en física, estaba investigando en la Universidad de Tokio cuando recibió una invitación de Oxford para unirse al grupo de John Goodenough para buscar nuevos materiales para los ánodos de la batería. Este era un proyecto muy prometedor, ya que el potencial de las fuentes de energía de litio ya era conocido, pero realmente no podían domesticar el caprichoso metal: los recientes experimentos de Whittingham mostraron que el comienzo de la producción en masa de las codiciadas baterías de iones de litio aún estaba muy lejos.
Las baterías experimentales usaban un cátodo de litio y un ánodo de sulfuro. La superioridad de los sulfuros sobre otros materiales en los ánodos les dio a Mizushima y sus colegas una dirección para buscar. Los científicos ordenaron un horno de sulfuro en su laboratorio en el sitio para experimentar con diferentes compuestos más rápido. El trabajo con la estufa no terminó muy bien: un día explotó y provocó un incendio. El incidente obligó a un equipo de investigadores a reconsiderar sus planes: quizás los sulfuros, a pesar de su efectividad, no eran la mejor opción. Los científicos han cambiado su atención hacia los óxidos, que eran mucho más seguros para sintetizar.
Después de muchas pruebas con varios metales, como hierro y manganeso, Mizushima descubrió que el óxido de litio y cobalto muestra los mejores resultados. Simplemente no lo use de la misma manera que el equipo de Gudenaf había supuesto antes, para buscar no material que absorba iones de litio, sino material que proporcione iones de litio más fácilmente. El cobalto también fue mejor que otros porque cumple con todos los requisitos de seguridad y también aumenta el voltaje de la celda a 4 voltios, es decir, el doble en comparación con las opciones de batería anteriores.
El uso de cobalto fue el más importante, pero no el último paso en la creación de baterías de iones de litio. Tras abordar un problema, los científicos se enfrentaron a otro: la densidad de corriente era demasiado baja para que el uso de células de iones de litio fuera económicamente viable. Y el equipo que hizo un gran avance hizo el segundo: al reducir el grosor de los electrodos a 100 micras, fue posible aumentar la intensidad de corriente al nivel de otros tipos de baterías, al mismo tiempo con el doble de voltaje y capacidad.
Primeros pasos comerciales
La historia de la invención de las baterías de iones de litio no termina ahí. A pesar del descubrimiento de Mizushima, el equipo de Gudenaf aún no tenía una muestra lista para la producción en masa. Debido al uso de metal de litio en el cátodo durante la carga de la batería, los iones de litio regresaron al ánodo no en una capa uniforme, sino por dendritas, cadenas en relieve que, al crecer, causaron un corto circuito y fuegos artificiales.
En 1980, el científico marroquí Rachid Yazami descubrió que el grafito hace frente al papel de un cátodo, y es absolutamente incombustible. Los electrolitos orgánicos existentes en ese momento se descompusieron rápidamente en contacto con el grafito, por lo que Yazami los reemplazó con electrolitos sólidos. El cátodo de grafito de Yazami se inspiró en el descubrimiento de la conductividad del polímero por el profesor Hideki Shirakawa, por el cual recibió el Premio Nobel de Química. Y el cátodo de grafito Yazami todavía se usa en la mayoría de las baterías de iones de litio.
¿Lanzamiento en producción? Y de nuevo no! Pasaron otros 11 años, los investigadores mejoraron la seguridad de la batería, aumentaron el voltaje, experimentaron con diferentes materiales catódicos antes de que saliera a la venta la primera batería de iones de litio.
La muestra comercial fue desarrollada por Sony y el gigante químico japonés Asahi Kasei. Se convirtió en la batería de la videocámara amateur de cine Sony CCD-TR1. Soportó 1000 ciclos de carga, y la capacidad residual después de tal desgaste fue cuatro veces mayor que la de un tipo similar de batería de níquel-cadmio.
Piedra de tropiezo de cobalto
Antes del descubrimiento del óxido de litio-cobalto de Koichi Mizushima, el cobalto no era un metal muy buscado. Sus depósitos principales fueron descubiertos en el territorio de África en el estado ahora conocido como la República Democrática del Congo. Congo es el mayor proveedor de cobalto: aquí se extrae el 54% de este metal. Debido a la agitación política en el país en la década de 1970, el precio del cobalto se disparó en un 2000%, pero luego volvió a sus valores anteriores.
La alta demanda crea precios altos. Ni en la década de 1990 ni en la de 2000, el cobalto fue uno de los principales metales del planeta. ¡Pero qué comenzó con la popularización de los teléfonos inteligentes en la década de 2010! En 2000, la demanda de metal fue de aproximadamente 2.700 toneladas por año. Para 2010, cuando los teléfonos inteligentes iPhone y Android marchaban triunfalmente alrededor del planeta, la demanda aumentó a 25,000 toneladas y continuó creciendo año tras año. Ahora el número de pedidos supera el volumen de cobalto vendido en 5 veces. Como referencia: más de la mitad del cobalto extraído en el mundo se destina a la producción de baterías.
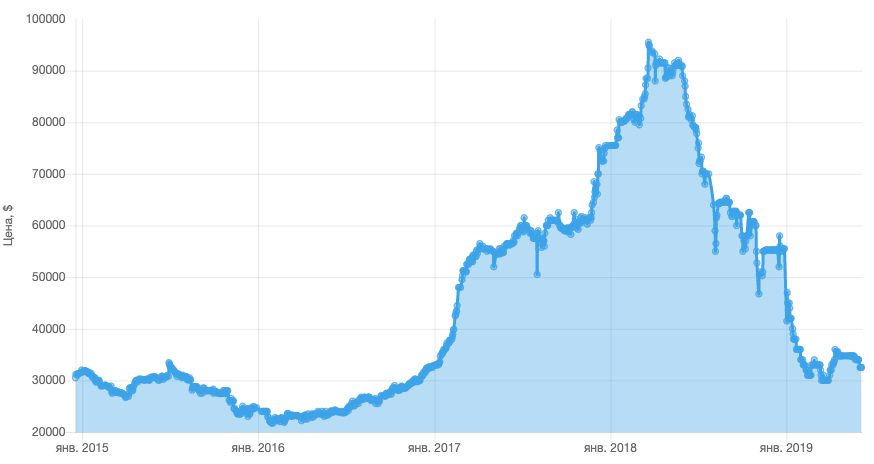 Gráfico de precios de cobalto de los últimos 4 años. Los comentarios son redundantes. Fuente: Elec.ru
Gráfico de precios de cobalto de los últimos 4 años. Los comentarios son redundantes. Fuente: Elec.ru
Si en 2017 el precio por tonelada de cobalto promedió $ 24,000, entonces desde 2017 ha aumentado abruptamente, en 2018 alcanzando un máximo de alrededor de $ 95,500. Aunque los teléfonos inteligentes usan solo 5-10 gramos de cobalto, el aumento de los precios del metal ha afectado el costo de los dispositivos.
Y esta es una de las razones por las cuales los fabricantes de automóviles eléctricos están preocupados por la disminución en la proporción de cobalto en las baterías de los automóviles. Por ejemplo, Tesla redujo la masa de metal escaso de 11 a 4.5 kg por máquina, y en el futuro planea encontrar compuestos efectivos sin cobalto. Para 2019, el precio del cobalto aumentó de manera anormal y cayó a los valores de 2015, pero los desarrolladores de baterías han intensificado los esfuerzos para rechazar o reducir la proporción de cobalto.
En las baterías de iones de litio tradicionales, el cobalto es aproximadamente el 60% de la masa total. La composición de litio-níquel-manganeso utilizada en automóviles comprende de 10% a 30% de cobalto, dependiendo de las características deseadas de la batería. La composición de litio-níquel-aluminio es solo del 9%. Sin embargo, estas mezclas no son un reemplazo completo para el óxido de litio y cobalto.
Problemas de iones de litio
Hasta la fecha, varios tipos de baterías de iones de litio son las mejores baterías para la mayoría de los consumidores. Capaces, potentes, compactos y económicos, todavía tienen serios inconvenientes que limitan el alcance del uso.
Peligro de incendio. Para un funcionamiento normal, una batería de iones de litio necesita un controlador de potencia para evitar sobrecargas y sobrecalentamientos. De lo contrario, la batería se convierte en una cosa muy inflamable, esforzándose por hincharse y explotar en el calor o cuando se carga desde un adaptador de baja calidad. El peligro de explosión es quizás el principal inconveniente de las baterías de iones de litio. Para aumentar la capacidad dentro de las baterías, la disposición se compacta, debido a que incluso un daño leve en la carcasa conduce instantáneamente a un incendio. Todos recuerdan la historia sensacional con el Samsung Galaxy Note 7, en el que, debido a la rigidez dentro de la carcasa, la carcasa de la batería se frotó con el tiempo, el oxígeno penetró en el interior y el teléfono inteligente brilló repentinamente. Desde entonces, algunas aerolíneas han solicitado que las baterías de iones de litio se lleven solo en el equipaje de mano, y en los vuelos de carga, se hace una gran etiqueta de advertencia en el embalaje con baterías.
La despresurización es una explosión. La recarga es una explosión. Debe pagar el potencial energético del litio con precaución.Envejecimiento Las baterías de iones de litio son propensas al envejecimiento, incluso si no se usan. Por lo tanto, comprado como un colector de teléfonos inteligentes desempaquetados hace 10 años, por ejemplo, el primer iPhone tendrá una carga mucho menor debido al envejecimiento de la batería. Por cierto, las recomendaciones para mantener las baterías cargadas hasta la mitad de la capacidad están justificadas: cuando están completamente cargadas durante un almacenamiento prolongado, la batería pierde su capacidad máxima mucho más rápido.
Autodescarga. Acumular energía en baterías de iones de litio y almacenarla durante muchos años es una mala idea. En principio, todas las baterías pierden su carga, pero el ion de litio lo hace especialmente rápido. Si las células NiMH pierden 0.08–0.33% por mes, entonces las células Li-Ion pierden 2-3% por mes. Por lo tanto, en un año, la batería de iones de litio perderá un tercio de la carga, y después de tres años se "sentará" a cero. Para ser justos, digamos que las baterías de níquel-cadmio son aún peores: 10% por mes. Pero esta es una historia completamente diferente.
Sensibilidad a la temperatura. El enfriamiento y el sobrecalentamiento afectan fuertemente los parámetros de dicha batería: los grados de +20 ° C se consideran la temperatura ambiente ideal para las baterías de iones de litio; si se reduce a +5 ° C, la batería le dará al dispositivo un 10% menos de energía. El enfriamiento por debajo de cero toma decenas de por ciento de la capacidad y también afecta la salud de la batería: si intenta cargarla, por ejemplo, desde un banco de energía, aparecerá un "efecto de memoria", y la batería perderá capacidad irrevocablemente debido a la formación de metal de litio en el ánodo. A las temperaturas promedio de Rusia en invierno, la celda de iones de litio no funciona: deje el teléfono en enero en la calle durante media hora para verificar esto.
Para hacer frente a los problemas descritos, los científicos están experimentando con materiales de ánodos y cátodos. Al reemplazar la composición de los electrodos, un gran problema se reemplaza por problemas más pequeños: la seguridad contra incendios conduce a una disminución en el ciclo de vida y una corriente de descarga alta reduce el consumo de energía específico. Por lo tanto, la composición de los electrodos se selecciona según la aplicación de la batería.
¿Quién robó la revolución?
Cada año, en las noticias hay informes de otro avance en la creación de baterías extremadamente potentes y duraderas: parece que los teléfonos inteligentes funcionarán durante un año sin recargarse y se cargarán en diez segundos. ¿Y dónde está la revolución de la batería que los científicos prometen a todos?
A menudo, en tales informes, los periodistas distorsionan los hechos, omitiendo detalles muy importantes. Por ejemplo, una batería con carga instantánea puede tener una capacidad muy baja, adecuada solo para alimentar un despertador de cabecera. O el voltaje no alcanza un voltio, aunque los teléfonos inteligentes necesitan 3,6 V. Y para obtener un boleto a la vida, la batería debe tener un bajo costo y una alta seguridad contra incendios. Desafortunadamente, la gran mayoría de los desarrollos fueron inferiores en al menos un parámetro, debido a que las baterías "revolucionarias" nunca fueron más allá del laboratorio.
 A finales de los años 00, Toshiba experimentó con pilas de combustible de metanol recargables (recarga de combustible con metanol en la foto), pero las baterías de iones de litio eran aún más convenientes. Fuente: Toshiba
A finales de los años 00, Toshiba experimentó con pilas de combustible de metanol recargables (recarga de combustible con metanol en la foto), pero las baterías de iones de litio eran aún más convenientes. Fuente: Toshiba
Y, por supuesto, dejamos de lado la teoría de la conspiración "las baterías interminables no son rentables para los fabricantes". Hoy en día, las baterías en los dispositivos de consumo son insustituibles (o mejor dicho, se pueden cambiar, pero son difíciles). Hace 10-15 años, reemplazar una batería dañada en un teléfono móvil era simple, pero luego las fuentes de energía realmente perdieron mucha capacidad en un año o dos de uso activo. Las baterías modernas de iones de litio duran más que el ciclo de vida promedio del dispositivo. En los teléfonos inteligentes, puede pensar en reemplazar la batería no antes de 500 ciclos de carga cuando pierde del 10 al 15% de su capacidad. Y más bien, el teléfono perderá relevancia antes de que la batería finalmente falle. Es decir, los fabricantes de baterías no ganan en reemplazo, sino en la venta de baterías para nuevos dispositivos. Por lo tanto, la batería "eterna" en un teléfono de diez años no perjudicará a las empresas.
El equipo de Goodenough vuelve a los negocios
Pero, ¿qué pasó con los científicos del grupo John Goodenough, que descubrieron el óxido de litio-cobalto y, por lo tanto, dieron vida a baterías eficientes de iones de litio?
En 2017, Goodenough, de 94 años, anunció que, junto con científicos de la Universidad de Texas, había desarrollado un nuevo tipo de batería de estado sólido que podría almacenar entre 5 y 10 veces más energía que las baterías de iones de litio anteriores. Para esto, los electrodos estaban hechos de litio puro y sodio. Precio prometido y bajo. Pero todavía no hay detalles y pronósticos sobre el comienzo de la producción en masa. Dado el largo camino entre la apertura del grupo Gudenaf y el inicio de la producción en masa de baterías de iones de litio, se pueden esperar muestras reales en 8-10 años.
Koichi Mizushima continúa investigando en Toshiba Research Consulting Corporation. “Mirando hacia atrás, me sorprende que nadie antes que nosotros supusiera utilizar un material tan simple como el óxido de litio y cobalto en el ánodo. Para entonces, se habían probado muchos otros óxidos, por lo que probablemente si no fuera por nosotros, alguien más habría hecho este descubrimiento en unos pocos meses ", dijo.
 Koichi Mizushima recibió un premio de la Royal Chemical Society de Gran Bretaña por participar en la creación de baterías de iones de litio. Fuente: Toshiba
Koichi Mizushima recibió un premio de la Royal Chemical Society de Gran Bretaña por participar en la creación de baterías de iones de litio. Fuente: Toshiba
La historia no tolera los estados de ánimo subjuntivos, especialmente desde que el propio Sr. Mizushima admite que un avance en la creación de baterías de iones de litio era inevitable. Pero aún así es interesante imaginar cómo sería el mundo de la electrónica móvil sin baterías compactas y de gran capacidad: computadoras portátiles con un grosor de unos pocos centímetros, enormes teléfonos inteligentes que deben cargarse dos veces al día, y sin relojes inteligentes, pulseras de ejercicios, cámaras de acción, cuadricópteros y incluso vehículos eléctricos. Todos los días, los científicos de todo el mundo están acercando una nueva revolución energética, lo que nos dará baterías más potentes y más compactas, y con ellos una electrónica increíble, con la que solo podemos soñar.