في منشوري السابق ، تم النظر في سؤالين: أساسيات البيولوجيا الجزيئية وطرق إنشاء التركيبات التي نحتاجها للجينات القائمة على ناقلات البلازميد. تحتاج الآن إلى معرفة كيفية إدخال ناقل البلازميد في الخلية البكتيرية ، أي "التحول". في الوقت نفسه ، سوف نتعلم شيئًا عن بنية الغشاء البكتيري وكيف يمكن التغلب عليه ، وكذلك لماذا تسمى بعض البكتيريا المختصة ، وكيف يرتبط كل ذلك بالسموم البكتيرية والمقاومة البكتيرية للمضادات الحيوية ، والعديد من الحقائق الأخرى المثيرة للاهتمام.
لذا ، لدينا ناقل بلازميدي على أيدينا وهناك سلالة بكتيرية مناسبة لهذا الناقل ، يبقى إدخال المتجه في البكتيريا.
في
مقال سابق ، تم ذكر
عمل فريدريك غريفيث ، والذي يوضح بوضوح حقيقة أن الحمض النووي يمكن أن يخترق الخلايا البكتيرية تلقائيًا. تسمى قدرة الخلية البكتيرية على امتصاص جزيء الحمض النووي البيئي بـ "الكفاءة" (التي تثير الكثير من النكات حول حقيقة أنه حتى خلية واحدة في المختبر كفؤة ، وزميلك في المختبر ليس كذلك). إذا لم يحدث الامتصاص تحت تأثير بعض الظروف المصطنعة ، فنحن نتحدث عن "الكفاءة الطبيعية". كيف يحدث هذا انتقال الحمض النووي داخل البكتيريا؟
1) هيكل غشاء الخلية من البكتيريا
بادئ ذي بدء ، نعتبر بإيجاز بنية غشاء البكتيريا الموجبة والسالبة الجرام.
يتكون غلاف البكتيريا سالبة الجرام من اثنين من ثنائيات الدهون: الغشاء الخارجي والغشاء الداخلي (يسمى الداخلي أيضًا البلازما). بينهما مساحة محيط بالتشنج مليئة بالبروتينات والببتيدوغليكان تؤدي وظائف مهمة.
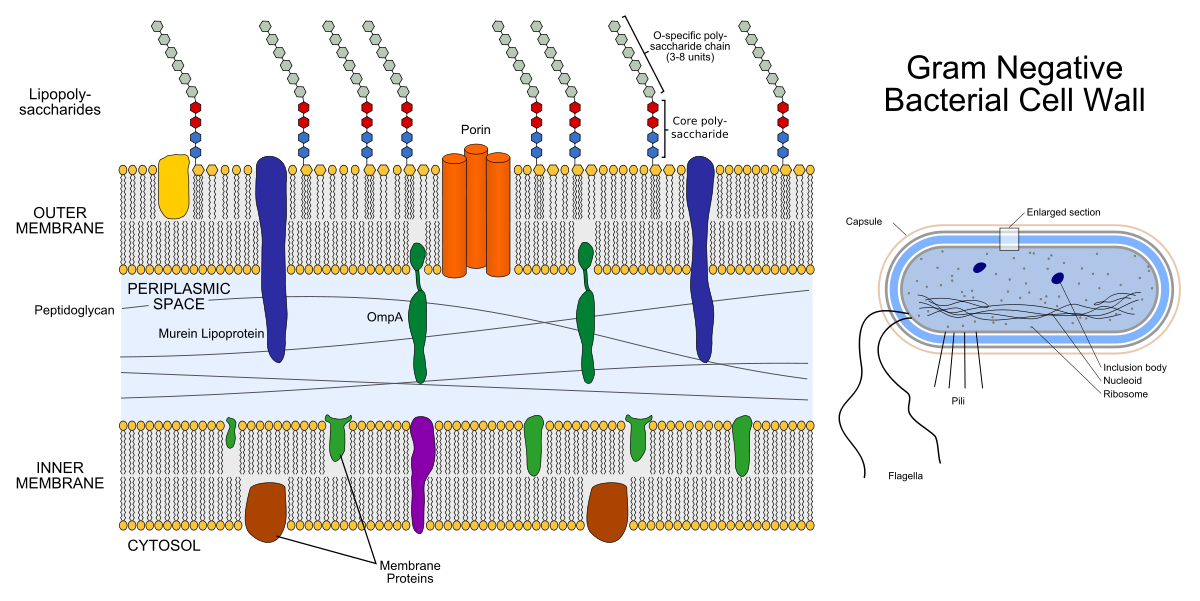 على اليسار هو هيكل غشاء البكتيريا سالبة الجرام. الأدوات الملونة الموجودة داخل الأغشية هي بروتينات غشائية ، والسلاسل البارزة هي عديدات السكاريد الدهنية. على اليمين هي بنية البكتيريا سالبة الجرام نفسها.
على اليسار هو هيكل غشاء البكتيريا سالبة الجرام. الأدوات الملونة الموجودة داخل الأغشية هي بروتينات غشائية ، والسلاسل البارزة هي عديدات السكاريد الدهنية. على اليمين هي بنية البكتيريا سالبة الجرام نفسها.الببتيدوغليكان عبارة عن بوليمر غير متجانس يتكون من N-acetylglucosamine متشابك تساهميًا (NAG) وحمض N-acetylmuramic (NAM). اتضح أن السلسلة ....- NAG-NAM-NAG-NAM-NAG- .... يعني "Hetero" في كلمة "heteropolymer" أن البوليمر لا يتكون من نفس العناصر (مثل البولي إيثيلين) ، ولكن من عنصرين مختلفين. إن إنزيم الببتيدوغليكان المركب ، transpeptidase ، هو هدف للمضادات الحيوية β-lactam (المضادات الحيوية البنسلين والسيفالوسبورينات): فهي تمنع نشاطها ، نتيجة لعملية الانقسام البكتيري ، لا يوجد ما يكفي من الببتيدوغليكان لكلتا الخلايا الابنة. تعتبر طبقة الببتيدوغليكان أيضًا هدفًا لإنزيم الليزوزيم: فهي تدمر الرابطة التساهمية بين NAG و NAM. في الطب ، يتم استخدام الليزوزيم كمطهر ، على سبيل المثال ، فهو مكون نشط لبعض الأدوية لعلاج التهاب الحلق ، وفي صناعة المواد الغذائية يمكن استخدامه كمادة حافظة (المكمل الغذائي E1105 - هذا هو الليزوزيم).
الببتيدوغليكان. يوضح الشكل الجزء المقابل لـ NAG واحد (إنه على اليسار) و NAM واحد (إنه على اليمين) ، وهما مترابطان عبر ذرة أكسجين. (بالنسبة لأولئك الذين لا يحبون مثل هذه الحريات في الكيمياء: يسمى هذا "الترابط من خلال ذرة الأكسجين" β- (1،4) - جليكوسيد).يتكون غلاف البكتيريا الموجبة للجرام فقط من غشاء داخلي (بلازما) ومساحة محيطية رقيقة للغاية وطبقة ببتيدوغليكان خارجية أكثر سمكًا من تلك الخاصة بالبكتيريا سالبة الجرام.
مثل هذه العوائق التي تقف في طريق أي مركب في السيتوبلازم الجرثومي لا يمكن التغلب عليها لكل شيء باستثناء الماء ، وكذلك الجزيئات الصغيرة غير القطبية والمائية (الأكسجين الجزيئي والنيتروجين وثاني أكسيد الكربون وغيرها). ويطلق على اختراق هذه المركبات من خلال القشرة "النقل السلبي" ("الانتشار البسيط") ، ويحدث دائمًا على طول تدرج التركيز. الجزيئات غير القطبية قادرة على المرور بحرية عبر الأغشية لأن الحجم الداخلي للأغشية هو أيضًا غير قطبي (داخل الغشاء أنها تتكون من بقايا مسعور من الأحماض الدهنية) ، وتذوب المركبات غير القطبية جيدًا في المذيبات غير القطبية (الكحول والأسيتون والأحماض الدهنية).
صورة هزلية تظهر فيها رهاب الماء (رهاب الماء) من بقايا الأحماض الدهنية داخل غشاء من طبقتين.في المقابل ، لا يمكن للجزيئات القطبية الكبيرة (الأحماض الأمينية ، السكريات الأحادية ، النوكليوتيدات) والجسيمات المشحونة (الأيونات) والجزيئات الكبيرة (DNA والبروتينات) أن تخترق غشاء الخلية بهذه الطريقة ، لأنها قابلة للذوبان بشكل جيد فقط في المذيبات القطبية (على سبيل المثال ، في الماء) . ثم كيف تدخل جزيئات الدنا داخل الخلية البكتيرية؟
2) آليات نقل المركبات إلى الخلايا من البيئة
بادئ ذي بدء ، لدينا حقيقة واضحة هي أن البكتيريا لا يمكن أن تعيش فقط على الماء والأكسجين وثاني أكسيد الكربون ، لأنها تحتاج إلى العديد من المركبات الأخرى مدى الحياة. لذلك هناك طرق لإدخال هذه المركبات في الخلية. مثل هذه الأساليب هي "الانتشار الميسر" و "النقل النشط".
2.1) انتشار الضوء
مثال على الانتشار الميسر (على الرغم من أن هذه الحالة الخاصة ، على العكس من ذلك ، ضارة للبكتيريا) هو نقل أيونات البوتاسيوم عبر غشاء الخلية البكتيرية بالاشتراك مع فالينوميسين ، مضاد حيوي يتم تصنيعه بواسطة بعض الفطريات. فالينوميسين الحر لا يمكن أن يخترق الخلية ، لأن المجموعات القطبية معرضة خارجيًا. أيون البوتاسيوم هو أيضا "طريق مغلق".
 تمثال يصور البنية الثلاثية الأبعاد لمركب فالينوميسين وأيون البوتاسيوم (يصور أيون على شكل كرة في المركز). تم تثبيته أمام مدخل معهد M.M.Shemyakin و Yu A. A. Ovchinnikov للكيمياء العضوية الحيوية ، الأكاديمية الروسية للعلوم (موسكو) ، حيث تم إنشاء آلية النشاط المضاد للبكتيريا من فالينوميسين والهيكل ثلاثي الأبعاد لمجمعه مع أيون البوتاسيوم.
تمثال يصور البنية الثلاثية الأبعاد لمركب فالينوميسين وأيون البوتاسيوم (يصور أيون على شكل كرة في المركز). تم تثبيته أمام مدخل معهد M.M.Shemyakin و Yu A. A. Ovchinnikov للكيمياء العضوية الحيوية ، الأكاديمية الروسية للعلوم (موسكو) ، حيث تم إنشاء آلية النشاط المضاد للبكتيريا من فالينوميسين والهيكل ثلاثي الأبعاد لمجمعه مع أيون البوتاسيوم.ولكن بعد تكوين مركب فالينوميسين مع أيون البوتاسيوم ، فإنه يغير هيكله ثلاثي الأبعاد بحيث يصبح سطحه الخارجي بأكمله مسعورًا (غير قطبي) ، ويتم إخفاء جميع المجموعات المحبة للماء في الداخل. في هذه الحالة ، يتم إخفاء أيون البوتاسيوم داخل جزيء فالينوميسين ، وبالتالي ، يمكن أن يخترق مركب أيون فالينوميسين + البوتاسيوم من خلال الغشاء. يمكن أن يتحلل المجمع إلى فالينوميسين وأيون حر في أي وقت داخل الخلية وخارجها ، ولكن الانتشار السهل للأيونات يؤدي بشكل عام إلى معادلة تركيزها في المساحات داخل الخلايا وخارجها ، وتتحكم الخلية في نقل الأيونات لسبب ما: تركيزها العالي قاتلة. وعلى هذا يعتمد التأثير المضاد للبكتيريا للالينوميسين.
التمثيل التخطيطي للمضادات الحيوية الفطرية فالينوميسين مركب مع أيون البوتاسيوم.مثال آخر هو المسام غير المنضبط ، وهي بروتينات غشائية كبيرة تسمح لمواد معينة بالمرور بحرية عبر الغشاء وفقًا للتدرج. مثال على مسام الغشاء هو
المكورات العنقودية الذهبية Staphylococcus aureus α-toxin (اسم آخر للسم هو α-hemolysin. يتكون من أجزاء "hemo" و "lysine". "Hemo" تعني خلايا الدم الحمراء ؛ يعني "lysine" من كلمة "تحلل" ، أي "موت الخلية")
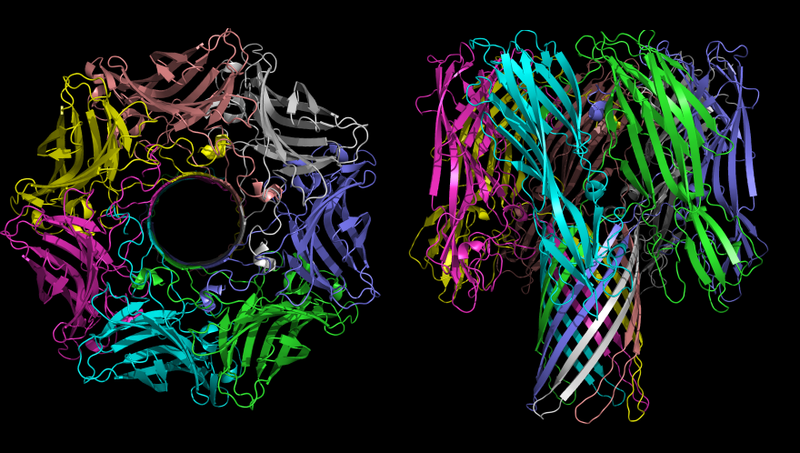 التركيبة ثلاثية الأبعاد لأوليغومير ألفا هيموليسين - سم البكتريا Staphylococcus aureus. في الصورة على اليسار ، الوقت واضح.
التركيبة ثلاثية الأبعاد لأوليغومير ألفا هيموليسين - سم البكتريا Staphylococcus aureus. في الصورة على اليسار ، الوقت واضح.تتمثل الوظيفة الرئيسية لهيموليسين ألفا في العملية المسببة للأمراض في إنشاء قنوات غير خاضعة للرقابة في غشاء الخلية ، والتي يمكن أن تمر ، حسب الظروف البيئية ، أيونات أحادية التكافؤ أو أيونات الكالسيوم أو ATP. كما ذكرنا أعلاه ، فإن عدم التوازن الأيوني سمي للغاية ، ونقل ATP
من الخلية ضار ، لأن ATP هو رابط لا غنى عنه في جميع العمليات الكيميائية تقريبًا لأي خلية.
2.2) النقل النشط
كما يتبين من الأمثلة أعلاه ، فإن الانتشار الميسر لا يتطلب طاقة. على العكس من ذلك ، فإن النقل النشط هو امتصاص أو إطلاق شيء ما بواسطة خلية مع إنفاق الطاقة لكل فعل نقل. يمكن أن يكون هذا نقل جزيئات أو أيونات قطبية كبيرة ، ويمكن أن يتم نقل الأيونات على طول تدرج التركيز وضدها. بالطبع ، النقل النشط هو عملية يتم التحكم فيها حيث يتم تضمين مجموعة كاملة من البروتينات داخل الخلايا والغشاء. وبالتالي ، تحتاج الخلية أولاً إلى إنفاق الموارد على تجميع جميع هذه البروتينات ، ثم تنفق الطاقة مرة أخرى على استخدام نظام النقل هذا.
مثال على النقل النشط هو نظام النقل المعتمد على الطاقة لمركبات مسعور ومضخة من خلية إلى البيئة (تدفق).
نظام النقل الفعال لمضاد حيوي من خلية بكتيرية إلى الخارج ، ويتكون من ثلاثة بروتينات تشكل معقدًا واحدًا عبر الغشاء. يعكس الشكل حقيقة أن بروتين ناقل التدفق (البنفسجي) يمكن أن "يمسك" جزيئات الدواء مباشرة في السيتوبلازم وفي الغشاء.هذا النظام له أهمية خاصة لأنه يسبب المقاومة المتعددة لبعض البكتيريا للمضادات الحيوية: تتخلص الخلية منها قبل أن تتمكن من إلحاق الضرر بها بشكل خطير. علاوة على ذلك ، فإن أكثر من نصف حالات المقاومة المتعددة للأدوية من
Pseudomonas aeruginosa Pseduomonas aeruginosa ترتبط بالنقل الفعال للمضادات الحيوية. والأهم من ذلك ، تم اكتشاف أنظمة تدفق نشطة للمضادات الحيوية "الجديدة" بالفعل تستخدم ضد البكتيريا المقاومة للأدوية المضادة للبكتيريا شائعة الاستخدام. على سبيل المثال ، يتم
إرجاع الدواء
Linezolid المستخدم في حالة عدم فعالية المضادات الحيوية الكلاسيكية من خلال نظام التدفق القائم على بروتينات AcrAB و TolC. حقيقة أخرى مثيرة للاهتمام هي أن البكتيريا الذكية لا تهدر الطاقة على توليف واسع النطاق من بروتينات نظام التدفق في تلك الحالات عندما لا تكون هناك حاجة إليها. ولكن بمجرد ظهور المواد الضارة بالخلية ، يتم تنشيط التوليف بسرعة وتبدأ البكتيريا في المقاومة بنشاط. بالمناسبة ، ليس التدفق هو الآلية الوحيدة لحماية البكتيريا من المضادات الحيوية ، سأكتب مقالًا عن طرق أخرى أيضًا.
هيكل linezolid هو مضاد حيوي يستخدم ضد السلالات المقاومة للبكتيريا إيجابية الجرام.3) كفاءة الخلايا البكتيرية
لذا ، قمنا بفحص آليات النقل عبر الغشاء للمركبات التي لا يمكنها اختراق هذا الحاجز دون مساعدة خارجية. في الظروف الطبيعية ، لا يتم نقل الحمض النووي إلى البكتيريا إلا من خلال النقل النشط بسبب تعاون مجموعة كاملة من البروتينات داخل الخلايا وغشاء عبر. تسمى القدرة غير المستغلة للخلية لامتصاص الحمض النووي من الخارج "الكفاءة الطبيعية".
3.1) الكفاءة الطبيعية للخلايا البكتيرية
إن الفرضية الأكثر إثباتًا لظهور الكفاءة الطبيعية للبكتيريا هي الافتراض بأن هذه الآلية تسمح للبكتيريا بالبقاء في الظروف القاسية بالنسبة لها (تسمى الظروف القاسية للخلية "الإجهاد"). والحقيقة هي أن الإجهاد غالبًا ما يؤدي إلى تلف الحمض النووي "الكروموسومي" للبكتيريا ، وإذا أرادت الخلية البقاء على قيد الحياة ، فإنها تحتاج إلى "إصلاح" بطريقة ما "كروموسوم" (يسمى هذا "الإصلاح" "الإصلاح"). علاوة على ذلك ، من المعروف أنه إذا تم إدخال تسلسل الحمض النووي في الخلية يشبه جزءًا من الحمض النووي للخلية ، فمن المحتمل جدًا أن يدمج هذه القطعة "الجديدة" في جينومها. ماذا يحدث في ظل الظروف العصيبة؟ تموت بعض الخلايا ، ليصبحوا متبرعين بالحمض النووي لأخوتهم الذين لا يزالون يقاتلون من أجل الحياة. في الواقع ، في نفس الثقافة البكتيرية ، من المحتمل جدًا أن تكون جينومات الممثلين متشابهة جدًا ، لذلك يمكن للبكتيريا الباقية استخدام الحمض النووي للأقارب الميتين لإصلاح الجينوم الخاص بهم.
علاوة على ذلك ، في ظل ظروف مريحة في ثقافة الخلية ، فإن جزءًا منها فقط يتمتع بالكفاءة الطبيعية ، ونسبة الخلايا المختصة من العدد الإجمالي هي الأكبر ، ثم تكون الثقافة في مرحلة نمو معينة - مرحلة
السجل .
 مؤامرة نموذجية من البكتيريا في الثقافة مع مرور الوقت. مرحلة السجل هي مرحلة النمو ، تليها الهضبة ومرحلة الانقراض ، حيث تفتقر الخلايا بالفعل إلى العناصر الغذائية وتتراكم السموم.
مؤامرة نموذجية من البكتيريا في الثقافة مع مرور الوقت. مرحلة السجل هي مرحلة النمو ، تليها الهضبة ومرحلة الانقراض ، حيث تفتقر الخلايا بالفعل إلى العناصر الغذائية وتتراكم السموم.بالطبع ، يرغب الباحث في جعل عملية نقل ناقلات البلازميد إلى الخلية بأكبر قدر ممكن من الفعالية: كلما كانت عملية التحول أكثر كفاءة ، كانت هناك حاجة إلى ناقل بلازميد أقل لضمان نتائج جيدة. لذلك ، في الظروف المختبرية ، لا يعتمدون عادةً على الخلية نفسها ، بل يقومون بدلاً من ذلك بإنشاء خلايا ذات كفاءة اصطناعية.
3.2) الكفاءة الاصطناعية للخلايا البكتيرية
هناك طريقتان رئيسيتان لخلق الكفاءة البكتيرية الاصطناعية: معالجة ثقافة الخلية بالأيونات ثنائية التكافؤ يليها التسخين قصير المدى وما يسمى بالتنقيب الكهربائي.
3.2.1) معالجة ثقافة الخلية بالأيونات ثنائية التكافؤ ، يليها التسخين قصير المدى.
كقاعدة عامة ، يوجد في المختبر ثلاجة تبلغ درجة حرارتها حوالي -80 درجة مئوية (أحيانًا يطلق عليها "kelvinators" تكريمًا لإحدى شركات التصنيع) ، مسدودة بأنابيب اختبار مع خلايا في مرحلة
اللوغاريتم . يتم ذلك حتى لا تضيع الوقت في إنشائها في كل مرة تكون هناك حاجة إليها (ويستغرق الأمر الكثير من الوقت ، لن يعمل بشكل أسرع من اليوم). وحتى أثناء التخزين لا تموت الخلايا بسبب التجمد ، تضاف المواد الواقية من البرودة إلى الوسط: الجلسرين أو البروبيلين جليكول أو ثنائي ميثيل سلفوكسيد.
ثلاجة المختبر في رأي مؤلف الصورة.عندما يحتاج الباحث إلى تحويل سلالة معينة ، يزيل الخلايا من كلفيناتور ويضع الأنبوب في الثلج. ثم ، تتم إضافة الكاتيونات ثنائية التكافؤ وناقلات البلازميد التي نحتاجها إلى الخلايا في مرحلة
السجل للنمو. يجب ألا يترك أنبوب الاختبار الجليد. كل مانح نموذجي لمثل هذه الكاتيونات هو كلوريد الكالسيوم (CaCl2) ، في هذه الحالة ، الكاتيون الثنائي التكافؤ هو Ca2 +. لا يوجد تفسير لا لبس فيه لكيفية مساعدة Ca2 + للحمض النووي لاختراق البكتيريا:
- تدعي بعض المصادر أن تركيزات Ca2 + العالية تسبب فجوات في غشاء الخلية وتلف الحمض النووي ، وفي وقت سابق وجدنا أن تلف الحمض النووي هو إشارة للخلية لتصبح كفؤة.
- وفقًا لمصادر أخرى ، تعمل هذه الأيونات "كجسر" يربط ناقل البلازميد بالخلية. والحقيقة هي أن الأيونات المشحونة إيجابيا ترتبط في وقت واحد بمجموعات السكاريد المشحونة سلبًا على الغشاء الخارجي للبكتيريا ومجموعات سالبة الحمض النووي البلازميد. إذا لم يكن هناك أيونات في الوسط ، فسيتم طرد الحمض النووي من الخلية ، وهذا غير مفيد تمامًا للباحث.
من الممكن أن تكون كلتا الفرضيتين صحيحتين.
الآلية المفترضة لمشاركة أيونات Ca2 + في التحول. أولاً ، ترتبط الأيونات بمجموعات سالبة الحمض النووي (الدوائر الصفراء) وعديد السكاريد الراسية في الغشاء (الدوائر الصفراء). ثم ، بسبب أيون ، يتم تشكيل نوع من الجسر: "عديد السكاريد (-)" - "أيون الكالسيوم (2+)" - "DNA (-)" ، الذي يثبت الحمض النووي على سطح الخلية.بعد الحضانة البكتيرية عند درجة حرارة قريبة من الصفر ، يتم إنتاج ما يسمى بالصدمة الحرارية - تسخين قصير المدى للثقافة إلى 42 درجة. عادة ، تكون مدة المعالجة الحرارية 30-45 ثانية ، وبعد ذلك يعود أنبوب الاختبار مع البكتيريا إلى الحمام الجليدي (مع صدمة حرارية أطول قد تموت الخلايا). الأسباب المحتملة لفعالية الصدمة الحرارية هي نفس الآليات: يمكن أن تتسبب درجة الحرارة المرتفعة في تلف الحمض النووي والبروتينات (وهذا يؤدي إلى الكفاءة) ، ويمكن أيضًا أن تخلق "ثقوب" في غشاء الخلية يتم من خلالها اختراق ناقلات البلازميد المرتبطة بالغشاء من خلال أيونات الكالسيوم.
ثم يتم طلاء الخلايا على أطباق بتري مع وسط انتقائي وتنمو عليها مستعمرات.
3.2.2) Electroporation
أساس طريقة
Electroporation هو حقيقة أن المجال الكهربائي يمكن أن يدمر غشاء الخلية. بمعنى حرفي ، فإن Electroporation هو إنشاء المسام عن طريق المجال الكهربائي.
أولاً ، يتم وضع البكتيريا وناقلات البلازميد في أنبوب خاص (كوفيت). ثم يتم وضع الكفيت في جهاز خاص ، والذي يخلق فرقًا محتملاً لجزء من الثانية قدره 0.1-10 كيلو فولت ، والذي يؤدي بدوره إلى تلف عكسي للأغشية والنواقل يمكن أن يخترق الخلايا بحرية. بعد مرور بعض الوقت ، يتم زرع الثقافة البكتيرية على أطباق بتري مع وسط انتقائي.
من المتطلبات المهمة للوسط السائل الذي توجد فيه الخلايا والمتجه في وقت Electroporation هو تركيز منخفض من الأيونات: وإلا ، قد تحدث دائرة كهربائية قصيرة.
خاتمة
كل مستعمرة على صفيحة هي سلالة
تكاثرية واحدة من بكتيريا واحدة (أي إذا رأينا 100 مستعمرة على صفيحة ، فهذا يعني أنه كان هناك في البداية 100 بكتيريا قابلة للحياة ، ثم بدأت في الانقسام).
بعد ظهور المستعمرات على الأطباق ، يختار الباحث إحدى المستعمرات وينقل الخلايا من المستعمرة إلى وسيط مغذي انتقائي جديد. بعد "نمو" ثقافة الخلية الجديدة يتم زراعتها مرة أخرى على فنجان جديد بنفس الوسط المغذي الانتقائي. ونتيجة لذلك ، نحصل على فنجان ينمو عليه فقط أحفاد البكتيريا من مستعمرة واحدة (أي أنها في الواقع كلها مستنسخات من بكتيريا واحدة). وسيتم استخدام هذه الخلايا فقط في المستقبل للحصول على البروتين الذي نحتاجه بكميات كبيرة من الوسط المغذي الانتقائي السائل.حسنًا ، دعنا نلخص النتائج المتوسطة:- قمنا بتجميع الجين الذي نحتاجه ؛
- أدخله في ناقلات البلازميد المناسبة ؛
- تم اختيار وتحويل سلالة منتج مناسبة.
- حصلت على ثقافة استنساخ.
- وأخيرًا ، قمنا بنقل جزء من هذه الحيوانات المستنسخة إلى كمية كبيرة من المواد المغذية للحصول على البروتين الذي نحتاجه بكميات كبيرة.
الخطوة التالية: عزل البروتين من الكتلة الحيوية الناتجة في شكل نقي قدر الإمكان. لكن هذه قصة مختلفة تمامًا.