تعد طرق إيصال الأدوية المستهدفة إلى ذروتها - حيث يتيح لك التأثير البؤري على بؤرة الآفة محاربة المرض ، دون التأثير على الأنسجة السليمة تقريبًا. ومع ذلك ، تبقى الأسئلة: كيف تزيد من فعالية هذا العلاج ، وتسريع تأثير الدواء ، وتقليل تراكمه في الجسم؟ يعمل العلماء في مختبر المواد النانوية البيولوجية التابع لـ NUST MISiS في هذا الاتجاه منذ عدة سنوات ، ومن بين أحدث الاكتشافات التي قام بها الفريق كانت هناك زيادة بنسبة 30 ٪ في كفاءة إيصال الدواء إلى ورم خبيث باستخدام العدلات - خلايا الجهاز المناعي. يتم نشر النتائج في المجلة العلمية الدولية
ACS Nano .

أجرى العلماء دراسة داخليا (على الأنسجة الحية) لآلية إيصال الدواء المستهدف للأورام الخبيثة التي تستخدم الجسيمات الشحمية. اتضح أن الخلايا المناعية العدلات تزيد من كفاءة تسليم الدواء إلى الورم بنسبة 30 ٪.
تخترق الجسيمات الشحمية - الحويصلات الدهنية المصطنعة - الورم بسبب ما يطلق عليه تأثير النفاذية والاحتفاظ المحسن. داخل الجسيمات الشحمية ، يتم "خياطة" الدواء ، وعندما يدخل في الأنسجة الخبيثة ، يتم إطلاقه.
يحدث تأثير EPR بسبب النمو المفرط للأوعية الدموية الناجم عن الحاجة غير الطبيعية للورم للأكسجين والتغذية ، ومع النمو المرضي ، تظهر المسام الضخمة في جدران الأوعية الدموية التي يصل قطرها إلى 200 نانومتر. أيضا ، فإن نمو الورم يسبب ضغط الأوعية اللمفاوية ويمنع التدفق الطبيعي للسائل بين الخلايا. وهكذا ، تخترق الجسيمات الشحمية الورم ولا يمكنها الخروج بسبب ضعف التصريف اللمفاوي.
من المعتقد أنه بسبب تأثير EPR ، يمكن أن تخترق الجسيمات الشحمية فقط في الورم ، ولكن ليس في الأنسجة السليمة. ولكن هل هذا حقا هكذا؟ وماذا يحدث في السفينة؟
خلال الدراسة ، لاحظ العلماء تسليم الدواء إلى أنسجة الفئران السليمة وأنواع مختلفة من الأورام الخبيثة: سرطان الثدي وسرطان البروستاتا وسرطان الجلد. تم تنفيذ الملاحظات باستخدام مجهر intravital ، والذي يسمح لك بدراسة العمليات مباشرة في كائن حي.
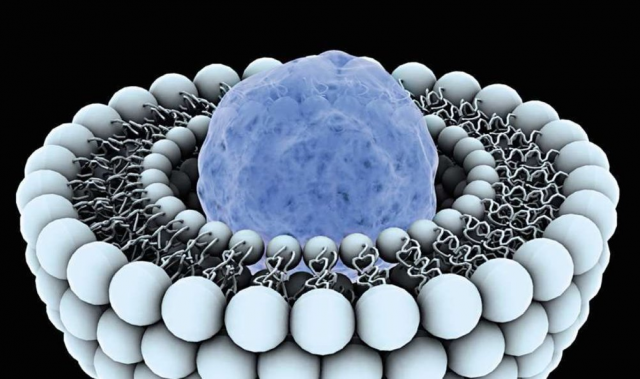 الجسيمات الشحمية "تتشبث" بالخلية السرطانية
الجسيمات الشحمية "تتشبث" بالخلية السرطانيةالاستنتاج الأول الذي تلقيناه نتيجة الدراسة هو أن هناك نوعين من تغلغل الجسيمات الشحمية من الأوعية الدموية إلى الأنسجة يحدثان في الأنسجة الحية. microleak هو تراكم صغير معزول من الجسيمات الشحمية حول السفينة. هذه العملية غير مجدية لعلاج الأورام ، لأنها لا تسمح للدواء بالوصول إلى خلايا الورم. علاوة على ذلك ، تم العثور على تسريبات صغيرة في الأنسجة السليمة ، وهو ما يفسر سمية الأدوية المستندة إلى الجسيمات الشحمية المستخدمة في عيادة حديثة "، كما يقول فيكتور ناومينكو ، مؤلف العمل ، الباحث في مختبر المواد الطبية الحيوية النانوية في NISU MISiS .
والنتيجة الثانية الأكثر إثارة للاهتمام هي العدلات ، وهي نوع من خلايا الدم البيضاء ، وخلية المناعة في الجسم التي تتسرب إلى نسيج الورم. عندما تغادر العدلة الوعاء ، عبره ، من خلال "الباب الخلفي" في جدار الأوعية الدموية ، فإن الجسيمات الشحمية تنجح في اختراق الورم. وفقًا للنتائج التي حصل عليها الفريق العلمي ، تزيد العدلات من كفاءة تغلغل الجسيمات الشحمية في الورم بمقدار الثلث.
يعطي هذا الاكتشاف نمطًا واضحًا: تؤدي العدلات إلى زيادة نفاذية الأوعية الدموية للورم من أجل الولادة المستهدفة لعقاقير ليبوسومال ، وبالتالي تزيد من فرصة الشفاء. علاوة على ذلك ، يحدث هذا فقط في حالة وجود macroleak ، وهو "سحابة" منتشرة كبيرة من الجسيمات الشحمية التي تخترق عمق الورم ، وبالتالي ضمان إيصال الدواء المستهدف.
"إن التمييز بين نوعي التسرب مهم لفهم آلية كيفية عمل الأدوية التي أساسها الجسيمات الشحمية. تشير نتائجنا إلى أن التسريبات الدقيقة لا تسهم فقط في إيصال الأدوية إلى الخلايا السرطانية ، ولكنها أيضًا مسؤولة عن تراكمها غير المرغوب فيه في الأنسجة السليمة. وأكد فيكتور ناومينكو أن التأثير العلاجي يتحقق نتيجة للإنكماش الكلي ، ويمكن أن تساعد العدلات في تقويته.
يواصل الفريق حاليًا إجراء دراسات مخبرية للحد من الآثار الجانبية غير المرغوب فيها للعلاج بالليبوزوم. يعد تطوير آليات التحفيز الصناعي لإنتاج العدلات في جسم المريض لتعزيز علاج الأورام أحد المجالات الواعدة لتطبيق البيانات التي تم الحصول عليها.