Forscher neigen dazu, entzündlichen Prozessen im Gehirn bei degenerativen Erkrankungen immer mehr Aufmerksamkeit zu schenken, sowohl in der Rolle der Grundursache als auch in der Rolle des sekundären Faktors, der durch Schädigung des Nervengewebes verursacht wird. Neuroinflammation kann sich als zentraler Prozess bei der Alterung des Körpers herausstellen.
Es ist sehr schwierig, eine Neuroinflammation im Zusammenhang mit neurodegenerativen Erkrankungen zu bestimmen, obwohl dies beispielsweise bei Multipler Sklerose (einer Autoimmunerkrankung, die nichts mit Haushaltssklerose zu tun hat) nicht schwierig ist. Im letzteren Fall dringen überschüssige Lymphozyten und Monozyten über die Barriere hinaus ein, die das Nervengewebe vom Blutkreislauf trennt, was zu Funktionsstörungen führt.
Mit Pathologien wie der Alzheimer-Krankheit, die Sie wahrscheinlich aus dem Zustand des Schriftstellers Terry Pratchett vor seinem Tod kennen, der Parkinson-Krankheit, an der der Maler Salvador Dali in seinen letzten Jahren litt, der amyotrophen Lateralsklerose, die im Zusammenhang mit dem Zustand des Physikers Stephen bekannt wurde Hawking, die Beschreibung erfolgt nach der Reaktion, ausgedrückt in einer Veränderung der Form und Struktur der Gliazellen - Astrozyten und Mikroglia. Viele dieser Krankheiten manifestieren sich in einem höheren Alter, sie sind mit dem Altern verbunden und möglicherweise dadurch verursacht. Das Verständnis der Neuroinflammation, ihrer Ursachen und Folgen kann möglicherweise die Behandlung vieler Krankheiten verbessern, von denen einige nur symptomatisch behandelt werden.
Um das Phänomen der Neuroinflammation zu verstehen, müssen Sie zunächst verstehen, was Entzündung ist. Die vorgeschlagene Frage ist mehr als 2000 Jahre alt, aber die Definition von Entzündung, die Wissenschaftler und Ärzte auf der ganzen Welt zu einem Konsens führen würde, wurde noch nicht vorgeschlagen.
Was ist eine Entzündung?
"Rubor et Tumor, cum calore et dolore." Rötung, Schwellung mit Fieber und Schmerzen - so beschreibt der antike römische Arzt Cornelius Celsus Entzündungen. Dieser Definition fehlen wichtige Details, die von seinem Kollegen, dem Chirurgen Galen, etwa 100 Jahre nach seinem Vorgänger - functio laesa oder Funktionsstörung - geklärt werden.
Zusammen vermitteln diese fünf beschriebenen Zeichen kurz die Essenz der Manifestationen der Entzündung und erreichen in nahezu unveränderter Form unsere Tage. Medizinstudenten sind immer noch das erste, woran sie sich bei der Beantwortung der Prüfung an den lateinischen Zungenbrecher erinnern.
Eine solche Definition passt jedoch kategorisch nicht zu uns, da sie nichts über die Mechanismen der Entwicklung der Pathologie und ihrer Ätiologie aussagt. Mit der Offenlegung der Details des letzteren mussten Physiologen basteln. Die Geschichte erinnert sich an viele Theorien, die sich hauptsächlich mit der Rolle von Blutgefäßen bei der Entwicklung von Entzündungen befassten. Ein umfassenderes Verständnis zeigte sich jedoch, nachdem Ilya Mechnikov auf die Zellen aufmerksam gemacht und seine Definition abgeleitet hatte:
„Eine Entzündung in ihrer Gesamtheit sollte als eine phagozytische Reaktion des Körpers gegen störende Figuren betrachtet werden. Diese Reaktion wird entweder durch Bewegen von Phagozyten allein oder durch die Wirkung von Gefäßphagozyten oder des Nervensystems durchgeführt. “
Phagozyten, Zellen, die schädliche Fremdpartikel aufnehmen und zerstören können, standen im Mittelpunkt von Mechnikovs Arbeit. Dementsprechend war der Hauptgrund für die Kritik an seiner Definition die mangelnde Anerkennung der Rolle von in Körperflüssigkeiten gelösten Proteinen, die bekanntlich einen signifikanten Einfluss auf den Prozess haben. Wir sind beeindruckt von dieser Definition aufgrund der Erwähnung des Nervensystems, lassen Sie Mechnikov und fügen Sie es nur hinzu, um die Nervenregulation der Gefäßwand zu erkennen, die auch den Verlauf der Entzündung moduliert.
Mit einer Definition für Neuroinflammation sind die Dinge wirklich schlecht. Wenn Sie Wikipedia öffnen, können Sie feststellen, dass "Neuroinflammation eine Entzündung des Nervengewebes ist". Hier ist ein solcher Zirkulus in definiendo, ein logischer Fehler, bei dem die Aussage von sich selbst abgeleitet wird.
LinkEine interessante Definition findet sich in der redaktionellen Spalte ACS Chemical Neuroscience, in der Neuroinflammation als nicht autonome Zellprozesse definiert wird, die während einer neurodegenerativen Erkrankung Zelltod, Dysfunktion oder Wiederherstellung von Neuronen und Oligodendrozyten verursachen.
"Nicht zellautonome Prozesse, die den Zelltod, die Dysfunktion oder die Wiederherstellung des ZNS für Neuronen und Oligodendrozyten im Verlauf einer neurodegenerativen Erkrankung bestimmen."
LinkDies ist eine sehr gute Definition, die die guten und schlechten Seiten der Neuroinflammation beschreibt, sie beschränkt diesen Prozess jedoch auf den Umfang einer neurodegenerativen Erkrankung. Was passiert also, bevor eine Person Alzheimer oder Parkinson nicht bemerkt hat und keine Entzündung im Gehirn hat?
Hierfür bleibt die Frage der Definition offen. Berücksichtigen Sie die Fakten und die Interpretation der Forschung in diesem Bereich.
Warum ist eine Entzündung notwendig?
Wenn es keine Regeneration gäbe, wäre das Leben unmöglich.
Wenn sich alles regenerieren würde, wäre der Tod unmöglich.
"Wenn es keine Regeneration gäbe, könnte es kein Leben geben.
Wenn sich alles regenerieren würde, gäbe es keinen Tod. “
- Richard Goss
Was ist das Wesen der Entzündung? Freund oder Feind? - Freund oder Feind? - wie internationale wissenschaftliche Publikationen und populärwissenschaftliche Portale in ihrem Wunsch schreiben, dem Leser die Komplexität der laufenden Prozesse des beschriebenen Phänomens zu vermitteln.
Das Hauptziel eines solchen Prozesses wie einer Entzündung besteht darin, den Körper über Schäden oder Brüche zu informieren. Und der Körper muss bereits "eine Entscheidung treffen und entsprechend handeln". Meistens wird diese Entscheidung von einer Genossenschaft lokaler und systemischer Immunzellen getroffen, die zuerst den schädlichen Faktor entfernen und dann gemeinsam die Homöostase des betroffenen Gewebes wiederherstellen, soweit dies gelingt.
Ereignisse nehmen eine solche Wendung, zum Beispiel mit traumatischen Schäden am Nervengewebe. In den ersten Augenblicken nach einer unglücklichen Situation oder der geplanten Laboraktion bei Wirbeltieren kommt es zu einem massiven Tod der vom Trauma betroffenen Zellen.
Die erste Welle des Zelltods aufgrund von Nekrose und Apoptose (ein programmierter Zellsuizid, bei dem lebensunverträgliche Verletzungen auftraten) lässt nach einigen Stunden nach. Danach folgt eine längere zweite Welle, die wahrscheinlich durch die Wirkung von Zerfallsprodukten auf das umliegende Gewebe verursacht wird. In diesem Fall kann die Wechselwirkung von Nervengewebe und Gefäß gestört werden, wodurch Unterbrechungen bei der Versorgung mit Energie, Ionen und notwendigen Substanzen auftreten.
Die Aktivierung der Mikroglia als Reaktion auf eine Beschädigung erfolgt sofort. Mikrogliazellen, diese winzigen Makrophagen, führen direkt die von Mechnikov beschriebene „phagozytische Reaktion des Körpers gegen störende Figuren“ durch.
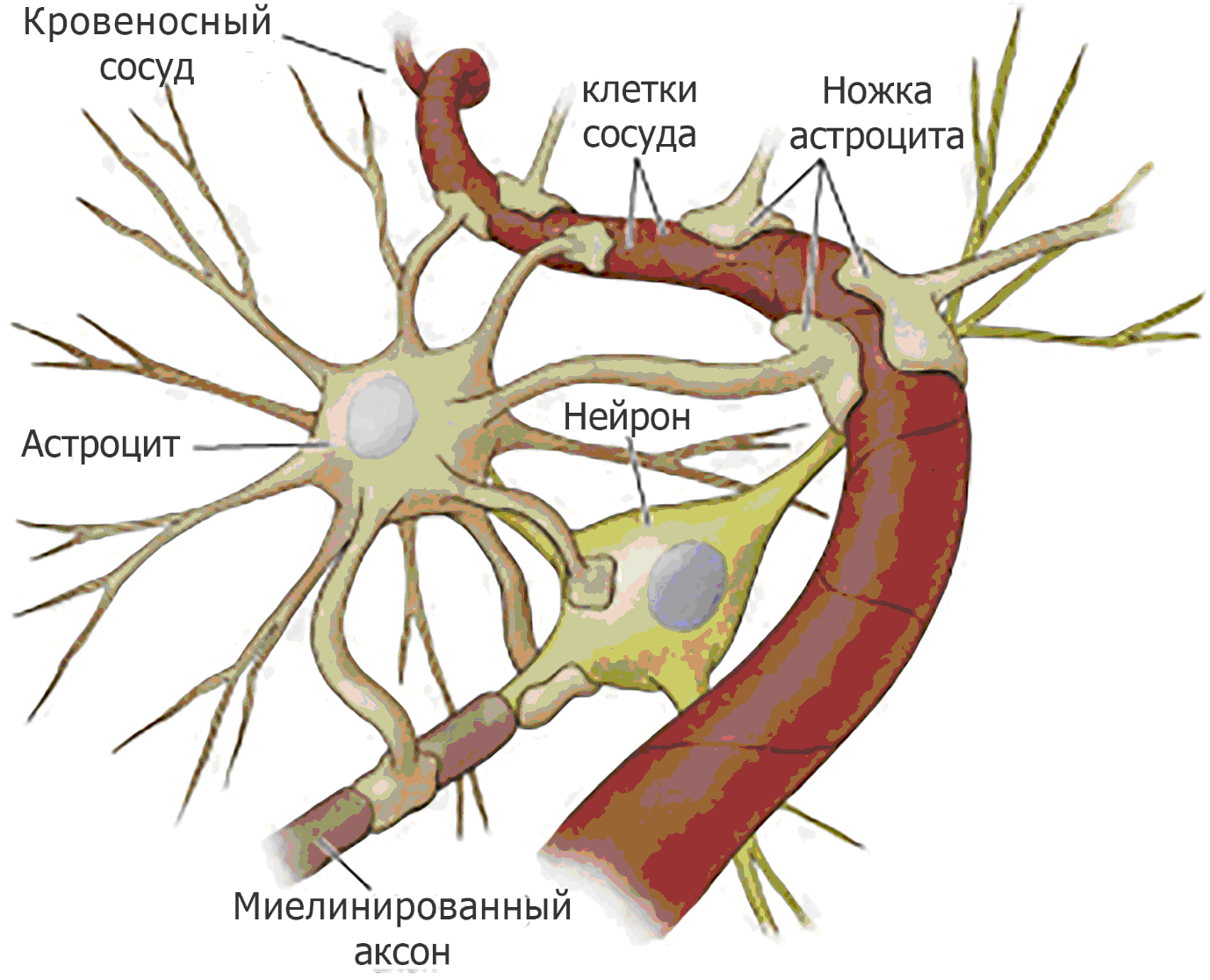 Schematische Darstellung eines Astrozyten und eines Neurons in der Nähe eines Blutgefäßes
Schematische Darstellung eines Astrozyten und eines Neurons in der Nähe eines BlutgefäßesSie untersuchen ständig die Umgebung auf Substanzen, die auf eine Schädigung von Neuronen hinweisen oder deren Integrität gefährden können. In Abwesenheit solcher Gefahrensignale wird die Aktivität von Makrophagen im Nervengewebe durch von Neuronen sezernierte Peptide unterdrückt, die sie nicht bedrohen. Andernfalls wird bei einer Verletzung die Mikroglia in wenigen Minuten aktiviert! Dies spiegelt sich in ihrer Form und Funktion wider. Zellen werden mobiler, können sich teilen, zeigen zahlreiche Rezeptoren auf der Außenmembran an, um die Situation genauer einschätzen zu können. Wenn sie aktiviert sind, stoßen sie Komplementproteine und Chemokine in den Interzellularraum aus, die mehr Immunzellen anziehen, Zytokine, die Nachbarn dazu bringen, auf die Situation zu reagieren, proteolytische Enzyme, die extrazelluläre Matrixproteine abbauen, den Handlungsspielraum vergrößern, sowie aktive Formen Sauerstoff und Stickstoff, um ein Gefahrensignal zu verbreiten.
LinkAstrozyten sind nicht weit hinter ihren glialen Gegenstücken. Sie werden von der größten Klasse in der Anzahl der Zellen im Zentralnervensystem repräsentiert und nehmen eine strategische Position zwischen den Endothelzellen von Blutgefäßen und Neuronen ein und regulieren die Arbeit der Barriere zwischen Blut und Gehirn. Nach einer Verletzung reagieren sie entweder auf Gefahrensignale, die von Neuronen kommen, oder auf Substanzen, die von aktivierten Mikroglia freigesetzt werden. Dann nehmen die Astrozyten an Größe zu, hypertrophieren und setzen neuroregulatorische Peptide frei, beispielsweise BDNF (vom Gehirn abgeleiteter neurotropher Faktor) oder neurotropher Faktor des Gehirns, was zum Überleben beschädigter Neuronen beiträgt. Sie produzieren und sezernieren auch fibrilläre Proteine, die die extrazelluläre Matrix wiederherstellen und eine Glia-Narbe bilden. Dies ist einerseits eine gute Sache, da die Schadensstelle isoliert ist, andererseits wird in diesem Bereich die Regeneration von Neuronen schwierig sein.
 Migration weißer Blutkörperchen zum Ort der Verletzung
Migration weißer Blutkörperchen zum Ort der VerletzungMikroglia und Astrozyten spielen bei traumatischen Verletzungen die Hauptrolle. Dieses Szenario hat jedoch eine umfangreiche Crowd-Szene. In der kürzesten Zeit nach der Schädigung rollen Leukozyten buchstäblich an den Wirkort (dies ist ihre normale Form der Bewegung entlang des Endothels mit Entzündung). Von dem gesamten Leukozytenwirt kommen als erste Neutrophile an, die beginnen, proinflammatorische Zytokine, reaktive Sauerstoffspezies und Peptide, die Zellen zur Apoptose induzieren, aktiv abzuscheiden. Ihr Aufenthalt am Ort der Verletzung ist vorübergehend, nach 48 Stunden werden sie nicht mehr beobachtet, dennoch ist ihr Auftreten eines der wichtigsten frühen Ereignisse.
Dahinter werden Mikroglia aktiviert, T- und B-Lymphozyten rekrutiert, die auf durch Schäden verursachte Proteinveränderungen reagieren. In den frühen Stadien werden manchmal auch rote Blutkörperchen und Blutplättchen beschädigt. Sie sind auch sehr aktiv an der Regulation der Neuroinflammation beteiligt, obwohl dies nur geschieht, wenn die Gefäßwand beschädigt ist. Diese Zellen produzieren einen Thrombozytenaktivierungsfaktor, der an der Regulation der Mikroglia-Aktivierung beteiligt ist, und zusätzlich zu dem, was unerwartet klingen mag, sind sie eine zusätzliche Quelle für Serotonin (es wird nicht nur im Nervensystem, sondern auch weit darüber hinaus produziert). Serotonin hilft in diesem Fall, den Blutfluss aus Blutgefäßen, das Überleben von Neuronen und die Erhaltung ihrer Plastizität zu stoppen.
www.sciencedirect.com/science/article/pii/S0889159118305786?via%3DihubNervenzellen werden nicht wiederhergestellt?
Wie Santiago Ramon-i-Cahal, der Begründer der modernen Neurobiologie, zu Beginn des 20. Jahrhunderts postulierte, werden Nervenzellen im Körper eines Erwachsenen nicht wiederhergestellt. Sie müssen diese Aussage mehr als einmal in Form des Satzes "Verlorene Nerven werden nicht wiederhergestellt" gehört haben. In den 60er Jahren des letzten Jahrhunderts kündigte Joseph Altman jedoch die Entdeckung der Teilung von Neuronen im Hippocampi reifer Meerschweinchen an.
LinkDieser Beweis für die Neurogenese bei Erwachsenen wurde erst in den 90er Jahren des letzten Jahrhunderts ernst genommen. Akkumulierte Daten zur Neurogenese verschiedener Arten, einschließlich Primaten, führten zu einem Paradigmenwechsel.
LinkDie Forscher bestätigten, dass die Neurogenese tatsächlich im Gehirn verschiedener erwachsener Tiere stattfindet, und fanden schließlich Spuren neu gebildeter Neuronen im Gehirn eines Erwachsenen. Es wird geschätzt, dass täglich Hunderte solcher Zellen im Hippocampus produziert werden, wo sie das Gedächtnis und neue Fähigkeiten formen. Dieses Konzept wird von Wissenschaftlern weitgehend akzeptiert, und Sie können sogar Diäten und spezielle Übungen finden, die es angeblich stärken. Vorhersehbar kann sogar TED über dieses Phänomen sprechen.
Das ist nur das Problem: Eine solche Erneuerung von Neuronen kann es tatsächlich nicht sein. Studien, die die Existenz der adulten Neurogenese widerlegen, erscheinen bis heute. Die letzte derart große Studie wurde am 15. März dieses Jahres in der Zeitschrift Nature veröffentlicht. Darin schließen Wissenschaftler des California Institute in San Francisco, dass sie nicht in der Lage waren, zumindest einige Spuren in mehreren Dutzend Hippocampi zu entdecken, die aus dem Gehirn von Erwachsenen stammen, die ihren Körper der Wissenschaft hinterlassen haben. Den Forschern zufolge fanden sie auch bei den am besten erhaltenen Exemplaren keine Anzeichen.
LinkWie üblich ist es sehr schwierig zu beweisen, dass tatsächlich etwas fehlt, und viele Wissenschaftler stehen den Ergebnissen der Arbeit skeptisch gegenüber. Viele weisen darauf hin, dass die Zählung indirekt durchgeführt wurde - durch das Vorhandensein von Proteinen, die normalerweise von jungen, kürzlich geteilten Zellen produziert werden. Diese Proteine könnten sich bald nach dem Tod des Körpers leicht abbauen.
Es ist sehr wahrscheinlich, dass die Debatte weiter fortgesetzt wird, und das letzte Wort in dieser Angelegenheit wird nur dann geliefert, wenn Methoden zur Beobachtung von Neuronen im Gehirn lebender Menschen entwickelt werden.
Im Gehirn eines Zebrafischs können sich Neuronen der lateralen Ventrikelwand teilen und sich dann in den betroffenen Bereich bewegen, wodurch junge Neuronen gebildet werden, die die Toten ersetzen. Die entsprechenden Zellen der Mäuse, die näher bei uns liegen, sind nicht mehr zu einem solchen Fokus fähig, obwohl die Fähigkeit wiederhergestellt wird, wenn sie in vitro platziert werden. Es wird angenommen, dass es die Mikroumgebung am Ort der Verletzung bei solch hoch entwickelten Tieren ist, die die Entwicklung neuer Neuronen behindert.
LinkIm Falle einer Gewebeschädigung wird die Mikroumgebung aufgrund der Abbauprodukte von Proteinen und anderen Makromolekülen, aus denen sie besteht, sowie aufgrund von Substanzen, die von umgebenden Zellen sekretiert werden, gebildet. Die spezifischen Wirkungen von Gliazellen und ihre Rolle bei der Wiederherstellung hängen stark von der Art der Verletzung ab. Bei übermäßiger und ständiger Aktivierung der Mikroglia werden die von ihr in hohen Konzentrationen sezernierten Substanzen für die umgebenden Zellen toxisch, die produzierten Zytokine stören die Arbeit der Neuronen; Von Astrozyten sezernierte fibrilläre Proteine hemmen die Bildung funktioneller Bindungen.
Eine hohe Menge an Interleukin 1, einem der Hauptmediatoren der Entzündung, insbesondere seiner Beta-Form, kann zusammen mit dem Tumornekrosefaktor, den Interleukinen 6 und 10, die bei Schädigung im Zentralnervensystem produziert werden, zu Kopfschmerzen und Migräne führen.
Es sei daran erinnert, dass diese proinflammatorischen Zytokine für die Wiederherstellung des betroffenen Gewebes notwendig sind, obwohl sie wiederum Zelltod und sekundären Gewebeschaden verursachen können. Beispielsweise ist der Tumornekrosefaktor Alpha in den Anfangsstadien der Entzündung für Neuronen toxisch, fördert jedoch die Regeneration in späteren Stadien.
Neuroinflammation bei Alzheimer
Wie aus der obigen Definition offensichtlich hervorgeht, ist die Neuroinflammation ein häufiger Begleiter neurodegenerativer Erkrankungen. Solche Krankheiten sind durch den Verlust von Struktur, Funktion und Anzahl von Neuronen gekennzeichnet.
Die Krankheit, die zuerst vom deutschen Psychiater Alois Alzheimer beschrieben wurde, betrifft normalerweise Menschen über 65 Jahre, obwohl manchmal andere Formen gefunden werden. Mit der Entwicklung der Krankheit verlieren Patienten die Fähigkeit, sich an Informationen zu erinnern, und im Extremfall verlieren sie ihr Langzeitgedächtnis, die Fähigkeit zu sprechen, zu navigieren und für sich selbst zu sorgen. Die Ursache für viele kognitive Beeinträchtigungen in dieser Pathologie ist die Degeneration von Neuronen und Synapsen, die zu einer Atrophie der Großhirnrinde führt.
Mikroglia als einer der Hauptbeteiligten an Neuroinflammation wird aktiv, wenn es einem der vielen Reize ausgesetzt wird, nämlich Hypoxie, Trauma, Schlaganfall, zusammen mit Faktoren wie Viren, Bakterien und Toxinen. Zellen werden auch aktiviert, wenn Amyloid-Plaques und Cluster von Tau-Proteinen auftreten. Diese beiden Faktoren - neurofibrilläre Verwicklungen von Tau-Protein und Neuroinflammation - sind Schlüsselzeichen der Alzheimer-Krankheit.
LinkAktivierte Mikroglia werden im Gehirn des Patienten im Überschuss beobachtet, wenn sie von einem Post-Mortem-Pathologen untersucht werden. Offensichtlich verlieren Makrophagen des Gehirns in Gegenwart entzündungsfördernder Zytokine die Fähigkeit, extrazelluläre Ansammlungen von Amyloid Beta, einer Gruppe von Peptiden, die eine charakteristische Plaque bilden, zu phagozytieren. Darüber hinaus verhindert eine erhöhte Konzentration von Zytokinen wie Interleukin 1 beta die Bildung von Synapsen, was deren Verlust im pathologischen Prozess erklärt.
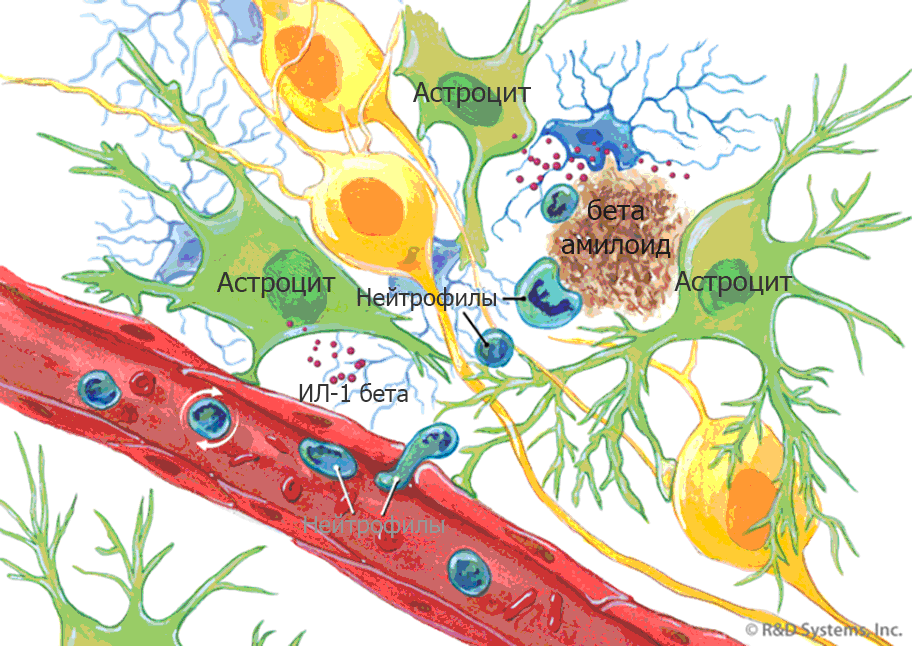 Neuroinflammation bei Alzheimer
Neuroinflammation bei AlzheimerAngesichts der enormen Schädigung des Gehirns durch chronische Entzündungen wurde vermutet, dass Substanzen, die Entzündungen unterdrücken, die Krankheit behandeln oder zumindest die Wahrscheinlichkeit ihrer Entwicklung verringern können. Es gibt Hinweise darauf, dass nichtsteroidale Antiphlogistika (NSAIDs) wie Ibuprofen Entzündungen durch Amyloid-Plaques reduzieren können. Klinische Studien wurden jedoch aufgrund des hohen Risikos von Nebenwirkungen nicht abgeschlossen. NSAIDs werden derzeit nicht als nützlich bei der Behandlung der Alzheimer-Krankheit angesehen, und keine der klinischen Studien zum Nachweis der Fähigkeit von NSAIDs, das Risiko der Entwicklung der Krankheit zu verhindern oder zu verringern, wurde abgeschlossen.
Jüngste Studien haben allgemein Zweifel an den Vorteilen einer täglichen Einnahme niedriger Dosen von Aspirin und möglicherweise anderen NSAIDs aufkommen lassen. Eine Studie, die in einer der einflussreichsten Fachzeitschriften in Lancet veröffentlicht wurde, in der Ärzte und Wissenschaftler mehr als 12.000 Patienten mit einem moderaten Risiko für die Entwicklung einer Herzerkrankung überwachten, bestätigte keinen Nutzen bei der Einnahme dieses Arzneimittels.
LinkParkinson-Krankheit Neuroinflammation
Aber was die verbleibenden neurodegenerativen Erkrankungen betrifft? Bei der Parkinson-Krankheit, die durch den Massentod von Neuronen der Dopamin sekretierenden Basalganglien gekennzeichnet ist, ist die Neuroinflammation fast der Hauptbestandteil der Krankheit.
Menschen mit Parkinson-Krankheit verlieren die Kontrolle über ihre Bewegungen, ihre Hände beginnen zu zittern, ihre Handschrift verschlechtert sich. Die Patienten beginnen langsamer zu gehen, sie haben Probleme beim Gehen. All dies sind frühe Manifestationen der Krankheit. Mit der Zeit verschlechtern sich abstraktes Denken und Aufmerksamkeitskontrolle und es treten Halluzinationen auf. Fast 50% der diagnostizierten haben letztere.Frühe Post-Mortem-Hirnstudien zeigen das gesamte Repertoire entzündungsfördernder Zytokine, einschließlich der Interleukine 1, 2, 6, Interferon Gamma, Tumornekrosefaktor Alpha und anderer. Der gleiche Satz wird in der Cerebrospinalflüssigkeit von Patienten beobachtet. Es werden auch hohe Konzentrationen von Stickoxid und Superoxid nachgewiesen, die direkt und indirekt den Tod von Neuronen verursachen können.LinkTrotz großer Erfolge bei der Untersuchung der vorgestellten Pathologie fällt es den Forschern schwer, mit Sicherheit zu sagen, ob eine Neuroinflammation die Ursache oder die Folge der Krankheit ist. Eines ist sicher: Sobald eine Entzündung im Spiel ist, wird sie zu einem Schlüsselspieler. Dies wird durch epidemiologische Studien bestätigt. Im Gegensatz zur Alzheimer-Krankheit können NSAIDs mit Ausnahme von Aspirin laut einer 2010 durchgeführten Metaanalyse das Risiko für die Entwicklung der Parkinson-Krankheit verringern.LinkEin charakteristisches Merkmal vieler neurodegenerativer Erkrankungen ist, dass das Risiko ihrer Entwicklung mit dem Alter zunimmt. Daraus lässt sich ableiten, dass Neuroinflammation und Altern auch irgendwie miteinander verbunden sind.Neuroinflammation beim Altern
Gehirnzellen leben und sterben, dies ist ein normaler Lebenszyklus. Neuronen werden allmählich durch Astrozyten ersetzt, und die Zytokine werden während ihrer Entzündung und Genesung zur Kontrolle des Todes ausgestoßen. Somit ist zu jedem ausgewählten Zeitpunkt ein bestimmter Gehalt an proinflammatorischen Zytokinen im Gehirn vorhanden. Mit zunehmendem Alter werden die Entzündungsmarker bei Glia jedoch größer und tragen zusätzlich zu einer übermäßigen Immunantwort während der Stimulation bei. Mikroglia werden hyperaktiv.Mit dem Altern gibt es auch Störungen der kognitiven Funktionen - Gedächtnis, Sprache, abstraktes Denken - wenn auch in geringerem Maße als bei neurodegenerativen Erkrankungen. Im Allgemeinen kann das Altern als Hauptrisiko einer leichten kognitiven Beeinträchtigung angesehen werden.Ältere Menschen zeigen häufig Anzeichen einer kognitiven Beeinträchtigung während oder nach einer Infektion oder Stress. Diese Beobachtungen werden in Laborexperimenten an Mäusen bestätigt, deren kognitive Beeinträchtigung durch die Verabreichung von Lipopolysaccharid (einem Bestandteil der Bakterienwand, auf die sich die Immunantwort entwickelt) verursacht werden kann, das jedoch mit Resveratrol, einem starken entzündungshemmenden Mittel, abgeschwächt werden kann.LinkHippocampus altern
Jede Beschreibung des Alterns des ZNS beginnt immer mit dem Hippocampus, dem Bereich des Gehirns, der für die Bildung von Erinnerungen verantwortlich ist. Es ist sowohl beim normalen Altern als auch bei der Alzheimer-Krankheit betroffen. Neben dem Gedächtnis fasziniert der Hippocampus die Forscher mit den Auswirkungen von Stress. Da der Hippocampus ein wichtiges Rückkopplungselement ist, das für die Einstellung der Produktion von Glukokortikoiden verantwortlich ist, wird die Auswirkung von chronischem Stress auf seine Alterung genau untersucht.In frühen Studien zum Altern des Hippocampus wurde gezeigt, dass bei älteren Menschen die Anzahl der Neuronen signifikant abnimmt. In späteren Studien mit präzisen Techniken fanden Physiologen jedoch minimale Unterschiede zwischen der Anzahl der Neuronen im Hippocampi von jungen und alten Menschen.Eine sehr ähnliche Situation hat sich mit dem Volumen des Hippocampus entwickelt, gemessen durch Magnetresonanztomographie. Es ist zuverlässig bekannt, dass die Erinnerung an eine ältere Person umso schlimmer ist, je kleiner das Volumen des Hippocampus ist. Glücklicherweise gibt es Studien, die zeigen, dass moderates Aerobic-Training dazu beiträgt, das Volumen des Hippocampus aufrechtzuerhalten. Die Auswirkungen von Cortisol auf Teile des Gehirns unter StressDa Hippocampus-Neuronen eine erhebliche Menge an Glukokortikoidrezeptoren aufweisen, sind sie anfällig für anhaltenden Stress. Bei Menschen, die unter schwerem und langfristigem traumatischem Stress leiden, verkümmert der Hippocampus schneller als der Rest des Gehirns.Ähnliche Effekte werden bei posttraumatischer Belastungsstörung, Schizophrenie und Depression beobachtet. Interessanterweise kann die Atrophie bei Depressionen durch die Einnahme von Antidepressiva verlangsamt werden, auch wenn sie nicht zur Bewältigung anderer Symptome beitragen.
Die Auswirkungen von Cortisol auf Teile des Gehirns unter StressDa Hippocampus-Neuronen eine erhebliche Menge an Glukokortikoidrezeptoren aufweisen, sind sie anfällig für anhaltenden Stress. Bei Menschen, die unter schwerem und langfristigem traumatischem Stress leiden, verkümmert der Hippocampus schneller als der Rest des Gehirns.Ähnliche Effekte werden bei posttraumatischer Belastungsstörung, Schizophrenie und Depression beobachtet. Interessanterweise kann die Atrophie bei Depressionen durch die Einnahme von Antidepressiva verlangsamt werden, auch wenn sie nicht zur Bewältigung anderer Symptome beitragen.Neuroinflammation bei psychischen Störungen
Im Allgemeinen bildet sich ein interessantes Bild um Depressionen. Ihre Ursachen sind noch unbekannt; Die populärste Serotonin-Theorie wird ständig kritisiert. Gleichzeitig zeigen Patienten mit chronischer Entzündung häufig Anzeichen und Symptome einer Depression. In diesem Jahr wurde eine Arbeit veröffentlicht, in der Wissenschaftler feststellten, dass psychischer Stress, der unter anderem durch soziale Faktoren verursacht wird, das Entzündungsniveau im Gehirn von Mäusen erhöht. Mäuse trafen sich regelmäßig 10 Tage lang mit einem aggressiven Mann. Dieser Stress verursachte einen Anstieg der Menge an Interleukin 1 und des Nekrosefaktors im Tumor, der von aktivierten Mikroglia im präfrontalen Kortex, dem Bereich des Gehirns, der für die Entscheidungsfindung verantwortlich ist, ausgeschieden wird. Eine solche Verletzung führte letztendlich zu Episoden schwerer Depressionen, die durch Neutralisierung der Entzündung geheilt werden konnten.Die unter Versuchsbedingungen beschriebene Schlafstörung bewirkt die Aktivierung der gleichen angeborenen Immunrezeptoren wie sozialer Stress.LinkAufgrund der Tatsache, dass Neuroinflammation eine Schlüsselrolle bei psychiatrischen Erkrankungen spielen kann - Depression, Schizophrenie, bipolare Störung - wird dieses Phänomen äußerst merkwürdig, da die Ergebnisse dieser Experimente darauf hindeuten, dass diese Krankheiten verhindert werden können, lange bevor sie durch den Lebensstil korrigiert werden. Diät- und Schlafmuster.LinkHypothalamus-Alterung
Im Gegensatz zum Hippocampus, dessen Veränderungen das Auftreten einer kognitiven Beeinträchtigung mit dem Alter erklären, kontrolliert der Hypothalamus möglicherweise das Altern.Diese Struktur im Gehirn ist ähnlich wie die Mandel eine Brücke zwischen dem nervösen und dem endokrinen System des menschlichen Körpers. Es hilft, das Verhalten und zahlreiche Grundbedürfnisse wie Hunger, Schlaf, Angst und Aggression zu regulieren. Dementsprechend wird mit zunehmendem Alter die Homöostase der sekretierenden Nervenzellen, aus denen der Hypothalamus besteht, gestört, und mit dem Altern verbundene Manifestationen manifestieren sich.Die ersten Suchanfragen in diese Richtung betrafen die Bildung von Rückkopplungsketten verschiedener Hormone, oft sexuell. Rückkopplungsstörungen und das Auftreten von Resistenzen gegen Östrogen, Insulin, Wachstumshormon und andere regulatorische Moleküle sind jedoch eine Folge und keine Ursache. Die zellulären und molekularen Mechanismen, die den Verlust der Homöostase erklären, sind noch nicht gut verstanden.In den letzten Jahren wurden verschiedene molekulare Wege und Gene untersucht, die mit dem Einsetzen und Fortschreiten altersabhängiger degenerativer Prozesse verbunden sind. Unter ihnen waren jetzt Sirtuine, SIRT, Rapamycin-Zielprotein von Säugetieren, mTOR, Transkriptionsfaktor NF-kB und andere sehr beliebt.mTOR ist ein Enzym aus der Proteinkinase-Familie, das das Ziel des Krebsmedikaments Rapamycin ist. Als Ergebnis von Studien zu Zittern, Würmern, Fliegen und einigen Säugetieren wurde gezeigt, dass Rapamycin das Leben dieser Modellorganismen verlängern kann. Damit hat sich mTOR einen Ruf als zentrale, evolutionär konservative Determinante der Lebenserwartung erworben.mTOR reagiert sehr empfindlich auf Insulin und Wachstumsfaktoren. Er kontrolliert den Stoffwechsel der Zelle, ihr Wachstum und Überleben. Bei chronisch hoher Stimulation führt übermäßige Arbeit von mTOR jedoch zu oxidativem Stress, Anhäufung von Schäden und Alterung der Zelle - alles Anzeichen für die Entzündungsreaktion der Zelle.Die Aktivierung des Transkriptionsfaktors NF-kB trägt zur weiteren Entwicklung der Entzündungsreaktion bei, da er die Gene kontrolliert, die für seine Aufrechterhaltung verantwortlich sind. Neuere wissenschaftliche Arbeiten haben gezeigt, dass ein konstanter Kalorienüberschuss in Lebensmitteln zur Entwicklung von Entzündungsreaktionen im Hypothalamus beitragen kann.Übermäßige Neuroinflammation
Überschüssige Nährstoffe haben einen "Dominoeffekt". Zuallererst leidet das endoplasmatische Retikulum darunter - ein verzweigtes Netzwerk von Hohlräumen, Vesikeln und Tubuli, das mit einer Vielzahl von Stoffwechselfunktionen verbunden ist: Transport von Proteinen und Lipiden, Calciumakkumulation und so weiter. Wenn dieses wichtige Organoid Stress in den Mikroglia des Hypothalamus erfährt, wird NF-kB in diesen Zellen aktiviert. Mikrogliazellen stehen über proinflammatorische Zytokine wie Tumornekrosefaktor Alpha und Interleukin 1 Beta in ständiger Kommunikation mit Neuronen.Eine Erhöhung ihrer Expression aktiviert NF-kB bei der Sekretion von Neuronen, hemmt die Produktion von Gonadoliberin, einem Hormon, das die Produktion der Hypophysen-Gonadotropin-Hormone steuert, und fördert die Insulin- und Leptinresistenz.Dies schwächt im Laufe der Zeit die hypothalamische Homöostase. Diese Dysregulation ist mit systemischem Altern und der Entwicklung altersabhängiger Pathologien verbunden - Diabetes, Fettleibigkeit, Herz-Kreislauf-Erkrankungen, Demenz und reproduktive Dysfunktion.www.ncbi.nlm.nih.gov/pmc/articles/PMC2586330www.ncbi.nlm.nih.gov/pmc/articles/PMC3756938www.ncbi.nlm.nih.gov/pubmed/23636330www.ncbi.nlm.nih .gov / pmc / articles / PMC4313775Stammzellen und Neuroinflammation
2013 entdeckten Forscher des Albert Einstein College of Medicine die Stammzellen des Hypothalamus, die ihrer Meinung nach auch die Alterung des Körpers kontrollieren können. Sie berichten, dass die Anzahl der hypothalamischen Stammzellen bei Mäusen, die Gegenstand der Studie waren, mit der Zeit abnimmt. Mit zwei Jahren - dem Alter alter Mäuse - haben die meisten dieser Zellen keine mehr.Experimentatoren transplantierten Stammzellen in normale Mäuse sowie in Mäuse, denen sie zuvor die hypothalamischen Stammzellen zerstört hatten. Beide Gruppen zeigten Anzeichen einer verzögerten Alterung. Es stellte sich heraus, dass spezifische miRNAs der Schlüsseleffektor für dieses Phänomen waren. Diese Gruppe von Molekülen unterscheidet sich von gewöhnlichen RNAs dadurch, dass sie nicht am Prozess der Proteinsynthese beteiligt sind, sondern an der Regulation der Expression anderer Gene in Zellen. Eine Zelle kann microRNA in speziellen Behältern - Exosomen - sezernieren.Um ihre Hypothese zu bestätigen, isolierten die Experimentatoren Exosomen hypothalamischer Stammzellen und injizierten normale Mäuse und Mäuse, bei denen hypothalamische Stammzellen zerstört wurden, in die Cerebrospinalflüssigkeit. Das Ergebnis übertraf alle Erwartungen: Wiederum wurden beide Gruppen von Mäusen langsamer älter - sie bewerteten Muskelkraft, motorische Koordination, soziales Verhalten und kognitive Fähigkeiten.LinkObwohl bereits mehrere microRNAs bekannt sind, die eine wichtige Rolle bei Entzündungen spielen, wie miR-107, miR-155 und miR-223, wurde diese microRNA nicht untersucht, welche microRNA für die Verlangsamung des Alterns verantwortlich war.MicroRNA-Studien stehen noch am Anfang der Reise, und Erkenntnisse darüber, wie sie zur Erhöhung der gesunden Lebenserwartung eingesetzt werden können, könnten in naher Zukunft auf uns warten.Fazit
Wie Sie jetzt sehen können, ist Neuroinflammation ein äußerst komplexer Prozess. Damit gibt es keine klassischen Manifestationen von Entzündungen, die von Celsus beschrieben werden, nämlich Rötung, Schwellung durch Hitze und Schmerz. Bei einer Neuroinflammation sind die molekularen und zellulären Mechanismen jedoch teilweise dieselben wie bei einer Entzündung. In beiden Fällen sind Signalmoleküle oder Zytokine wie Interleukine, Chemokine und Tumornekrosefaktor beteiligt. Sowohl der eine als auch der andere Prozess haben positive und negative Seiten.
Der Schlüssel zu diesen Prozessen ist der Versuch des Körpers, beschädigtes Gewebe auf die ihm zur Verfügung stehende Weise zu reparieren. Es gibt Unterschiede. Residente Makrophagen im Gehirngewebe sind Mikrogliazellen. Sie kommen in anderen Geweben des Körpers nicht vor. Anstelle der üblichen Narbe bildet das Nervengewebe aufgrund der Aktivierung von Astrozyten Gliazellen.
Es ist nicht überraschend, dass Entzündungen im Nervengewebe, insbesondere im Zentralnervensystem, weitreichende Folgen haben. Neuroinflammation ist an Alterung, altersbedingten Pathologien, Fettleibigkeit und einigen Arten von Demenz beteiligt.
Trotz der Tatsache, dass viel Gesundheit von der Genetik abhängt, bestimmt unser Verhalten teilweise auch, wie wir leben und altern. Mäßige körperliche Aktivität und wiederum eine moderate, gesunde und abwechslungsreiche Ernährung sowie gesunder Schlaf können die Neuroinflammation verringern und die Gesundheit von Gehirn und Körper verlängern. Es ist auch notwendig, rechtzeitig die Hilfe von Ärzten in Anspruch zu nehmen, auch wenn es sich um eine Art Depression handelt, die von selbst vergeht. Und lassen Sie sich auch nicht auf Selbstmedikation und Wahrsagerei durch Pubmed ein, die in unsere Gesellschaft gekommen ist, um die Diagnose von Google zu ersetzen.
www.ncbi.nlm.nih.gov/pmc/articles/PMC4588685www.ncbi.nlm.nih.gov/pubmed/25527485Autor Wassili Tsvetkov