Ich denke, die regelmäßigen Leser meiner Notizen haben bereits meine eher skeptische Haltung gegenüber allen Arten von sozusagen Nahrungsmitteln und diätetischen Abweichungen wie Rohkost, Monoedikation, Pranoediation („Tausende von ihnen“) bemerkt. Aber heute möchte ich über solche "Nährstoffe" von Kartoffeln sprechen, die in den meisten Fällen nur für diejenigen verfügbar sind, die rohe Kartoffeln essen (naja oder Kartoffelsaft herstellen) und "Herden und Röstern aller Art" (einschließlich) keinen besonderen Nutzen bringen. übrigens und der Autor dieser Zeilen). Es muss auch einen Urlaub in der Syroed Street geben. Dieser Tag ist gekommen ...
Um zu lernen, wie man Arthritis mit Kartoffeln heilt und den Blutdruck senkt, wie groß das Kartoffelgenom ist und wo jetzt Kartoffelkwas produziert wird, muss man im Allgemeinen nach unten schauen.
- Biochemie! Biochemie! - Pioniere schrien und holten Notizbücher heraus.paraphrasiert von einem berühmten WitzBulbyany tlushch, auch bekannt als Fat of the ... Kartoffel
Um ehrlich zu sein, ist die Einführung eines solchen Konzepts wie „Kartoffelfett“ sogar irgendwie nicht üblich, da der Fettgehalt (sie sind Lipide) in Knollen sehr niedrig ist - nur etwa 0,2 - 2 Gramm / kg Frischgewicht (oder
durchschnittlich 1,2 g / kg). Meine Lieblings-
USDA-Basis spricht ungefähr das Gleiche und schreibt 100 Gramm Pellkartoffeln mit 0,1 g Lipiden zu, von denen 0,03 g gesättigte Fettsäuren, 0,002 einfach ungesättigte Fettsäuren und 0,043 g mehrfach ungesättigte Fettsäuren sind. Und das trotz der Tatsache, dass ein gesunder erwachsener Körper bis zu 17 Gramm Omega-6 und bis zu 2 Gramm mehrfach ungesättigte Omega-3-Fettsäuren pro Tag benötigt. Im Allgemeinen können wir mit Sicherheit sagen, dass es nicht möglich sein wird, von Kartoffeln mit Fett zu profitieren ... Aber im Allgemeinen ist nicht alles so einfach, weil wir Qualität suchen, nicht Quantität.
Zunächst werden überraschenderweise alle Lipide in Saccharose-Kartoffelknollen synthetisiert. Unter dem Spoiler für fortgeschrittene Leser -
BiosyntheseschemaSchema für die Synthese von Stärke und Fett in KartoffelnSaccharose wird in Knollenzellen unter Verwendung von Saccharosesynthetase in UDP-Glucose und Fructose umgewandelt. Die meisten Kohlenhydrate gelangen in pflanzliche Amyloplasten und werden zur Herstellung von ADP-Glucose verwendet, einem Vorläufer der Stärkesynthese. Eine kleine Menge an Kohlenhydraten wird durch Glykolyse metabolisiert oder zur Synthese von Fettsäuren in demselben Amyloplasten in Acetyl-CoA und Malonyl-CoA umgewandelt. Fettacylgruppen werden von spezialisierten Proteinen auf das endoplasmatische Retikulum übertragen, wo sie anschließend für die Lipidbiosynthese verwendet werden.
Bezeichnungen: ACCase - Acetyl-CoA-Carboxylase, AGP - ADP-Glucosepyrophosphorylase, ACP - Trägerprotein für Acylgruppen, AATP - Plastid ATP / ADP-Träger, bP - Bisphosphat, CoA - Coenzym A, DAG - Diacylglycerin, D. CoA-Diacylglycerolacyltransferase, Frc-Fructose, Glc-Glucose, P-Phosphat, PGM-Plastid-Phosphoglucomutase, TAG-Triglyceride
Es gibt Spuren von freien Fettsäuren und Triglyceriden in Kartoffeln, aber es gibt
Phospholipide (Phosphatidylcholin - 30,7 Mol-%, Phosphatidylethanolamin - 19,6%, Phosphatidylinositol - 9,3%, Phosphatidsäure - 3,2%, Phosphatidylserin - 1 5% Phosphatidylglycerin - 1,2% und Diphosphatidylglycerin (
Cardiolipin ) - 0,7%) und Galactolipide. Wenn ich bereits im Abschnitt "
Fett der ... Banane " meines letzten "Bananen" -Artikels über Phospholipide und ihre Eigenschaften gesprochen habe (was bedeutet, dass alles, was dort gesagt wird, für Kartoffeln gilt), dann werde ich hier kurz über Galactolipide sprechen. Tatsächlich handelt es sich um eine Art Glykolipid, eine Substanz, die einen unpolaren „Schwanz“ enthält - einen Lipid- (Fettsäure-) Rest, der durch eine kovalente (glykosidische) Bindung an einen polaren Kohlenhydratrest (wörtlich Zucker- „Kopf“) gebunden ist. Bei Galactolipiden wirkt Galactose als Kohlenhydratrückstand.
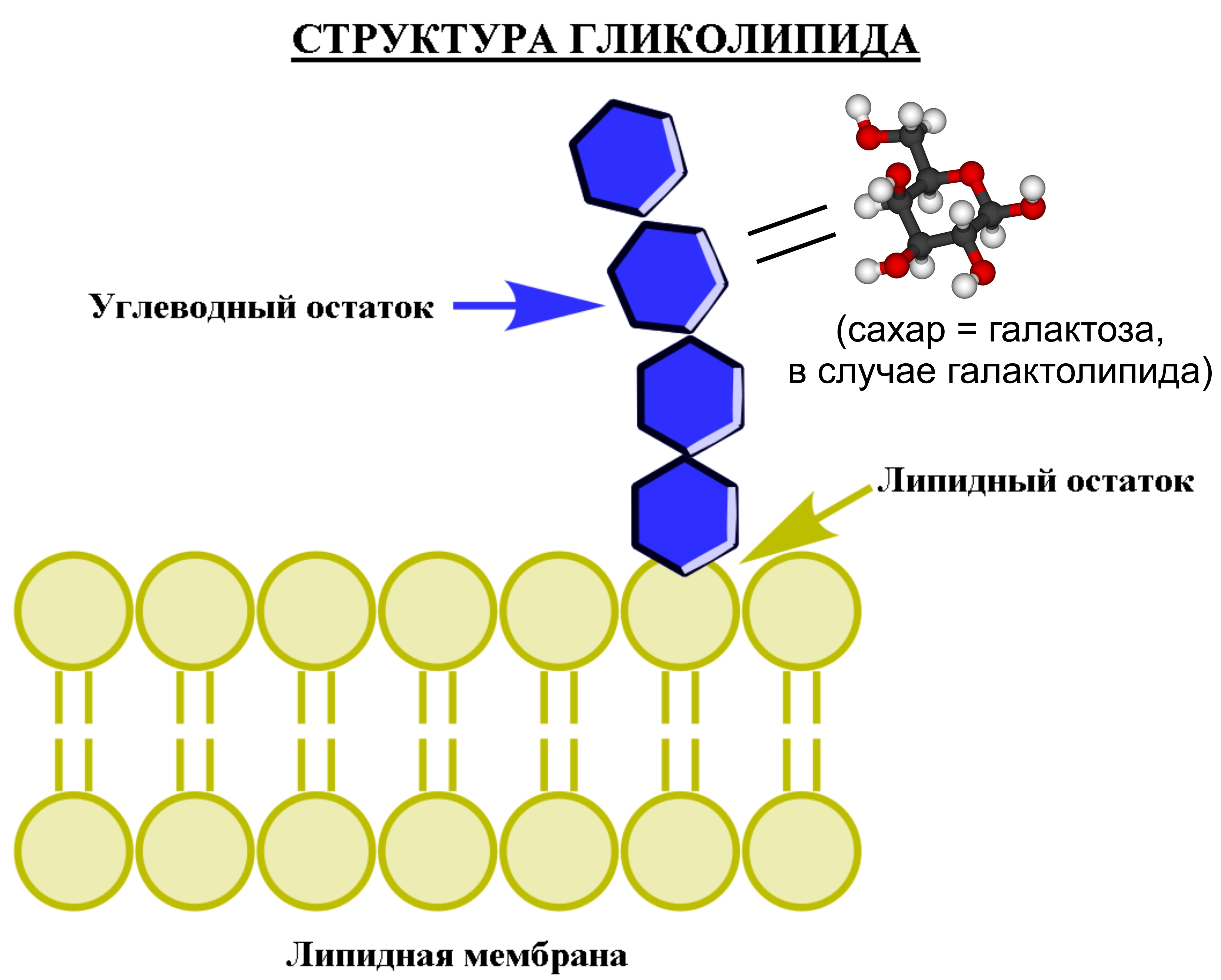
Im Allgemeinen sind Glykolipide für die Stabilität der Zellmembran und für die Erkennung von "Freund oder Feind" verantwortlich, die sowohl der Immunantwort zugrunde liegen als auch das Zusammenwachsen von Zellen ermöglichen und Gewebe bilden. Darüber hinaus befinden sich Glykolipide auf der Oberfläche eukaryotischer Zellmembranen, die sich von der doppelten Lipidschicht in den „Weltraum“ des extrazellulären Mediums erstrecken. Zurück zu den Galactolipiden: Wir können sagen, dass sie meistens direkt an den Photosyntheseprozessen beteiligt sind und als Backup-Analogon für Phospholipide fungieren, wenn im Körper kein Phosphor vorhanden ist. Neben der Tatsache, dass Galactolipide eine höhere Bioverfügbarkeit aufweisen als freie Fettsäuren, können sie auch eine gute entzündungshemmende Aktivität aufweisen. Beispielsweise kann eine Wildrose dienen, die Galactolipide enthält und
eine ausgeprägte entzündungshemmende Wirkung hat (insbesondere antiarthritisch).
Eine interessante Tatsache ist, dass Galactolipide auch als Abschreckungsmittel (Antifidant) für Meerespflanzen (sowie für alle Arten von Tanninen für Landpflanzen) wirken können. Ein Beispiel ist der
Fucus- Seetang, der an den Ufern des Atlantiks und des Pazifischen Ozeans weit verbreitet ist und aufgrund des Vorhandenseins von Galactolipiden
nicht denselben niedlichen
Igel fressen
kann .
Absolut die Tipps zu fettbezogenen Verbindungen in Knollen:
Erstens sind dies Phytosterole, die uns bereits bekannt sind (siehe den Artikel
Anmerkungen eines Phytochemikers. Sonnenuntergang der Habra-Bananen-Ära , um das Wissen über Phytosterole / Sterole aufzufrischen). In frischen Kartoffelknollen finden Sie viele freie Sterole. Frische Kartoffelknollen enthalten etwa 43,1–43,7% β-Sitosterol (der gesamten Pflanzensterine), Campesterol (26%), Δ5-Avenasterol (20%) und 10% des Restes sind ungefähr zu gleichen Teilen auf Brassicasterin, Δ7-Avenasterin und Stigmasterol verteilt und ihre Ester. Also was? Subj ist also falsch (
warum - siehe den oben bereits erwähnten Bananenartikel ):
Aber warum isst du dieses Fleisch mit einer Bulba und gehst ins Bett?Und dann, dass die Zwiebel-Phytosterole die Absorption von Fleischcholesterin reduzieren, ist es kein langmütiges Fleisch mit einer Banane, durch Golly, essen ...
Zweitens das lipophile Biopolymer
Suberin , das der Hauptbestandteil des Inneren der Kartoffelschale ist. Suberin besteht aus dem sogenannten Suberinsäuren (Korksäuren) und Glycerin. Säuren selbst werden manchmal verwendet, um Medikamente (
wie hier laut russischer Wikipedia) und biologisch abbaubare Kunststoffe zu synthetisieren. Und Suberin - Suberin, Freunde, das ist grob gesagt der Korken, genau wie in einer Weinflasche, die in Form von Dekorationsmaterial an der Wand der Küche vorliegt. Grob gesagt, denn Kork ist eine Mischung aus Suberin, Ballaststoffen, Lignin und verschiedenen Pflanzenwachsen.
Und drittens sind es Fette, die für den gleichen Kartoffelgeruch verantwortlich sind. Es ist wichtig, dass rohe Kartoffeln praktisch geruchlos sind, da sie sehr geringe Mengen an flüchtigen Substanzen enthalten. Sobald die Lipidoxidation begann, begannen auch Gerüche (übrigens bekämpfen alle Antioxidantien die Lipidoxidationsprozesse). Der angenehme Geruch von frisch gekochten Kartoffeln sowie gebratenen und gebackenen Kartoffeln entsteht durch die Tatsache, dass die Oxidation von ungesättigten Fettsäuren (die eine geringe Menge enthalten) auftritt - hauptsächlich Linolsäure und Linolensäure. Als Ergebnis
wird eine Reihe von flüchtigen Aldehyden, Ketonen, Alkoholen und Alkylfuranen gebildet. Laut den Autoren der
Arbeit hängt der Unterschied im Geschmack von Salzkartoffeln verschiedener Sorten mit dem Gehalt an Linolsäure und der
cis-4-Heptenal-Verbindung zusammen , die durch Oxidation entsteht (diese Verbindung wird übrigens als Lebensmittelaroma verwendet). Als Fliege in der Salbe können Sie hinzufügen, dass unangenehme Gerüche ("Ranzigkeit" usw.) ihr Aussehen auch ungesättigten Fettsäuren verdanken, die während der Lagerung leicht oxidiert werden (insbesondere dehydrierte Kartoffeln und Produkte daraus). In der
Arbeit zeigten
die Autoren, dass der unangenehme Geruch, der sich bei längerer Lagerung von Kartoffelflocken bildet, auf die Zersetzungsprodukte von Linolsäure (die beim Abbau der Peroxokomplexe von Linolsäure entsteht), insbesondere
Hexanal (das den Geruch von „frisch geschnittenem Gras“ erzeugt) zurückzuführen ist.
Ich vermute, dass Kommentatoren verpflichtet sind, alle Arten von Pyrazinen zu erwähnen, die Kartoffeln „den gleichen Geschmack verleihen, den sie seit ihrer Kindheit kennen“, wenn sie den Geruch von thermisch verarbeiteten Kartoffeln erwähnen. Deshalb mache ich eine Klarstellung: „Für den Geruch sind Fette verantwortungsbewusster und für den Geschmack - alles andere, was sich aus der
Maillard-Reaktion ergibt, die jedem Koch bekannt ist.
Die Maillard-Reaktion (Zuckerkondensationsreaktion) ist eine chemische Reaktion zwischen Aminosäuren und Zuckern, die beim Erhitzen auftritt. Ein Beispiel für eine solche Reaktion ist das Braten von Fleisch oder das Backen von Brot, wobei während des Erhitzens eines Lebensmittelprodukts ein typischer Geruch, eine typische Farbe und ein typischer Geschmack von gekochtem Essen auftreten. Diese Veränderungen werden durch die Bildung von Maillard-Reaktionsprodukten verursacht. Benannt nach dem französischen Chemiker und Arzt Louis Camille Maillard, der als einer der ersten die Reaktion in den 1910er Jahren untersuchte.
Vielleicht wird es später notwendig sein, den Prozess der Wärmebehandlung von Kartoffeln separat zu betrachten und seine Chemie zu betrachten. In der Zwischenzeit möchte ich einfach sagen, dass an der Bildung des Geschmacks von gekochten / gebratenen Kartoffeln (und des damit verbundenen Aromas) hauptsächlich verschiedene Alkylfurane (dort Pyrazine) beteiligt sind, die in derselben Maillard-Reaktion gebildet wurden.
Hinweis : Eine interessante Tatsache ist, dass RNA-Abbauprodukte - einige Ribonukleotide, die beim Backen / Braten von Kartoffeln gebildet werden, als Vorläufer (Vorläufer) von „glutamatähnlichen“ Geschmacksverstärkern, Stimulatoren der „
Umami “ -Klasse von Rezeptoren, wirken. Also, wenn "die Sprache nicht zu Glutamat geht, geht das Glutamat zu der Sprache", und Sie,% USERNAME%, raten nicht einmal darüber :)
Kartoffelprotein
Es gibt wenig Fett, wenig mehr Protein (natürlich in Kartoffeln). Aber selbst mit dem großen Wunsch, Produkte tierischen Ursprungs zu erreichen, wird es nicht funktionieren. Im Durchschnitt enthält eine Kartoffelknolle etwa 20 Gramm Protein (6,9-46,3) pro Kilogramm Nassgewicht. Und laut USDA enthält das Fruchtfleisch einer gekochten Kartoffelhülle etwa 1,87 Gramm Protein pro 100 g Produkt. Somit ist das Protein, das mit Kartoffeln in den Körper gelangen kann, ein winziger Bruchteil der gesamten täglichen Proteinaufnahme, die für den Körper notwendig ist. Es ist jedoch anzumerken, dass Wurzelfrüchte (wie Kartoffeln und Süßkartoffeln) auch bei einem so geringen Gehalt weltweit eine wertvolle Proteinquelle ohne Getreide sind. Darüber hinaus ist Kartoffelprotein aufgrund des hohen Gehalts an essentiellen Säuren wie Lysin, Methionin, Threonin und Tryptophan von gewissem Wert. Trotzdem lassen sich die endogenen Proteine, die sozusagen in Kartoffeln vorkommen, in drei Klassen einteilen: Patatine, Proteaseinhibitoren und Proteine mit hohem Molekulargewicht. Über jeden im Detail weiter unten.
Das Hauptprotein in Kartoffeln ist
Patatin , auch bekannt als
Tuberin (wie sich auf Russisch herausstellt - "Kartoffel" oder so ...). Es kommt hauptsächlich in Knollen oder
Stolonen der Pflanze (in Parenchymvakuolen) vor. 40–60% aller Kartoffelproteine, auf die Patatine entfallen, sind Glykoproteine vom Reservetyp (dh Proteine, die während des Wachstums und der Entwicklung des Fötus als Nährstoffe akkumuliert werden, die für die Pflanzenentwicklung in den Anfangsstadien der Keimung erforderlich sind), die die enzymatische Aktivität von Lipidacylhydrolasen aufweisen ( L. AH, das in der Lage ist, Fettsäuren von Membranlipiden abzuspalten, dies ist übrigens die Hauptursache für Kartoffelallergien und hat ein Molekulargewicht von 40 bis 45 kDa.
Patatin besteht aus ungefähr 366 Aminosäuren und liegt in Kartoffeln als Dimer mit einem Molekulargewicht von ungefähr 88 kDa vor. Die Tertiärstruktur des Proteins ist bis zu 45 ° C stabil, mit steigender Temperatur beginnt sich die Sekundärstruktur zu entfalten und bei 55 ° C denaturiert die α-Helix. Also, freut euch, O Fans und Fans des
aktuellen SU-VID-Stroms , auch wenn ihr Kartoffelprotein sparen könnt.
Es ist interessant, dass Patatin im Vergleich zu anderen gängigen Proteinquellen pflanzlichen Ursprungs die gleiche ernährungsphysiologische Wirksamkeit wie Eiweiß aufweist und gleichzeitig bessere Emulgiereigenschaften aufweist als Sojaproteine (
Hersteller aller Arten vegetarischer Surrogate sollten hier innehalten und nachdenken ).
Die zweite Gruppe von Kartoffelproteinen sind Proteaseinhibitoren (das sogenannte Tuberinin), die ein Molekulargewicht im Bereich von 5 bis 25 kDa haben. Proteaseinhibitoren machen wie Patatin 30–40% des gesamten Knollenproteins aus. Und ja, wenn jemand schon vergessen hat, nicht weniger, aber
ernährungshemmende Substanzen . Proteaseinhibitoren blockieren die Arbeit von Serin, Cystein (hemmt Papain = essen Sie keine rohen Kartoffeln mit Papaya), Asparaginprotease (kann Trypsin, Chymotrypsin und menschliche Leukozytenelastase hemmen, ja), einigen Invertasen und metallhaltigen Carboxypepsidasen (PCI). Im Allgemeinen wurden bisher fünf Familien dieser Inhibitoren identifiziert (A - mit einer Masse von bis zu 8,1 kDa, B - mit einer Masse von bis zu 12,3 kDa, C - mit einer Masse von 22–25 kDa, K, M), die sich in ihrer Aminosäuresequenz unterscheiden , Kettenlänge und Zusammensetzung der Untereinheit (vom Monomer zum Pentamer). 70% der Kartoffelproteaseinhibitoren gehören zu den sogenannten "
Kunitsa-Domänen " (Akzent auf der ersten Silbe), die übrigens aktiv als Grundlage für die Entwicklung neuer Arzneimittel verwendet werden. Im Vergleich zu Patatin sind Proteaseinhibitoren im Allgemeinen hydrophiler, jedoch neigen beide Fraktionen des Proteins dazu, unter dem Einfluss der Wärmebehandlung zu koagulieren (d. H. Sie sind auch anfällig für
Sous-Vide ). Ich erinnere Sie noch einmal daran, dass Proteasehemmer den Status von Anti-Ernährungssubstanzen erhalten haben, weil sie die Verdaulichkeit und den biologischen Wert des Proteins verringern, was jedoch nur dann geschieht, wenn rohe oder nicht ordnungsgemäß zubereitete Produkte aus Kartoffeln konsumiert werden.
Und schließlich die
dritte, "NONAME" , eine Gruppe von Kartoffelproteinen (20-30% des gesamten Kartoffelproteins). Dazu gehören hauptsächlich hochmolekulare Proteine, die beispielsweise an der Stärkesynthese beteiligt sind
, wie beispielsweise Phosphorylase L-1 mit einem Molekulargewicht von 80 kDa (4%). Sie können sich auch an Lipoxygenasen (10%), Defensin (5%), Annexin, Glyoxylase I, Enolase, Katalase, UDP-Pyrophosphorylase usw. erinnern. Bisher hat niemand
die Familie wirklich
studiert . Es gibt also immer noch weiße Flecken
(belarussische Kartoffelexperten, ja! Arbeiten Sie für Sie) .
Die Beschreibung ist also gegeben und es lohnt sich zu erzählen, aber warum ist das alles interessant? Und es ist insofern interessant, als der enzymatische Abbau vieler der genannten Polypeptide zur Bildung kurzkettiger Proteine führt, die eine hormonähnliche (antithrombotische, blutdrucksenkende, immunmodulierende usw.) Aktivität aufweisen können. Peptide mit 3-20 Aminosäureresten, die das Darmepithel durchdringen oder an spezifische Rezeptoren von Darmepithelzellen binden können, besitzen normalerweise Bioaktivität.
Bisher ist zu beachten, dass weder die physiologische Rolle noch die biologische Aktivität von Kartoffelproteinen ausreichend untersucht wurden (lesen Sie und warten Sie auf Ihre Forscher). Basierend auf den Aminosäuresequenzen von Kartoffelproteinen schlagen die Forscher das Vorhandensein mehrerer potenzieller „Vorläuferproteine“ (Vorläufer) vor, die Peptide mit unterschiedlichen Aktivitäten im menschlichen Körper bilden.
Text über Kartoffelgenom und Kartoffelkwas aus WeißrusslandIch weiß nicht, wie viele Leute es wissen, aber das Kartoffelgenom wurde bereits entschlüsselt. Und Sie können es sogar herunterladen, auf DVD-R brennen und Ihrer Großmutter geben, von der wir im Herbst ein paar Taschen nehmen werden ... Zum Glück sind es nur 844 MB (dies ist nicht das
Weizengenom , ungefähr 15 GB groß, und alle Arten von
Erbsen ,
Erdbeeren ,
Kakao ,
Gurke ,
Sojabohnen usw. usw. sind ebenfalls nicht klein). Das sieht optisch ungefähr so aus:
Ein Bild übrigens aus diesem sehr
legendären Artikel in der ebenso legendären Natur. Das Kartoffelgenom wurde 2011 vom International Potato Sequencing Consortium sequenziert. Dieses Team bestand aus 16 wissenschaftlichen Gruppen aus verschiedenen Ländern, aus Russland gab es Experten, aber ob ich aus "Kartoffel" Weißrussland stamme, ich weiß nicht, ob Kommentatoren es mir sagen, ich werde den Artikel korrigieren.
Aber höchstwahrscheinlich, während die internationale Gemeinschaft sequenzierte, aber nicht sequenzierte, „wusch und lief“ unser Bruder (= wie Großvater Michurin uns hinterlassen hat) mit seinen Auswahlmethoden, um „
Kartoffeln mit rosa, blauem und lila Fruchtfleisch “ zu brauen. Es ist nicht so wichtig, dass bereits 2003 Forscher der Cornell University in den USA das neue Jahr mit lila Kartoffeln der Sorte
Adirondack Blue feierten, da es möglich ist,
Kartoffelkwas Mikola aus Belorusskaya Tsvetnoy herzustellen (Mikola ist Nikolay auf Russisch, wenn das so ist) (
für die European Games 2019, ja ).
Ein Beispiel für biologische Aktivität ist die
Arbeit, in der der „Kartoffel“ -Effekt gezeigt wird, der zu einer erhöhten Hemmung des
Angiotensin-Converting-Enzyms (ACE) führt, das für die Kontrolle des Blutdrucks verantwortlich ist (und eine Reihe anderer Folgen verschiedener Krankheiten). Darüber hinaus waren Proteine aus dem sogenannten am aktivsten auf diesem Gebiet. "Gefäßbündel" und innere Knollen. Es hatte Auswirkungen und Alter dieser Knollen (Liebhaber von jungen Kartoffeln, was auch immer man sagen mag, sie haben Recht mit ihren Geschmackspräferenzen).
Wenn wir jedoch über die Senkung des Blutdrucks sprechen, sollten wir so etwas wie Cucoamine erwähnen (auf dem Bild - Cucoamin A).Im Jahr 2005 Britische Forscher haben herausgefunden , diese Verbindungen in Kartoffeln. Chemisch gesehen sind Cucoamine Catechine (d. H. Sie gehören zu einer Untergruppe von Antioxidantien) sowie Derivate von Diamindihydrocophesesäuren. Zuvor wurden ähnliche Verbindungen in einer einzigen Pflanze Lycium chinense (Solanaceae) alias Dereza Chinese gefundenWenn überhaupt, gehört die Dereza vulgaris zur selben Familie , deren Früchte auch als „Wolfsbeere“ bezeichnet werden. Da es hier jedoch kein System gibt, versuchen Sie nicht, Wolfsbeeren nach Belieben zu greifen. Der Druck wird trotz äußerer Ähnlichkeit nicht sinken (finden Sie zehn Unterschiede zu Lycium chinense).Chinesische Dereza wird traditionell in der Phytomedizin eingesetzt, um den Blutdruck wirksam zu senken. Kartoffelkochamine haben ähnliche Eigenschaften. Es ist wahr, dass es in derselben Arbeit von 2005 Links zu Studien gibt, die das Vorhandensein von Cucoaminen in Waldtabak (Nicotiana sylvestris) und Tomaten (Lycopersicon esculentum) belegen. Während die Rolle von Cookoaminen in Kartoffeln nicht gut verstanden ist, gibt es Artikel, in denen Autoren ihnen die Regulation der Stärkebiosynthese , die Bildung von Krankheitsresistenz und die Stimulierung der Keimung zuschreiben. Was die biologische Aktivität im menschlichen Körper betrifft, müssen noch die thermische Stabilität von Kartoffelaminen (und heute werden etwa 30 davon gefunden) und ihre Bioverfügbarkeit bewertet werden.Die zweite interessante Tatsache der Protein-Natur kann die Arbeit sein ( ay , zwei ). Die Forscher fanden heraus, dass Kartoffelproteine, insbesondere Inhibitoren der Aspartatprotease, die Freisetzung von Cholestistokinin (CCK) in Mäusen stimulieren und Zellen stimulieren, die CCKAR (englischer Cholecystokinin A-Rezeptor) produzieren, der bei Wechselwirkung mit Lebensmittelproteinen zum Sättigungseffekt beiträgt.In Anbetracht all dieser Faktoren können Kartoffelproteine eine hervorragende Komponente für die Herstellung von funktionellen Lebensmitteln darstellen (ich habe dies in meinen „Bananen“ -Artikeln mehrmals erwähnt).Darüber hinaus können Kartoffeln aufgrund der großen Menge an tatsächlich freien Polypeptiden als ausgezeichneter In-vitro-Nanoreaktor für viele notwendige biologische Verbindungen fungieren. Forscher bei der Arbeitfanden beispielsweise heraus, dass kleine Kartoffelpeptide, die durch alkalische enzymatische Hydrolyse erhalten wurden, einen positiven Effekt auf den Lipidstoffwechsel bei Ratten hatten. Als Ergebnis dieser Arbeit wurden die hochmolekularen Proteine der Kartoffel in Peptide mit einem Molekulargewicht von 700 bis 1840 Da "zerlegt", wobei das Hauptmolekulargewicht (90% der Gesamtmenge) 850 Da betrug. Infolgedessen wurde der Schluss gezogen, dass dieses Verfahren zur Gewinnung von Peptiden mit niedrigem Molekulargewicht das wirtschaftlichste unter den vorhandenen ist und hervorragende Möglichkeiten für die industrielle Skalierung bietet (ganz zu schweigen von der Tatsache, dass Peptide mit niedrigem Molekulargewicht einen breiteren Bereich funktioneller Eigenschaften aufweisen als ihre „Peers“ mit hohem Molekulargewicht).Warum ist das alles? Und aufgrund der Tatsache, dass sie heute versuchen, Kartoffelprotein am häufigsten bei der Herstellung von Stärke zu entfernen und es nicht immer als Tierfutter verwenden (aufgrund des bitteren Geschmacks, den einige Verbindungen geben können, das gleiche Solanin), werden Kartoffelproteine praktisch nicht verwendet Emulgieren und Schäumen, obwohl ich denke, jeder, der mindestens einmal Kartoffeln gekocht hat, weiß, wie stabil der beim Kochen gebildete Schaum sein kann. Es stellt sich jedoch heraus, dass diese Sache interessant und nicht ausreichend untersucht ist. Ihr einziges Minus ist, dass alle interessantesten Eigenschaften nur bei Verwendung wie sie sind angezeigt werden, d. H. roh ... Chemiker, Rohkosthändler, Ihr Umzug!Fortsetzung folgt...Wichtig!Alle Aktualisierungen und Zwischennotizen, aus denen dann die Habr-Artikel reibungslos gebildet werden, sind jetzt in meinem Telegrammkanal lab66 zu sehen . Abonnieren Sie, um nicht den nächsten Artikel zu erwarten, sondern um sofort über alle Forschungsergebnisse informiert zu sein :)Gebrauchte LiteraturLiyanage, R., Han, K.-H., Watanabe, S., Shimada, Ki., Sekikawa, M., Ohba, K., et al., 2008. Potato and soy peptide diets modulate lipid metabolism in rats. Bioscience, Biotechnology, and Biochemistry 943–950.
Pots, AM; Gruppen, H.; Diepenbeek, R. v.; Lee, JJ vd; Boekel, M. v.; Wijngaards, G.; Voragen, AGJ The effect of storage of whole potatoes of three cultivars on the patatin and
protease inhibitor content; a study using capillary electrophoresis and MALDI-TOF mass spectrometry. J. Sci. Food Agric. 1999, 79, 1557-1564.
van Koningsveld, GA, Walstra, P., Gruppen, H., Wijngaards, G., van Boekel, MA, Voragen, AG, (2002). Formation and stability of foam made with various potato protein preparations. Journal of Agricultural and Food Chemistry 7651–7659.
Løkra, S., Helland, MH, Claussen, IC, Straetkvern, KO, Egelandsdal, B., (2008). Chemical characterization and functional properties of a potato protein concentrate prepared by large-scale expanded bed adsorption chromatography. Swiss Society of Food Science and Technology 1089–1099.
Dobson, G., Griffiths, DW, Davies, HV, & McNicol, JW (2004). Comparison of fatty acid and polar lipid contents of tubers from two potato species, Solanum tuberosum and Solanum phureja. J. Agric. Food Chem., 52, 6306–6314.
Petersen, MA, Poll, L., & Larsen, LM (1998). Comparison of volatiles in raw and boiled potatoes using a mild extraction technique combined with GC odour profiling and GC-MS. Food Chem., 61, 461–466.
Oruna-Concha, MJ, Bakker, J., & Ames, JM (2002). Comparison of the volatile components of two cultivars of potato cooked by boiling, conventional baking and microwave baking. J. Sci. Food Agric., 82, 1080–1087.
Laine, G., Göbel, C., du Jardin, P., Feussner, I., & Fauconnier, M. -L. (2006). Study of precursors responsible for off-flavor formation during storage of potato flakes. J. Agric. Food Chem., 54, 5445–5452.
Klaus, D., Ohlrogge, JB, Ekkehard Neuhaus, H., & Dörmann, P. (2004). Increased fatty acid production in potato by engineering of acetyl-CoA carboxylase. Planta, 219, 389–396.
Dobson, G., Griffiths, DW, Davies, HV, & McNicol, JW (2004). Comparison of fatty acid and polar lipid contents of tubers from two potato species, Solanum tuberosum and Solanum phureja. J. Agric. Food Chem., 52, 6306–6314.
Shewry PR (2003). Tuber storage proteins. Ann. Bot. 91 (7): 755–69.
Pihlanto, A. and Korhonen, HJT (2003) Bioactive peptides and proteins. Advances in Food and Nutrition Research 47, 175-276.
Pihlanto, A., Akkanen, S. and Korhonen, HJ (2008) ACE-inhibitory and antioxidant properties of potato (Solanum tuberosum). Food Chemistry 109, 104-112.
Makinen, S., Kelloniemi, J., Pihlanto, A., Makinen, K., Korhonen, M., Hopia, A. and Valkonen, JPT (2008) Inhibition of angiotensin converting enzyme I caused by autolysis of potato proteins by enzymatic activities confined to different parts of the potato tuber. Journal of Agricultural and Food Chemistry 56, 9875-9883.
Foltz, M., Ansems, P., Schwarz, J., Tasker, MC, Lourbakos, A. and Gerhardt, CC (2008) Protein hydrolysates induce CCK release from enteroendocrine cells and act as partial agonists of the CCK1 receptor. Journal of Agricultural and Food Chemistry 56, 837-843.
Parr, AJ, Mellon, FA, Colquhoun, IJ, & Davies, HV (2005). Dihydrocaffeoyl polyamines (kukoamine and allies) in potato (Solanum tuberosum) tubers detected during metabolite profiling. J. Agric. Food Chem., 53, 5461–5466.
Tanemura, Y., & Yoshino, M. (2006). Regulatory role of polyamine in the acid phosphatase from potato tubers. Plant Physiol. Biochem., 44, 43–48.
Stenzel,O.,Teuber,M.,&Drager,B.(2006).Putrescine N-ethyltransferase in Solanum tuberosumL., a calystegine-forming plant. Planta, 223, 200–212.
Matsuda, F., Morino, K., Ano, R., Kuzawa, M., Wakasa, K., & Miyagawa, H. (2005). Metabolic flux analysis of the phenylpropanoid pathway in elicitor-treated potato tuber tissue. Plant Cell Physiol., 46, 454–466.
Kaur-Sawhney, R., Shih, LM, & Galston, AW (1982). Relation of Polyamine Biosynthesis to the Initiation of Sprouting in Potato Tubers. Plant Physiol., 69, 411–415.