
Einer der berühmtesten Marvel-Superhelden war und ist Logan, auch bekannt als Wolverine. Und welche Eigenschaft seines Körpers fällt ihm zuerst ein, außer natürlich die Regeneration mit Blitzgeschwindigkeit? Mit einem Wort - Adamantium. Dieses seltene Metall hat einzigartige Eigenschaften, es ist fast unmöglich, es zu zerstören, und die Verarbeitung ist sehr aufwändig. Diese fiktive Substanz hat in unserer Realität mehrere Äquivalente, die auch sehr spezifische Eigenschaften haben. Unter ihnen verdiente Iridium besondere Aufmerksamkeit von Wissenschaftlern. Dieses Metall kann aus einer einfachen Person kaum einen Superhelden machen, aber er weiß, wie man Krebszellen zerstört (Deadpool würde so etwas nicht ablehnen). Wie sind Wissenschaftler zu diesem Schluss gekommen: Wie effektiv ist Iridium im Kampf gegen Krebs und wie sieht seine Zukunft in der Onkologie aus? Tauchen Sie in den Studiengruppenbericht ein, um Antworten zu erhalten. Lass uns gehen.
MetallwissenschaftIridium (Ir) ist ein extrem festes Übergangsmetall aus der Platingruppe. Wie fiktives Adamantium ist Iridium auch bei Temperaturen von 2000 ° C sehr korrosionsbeständig. Eine weitere Ähnlichkeit dieser beiden Metalle in ihrem außerirdischen Ursprung. Genauer gesagt ist Iridium auf unserem Planeten sehr klein, daher wird es in hoher Konzentration an Orten gefunden, an denen Meteoriten fallen.
 Iridium (Ir)
Iridium (Ir)Iridium ist ein relativ junges Metall in der wissenschaftlichen Welt, da es 1803 vom Chemiker Smithson Tennant entdeckt wurde. Er arbeitete an Platin mit einer Mischung aus Salpetersäure und Salzsäure, die einen sehr ungewöhnlichen Namen hat - Königswasser. Und wie aus der Zusammensetzung dieser Lösung hervorgeht, werden Sie nach ihrer Verwendung kein „betrunkener Meister“ wie Jackie Chan im gleichnamigen Film, sondern ein toter Meister. Für das Wort "Wodka" bedeutete ursprünglich klares Wasser und erst nach dem XIV. Jahrhundert wurde es als alkoholisches Getränk verwendet.
Mit Hilfe von königlichem Wodka konnte Herr Tennant die in Platin enthaltenen Verunreinigungen, nämlich Osmium und Iridium, in reiner Form erhalten.
Wie bereits erwähnt, gibt es sehr wenig Iridium - etwa 3 Tonnen dieses Metalls werden pro Jahr abgebaut. Zum Vergleich: Der Silberabbau überschreitet nach einigen Quellen die Marke von 27.000 Tonnen pro Jahr.
StudienbasisDie Studie basiert auf der bereits angewandten Methode zur Behandlung von Krebs (und einigen anderen auch) - der photodynamischen Therapie (PDT). Die Hauptfiguren dieser Methode sind Photosensibilisatoren und Licht.
Photosensibilisatoren * - Substanzen, die die Lichtempfindlichkeit in biologischen Geweben erhöhen.
Sensibilisatoren sind ziemlich wählerisch, das heißt, sie reichern sich nur in den Geweben an, die für das weitere Bestrahlungsverfahren mit Licht gewechselt werden müssen.
Wenn Licht in das Zielgewebe eintritt, tritt eine photochemische Reaktion auf - molekularer Triplettsauerstoff (
3 O
2 ) wird in Singulettsauerstoff umgewandelt. Zusätzlich werden hochaktive Radikale gebildet. Zusammen führt dies zum Tod von Krebszellen.
Wissenschaftler zitieren Photofrin und Aminolevulinsäure als die häufigsten Photosensibilisatoren in der PDT-Therapie. In den letzten Jahren wurde Metallen mit einem hohen Lumineszenzkoeffizienten jedoch immer mehr Aufmerksamkeit geschenkt, da sie ungewöhnliche und nützliche photochemische und photophysikalische Eigenschaften aufweisen. Zum Beispiel TLD1433 (Ruthenium) zur PDT-Behandlung der Blase und WST11 (Palladium) zur Behandlung von Blutgefäßen.
ForschungsergebnisseWarum also nicht Iridium verwenden, dachten Wissenschaftler. Aber zuerst benötigen Sie einen Mechanismus, mit dem dieses Metall verwendet werden kann. Der Patient wird Iridium nicht wie normale Tabletten oral einnehmen. Und hier ist menschliches Serumalbumin (
HSA ) mit der Arbeit verbunden, die aufgrund ihrer Eigenschaften und Menge (etwa 55% aller Blutproteine) ein ausgezeichneter Träger verschiedener Substanzen ist (in unserem Fall medizinisch). Einfach ausgedrückt kann CSA verwendet werden, um Krebsmedikamente an den gewünschten Körperbereich des Patienten abzugeben, was bereits in früheren Studien mit Osmium, Ruthenium und Palladium gezeigt wurde.
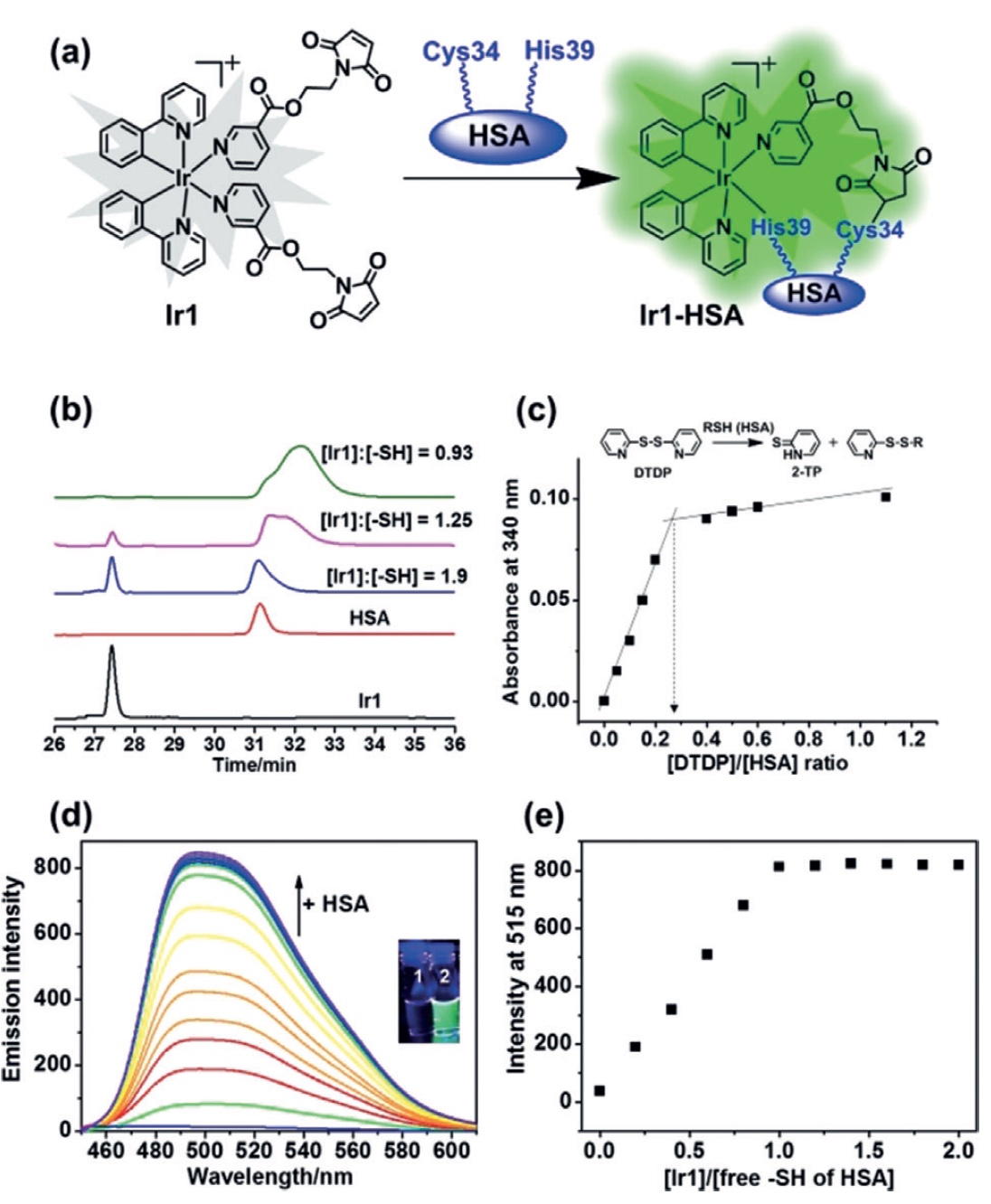 Bild Nr. 1
Bild Nr. 1In unserer Studie haben Wissenschaftler einen Maleimid-funktionalisierten oktaedrischen Organo-Iridium (III) -Komplex Ir1 (
1a ) in Kombination mit HSA entwickelt. Dieser Komplex (Ir1-HSA) erwies sich als viel wirksamer bei der Erhöhung der Phosphoreszenz im Vergleich zu „reinem“ Ir1, dh ohne HSA.
Im Dunkeln ist Ir1-HSA für gewöhnliche Zellen weitgehend ungiftig, zeigt jedoch eine starke Photozytotoxizität gegenüber Krebszellen und ihren Sphäroiden (Zellbildungen).
Das synthetisierte Ir1 war 12 Stunden im Dunkeln und nach 1 Stunde Exposition gegenüber blauem Licht stabil. Es war notwendig, die Kohlenstoff-Kohlenstoff-Bindung (C = C) zu überprüfen. Hierzu wurde ein Komplex aus Ir1 und Cystein (Cys) in einem Molverhältnis von Cys: Ir1 - 2: 1 in [D
6 ] DMSO / D
2 O bei einer Temperatur von 298 K 30 Minuten lang umgesetzt. Als Ergebnis der Protonenmagnetresonanz fanden die Wissenschaftler den Spitzenwert von Vinylprotonen von Maleimidgruppen bei etwa 6,62 ppm (Millionstel eines Anteils). Mit der Zugabe von Cystein verschwanden die Peaks, aber dann traten sie bereits im Bereich von 2,9 ... 3,9 ppm wieder auf. Wissenschaftler führen dies auf die Konjugation von Cystein zurück.
Als nächstes überprüften die Wissenschaftler, ob das freie Thiol Cys34 aus HSA mit C = C reagieren kann. Hierzu wurden 30 μM (Mikromol) Ir1 1 Stunde mit HSA (0-120 μM) inkubiert. Ferner wurden die resultierenden Reaktionsprodukte unter Verwendung von Umkehrphasen-Hochleistungsflüssigchromatographie (RP-HPLC) getrennt.
Als die HSA 120 uM erreichte, verschwand der Peak von Ir1 vollständig (Verhältnis von HSA: Ir1 = 4: 1). Somit betrug der Thiol (SH) -Gehalt 0,27 ± 0,1 Mol SH pro 1 Mol HSA (
1 s ). Folglich beträgt die Konzentration an freien SH-Gruppen von 120 & mgr; M HSA 32,4 ± 1,2 & mgr; M. Mit diesem Indikator tritt eine Reaktion mit 30 μM Ir1 auf, die zum Auftreten eines Addukts (direkte Verbindung von Molekülen) Ir1 und HSA im Verhältnis 1: 1 führt.
Reines Ir1 zeigte im Gegensatz zum Ir1-HSA-Komplex (
1d ) in wässriger Lösung keine starke Strahlung. Je höher die HSA-Konzentration ist, desto stärker wird die Phosphoreszenz von Ir1 selbst (
1e ).
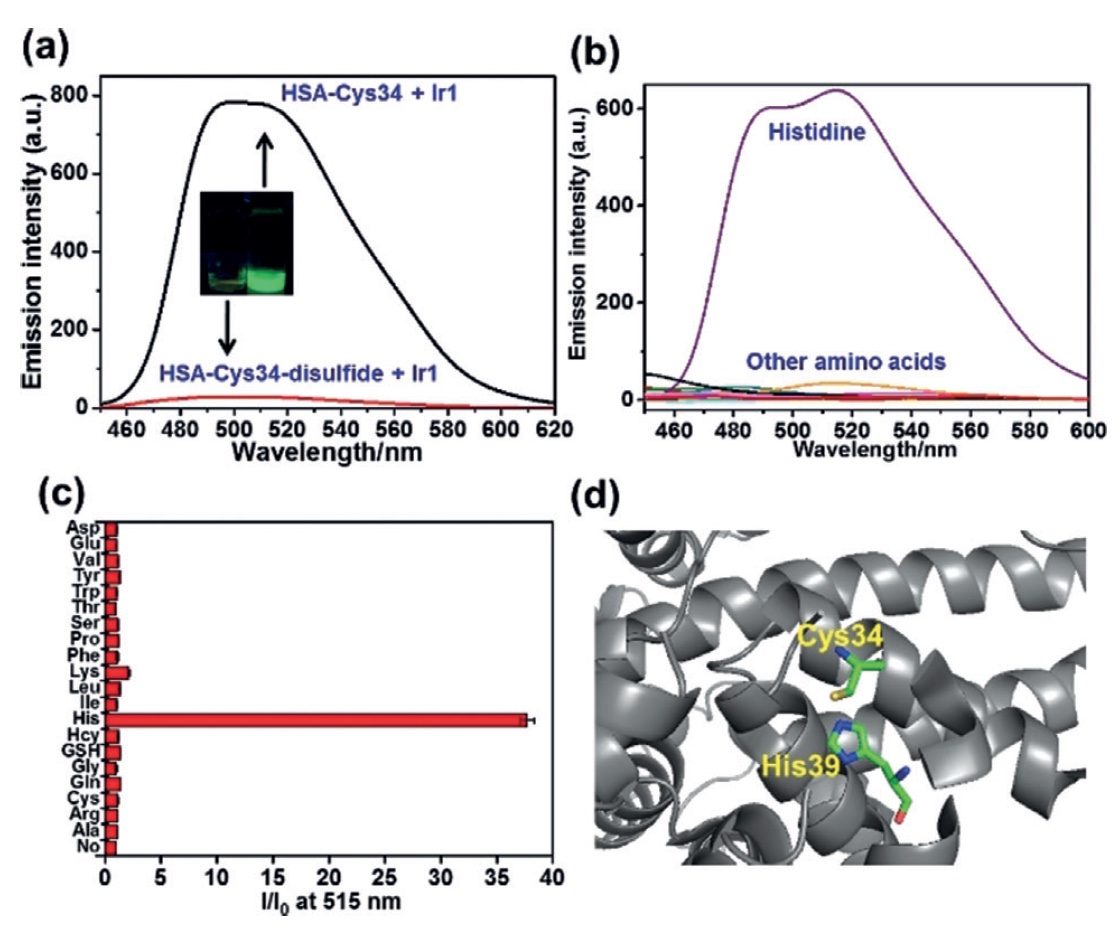 Bild Nr. 2
Bild Nr. 2Um die freien Thiolgruppen aus HSA zu entfernen, wurden der Lösung 100 & mgr; M Cystin pro Tag bei einer Temperatur von 277 K zugesetzt. Das resultierende Produkt wurde 30 Minuten mit Ir1 kombiniert. Beobachtungen zeigten eine signifikante Abnahme der Phosphoreszenz. Im Fall des HSA-Cys34- und Ir1 (
2a ) -Konjugats war die Situation umgekehrt, und dies legt nahe, dass das freie Thysol Cys34 das Verbindungsglied (genauer gesagt die Bindungsdomäne) für Ir1 ist.
Nun war es notwendig, den CSA genauer zu untersuchen und in seine Komponenten zu analysieren. Humanserumalbumin hat eine Kette von 585 Aminosäureresten, unter denen Wissenschaftler genau diejenigen finden mussten, die die Lumineszenz von Ir1 verstärken. Hierzu wurde eine Lumineszenzanalyse der Wechselwirkung von Ir1 mit verschiedenen Aminosäuren (
2b und
2c ) durchgeführt. Und wie wir in Grafik
2b sehen können , ist Histidin (His) der Anführer unter den Aminosäuren mit einem großen Rand, der die Lumineszenz von Ir1 um das 37-fache erhöht.
Nachdem die Wissenschaftler ein wenig verstanden hatten, was und wie es in den Bestandteilen des Ir1-HSA-Komplexes funktioniert, wechselten sie zur praktischen Anwendung, dh zu Experimenten.
Zuerst wurden 0,4 Millimol Ir1 in 20 ml MeOH: H 2 O verdünnt, 0,4 Millimol HSA wurden zugegeben und 1 Stunde gerührt. Konfokale Mikroskopie wurde dann verwendet, um die Verteilung von Ir1-HSA in lebenden Lungenkrebszellen (A549) zu untersuchen.
Bereits nach 30 Minuten war Ir1-HSA hauptsächlich im Zytoplasma von Krebszellen konzentriert. 60 bis 120 Minuten nach Beginn der Inkubation drang der Komplex in die Kerne von Krebszellen ein.
 Bild 3: Konfokale Mikroskopie von Lungenkrebszellen A549.
Bild 3: Konfokale Mikroskopie von Lungenkrebszellen A549.Es ist jedoch anzumerken, dass nicht der gesamte Komplex in die Kerne von Krebszellen eingedrungen ist, sondern nur Ir1. Ein Immunfluoreszenztest zeigte, dass HSA in den Kernen von Zellen, die Ir1 ausgesetzt waren, einfach nicht vorhanden war.
 Bild Nr. 4: Immunfluoreszenzanalyse des Vorhandenseins von HSA in Lungenkrebszellen.
Bild Nr. 4: Immunfluoreszenzanalyse des Vorhandenseins von HSA in Lungenkrebszellen.Die HSA verschwindet jedoch nicht spurlos, sondern verbleibt einfach im Zytoplasma und in der Membran des Zellkerns der Krebszelle. Es stellt sich heraus, dass die HSA ihre Funktion vollständig erfüllt: Er lieferte Ir an den Zellkern und blieb draußen.
 Bild Nr. 5: Quantenausbeute und Lebensdauer der Ir1-Phosphoreszenz und des Ir1-HSA-Komplexes.
Bild Nr. 5: Quantenausbeute und Lebensdauer der Ir1-Phosphoreszenz und des Ir1-HSA-Komplexes.Die Wissenschaftler überprüften auch die Quantenausbeute (übertrieben, Stärke) und die Lebensdauer der Ir1-Phosphoreszenz (an sich) und des Ir1-HSA-Komplexes.
Die Quantenausbeute von Ir1 war sehr gering (nur 0,001) und die Lebensdauer bei einer Temperatur von 298 K betrug 182,7 Nanosekunden (
5a ). Die Ir1-CSA-Quantenausbeute betrug jedoch bereits 0,036 und die Lebensdauer 871,8 ns. Diese Dauer der Phosphoreszenz trägt zur Erzeugung von Singulettsauerstoff (
1 O
2 ) bei.
Elektronenparamagnetische Resonanzspektroskopie unter Verwendung von 2,2,6,6-Tetramethylpiperidin als Spinfalle half beim Nachweis der 1O2-Erzeugung in reinem Ir1 und im Ir1-HSA-Komplex bei 20-minütiger Bestrahlung bei 465 nm (
5b ). Wie erwartet war die 1O2-Quantenausbeute von Ir1-HSA signifikant höher (0,83) als die von Ir1 (0,06).
Es war auch notwendig, den Grad der Wirkung von Ir1-HSA und Ir1 auf Krebszellen und auf gesunde Zellen zu überprüfen. Drei Optionen wurden als Krebszellen verwendet: Lungenkrebs A549, Hepatom Hep-G2 und Cisplatin-resistenter Lungenkrebs A549R. Als gesunde Zellen wurden MRC-5 (Lunge) und LO2 (Leber) verwendet. Das Experiment wurde in zwei Beleuchtungsvarianten durchgeführt: völlige Dunkelheit während des gesamten Experiments und blaues Licht.
Die Zellen wurden 2 Stunden mit Ir1 oder Ir1-HSA inkubiert, mit Natriumperborat gewaschen und 20 Minuten mit blauem Licht bestrahlt oder im Dunkeln gelassen (zweites Experiment). Danach wurden die Zellen innerhalb von 46 Stunden wiederhergestellt.
Die Wirkung von Ir1 auf A549-Zellen im Dunkeln (89,6 uM) und unter Beleuchtung (53,3 uM) war praktisch nicht vorhanden.
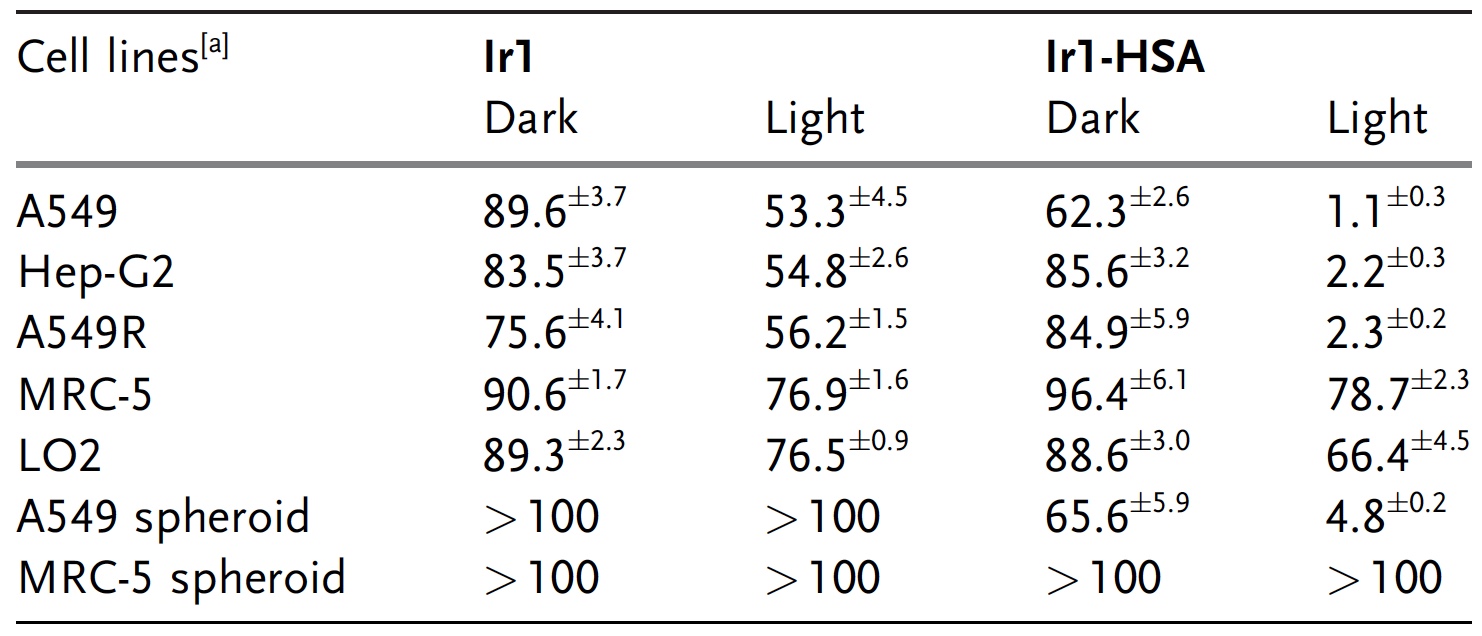 Tabelle der Wirkungen von Ir1 und Ir1-HSA auf Krebszellen: Je größer die Anzahl, desto weniger Exposition (d. H. Mehr Krebszellen blieben unversehrt).
Tabelle der Wirkungen von Ir1 und Ir1-HSA auf Krebszellen: Je größer die Anzahl, desto weniger Exposition (d. H. Mehr Krebszellen blieben unversehrt).Ir1-CSA zeigte jedoch sehr unterschiedliche Ergebnisse. Im Dunkeln wirkte sich der Testkomplex in keiner Weise auf Krebszellen aus, aber wenn er beleuchtet wurde, nahm seine Zytotoxizität signifikant zu. Ähnliche Ergebnisse, wie wir aus der obigen Tabelle sehen, zeigten Ir1 und Ir1-HSA in Bezug auf andere Krebszellen. Gleichzeitig waren gesunde Zellen im Dunkeln und unter Beleuchtung nicht von Ir1 und Ir1-HSA betroffen.
Schließlich führten die Wissenschaftler nach Belichtung eine Analyse der reaktiven Sauerstoffspezies (ROS) in Zellen durch. Im Dunkeln wurden erwartungsgemäß keine ROS festgestellt. In Zellen, die nach der Anwendung von Ir1-HSA einer leichten Bestrahlung unterzogen wurden, wurden ROS nachgewiesen (
5c ).
Für eine detailliertere Kenntnis der Studie empfehle ich dringend, dass Sie sich den
Bericht von Wissenschaftlern und
zusätzliche Materialien dazu ansehen.
NachwortMit dieser Studie haben Wissenschaftler nicht versucht, ein Fahrrad in Form der Verwendung seltener Metalle in der photodynamischen Therapie zu erfinden, da dies bereits früher mit Osmium und Palladium durchgeführt worden war. Bisher hat jedoch noch niemand versucht, Iridium zu verwenden, das die Forscher reparieren wollten. Ihre Arbeit war nicht nutzlos, da Iridium hervorragende Ergebnisse im Kampf gegen Krebszellen verschiedener Typen zeigte, ohne jedoch gesunde zu beeinträchtigen.
Onkologische Erkrankungen sind eine der häufigsten und fordern jedes Jahr Millionen von Menschenleben. Die Erfindung neuer Methoden zur Bekämpfung dieser Krankheit und die Verbesserung bestehender Methoden sollte und wird fortgesetzt werden. Natürlich sind wir noch weit von einem totalen Sieg über Krebs entfernt, aber Wissenschaftler auf der ganzen Welt setzen ihren Kampf in den Labors fort, wie Millionen von Patienten auf den Stationen.
Vergessen Sie auch nicht die Faktoren, die zum Auftreten von Krebs führen. Einige von ihnen (Ökologie, schlechte Gewohnheiten usw.) können von einer Person vollständig beseitigt werden.
Freitag offtopic:
Niemand, der bei klarem Verstand ist, wird sich über die Onkologie freuen. Solche Diagnosen lassen Sie aufgeben und alles vergessen. Aber du solltest niemals aufgeben. Wenn Sie nicht kämpfen, wird die Diagnose definitiv Vorrang haben. Aber wenn Sie die Krankheit bekämpfen, besteht immer die Möglichkeit, sie zu besiegen. Warum also nicht diese Chance nutzen?
Danke fürs Zuschauen, bleibt neugierig und habt ein tolles Wochenende euch allen, Jungs.
Vielen Dank für Ihren Aufenthalt bei uns. Gefällt dir unser Artikel? Möchten Sie weitere interessante Materialien sehen? Unterstützen Sie uns, indem Sie eine Bestellung
aufgeben oder Ihren Freunden empfehlen, einen
Rabatt von 30% für Habr-Benutzer auf ein einzigartiges Analogon von Einstiegsservern, das wir für Sie erfunden haben: Die ganze Wahrheit über VPS (KVM) E5-2650 v4 (6 Kerne) 10 GB DDR4 240 GB SSD 1 Gbit / s von $ 20 oder wie teilt man den Server? (Optionen sind mit RAID1 und RAID10, bis zu 24 Kernen und bis zu 40 GB DDR4 verfügbar).
VPS (KVM) E5-2650 v4 (6 Kerne) 10 GB DDR4 240 GB SSD 1 Gbit / s bis zum Frühjahr kostenlos, wenn Sie ein halbes Jahr bezahlen, können Sie
hier bestellen.
Dell R730xd 2 mal günstiger? Nur wir haben
2 x Intel Dodeca-Core Xeon E5-2650v4 128 GB DDR4 6 x 480 GB SSD 1 Gbit / s 100 TV von 249 US-Dollar in den Niederlanden und den USA! Lesen Sie mehr über
den Aufbau eines Infrastrukturgebäudes. Klasse mit Dell R730xd E5-2650 v4 Servern für 9.000 Euro für einen Cent?