
Aus welchem Büro in einem Krankenhaus schreien Kinder und manchmal Erwachsene von Zeit zu Zeit? Welche Eltern, die uns in ihrer Kindheit dreist täuschen, verglichen mit einem Mückenstich? Ich denke, Sie haben bereits vermutet, dass dies eine Blutuntersuchung ist. Jetzt ist dieser Vorgang schneller und weniger schmerzhaft geworden. Eines hat sich nicht geändert - seine Bedeutung. Die Diagnose in der Medizin spielt in den frühen Stadien des Kampfes gegen eine Krankheit die wichtigste Rolle. Um eine Krankheit zu besiegen, muss sie schließlich erst entdeckt werden. Nachdem Sie die Blutentnahme zur Analyse überstanden haben, machen Sie sich ruhig auf den Weg, um auf die Ergebnisse zu warten. Zu diesem Zeitpunkt analysieren Menschen in den Labors, die komplexe, sperrige und sehr teure Geräte verwenden, Ihr Blut und finden heraus, was in welcher Menge enthalten ist. Es ist gut, ein solches Labor in Ihrem örtlichen Krankenhaus zu haben, aber das ist nicht immer der Fall. Aber was wäre, wenn es ein kleines und kostengünstiges Taschenlabor gäbe, das gleichzeitig Proben mit der gleichen Genauigkeit und Effizienz wie ein gewöhnliches analysiert? Klingt nach Science Fiction, oder? Der Ausdruck „Taschenblutzuckeranalysator“ klang zu seiner Zeit ebenfalls futuristisch. Heute lernen wir die Forschung und Implementierung der Technologie zur quantitativen Analyse von Proteinen und Aminosäuren mit einem neuartigen Kompaktgerät kennen. Woraus besteht dieses Wunder, wie funktioniert es und wie effektiv? Antworten auf diese und andere Fragen erhalten wir im Bericht der Wissenschaftler. Lass uns gehen.
Studienbasis
Wir leben im Zeitalter der digitalen Technologie, die in verschiedenen Bereichen unseres Lebens erfolgreich umgesetzt wird. Laboruntersuchungen (diagnostisch) sind keine Ausnahme. Wissenschaftler stellen fest, dass die digitale Tropfanalyse 1000-mal genauer ist als herkömmliche Analysen und die parallele Durchführung von Millionen von Analysen innerhalb eines einzelnen Tropfens einer Probe mit einem in Femtolitern gemessenen Volumen (fl, 1 fl =
10-15 l) ermöglicht.
Die Verwendung der digitalen Analyse ist äußerst nützlich zum Nachweis von Nukleinsäuren und Proteinen, zur Analyse einzelner Zellen und sogar von Exosomen.
Exosomen * - extrazelluläre Vesikel (Durchmesser: 30-100 nm), die von Zellen in den Interzellularraum sekretiert werden. Exosomen sind an der Arbeit der Immunität, der Proteinsekretion usw. beteiligt.
Derzeit sind die bekanntesten digitalen Analysemethoden DELISA (Digital Enzyme Linked Immunosorbent Assay / DIA) und qPCR (Digital Polymerase Chain Reaction). Mit diesen Techniken können Sie mit einzelnen Zellen arbeiten und gleichzeitig sehr genaue Ergebnisse erhalten, die nicht korrigiert werden müssen. So wurde kürzlich mit diesen Methoden eine erfolgreiche quantitative Analyse von Protein und mRNA in einer Zelle gleichzeitig durchgeführt.
Ähnliche Techniken und eine Demonstration ihrer Talente zeigen einmal mehr, dass die Implementierung einer parallelen Analyse in einer extrem kleinen Umgebung (Stichprobe) durchaus möglich ist. Wie jede andere Technologie weisen diese Verfahren jedoch auch Nachteile auf. Sie sind ziemlich trivial - Abmessungen, Preis und Komplexität der Herstellung. Forscher erinnern uns daran, dass eine Installation für einen digitalen Verstärker (Quanterix's Simoa) etwa 100.000 US-Dollar kostet. Und nicht jede Privatklinik kann sich einen solchen Betrag leisten, ich schweige bereits über die staatlichen.
Natürlich ist Simoa von diesem "Biest" Quanterix sehr mächtig, wenn auch übertrieben. Es werden Tabletten mit Mikrozellen mit 200.000 Zellen zu je 40 fl verwendet.
 Quanterix Simoa
Quanterix SimoaGleichzeitig kann dieses Gerät bis zu 4 ELISA-Tabletten mit jeweils 96 Zellen parallel verarbeiten. Somit ist eine Vorrichtung in der Lage, die Ergebnisse von 66 Proben innerhalb einer Stunde zu erzeugen, von denen jede einer 10-Plex-Analyse unterzogen werden kann (d. H. 1 Probe wird gleichzeitig auf 10 Indikatoren analysiert). Die Zahlen sind wirklich unglaublich. Aber auch hier stellt sich die Frage nach dem Preis und den Abmessungen einer solchen Wundermaschine.
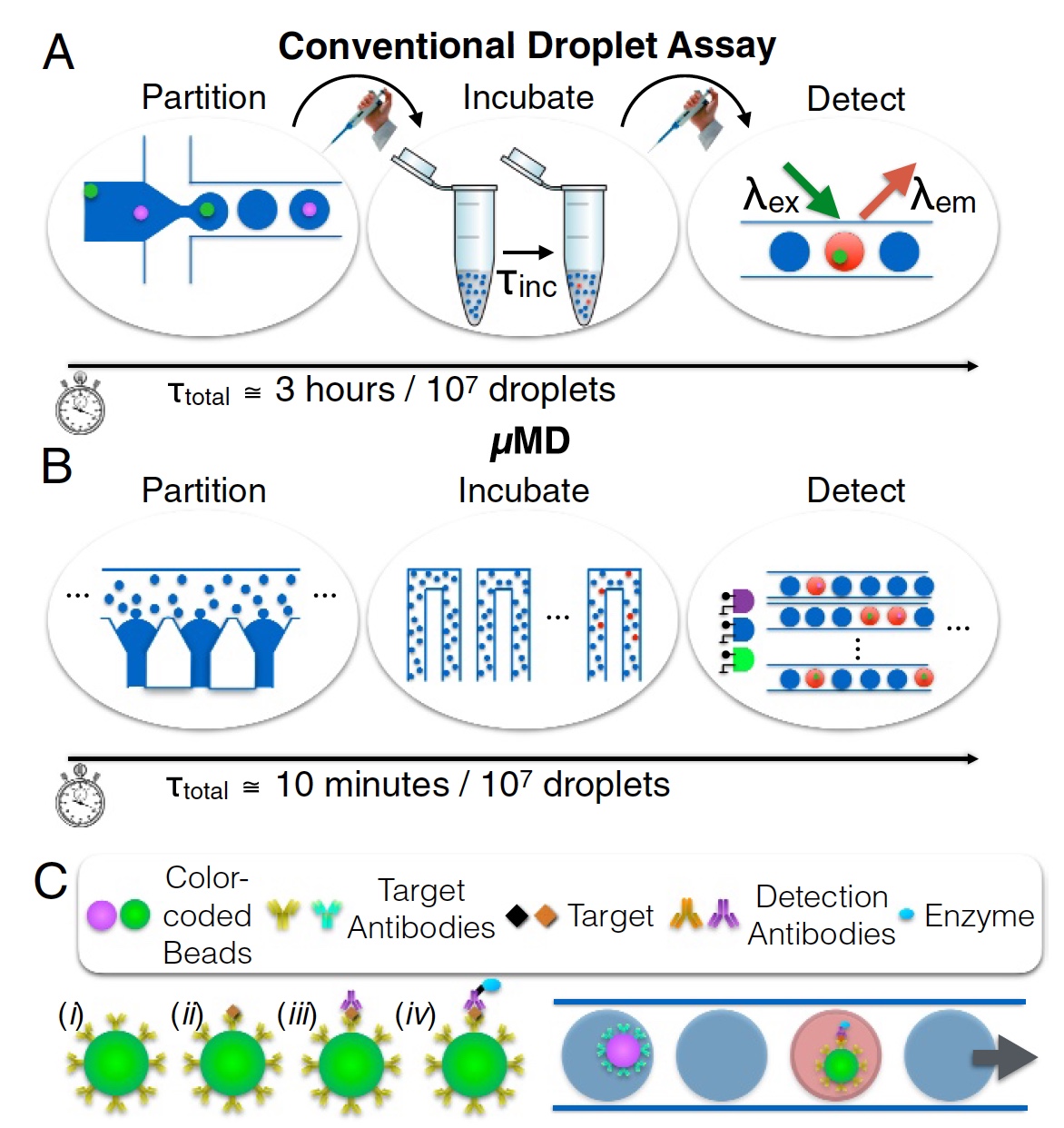 Bild Nr. 1
Bild Nr. 1Und hier schlagen Wissenschaftler vor, ihre Augen auf mikrofluidische Tropfensysteme zu richten. Klassische Systeme dieser Art können sich nicht der gewaltigen Leistung von Quanterix Simoa rühmen, sie können jedoch als Grundlage für ein neues Gerät dienen. Die kontinuierliche mikrofluidische Tröpfchentechnik kann theoretisch bis zu 1 Million Zellen analysieren. In der Praxis wurden solche Indikatoren jedoch aus mehreren Gründen noch nicht erreicht. Erstens Durchsatz (weniger als 104 Tropfen pro Sekunde), wenn Tropfen nacheinander (nicht parallel) erzeugt werden und monodispers sind. Zweitens wird die Fluoreszenzdetektion jedes Tropfens durchgeführt, indem sie einzeln durch einen Laserpunkt geleitet werden. Mit anderen Worten, alles ist nacheinander in einer Linie. Dieser Vorgang ist in Bild
1a dargestellt (Trennung, Inkubation und Bestimmung; 3 Stunden für die Analyse von 10
7 Tropfen).
Die Hauptprobleme bei der Umwandlung dieses Verfahrens in ein kompaktes Format sind die Schwierigkeit der Parallelisierung der Optik für die mehrfarbige Detektion der Fluoreszenz, die Komplexität der Integration des Probenvorbereitungsprozesses und die Notwendigkeit bestimmter Werkzeuge zur Erzeugung streng kontrollierter Tröpfchenströme. Wissenschaftler sind es jedoch nicht gewohnt, angesichts von Schwierigkeiten aufzugeben, egal wie beeindruckend sie sind.
Micro-Drop Megascale Detector (MD, Makro-Detektor) ist die Kreation unserer heutigen Helden. Dieses Gerät kann nicht nur in jedem mobilen (Taschen-) Gerät implementiert werden, sondern erfüllt auch die Standards der quantitativen Analyse gewöhnlicher Laboratorien in voller Größe. Der Prozess ist in Bild
1b dargestellt (Trennung, Inkubation und Bestimmung; 10 Minuten für die Analyse von 10
7 Tropfen).
Um dies zu erreichen, wurden nach Angaben der Forscher drei Hauptaufgaben umgesetzt:
- Anstatt jeweils 1 Tropfen zu erzeugen, wurde eine parallele Erzeugung von Mikrofluidik-Tröpfchen verwendet, die 100-mal schneller arbeiteten. Und die Leistungen von Kollegen auf dem Gebiet der Herstellung monodisperser Tropfen ( Link zu dieser Studie ) ermöglichten es, die Abhängigkeit der Monodispersität der Tropfen von der Durchflussrate zu beseitigen. Dies ermöglicht die Verwendung sehr kostengünstiger Schlauchpumpen, die in ein mobiles (Hand-) Gerät integriert werden können.
- Dank der Visualisierung auf der Basis eines Mobiltelefons, das 100-mal schneller ist als das herkömmliche Lesen (wenn Tropfen nacheinander gelesen werden), wurde ein schnelles Ablesen der Tröpfchenfluoreszenz mit einer Geschwindigkeit von mehr als 105 pro Sekunde (denken Sie an die oben erwähnte Grenze von 104) erreicht. In diesem Fall ist keine teure Optik erforderlich, und die Implementierung in mobilen Handheld-Geräten ist offensichtlich. Das Hauptunterscheidungsmerkmal dieser Innovation ist die Fähigkeit, die Einschränkungen der niedrigen Bildrate eines digitalen Bildes zu überwinden und eine Mehrfarben-Fluoreszenzdetektion bereitzustellen, indem mehrere Anregungsquellen von LEDs oder Laserdioden unterschiedlicher Farben mit einzigartigen nichtperiodischen Signalen moduliert werden. Video kann decodiert werden, um Tröpfchenfluoreszenzdaten zu erhalten und so die Grenzwerte für die Bildrate der Kamera zu überwinden. Somit ist es möglich, genau die (bereits erwähnten) Tropfen von 1 Million Tropfen pro Sekunde zu erreichen.
- Und schließlich die Integration der Verarbeitungseinheit von Mikrokügelchen (oder Mikrokügelchen, mikroskopisch kleinen kugelförmigen Objekten), eines Tröpfchengenerators, Verzögerungsleitungen für die Inkubation von Tröpfchen und eines Fluoreszenzdetektors. Alles in allem bietet dies ein kostengünstiges, kompaktes und effizientes Gerät zur Eingabe von unbehandeltem Serum (Probe) und zur Ausgabe molekularer Daten (Ergebnis).
Als Demonstration ihrer Erfindung implementierten die Wissenschaftler eine gemultiplexte DIGA unter Verwendung von Mikrogranulaten unterschiedlicher Farbe, die aus fluoreszierenden Farbstoffen erhalten wurden. Jede Farbe ist der Farbcode des Proteins, auf das der Mikrokügelchen-Antikörper abzielt (
1c ).
Eine Multiplex-Analyse von Serum-GM-CSF und IL6 im Serum wurde unter Verwendung von ultraviolettem und grün fluoreszierendem Granulat durchgeführt, wenn die Tropfen ein Mikrogranulat mit einem fluoreszierenden roten Immunkomplex enthielten. Rinderserum wurde als Medium für die quantitative Analyse verwendet, und die Bestimmungsgrenze betrug 0,004 pg / ml (Pikogramm pro Milliliter, 1 pg =
10–12 g). Dies ist 1000-mal genauer als der Standard-ELISA und entspricht dem Genauigkeitsgrad des digitalen ELISA.
Die Verarbeitung von 10 Millionen Tropfen dauert nur 10 Minuten. In diesem Fall umfasst der Prozess selbst die Erzeugung und Inkubation von Tropfen sowie den Nachweis fluoreszierender Tropfen für jede Probe.
Gerätestruktur und Analyseprozess
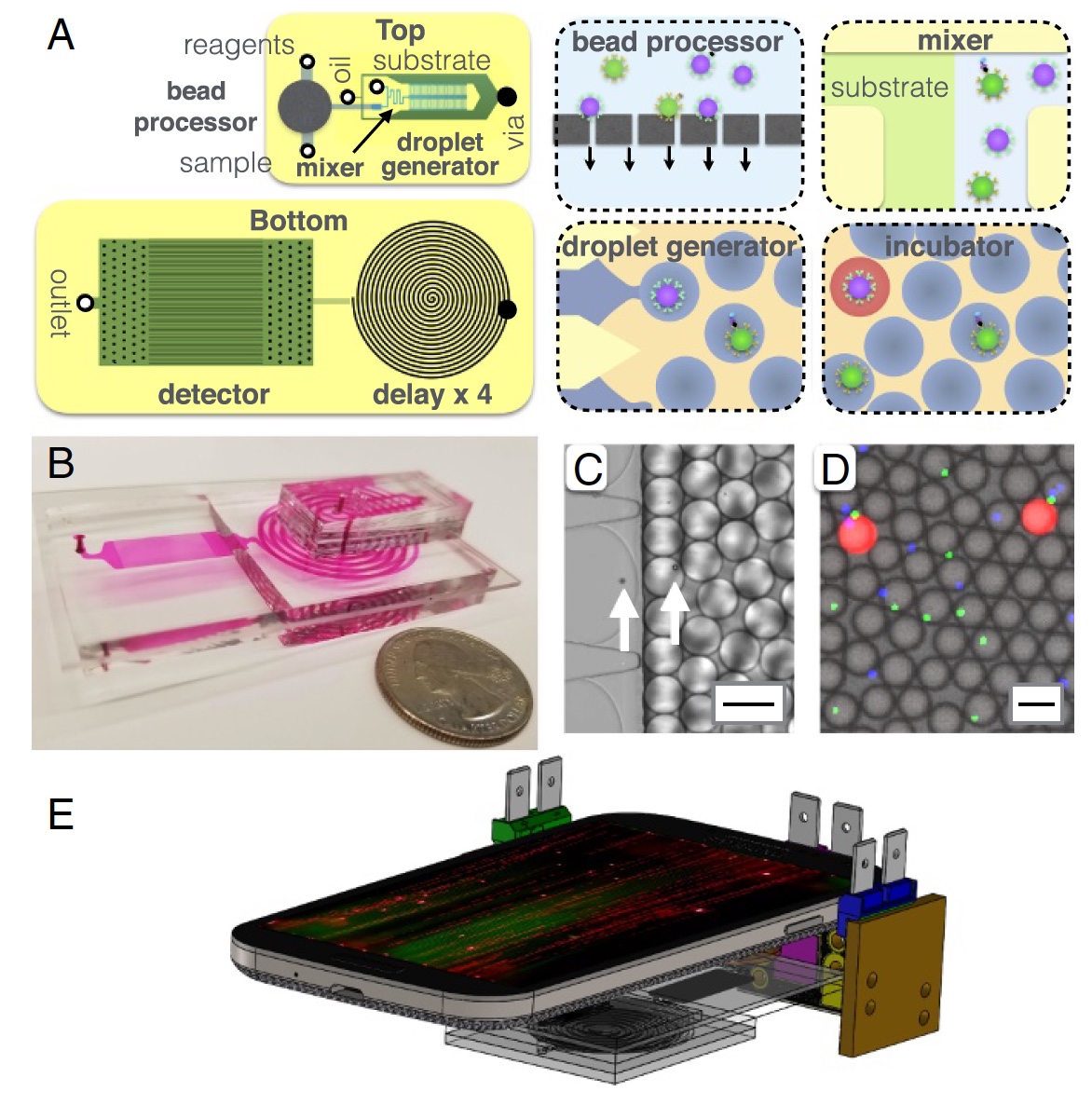 Bild 2: MD-Gerätestruktur.
Bild 2: MD-Gerätestruktur.Ein bisschen mehr über das Bild oben:
2a - Chipdiagramm, Draufsicht und Unteransicht;
2b ist ein Foto eines MD-Chips, auf dem alle Optofluidkanäle sichtbar sind;
2c ist eine mikroskopische Aufnahme des Prozesses des Einkapselens von Mikrokügelchen in Tröpfchen mit einem Durchmesser von 40 & mgr; m;
2d ist eine fluoreszenzmikroskopische Aufnahme von Tropfen nach einer Verzögerungslinie;
2e ist eine schematische Darstellung einer MD-Plattform (Mobiltelefon, 3 Lichtquellen und der MD-Chip selbst).
Die Hauptkomponenten von MD können als Mikrogranulat-Prozessor bezeichnet werden, bei dem letztere Zielproteine aus Serum einfangen. Danach werden die Granulate mit Immunkomplexen zur anschließenden Amplifikation innerhalb der Tröpfchen markiert. Zwischen jedem dieser Prozesse findet eine iterative (mehrfache) Reinigung statt. Ein Tröpfchengenerator ist ebenfalls vorhanden, bei dem die Mikrogranulate mit einem Enzymsubstrat gemischt und in Wasser-Öl-Tröpfchen eingekapselt werden.
Als nächstes kommt ein Mikrofluidikkanal, durch den Tröpfchen 3,2 Minuten lang laufen. Dieser Kanal ist als Verzögerung / Verzögerung des Prozesses notwendig, wodurch das Fluoreszenzsignal enzymatisch verstärkt werden kann. Der letzte Teil ist ein Detektor (oder Scanner), der auf einem Mobiltelefon (Kamera) basiert und bei dem die Fluoreszenz von Tröpfchen erfasst wird.
Der Mikrogranulatprozessor besteht aus einer semipermeablen Membran zur Immobilisierung des Granulats. Dem immobilisierten Granulat werden mehrere Reagenzien und Waschpuffer zugeführt. Danach wird das Granulat zur weiteren Analyse freigegeben.
Die Membran selbst besteht aus Polycarbonat. Eine geätzte Spur 300 mm
2 mit Poren von 3 & mgr; m Durchmesser wurde auf die Membran geätzt.
In diesem Experiment gab es zwei Gruppen von Mikrogranulaten: (d = 5,4 & mgr; m, ex / em = 470/490 nm, CFH-5052-2), funktionalisiert mit Anti-GM-CSF-Antikörper (MAB2172) und (d = 4,5 μm, ex / em = 370/410 nm, CFP-4041-2), funktionalisiert mit Anti-IL6-Antikörper (MAB206).
Zunächst durchlaufen die Mikrogranulate zusammen mit der Probe 1 Stunde lang den Inkubationsprozess und werden erst danach auf der oben genannten Membran eingefangen.
In diesem Stadium (innerhalb der Membran) wird das Granulat mit 1 ml T20-Puffer bei einer Flussrate von 10 ml / h gewaschen, mit 0,1 ml 0,7 nM Nachweisantikörper in T20-Puffer 0,5 Stunden inkubiert und erneut in 1 ml T20-Puffer gewaschen bei 10 ml / h und danach werden sie durch Ändern der Flussrate auf 6 ml / h aus der Membran freigesetzt.
Danach werden die freigesetzten Mikrokügelchen mit einem ELISA-Substrat gemischt und in Tröpfchen mit einem Durchmesser von 40 µm eingekapselt. Um ein genaues Mischen von Granulat und Substrat sicherzustellen und das Hintergrundsignal von Enzymen, die ein Fluoreszenzsignal erzeugen, zu minimieren, wird ein spezieller Kanal mit einer Länge von 14 mm verwendet.
Der Tröpfchengenerator ist so ausgelegt, dass der Tröpfchendurchmesser unabhängig von der Durchflussmenge ist. Dieses Gerät verfügt nur über 100 dieser Generatoren, die am Ausgang einen Durchsatz von 100.000 Tropfen pro Sekunde ergeben.
Jeder Tropfen ist entweder mit 1 Granulat eingekapselt oder bleibt unberührt. Gleichzeitig wird eine bestimmte Konzentration erreicht - 10 Tropfen mehr als Mikrogranulat (zum Beispiel 20 Tropfen - 10 mit Granulat und 10 ohne). Dies verringert die Wahrscheinlichkeit, dass in einem Tropfen zwei Körnchen vorhanden sind, um bis zu 0,5%.
Nach den Tröpfchengeneratoren gibt es eine Verzögerungsleitung ähnlich einer Spirale mit einer Kanalbreite von 1,8 mm und einer Höhe von 1,5 mm. Die Verzögerungsleitung sollte lang genug sein, aber Sie können das Gerät nicht vergrößern. Daher wurden 4 Spiralen einzeln hergestellt, um vollständig zu passieren, wobei bei einer Flussrate von 67 ml / h die Tropfen 3,2 Minuten dauern würden.
Um ein solches Gerät in eine mobile Plattform einzuführen, mussten bestimmte Aufgaben im Zusammenhang mit der Kamera des Telefons gelöst werden. Die Verwendung einer üblichen zeitkonstanten Lichtanregung führt dazu, dass Tröpfchen, die sich im Sichtfeld der Kamera bewegen, als Streifen dargestellt werden. Die Länge dieses Streifens legt den Mindestabstand zwischen den Tröpfchen fest und begrenzt somit den Durchsatz erheblich.
Wenn wir eine Lichtanregung mit einer pseudozufälligen Sequenz (in der Zeit) verwenden, können wir einzelne Tropfen „sehen“. Die Modulationsgeschwindigkeit des Lichts beträgt das 10-fache der Belichtungszeit der Kamera. Aufgrund dieses Unterschieds bilden Tröpfchen Streifen, deren Abstand (drei Tröpfchendurchmesser) für ihre individuelle Bestimmung ausreicht. In diesem Fall können Sie 120 parallele Tropfkanäle vor der Kamera überspringen.
Ein weiterer wichtiger Punkt beim Erfassen und Scannen ist die Fluoreszenz. Zur Durchführung eines Multiplex-ELISA werden mehrere unterschiedliche Fluoreszenzsignale benötigt. Hierzu wurden 3 Lichtquellen gleichzeitig verwendet, von denen jede die zur Anregung eines bestimmten Fluoreszenzfarbstoffs erforderliche Wellenlänge aufweist. Dieses Dreifachsystem besteht aus zwei Diodenlasern (blau, grün) und einer LED (UV).
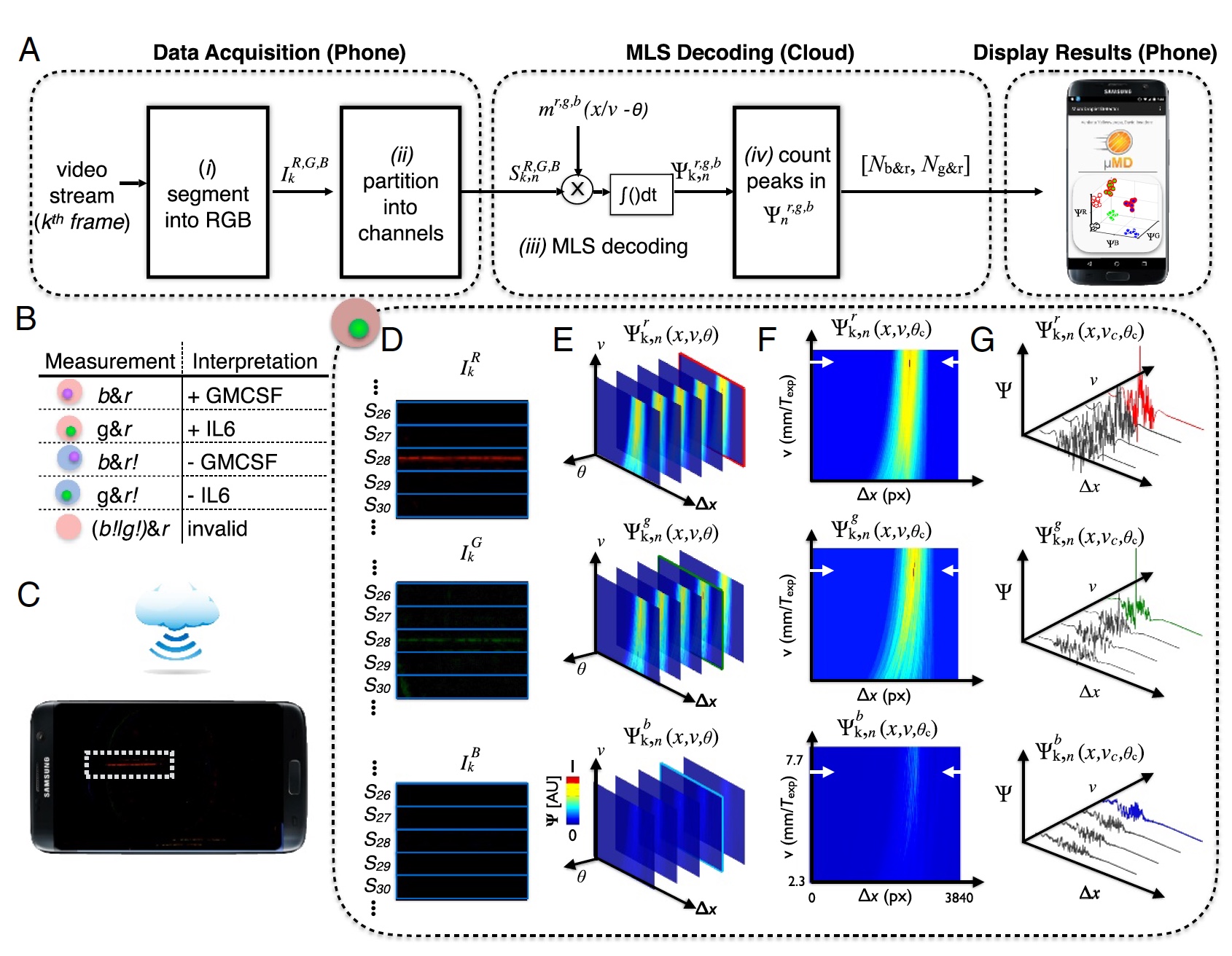 Bild Nr. 3: „Probenergebnis“ -Prozess (Dekodieren von Daten von der Kamera des Telefons).
Bild Nr. 3: „Probenergebnis“ -Prozess (Dekodieren von Daten von der Kamera des Telefons).Für eine genaue Dekodierung des Videos von der Kamera des Telefons war es erforderlich, eine Korrelationserkennung für die drei erwarteten Modulationsmuster (
m ) durchzuführen, die jeder der drei Lichtquellen entsprechen.
Das Ergebnis war ein Korrelationsvektor (
3a ), wobei:
k - Rahmen;
n = 1: 120 Kanäle im Gerät;
R ,
G ,
B - Farbkanäle der Digitalkamera;
r ,
g ,
b - Farbanregung.
Das Tröpfchenmuster wurde durch eine maximale Längensequenz (MLS) mit | m | erzeugt = 63 Bits. Darüber hinaus ist jedes Bit in einem digitalen Bild 10 Pixel groß, dh insgesamt 63 Bit sind 630 Pixel (1/3 eines Rahmens im Jahr 1920).
Ein Fluoreszenzscan ist erforderlich, um festzustellen, ob ein Tropfen ein Mikrogranulat enthält, wenn ja, um die Farbe zu bestimmen (UV- oder Grünprotein, Rotzielmolekül). Nach Erhalt dieser Daten müssen sie extrahiert werden. Zu diesem Zweck wird der Videorahmen gemäß den Sensoren der Kamera (
3d ) in rote, grüne und blaue Komponenten unterteilt.
Dieses Gerät verwendete Cloud-Technologie. Dies wurde durchgeführt, um die Belastung des Bügeleisens (dh des Telefons selbst) zu verringern. Anstatt die Tröpfchengeschwindigkeit oder -phase zu steuern, wurde Cloud Computing durchgeführt, um Tröpfchen mit einer unbekannten Phase oder Geschwindigkeit (
3s ) zu bestimmen. Nach der Bestimmung der optimalen Phasen und der Tröpfchengeschwindigkeit kann man die Peaks im Korrelationsraum Ψr
, g, bk, n (x, υc, θc) (
3f und
3g ) genau bestimmen.
Die gesammelten Daten werden in eine spezielle Anwendung (bisher nur unter Android) hochgeladen, die sie zur Verarbeitung mit MATLAB auf einem Remote-Server an die Cloud sendet. Danach werden die bereits verarbeiteten Daten an das Smartphone zurückgegeben und auf dem Bildschirm angezeigt.
Nach all den Vorbereitungs- und Testarbeiten beschlossen die Wissenschaftler, unter Beteiligung ihrer Kreation und des vorhandenen kommerziellen Full-Size-Geräts Simoa ein „Sparring“ durchzuführen.
Im Testduell wurden drei Versionen des Arbeitsmediums verwendet: PBS - Natriumphosphatpuffer, FBS - fötales Rinderserum und menschliches Blutserum. Der wichtigste Indikator war die Nachweisgrenze (LOD), dh der Mindestgehalt des Analyten in der Probe.
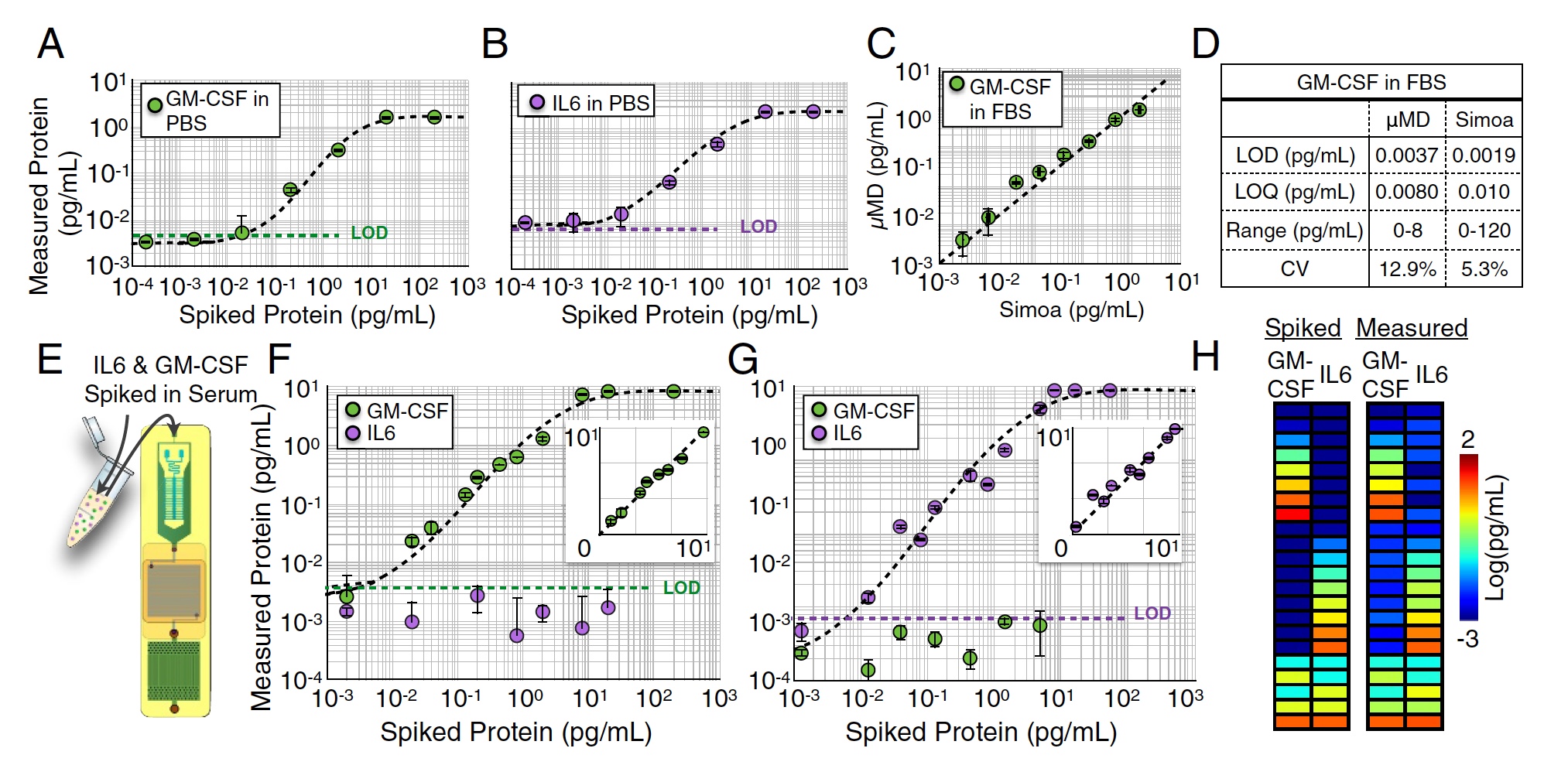
Testergebnisse für MD-Chips.
Mehrere Einzelplex-Messungen von M-CSF (Bild
A oben) und IL6 (Bild
B ) wurden in PBS-Medium durchgeführt, indem Reihenverdünnungen von 104 bis 102 pg / ml gemessen wurden. In diesem Test wurden sehr gute Nachweisgrenzen erhalten: LOD = 0,0045 pg / ml für GM-CSF und LOD = 0,0070 pg / ml für IL6.
Ähnliche Messungen wurden auch in FBS-Lösung (1: 4) durchgeführt. Zu diesem Zeitpunkt wurde die zu analysierende Probe zwischen dem untersuchten Gerät und dem kommerziellen "Schwergewicht" Simoa in zwei Hälften geteilt. Infolgedessen zeigte die Schaffung von Wissenschaftlern hervorragende Ergebnisse, die denen von Simoa praktisch nicht unterlegen waren (R2 = 0,95, Bild
C oben).
Aber es war eine One-Plex-Analyse, dh eine Analyse eines Indikators. Nun musste überprüft werden, wie der MD-Chip mit der parallelen Analyse mehrerer Proteine, dh mit der Duplex-Analyse von GM-CSF und IL6 gleichzeitig, fertig wird. Zunächst wurde dem FBS eine bestimmte Menge GM-CSF zugesetzt, und die IL6-Konzentration war Null (Bilder
F und
G ). Dann wurde das Gegenteil getan: Null-Konzentration von GM-CSF und etwas IL6.
In beiden Fällen unterschied sich die Nachweisgrenze nicht wesentlich von den Ergebnissen der zuvor durchgeführten Ein-Plex-Analyse (p> 0,88 für GM-CSF und p> 0,90 für IL6).
Danach wurde der Probe eine bestimmte Menge von GM-CSF und IL6 (Bild h) zugesetzt. Die Nachweisgenauigkeit war ausgezeichnet - R2> 0:99 für GM-CSF und R2> 0:99 für IL6.
Der signifikanteste Test war die Analyse von Humanserum. Von 14 Probanden wurden Blutproben entnommen. Die Forscher quantifizierten den GM-CSF und IL6 dieser Proben unter Verwendung eines MD- und Simoa-Chips.
 Quantitative Ergebnisse von Humanserum GM-CSF und IL6 unter Verwendung von MD und Simoa.
Quantitative Ergebnisse von Humanserum GM-CSF und IL6 unter Verwendung von MD und Simoa.Die Ergebnisse der Analyse mit dem MD-Chip lagen sehr nahe an den Ergebnissen von Simoa (R2 = 0: 96), dem derzeit genauesten Analysegerät.
Demonstration des Gerätes.Um die Nuancen und Details der Studie genauer kennenzulernen, empfehle ich Ihnen, den
Bericht der Forschungsgruppe und
zusätzliche Materialien zu lesen.
Nachwort
Geschwindigkeit spielt in der Medizin eine große Rolle. Je schneller die genaue Diagnose gestellt wird, desto schneller können Sie mit der Behandlung beginnen. Manchmal geht es nicht einmal um Tage, sondern um Minuten, die nicht verschwendet werden können. , - . , , .
, MD, , . , , , . 500 . - 5.
, . .
, , .
Vielen Dank für Ihren Aufenthalt bei uns. Gefällt dir unser Artikel? Möchten Sie weitere interessante Materialien sehen? Unterstützen Sie uns, indem Sie eine Bestellung
aufgeben oder Ihren Freunden empfehlen, einen
Rabatt von 30% für Habr-Benutzer auf ein einzigartiges Analogon von Einstiegsservern, das wir für Sie erfunden haben: Die ganze Wahrheit über VPS (KVM) E5-2650 v4 (6 Kerne) 10 GB DDR4 240 GB SSD 1 Gbit / s von $ 20 oder wie teilt man den Server? (Optionen sind mit RAID1 und RAID10, bis zu 24 Kernen und bis zu 40 GB DDR4 verfügbar).
VPS (KVM) E5-2650 v4 (6 Kerne) 10 GB DDR4 240 GB SSD 1 Gbit / s bis zum Sommer kostenlos, wenn Sie für einen Zeitraum von sechs Monaten bezahlen, können Sie
hier bestellen.
Dell R730xd 2 mal günstiger? 2 Intel Dodeca-Core Xeon E5-2650v4 128GB DDR4 6x480GB SSD 1Gbps 100 $249 ! Lesen Sie mehr über
den Aufbau eines Infrastrukturgebäudes. Klasse mit Dell R730xd E5-2650 v4 Servern für 9.000 Euro für einen Cent?