Die vorherige Veröffentlichung erhielt eine negative Bewertung mit dem Wortlaut „Warum solche elementaren Dinge hier posten“. Daher warne ich sofort, dass dieses Material in erster Linie für Schüler gedacht ist, die anfangen, Chemie zu studieren. Und auch für diejenigen, die dieses Thema in ihren Schuljahren nicht verstanden haben. Ich würde einen Artikel über eine beliebte Fachressource für Schulkinder veröffentlichen, wenn es sie gäbe.
Und ja, mir ist die Existenz eines Atommodells bekannt, bei dem das Elektron eine Wahrscheinlichkeitswelle in der Nähe des Kerns ist. In der Regel ist es für einen Schüler jedoch schwierig, sich vorzustellen, wie die Wahrscheinlichkeit Atome zu Molekülen verbinden kann. Deshalb sage ich "an den Fingern".
Die Verbindung von Atomen zu MolekülenUnsere Welt existiert nicht in Form von getrennten Atomen, sie verbinden sich irgendwie miteinander. Welches?
Nimm zwei Wasserstoffatome. Jedes von ihnen enthält ein Proton und ein Elektron, so dass die Gesamtladung jedes dieser Atome Null ist.
Anhängergesetz
F = k * q1 * q2 / r ^ 2sagt uns, dass neutrale Körper nicht voneinander angezogen werden sollten
(q1 = 0, q2 = 0) .
Wasserstoff (und jedes andere chemische Element) sollte also nur in Form von Atomen existieren und sich niemals zu Molekülen verbinden. Tatsächlich verbinden sich Wasserstoffatome immer paarweise. Warum?
Nehmen wir zwei Metallstücke und ordnen sie in geringem Abstand parallel an.

Beide Segmente enthalten die gleiche Anzahl von Protonen und Elektronen, daher ist die Gesamtladung von jedem von ihnen gleich Null. Sie haben also keinen Grund zur gegenseitigen Anziehung.
Wir wissen, dass in Metallen ein Teil der externen Elektronen ihre Atome verlässt und frei zwischen den Ionen (verlassenen Atomen) des Kristallgitters des Metalls wandert. Und diese Elektronen sind im Durchschnitt gleichmäßig verteilt.
Stellen Sie sich vor, wir haben es irgendwie geschafft, einen Teil dieser freien Elektronen auf die linke Seite des unteren Metallsegments zu bewegen. Außerdem wird es auf der rechten Seite ein Defizit an Elektronen geben.

Wir haben den sogenannten Dipol: Die linke Seite des Segments ist negativ geladen, die rechte ist positiv. Großartig. Und was wird im oberen Segment passieren? Wir wissen, dass sich die gleichen Ladungen gegenseitig abstoßen, während sich die anderen anziehen. Folglich gehen die Elektronen des oberen Segments ausgehend von den elektrischen Feldern der Elektronen des unteren Segments nach rechts. Das heißt, das Bild der Verteilung der Elektronen in diesen beiden Metallsegmenten wird zum Spiegel:
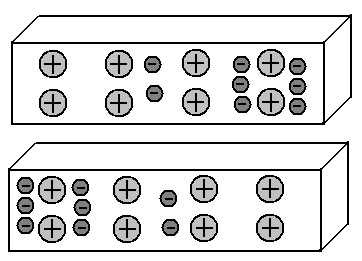
Dieser Effekt geladener Objekte auf benachbarte Objekte, der zu einer Umverteilung der Ladungen in diesen führt, wird als elektrostatische Induktion bezeichnet.
Das Interessanteste: Die positiv geladenen Atomkerne auf der linken Seite des oberen Segments waren gegenüberliegende Elektronen, die auf der linken Seite des unteren Segments gesammelt wurden. Und die entgegengesetzten Ladungen werden angezogen. Die linken Teile der Segmente ziehen sich also an!
Das gleiche passiert auf der rechten Seite der Segmente - nur gespiegelt. Und die rechten Enden der Segmente werden auch voneinander angezogen. Wunderbar, nicht wahr? Die Umverteilung der Ladungen innerhalb eines der Leitersegmente hat zur gegenseitigen Anziehung dieser beiden Segmente geführt!
Aber was passiert, wenn wir jetzt die freien Elektronen des unteren Segments an sein rechtes Ende bewegen? Dann bewegen sich die freien Elektronen des oberen Segments zum linken Ende. Das heißt, wenn wir Elektronen in einem der Segmente hin und her bewegen, bewegen wir die Elektronen des benachbarten Segments, das in keiner Weise mit dem ersten verbunden ist! Ein solcher Effekt der Bewegung von Elektronen in einem Leiter auf die Bewegung von Elektronen in einem benachbarten Leiter wird als elektrodynamische Induktion bezeichnet.
Obwohl dies für unser Thema nicht gilt, stellen wir fest, dass wir in etwas vereinfachter Form untersucht haben, wie Antenne und Empfänger während der Funkübertragung funktionieren.
Wir können diese beiden Metallteile unterschiedlich anordnen - wobei die Enden einander zugewandt sind:

Wenn wir zum Beispiel die Elektronen auf die rechte Seite des linken Segments bewegen können, bewegen sich die Elektronen des rechten Segments ausgehend von ihnen auch auf die rechte Seite des rechten Segments:

Und in diesem Fall beginnen sich diese beiden Metallstücke gegenseitig anzuziehen, da ihre proximalen Enden die entgegengesetzte Ladung haben. Es ist besonders zu beachten, dass in der zweiten Variante der Anordnung der Segmente die Kraft ihrer gegenseitigen Anziehung schwächer ist, da nur ihre entgegengesetzten Enden angezogen werden, während in der ersten Variante der Anordnung der Segmente sowohl links als auch rechts voneinander angezogen werden die Enden.
Aber wie hängt das mit der Bindung von Atomen zusammen? Schauen wir uns das Wasserstoffatom an. Es hat ein Elektron, das sich um den Kern bewegt. Und wenn das zweite Wasserstoffatom in der Nähe ist, bewirkt dieses Elektron, dass sich das Elektron des Nachbarn auf die gleiche Weise bewegt wie in unseren Metallsegmenten - während sich das Elektron eines der Atome auf einer Seite des Atomkerns befindet, muss sich das benachbarte auf der gegenüberliegenden Seite seines Atoms befinden.
Hier ist der Einfluss natürlich nicht einseitig, sondern gegenseitig - sowohl das erste Elektron beeinflusst das zweite als auch das zweite das erste. Das Wichtigste ist jedoch, dass diese beiden Atome auf die gleiche Weise angezogen werden, wie zwei Metallstücke in der zweiten Variante ihrer gegenseitigen Anordnung (mit einander zugewandten Enden) angezogen wurden.
Das Wesentliche ist dasselbe: Die Elektronen werden voneinander ferngehalten, so dass entgegengesetzte Ladungen voneinander angezogen werden können. Stellen Sie sich vor, das Elektron eines der Atome befand sich zwischen den Kernen zweier benachbarter Atome, während sich das Elektron des benachbarten Atoms am entgegengesetzten, entfernten Punkt der Umlaufbahn befand:

Jetzt haben wir ein negativ geladenes Elektron zwischen zwei positiv geladenen Atomkernen. Die Kerne beider Atome werden von diesem Elektron angezogen. Somit bindet ein Elektron derzeit zwei Atome.
Der Abstand zwischen den Atomkernen ist größer als der Abstand zwischen den einzelnen Kernen und dem zwischen ihnen befindlichen Elektron. Und wir erinnern uns, dass die Kraft der Wechselwirkung von Ladungen umgekehrt proportional zum Quadrat des Abstandes zwischen ihnen ist. Daher ist im Moment die Anziehungskraft der Kerne auf das Elektron größer als die gegenseitige Abstoßung der Kerne.
Aber die Elektronen bewegen sich ständig, und deshalb verlässt das erste Elektron nach einer Weile den Raum zwischen den Kernen, aber das zweite Elektron bewegt sich dorthin. In diesem Moment geht die Rolle des Bindemittels auf das Elektron des zweiten Atoms über (Moment 3 in der folgenden Abbildung).

Es ist zu beachten, dass zu den in den 2 und 4 gezeigten Zeitpunkten keine Elektronen zwischen den Atomkernen vorhanden sind. In diesen Momenten stoßen sich die Kerne gegenseitig ab. Aus diesem Grund variiert der Abstand zwischen Atomen - er ändert sich ständig während der Rotation der Elektronen um die Kerne, aber seine durchschnittliche Länge, die als Bindungslänge bezeichnet wird, bleibt erhalten. Die Bindungslänge - der Abstand zwischen den Atomkernen - ist für jedes Paar von Atomtypen, die zu einem Molekül zusammengefasst sind, individuell.
Die Elektronen dieser beiden Atome im gebildeten Wasserstoffmolekül versuchen so weit wie möglich voneinander entfernt zu sein, genau wie in Metallsegmenten. Aufgrund dessen tritt ihre Synchronisation auf - ihre Position relativ zueinander bei jeder Umdrehung um die Kerne ist ungefähr gleich.
Dies erinnert etwas an die kollektive Leistung eines Walzers, wenn sich die Paare mit der gleichen Geschwindigkeit drehen, so dass weder die Damen noch die Herren jemals nebeneinander stehen, sondern sich immer abwechseln:

Dieser Artikel ist ein Auszug aus dem Buch
"Clear Chemistry".Heilige Unsicherheit und heilige WahrscheinlichkeitDie Quantentheorie behauptet, dass es unmöglich ist, gleichzeitig den genauen Ort eines Elektrons im Raum und seinen Impuls (Richtung und Geschwindigkeit seiner Bewegung) zu bestimmen. Daher wird angenommen, dass es um den Kern eines Atoms bestimmte Stellen (Bereiche) gibt, an denen die Wahrscheinlichkeit, ein Elektron zu detektieren, hoch ist. Diese Bereiche werden Elektronenorbitale genannt.
Diese Theorie ist an einem Haushaltsbeispiel nicht schwer zu erklären. Angenommen, Sie wohnen in einer Wohnung, in der sich ein Schlafzimmer, eine Küche und ein Badezimmer befinden. Wenn Sie 90% der Zeit im Schlafzimmer, 8% der Zeit in der Küche und 2% der Zeit im Badezimmer verbringen, kann Ihr Orbital als Schlafzimmer und Küche betrachtet werden, da die Wahrscheinlichkeit, Sie im Badezimmer zu finden, sehr gering ist. Nach 100 Beobachtungen von Ihnen zu verschiedenen Zeitpunkten wird der Beobachter Sie höchstwahrscheinlich in 90 Fällen im Schlafzimmer und in 8 Fällen in der Küche finden. Und anhand dieser Zahlen wird eine Schlussfolgerung über das Gebiet Ihres Lebensraums gezogen.
Nun darüber, warum es unmöglich ist, gleichzeitig den Ort eines Elektrons im Raum und seine Geschwindigkeit sowie die Bewegungsrichtung zu bestimmen. Es ist noch einfacher. Tatsache ist, dass die Geschwindigkeit nur auf einem bestimmten
Abschnitt der zurückgelegten Strecke gemessen werden kann. Wenn wir die Länge dieses Segments durch die Zeit dividieren, für die es vergangen ist, können wir die Bewegungsgeschwindigkeit ermitteln. Wir können jedoch keinen Raumabschnitt als Ort des Körpers betrachten. Der Ort ist die genaue Koordinate des Körpers.
Stellen Sie sich eine Fliege vor, die in einem dunklen Raum fliegt. Indem wir den Raum mit einem sehr kurzen Lichtblitz beleuchten, können wir den Ort sehen, an dem sich die Fliege gerade befindet. Aber um zu verstehen, wo und mit welcher Geschwindigkeit es fliegt, müssen wir das Licht für eine längere Zeit einschalten. Dann werden wir eine Änderung der Position der Fliege im Laufe der Zeit sehen und in der Lage sein, die Geschwindigkeit dieser Änderung abzuschätzen. In diesem Fall können wir jedoch nicht mehr genau angeben, wo sich die Fliege während der Messung ihrer Geschwindigkeit befand, da sie sich während dieser Zeit um eine bestimmte Strecke bewegt hat. Das ist der springende Punkt des Unsicherheitsprinzips.
Elektronen, die sich um Atomkerne bewegen, ändern sehr schnell die Geschwindigkeit und Bewegungsrichtung, so dass es unmöglich ist, genau zu sagen, wo sie sich zu einem bestimmten Zeitpunkt befinden und wo sie sich bewegen.
Und in dem oben diskutierten Modell bewegen sich Elektronen wie Pfeile in einer Uhr. Und dies kann nur den gerechten Zorn der Anhänger der Heiligen Unsicherheit und der Heiligen Wahrscheinlichkeit verursachen.
Die Tatsache, dass wir nicht genau sagen können, wo sich dieses oder jenes Elektron befindet und zu welchem der Atome es „gehört“, ändert jedoch überhaupt nichts am elektrostatischen Mechanismus der Atombindung. Es ist unmöglich, zwei Protonen anders zu binden, als ein Elektron zwischen ihnen zu platzieren. Keine Wahrscheinlichkeit oder Unsicherheit kann Atome zu einem Molekül verbinden. Und es zeigt perfekt das molekulare Wasserstoffion H2 +. In diesem Ion gibt es weder ein Elektronendublett noch eine Kompensation der Spins gepaarter Elektronen oder eine Überlappung von Elektronenwolken. Dieses Ion existiert jedoch und ist stabil.
Vergessen Sie außerdem nicht, dass dies nur ein Modell ist und die „Erklärungsmöglichkeiten“ sowie die Fähigkeiten anderer Modelle begrenzt sind. Zum Beispiel erklärt es (wie es scheint) nicht, warum Wasserstoffatome sich nicht zu langen Ketten wie H3, H4 usw. verbinden können.
Wir können jedoch annehmen, dass aufgrund der Tatsache, dass die elektronischen Orbitale in den Wasserstoffmolekülen in die Mitte des Moleküls verschoben sind, sie nicht aus ihren Enden "herausragen" und daher benachbarte Wasserstoffmoleküle nicht in der Lage sind, unter Verwendung des Elektronensynchronisationsmechanismus aneinander zu haften.