Es gibt Wissensbereiche, die "nicht mit einem gemeinsamen Arshin gemessen werden können ...". Im Prinzip können Sie in meinem Heimatgebiet, der Kolloidchemie, unter dieser Richtung jedes grundlegende Konzept sicher platzieren, sei es Adsorption (mit Adsorbentien) oder Adhäsion (mit Klebstoffen). Ehrlich gesagt hatte ich keine Idee, über Leim zu schreiben. Aber wenn Leser in jedem Thema, das mit Polymeren zu tun hat, anfangen, nach Klebstoffen zu fragen, werden Sie unwillkürlich darüber nachdenken (natürlich möchte ich darüber parieren, dass „alles mit Sekundenkleber verklebt werden muss“). Adhäsion und Klebstoffe sind ein sehr breites Thema, daher habe ich mich immer noch entschlossen, es anzugehen, aber die Geschichte in mehrere Teile zu zerlegen. Heute ist der erste Teil ein einleitender informativer Teil. Um herauszufinden, worauf der Klebstoff klebt, welche Art von Klebstoff ist und welche Art von Klebstoff am besten zum Verkleben geeignet ist _____ (geben Sie ein, was Sie benötigen), gehen wir traditionell unter den Schnitt (und setzen ihn in Lesezeichen).

Bevor ich mit meiner Geschichte beginne, möchte ich eine kleine Exkurs-Widmung machen:
Memory Colloidal ChemistMein Leiter der Abschlusspraxis reagierte gern auf die Angriffe meiner Kollegen "Es gibt jetzt keine vernünftigen Schüler ..." mit dem Satz "Es gibt keine schlechten Schüler, es gibt einen Lehrer, der seinen falschen Platz einnimmt". Zunehmend stimme ich diesem Satz zu. Die Schüler fühlen sich im Fachgebiet aufrichtig und beherrscht und „stimmen“ mit Respekt und Anwesenheit ab.
Die belarussische Wissenschaft wurde nach dem Zusammenbruch der UdSSR im Allgemeinen zu einer Sache für sich, seltsam und manchmal sogar wild. Es ist nicht verwunderlich, dass viele belarussische Wissenschaftler in der Regel „in engen Kreisen weithin bekannt“ sind, nicht öffentliche Personen usw. Obwohl die Arbeit interessant war. Aber häufiger können trockene biografische Informationen zu einem selbst erstellten Layout der HTML-Site des Instituts nicht einmal annähernd sagen, was die Person war. Der Doktor der chemischen Wissenschaften, Professor
Thomas Fomich Mozheiko, war also ein besonderer Mann. Ohne falsche Bescheidenheit können wir sagen, dass das gesamte Soligorsk Klondike mit Hilfe seiner Hände und eines hellen Kopfes gebaut wurde. Ich hatte die Gelegenheit, diese Person zum ersten Mal zu treffen, als ich das Kandidatenminimum in der Kolloidchemie überschritten hatte. Danach begannen wir auf freundliche Weise, eng miteinander zu kommunizieren. Angesichts der Tatsache, dass die Postgraduierten in unserem Forschungsinstitut trotzig „auf keinen Fall“ waren, beeindruckte mich dies ... und vielleicht dank eines Treffens mit diesem Großvater, der kurz die Essenz des kompliziertesten Prozesses erklären und davon überzeugen konnte, dass unser gemeinsamer Bereich - Die Königin der Chemie, ich schreibe gerade einen chemischen Artikel über Habr und reibe mir nicht die Hosen für die Entwicklung oder das Testen ... Um ehrlich zu sein, sollten alle Artikel über kolloidale Themen mit einer Bemerkung versehen sein: „In Erinnerung an F.F. Mozheiko “, weil dieser Mann einer meiner Meister war. Helle Erinnerung an dich, F.F.!

Leim wird seit jeher vom Menschen verwendet. Man kann davon ausgehen, dass der Countdown der Klebepraxis begann, sobald ein primitiver Mann die Silikonspitze seines Speers mit Bitumen oder Kiefernharz an die Stange klebte. In der Antike wurde alles, was zur Hand kam, als Klebstoff verwendet. Am häufigsten wurden Produkte tierischen Ursprungs verwendet, die anfänglich klebrige Eigenschaften besaßen (Fischschuppen, Tieradern usw. Substanzen nach Wärmebehandlung). Es ist erwähnenswert, dass es Bereiche gibt, in denen organische Klebstoffe noch aktiv verwendet werden. Tischlerkleber, Kaseinkleber, Tapetenkleister. Trotz des Überflusses an synthetischen (= chemischen Klebstoffen) sind diese Optionen immer noch in Ordnung und besetzen fest ihre Nische umweltfreundlicher und billiger Klebstoffe. Übrigens werden viele moderne Klebstoffe nur zu Ehren der Tatsache als Kunstharze bezeichnet, dass Harz (ein Klebstoff, der in Kiefern und anderen Pflanzen vorkommt) einer der ersten weit verbreiteten Klebstoffe war.
Das gesamte Konzept der Bindung beruht auf zwei grundlegenden Phänomenen der kolloidalen Chemie -
Adhäsion und Kohäsion (okay, drei, noch Oberflächenspannung).
Adhäsion (aus dem Lateinischen adhaesio - sticking) in der Physik ist die Adhäsion von Oberflächen unterschiedlicher Feststoffe und / oder Flüssigkeiten. Die Adhäsion beruht auf intermolekularen Wechselwirkungen in der Oberflächenschicht und ist durch die spezifische Arbeit gekennzeichnet, die zum Trennen der Oberflächen erforderlich ist.
Bezogen auf den Klang und die Bedeutung der Adhäsion ist das Konzept des Zusammenhalts, das manche Leute manchmal gerne verwirren.
Verwechseln Sie die Haftung nicht mit der Kohäsion... was der Grund für die Existenz von Dingen in dem Zustand ist, in dem wir es gewohnt sind, sie zu sehen (d. h. in Form von Stücken, Tropfen usw. und nicht über die Moleküle verteilt). Dieses Phänomen nennt man
Zusammenhalt :
Kohäsion (dt. Kohäsion von lat. Cohaesus - „verbunden“, „verbunden“) ist die Verbindung zwischen denselben Molekülen (Atomen, Ionen) im Körper innerhalb derselben Phase. Der Zusammenhalt kennzeichnet die Stärke des Körpers und seine Fähigkeit, äußeren Einflüssen standzuhalten. Kohäsion ist eine Aktion oder Eigenschaft der gegenseitigen Anziehung identischer Moleküle. Dies ist eine innere Eigenschaft einer Substanz aufgrund der Form oder Struktur ihrer Moleküle, die eine Änderung der Verteilung der Elektronen der Moleküle verursacht, wenn sie sich nähern, wodurch eine elektrische Anziehungskraft erzeugt wird, die mikroskopische Strukturen bilden kann.
Der Unterschied zwischen diesen grundlegenden Konzepten der kolloidalen Chemie lässt sich am besten am Beispiel von Wassertropfen zeigen, die sich bei Regen auf einer Fensterscheibe bilden.
Das Bild zeigt die Konfrontation der "Elemente", von denen jedes sein eigenes Geschäft betreibt, um unser übliches Bild der Welt zu formen. Die Form des Tropfens gibt die
Oberflächenspannung an . Die Schwerkraft (Schwerkraft) - zieht einen Tropfen nach unten, läuft aus dem Glas. Diese unaufhaltsame Kraft wird durch die Kräfte der Adhäsion und des Zusammenhalts zusammen bekämpft. Der Zusammenhalt ist der erste, der sich manifestiert, da er bereits im Wassertropfen auftritt. Benachbarte Moleküle kleben zusammen und bilden die Tropfen, die dann malerisch über das Glas gleiten. Kohäsion bindet einzelne Moleküle zu Ensembles. Durch die Haftung werden die Ensembles jedoch in Form von Tropfen am Glas befestigt, sie halten sich am Glas fest, ziehen sich hoch und müssen sich der Bewegung unter ihrem eigenen Gewicht widersetzen. Darüber hinaus ist die Kohäsion stärker als die Adhäsion, da sich sonst keine Tropfen bilden könnten, d.h. Regenwasser verteilte sich einfach gleichmäßig auf dem Glas und bildete eine Art Ölfilm auf dem Wasser. Wenn Sie das Glas während des Regens genau beobachten, können Sie übrigens sehen, dass die Tropfen die bereits vorhandenen "Wasserwege" hinunter rollen. Dies liegt an der Tatsache, dass fallende Wassertropfen aufgrund von Kohäsionskräften versuchen, am bereits vorhandenen Wasser und nicht am Glas zu haften. Erwähnte Pfade entstehen übrigens dadurch, dass sich Wassermoleküle von vorbeiziehenden Tropfen lösen und von Glas erfasst werden, wenn Tropfen auf das Fenster fallen.
Was hat das alles mit Klebstoffen zu tun? Und das direkteste. Adhäsion und Kohäsion sind die wichtigsten aktiven Faktoren in Klebstoffen. Angenommen, Sie möchten zwei Holzstücke, A und B, mit Klebstoff B verbinden. Hier benötigen Sie drei verschiedene Kräfte: Adhäsionskräfte, die A und B halten können + Adhäsionskräfte, die B und B halten + Adhäsionskräfte, die Klebstoff B halten.
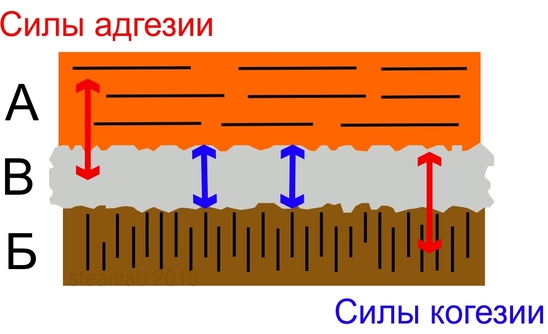
Wenn mit den ersten beiden Kräften alles klar ist, werde ich eine kleine Erklärung zu letzteren geben. Das beste Beispiel sind zwei mit Marmelade oder Marmelade geklebte Laibstücke. Marmelade ist ein klassischer natürlicher Kleber (ich werde später ein paar Worte dazu sagen) aus Zucker und Wasser. Darüber hinaus ist es sehr effektiv. Wenn Sie ziemlich starkes Brot (oder Cracker) und die richtige Marmelade der Mutter verwenden, ist es ziemlich realistisch, zwei Teile zusammenzuhalten und nur eine Ecke zu schmieren. Gute Marmelade hat ziemlich starke innere Kohäsionskräfte (daher ist es schwierig, sie aus der Dose herauszuziehen, insbesondere Birne), aber auch die Haftung auf anderen Oberflächen ist ausgezeichnet. Daher ist es schwierig, ein geklebtes Sandwich zu zerbrechen, ohne das Brot zu zerstören (es stellt sich am häufigsten heraus, wenn Sie die Schichten zur Seite bewegen und keine Kraft senkrecht ausüben). Aber wenn die Marmelade "einen schwachen inneren zusammenhängenden Kern hat", spielt es keine Rolle, wie gut sie am Brot haftet. Zwei Hälften können nicht zusammenkleben und fallen unter dem Einfluss der Schwerkraft auseinander.
Ein weiteres antagonistisches Beispiel: Wasser und ein Stück Eisen. Sowohl dieses als auch andere Objekte sind unter normalen Bedingungen zum Kleben sehr schlecht geeignet, jedoch aus verschiedenen Gründen. Wasser - weil seine Adhäsionskräfte hoch sind und es gut auf jeder Oberfläche haftet, aber aufgrund sehr schwacher Kohäsionskräfte sind diese Oberflächen nicht gut verbunden und leicht zu trennen. Im Gegensatz dazu gibt es in einem Stück Eisen unglaublich starke kohäsive Wechselwirkungen (die für die Bindung von Atomen verantwortlich sind), und dies ist so sehr ein „Ding an sich“, dass es fast unmöglich ist, eine Haftung an einem anderen externen Material daraus zu erreichen. Der Test auf innere Kohäsionskräfte kann die Möglichkeit sein, das Material in Stücke zu teilen. Ein „Stück“ Wasser kann leicht mit einem Finger / Löffel usw. von der Gesamtmasse getrennt werden und versucht, ein Stück Gusseisen mit dem Finger zu trennen :).
Aus dem Vorstehenden ist die Schlussfolgerung, dass in der Natur des Klebstoffs die Hauptkraft der Kohäsion die Hauptkraft ist und in der Natur der Bindung die Stärke der Haftung. Da es sich bei Klebstoffen in der Regel um sehr spezifische Substanzen handelt, deren Wirksamkeit von vielen durch die Erfahrung vieler Generationen getestet wurde, werde ich mich auf das Phänomen der Adhäsion konzentrieren (Klebstoff kann übrigens auch als Klebstoff bezeichnet werden). Bisher wurden verschiedene konkurrierende / komplementäre Theorien entwickelt, die versuchen, das Auftreten des Adhäsionsphänomens zu erklären:
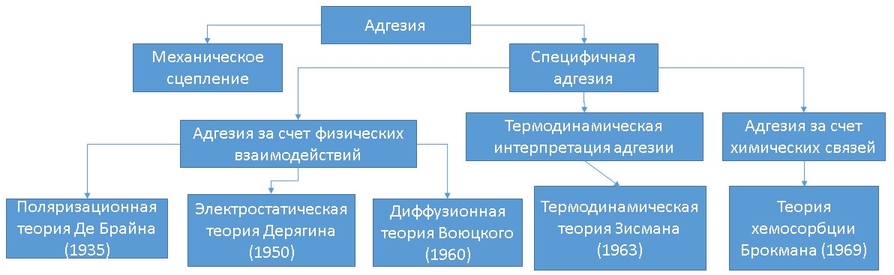
Trotz der Fülle an Geräten gibt es immer noch keine einheitliche Antwort auf die Frage "Was bringt den Kleber zum Kleben?" Dies ist jedoch nicht so überraschend, wenn man bedenkt, wie viele verschiedene Arten von Klebstoff existieren und wie viele verschiedene Arten, sie zu verwenden. Es wird angenommen, dass es für jeden einzelnen Klebstoff und für jede einzelne Oberfläche, auf der er verwendet wird, eine individuelle Kombination verschiedener Faktoren gibt, die diese Objekte zusammenhalten. Der Prozess der Untersuchung von Klebeprozessen wird bis heute fortgesetzt, da wir selbst im 21. Jahrhundert, wenn „Raumschiffe furchen ...“, immer noch nicht vollständig verstehen, warum Substanzen aneinander haften. Daher müssen wir mit Annahmen und Verallgemeinerungen arbeiten. In Anbetracht dessen stellt sich heraus, dass es vier mögliche Hauptbindungsmechanismen gibt: durch Adsorption, Chemisorption, mechanische Bindung und Diffusion.
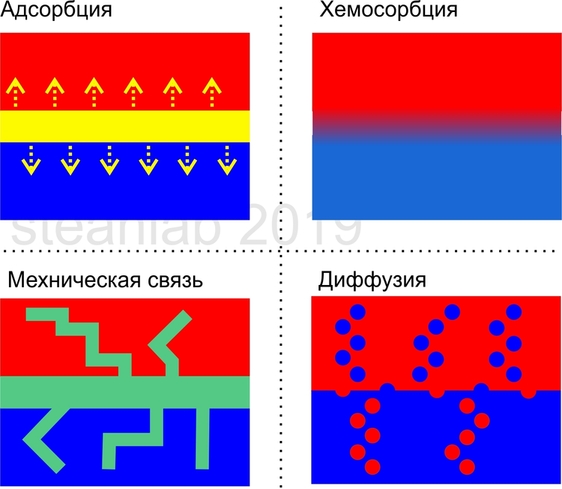
Adsorption ist der Effekt der Adhäsion von Oberflächen aneinander aufgrund
ultrakleiner Anziehungskräfte (die sogenannten Van-der-Waals-Kräfte (übrigens
erwähnte der Leser von
cck7777 , dass es richtiger wäre, „fan der“ wie in
de Nederlandse taal zu sagen), ein gebräuchlicher Name für alle intermolekulare Kräfte). Diese Kräfte werden außerdem weiter unterteilt in elektrostatische Wechselwirkungskräfte (
Kizom-Kräfte, die zwischen konstanten molekularen Dipolen auftreten), Polarisationskräfte (
intermolekulare Debye-Kräfte zwischen konstanten und induzierten Dipolen) und Dispersionswechselwirkungskräfte (
Londoner Kräfte zwischen sofort induzierten Dipolen). Dipol = zwei Ladungen gleicher Größe und entgegengesetztem Vorzeichen, die in einem Abstand voneinander angeordnet sind und im Vergleich zum Abstand zum Beobachtungspunkt sehr klein sind. Nun, dann "entgegengesetzt angezogen usw.". Darauf ruht die gesamte Elektrostatik (und damit alle Klebstoffe). Die Kräfte der intermolekularen Wechselwirkung treten übrigens auf, wenn sich die Teilnehmer (Atome und Moleküle) in einem sehr engen Abstand (weniger als 1 nm) befinden.
Beim Auftragen von Klebstoff wird die Oberfläche der zu klebenden Teile benetzt und die Gegenstände haften aneinander. Damit der Klebstoff funktioniert, sollten die Oberflächen so weit wie möglich entfettet werden (damit sich der Klebstoff auf der Oberfläche verteilt) und der Klebstoff gleichmäßig mit einer dünnen Schicht verteilt werden. Tatsächlich erinnert dieser Prozess an das Anhaften von Millionen mikroskopischer Magnete (einschließlich Klebemolekülen und Molekülen von Materialien, die gebunden werden sollen).
Eine kleine Bemerkung zu perfekt glatten OberflächenEin interessantes Klebeartefakt kann als
Gecko betrachtet werden . Dies ist eine Eidechse, die sich leicht auf verschiedenen vertikalen Flächen bewegen kann (in wunderbaren Begriffen „wie ein Spinnenmann“). Sogar Aristoteles machte sich müßige Gedanken über die Ursache dieses Phänomens. Moderne Wissenschaftler haben dieses Problem lange Zeit untersucht und die Vakuumtheorie (= klebt aufgrund der Druckdifferenz), die Theorie des biologischen Leims (= setzt Klebstoff frei) usw. schrittweise verworfen. Infolgedessen haben wir uns auf elektrostatische Wechselwirkungen (verursacht durch Kontaktelektrifizierung) und nicht auf Van-der-Waals- oder Kapillarkräfte festgelegt. Die Ursache des Phänomens waren die
Borsten , die Millionen von jedem Bein bedeckten. Die Länge jeder Borste beträgt etwa 0,1 mm (zwei Dicken eines menschlichen Haares). Quadratische Pfoten machen pro Millimeter bis zu 14400 Setae aus (~ 1,5 Millionen pro cm
2 ). Jedes Borstenende divergiert in 400-1000 Zweige und jeder Zweig endet am Ende mit einer dreieckigen Platte mit einer Breite von 0,2 Mikrometern. Das heißt, Ein Geckofuß mit einer Fläche von ungefähr einem Quadratzentimeter berührt eine Oberfläche von ungefähr zwei Milliarden Enden.
B. Foto von Gecko-Borsten. B. Foto einer Gecko-Borste. D. Foto des Astes am Ende der Borste.
Jüngste Studien zeigen, dass genau diese Fußgeometrie und die damit verbundenen elektrostatischen Kräfte (multipliziert mit Milliarden von Enden) zu einem Ergebnis führen, das das Gewicht des Geckos an der Decke halten kann.
Rikkitik Reader :
Über das Material, das die Beine eines Geckos imitiert, hier der
Artikel von 2016. Kurz gesagt - das Neugierigste war nicht, wie man klebt, sondern wie man abreißt, ohne die Funktionalität zu verlieren, dh um die Wiederverwendbarkeit der Verbindung zu erreichen.
Es scheint, dass sich gegenseitig ausschließende Anforderungen an die Zotten gestellt werden - Forscher, denen dies zu Beginn des 21. Jahrhunderts begegnet ist. Die Zotten sollten dünn sein, um die kleinsten Lücken und Gruben zu durchdringen, und gleichzeitig stark, damit sie nicht bei jedem Schritt von der Sohle abfallen. Sie sollten flexibel und relativ leicht zu dehnen sein, um die Vorsprünge einer komplexen rauen Oberfläche zu erreichen, und gleichzeitig nicht zu leicht von dieser Oberfläche zu trennen sein und nicht wie Kaugummi hinter die Sohle greifen.
Künstliche Strukturen aus solchen Zotten sollten so stabil wie möglich sein, sich nicht vom Fuß abreißen und einer großen Anzahl (bis zu einer Million) von Zyklen mit abklebendem Ablösen standhalten. Der Raum zwischen den Zotten sollte nicht zu stark mit Staub kontaminiert sein, der sich von der Oberfläche angesammelt hat, und die Zotten selbst sollten nicht zusammenkleben, da beide ihre Fähigkeit zur Anpassung an eine komplexe Oberfläche stark verringern.
Es wäre überraschend, wenn das Militär all dies nicht ausgenutzt hätte. Im Mai 2014 zeigte DARPA die Entwicklung von
Geckskin (Z-Man-Projekt), einem Handgerät, das Bewegungen auf vertikalen Flächen ermöglicht.
Zwar sind fünf Jahre vergangen, aber aus irgendeinem Grund ist nichts über Geckskin zu hören. Vielleicht, weil es klassifiziert ist, und vielleicht, weil es kein Ergebnis gibt.
Die Geckos und Darpa sind alle irgendwo mit ihnen da draußen. Und hier kann eine perfekt geschliffene Oberfläche die Kräfte intermolekularer Wechselwirkungen am besten veranschaulichen. Jeder Dreh- und Fräsmaschinenbediener sollte über Johanson-Fliesen oder
planparallele Endmaße der Länge Bescheid wissen. Diese Fliesen werden so poliert und geschliffen, dass sie ziemlich stark zusammenkleben, wenn sie mit glatten Kanten aneinander gelegt werden. Auf dem Bild werden sechsunddreißig Fliesen durch atmosphärischen Druck
und Van-der-Waals-Kräfte zusammengehalten:
Für diejenigen, die nicht glauben, dass dies möglich ist - ich empfehle eine visuelle Demonstration (anklickbar):
Auf die Adsorption folgt unerbittlich die Chemisorption, aber trotz der Ähnlichkeit der Namen ist das Wesen der Phänomene radikal anders. Chemisorption - Die Adhäsion erfolgt aufgrund der Bildung chemischer Bindungen zwischen dem Klebstoff und den geklebten Substanzen. Tatsächlich erzeugt die Bindung eine neue Chemikalie. Während der Diffusion tritt eine Bindung aufgrund des gegenseitigen Eindringens von Materialmolekülen ineinander auf. Leimmoleküle vermischen sich mit Molekülen geklebter Oberflächen und bilden eine starke Bindung. Und schließlich tritt eine mechanische Haftung auf, wenn Klebstoff in Mikrorisse und Hohlräume von Materialien eindringt und diese anschließend physikalisch zurückhält. Zur Veranschaulichung sind im Bild die numerischen Werte der Energien für verschiedene Kräfte dargestellt, die beim Kleben auftreten.
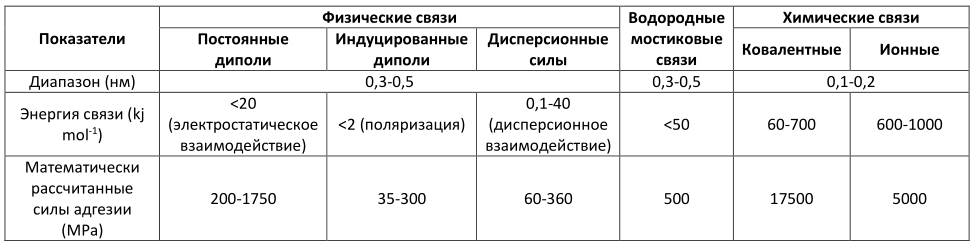
Offensichtlich wird die beste Haftung bei einer Chemisorptionswechselwirkung zwischen den geklebten Substanzen gebildet, obwohl dies nicht immer möglich ist (aber ein Streben ist notwendig).
Sorten von Klebstoffen
Aus alledem folgt, dass jeder Klebstoff das eine oder andere oben beschriebene Prinzip ausnutzt. Darüber hinaus haben auch bei Forschern wie bei Geckos die Forscher in der Regel keine gemeinsame Meinung. Dies ist jedoch im Prinzip nicht so wichtig, da genügend praktische Erfahrungen gesammelt wurden, mit denen Sie auf einfache Weise die optimalen Klebstoffe und Klebstoffe für die gesamte Materialvielfalt auswählen können. Es gibt viele Unterteilungen von Klebstoffen, die ich aufgrund ihrer chemischen Natur am einfachsten nennen werde:
Darüber hinaus möchte ich darauf hinweisen, dass wir bis heute hauptsächlich die Entwicklung von vor fast hundert Jahren aktiv nutzen. Überzeugen Sie sich selbst anhand einer kurzen Chronologie:
1920er Jahre : Klebstoffe auf Basis von Celluloseestern, Alkydharzen, cyclisiertem Kautschuk, Polychloropren (Neopren), Sojaklebstoffen1930er Jahre : erfundene Harnstoff-Formaldehyd-Klebebänder, Klebefolien auf Phenolharzbasis, Klebstoffe auf Polyvinylacetat (PVA) ) Klebstoffe für Holz1940 tH Jahren: synthetisierte nitrilfenol, chlorierter Kautschuk, Melamin - Formaldehyd, Acryl Polyurethane vinylphenol und1950 tH Jahren: dargestellt Epoxide, Cyanoacrylate, anaerobe Klebstoffe1960 tH Jahren: dargestellt Polyimide, polibenzimid sol, Polychinoxaline1970 -e Jahre: Acrylklebstoffe der zweiten Generation stellt eine druckempfindliche Acrylstruktur Polyurethane1980 - : , , ,
1990 - : , ,
2000 - : , ,
, tutorial (
3D-. +
Wir geben das Mädchen Geflügel oder RTFM per Definition von Kunststoffen zu Hause zurück , zumindest um uns an die Terminologie "Polymer" zu gewöhnen und grundlegende Informationen zu Polymeren zu erhalten.Heute ist die Hauptentwicklung von "kundenspezifischen" Klebstoffzusammensetzungen auf dem Weg zu einer Erhöhung der Umweltfreundlichkeit (oft übrigens zum Nachteil der Klebkraft). Strukturelle und industrielle Verbindungen sind dafür nicht besonders anfällig, aber im Allgemeinen werden dort immer noch traditionelle, bewährte Optionen verwendet. Wir suchen in der folgenden Tabelle nach unseren Verbindungsmaterialien und erinnern uns an die Art des Klebers, den wir benötigen.Bonus - eine vergleichende Überprüfung der Festigkeitseigenschaften verschiedener Arten von Klebstoffen. Manchmal ist es nützlich :)Ein klarer Vergleich der Festigkeitseigenschaften von Verbindungen, die unter Verwendung verschiedener Arten von Klebstoffen erhalten wurden
: CA-, MS- , PU- , - , -, -
In diesem Zusammenhang wird der einleitende Teil im Folgenden abgeschlossen. Wir werden nun bestimmte Arten von Leim und optimale Bedingungen / Materialien für seine Verwendung betrachten. Stellen Sie in den Kommentaren die Fragen, die Sie betreffen - im nächsten Teil ist die Wahrscheinlichkeit des Auftretens von Antworten hoch.NB Fortsetzung des Themas:Opus über Seine Majestät Clay. Zweiter Teil - Viva, Cyanacrylat! Viva, SuperkleberOpusa über Seine Majestät Clay. Dritter Teil - Polyurethan gegen Space ColdOpusa über Seine Majestät Clay. Vierter Teil - SilikoneWird der nächste Artikel von der Habr-Community abhängen, für
subj .
Wichtig!Alle Aktualisierungen und Zwischennotizen, aus denen dann die Habr-Artikel reibungslos gebildet werden, sind jetzt in meinem Telegrammkanal lab66 zu sehen . Abonnieren Sie, um nicht den nächsten Artikel zu erwarten, sondern um sofort über alle Forschungsergebnisse informiert zu sein :)Gebrauchte LiteraturHandbook of Rubber Bonding, Ed., B. Crowther, Rapra Technology Ltd, Shrewsbury, UK, 2000.
DE Packham, Handbook of Adhesion, Longman Scientific & Technical, Harlow, UK, 1992.
DJ Dunn, Engineering and Structural Adhesives, Rapra Review Report No.169, Rapra Technology Ltd, Shrewsbury, UK, 2004.
Skiest, I. The Handbook of Adhesives, 3rd ed., Van Nostrand Reinhold, New York, 1990.
Satas, D. The Handbook of Pressure Sensitive Adhesives, 2nd ed., Van Nostrand Reinhold, New York, 1989.
Petrie, EM, Handbook of Adhesives and Sealants, McGraw-Hill, New York, 2000.