
Vor dem Fenster scheint die helle Sonne, die Luft ist mit warmer Feuchtigkeit gefüllt, und die kühle Brise beschloss, Urlaub zu machen, und überließ uns der zerrissenen Hitze. Ich möchte meine Jeans in Shorts, einen Laptop in einen Volleyball und ein Büro in den Strand verwandeln. Sommer ist mit Feiertagen und Ferien verbunden, aber manchmal wird ein Gast, den wir normalerweise in den Wintermonaten erwarten, nämlich eine Erkältung, in diese müßige Liste hineingezwängt. Es gibt nichts Schlimmeres als die Temperatur, wenn die Lufttemperatur etwa 30 beträgt. Im Sommer verwandeln akute respiratorische Virusinfektionen eine Person in eine Schnecke, die sich langsam über heißen Asphalt schlängelt und eine schleimige Spur hinterlässt.
Kann uns die Rettungswissenschaft helfen, Rhinoviren zu bekämpfen? Natürlich werden Ihnen Wissenschaftler vielleicht antworten, wenn sie einen neuen Weg finden, um mit Nashörnern / Enteroviren umzugehen, die in der zuvor unerforschten „Tasche“ des Virus versteckt sind. Was ist das für eine Tasche, was wollen Wissenschaftler hineinstecken und wie wird dies helfen, Rhinoviren zu besiegen? Die Antworten finden wir im Bericht der Forschungsgruppe.
Studienbasis
Zunächst erinnern wir uns schnell daran, was wir über ARVI haben und was es wirklich ist.
 Visualisierung des Rhinovirus.
Visualisierung des Rhinovirus.ARVI, dh eine akute Virusinfektion der Atemwege, ist das Ergebnis der aktiven Aktivität des Virus im menschlichen Körper, nämlich in seinen Atemwegen. Diese Viren umfassen Rhinoviren aus der Gattung Enteroviren. Eines der Hauptstrukturmerkmale des Rhinovirus ist das offene Virion, dh ein Viruspartikel ohne Hülle.
Beim Menschen verursachen Rhinoviren eine Entzündung der oberen Atemwege, da sie es vorziehen, sich in der Schleimhaut zu vermehren, die den Nasopharynx bedeckt. Die Symptome im Falle einer Infektion sind ziemlich normal und jedem bekannt - Temperatur, laufende Nase, Schmerzen im Kehlkopf. Ohne Behandlung und verminderte Immunantwort des Körpers können sich akute Virusinfektionen der Atemwege zu Bronchitis, Sinusitis oder Mittelohrentzündung entwickeln.
Können Rhinoviren behandelt und / oder geimpft werden? Theoretisch möglich, aber fast unmöglich, da die Anzahl der serologischen Varianten des Erregers sehr groß ist. Rhinovirus-Infektionen werden behandelt, indem die Symptome gelindert werden, und das Virus selbst besiegt das Immunsystem.
Wenn wir über die Behandlung einer Virusinfektion als solche sprechen, lohnt es sich, den Prozess der Abtötung des Virus selbst zu verstehen. Dies geschieht in der Regel grob gesagt durch Einführen eines Arzneimittels. Derzeit sind die am meisten untersuchten Inhibitoren Kapsidbinder, die in die hydrophobe Tasche des viralen Kapsids eingebracht werden.
In der Studie, die wir heute betrachten, haben Wissenschaftler eine bisher unbekannte Tasche identifiziert, die von den viralen Proteinen VP1 und VP3 gebildet wird und ein gemeinsames Merkmal für verschiedene Arten von Entero-Rhinoviren ist. Die Einführung des Arzneimittels in diese Tasche stabilisiert die Schlüsselregion des Virions, wodurch die für die Freisetzung von viraler RNA erforderliche Konformationsexpansion verhindert wird. Daher kein Rotz, Husten und Fieber. Stimmen Sie zu, es klingt sehr inspirierend.
Forschungsergebnisse
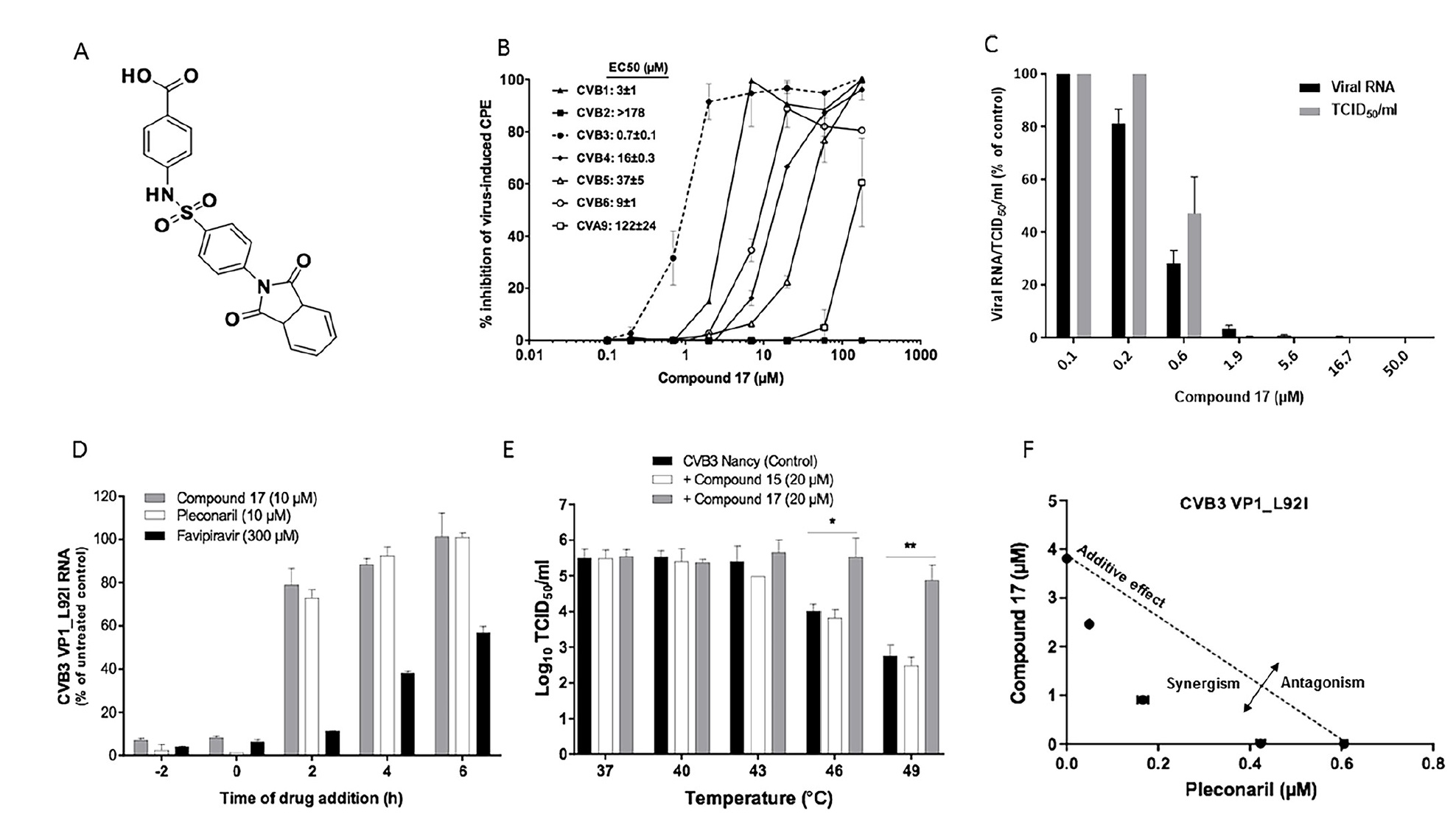 Bild Nr. 1
Bild Nr. 1Wissenschaftler haben herausgefunden, dass
Verbindung 17 (
1a ), die ein Derivat von Benzolsulfonamid ist, ein starker Inhibitor für den B3-Stamm des Coxsackie-Virus ist. Die halbmaximale effektive Konzentration (EC50) beträgt 0,7 ± 0,1 μM (
1b ).
Verbindung 17 hemmt auch die Replikation von CVB1 und CVB6, zeigt eine mäßige Aktivität gegen CVB4-, CVB5- und Coxsackie A9-Virus (CVA9), reagiert jedoch selbst bei der höchsten getesteten Konzentration nicht gegen CVB2 (
1b ). Diese Verbindung wird auch in CVA16 und EVA71 (Gruppe EV-A), CVA21 und PV1 (Gruppe EV-C), EVD68 (Gruppe EV-D) und Rhinovirus B14 (RVB14, RV-B) nicht gehemmt.
Die antivirale Aktivität von Verbindung 17 wurde zusätzlich in einer Viruslastanalyse bestätigt, in der die dosisabhängige Art der Bildung von CVB3- und CVB3-Virus-RNA mit EC50-Werten von 0,4 ± 0,01 uM bzw. 1,1 ± 0,3 uM (
1 s ) verringert wurde.
Verbindung 17 zielt wie Pleconaril (ein antivirales Medikament) auf die Replikation von CVB3 in den frühen Stadien des Viruszyklus ab. Bei der Einführung von Verbindung 17 2 Stunden nach der Infektion ist die antivirale Aktivität stark verringert (
1d ).
Wissenschaftler erinnern uns daran, dass Enterovirus-Inhibitoren im Frühstadium (z. B. Pleconaril) mit viralen Kapsiden interagieren und ihre Resistenz gegen thermische Inaktivierung erhöhen. Verbindung 17 erhöhte die thermische Stabilität von CVB3 um 1,5 bei einer Temperatur von 46 ° C und um 2,1 bei 49 ° C (
1e ).
Wenn Verbindung 17 und Pleconaril kombiniert werden, wird eine synergistische antivirale Aktivität beobachtet. Das heißt, diese beiden Substanzen haben unterschiedliche Mechanismen der antiviralen Wirkung (
1f ).
Beobachtungsdaten lassen den Schluss zu, dass Verbindung 17 für Tests im Zusammenhang mit der nachgewiesenen Tasche im viralen Kapsid gut geeignet ist.
Um den Wechselwirkungsprozess von Verbindung 17 und dem viralen Kapsid CVB3 besser zu berücksichtigen, führten die Wissenschaftler eine kryoelektronische Mikroskopie durch.
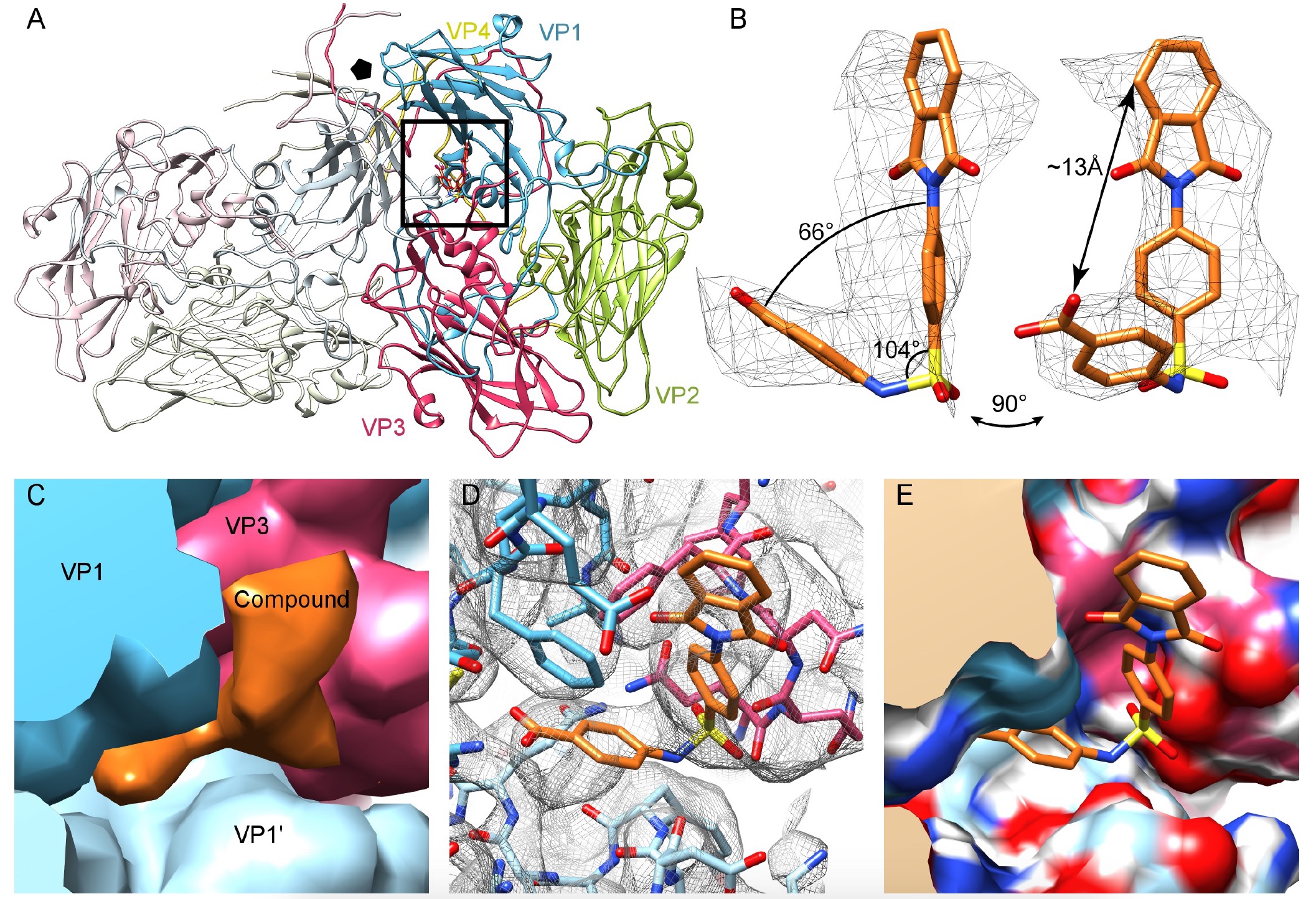 Bild Nr. 2
Bild Nr. 2Die Kapsidprotein-Seitenketten konnten leicht identifiziert werden, und das Nancy CVB3-Homologiemodell konnte leicht in die Versiegelungskarte passen. Zusätzlich zeigte der Kryo-EM-Stamm von Nancy einen Mangel an Lipidfaktor-Verdichtung in der hydrophoben Tasche von VP1. Eine Analyse der Unterschiede ergab jedoch eine zusätzliche Verdichtung, die mit dem Atommodell der Verbindung 17 (
2a ,
2c ) assoziiert sein kann.
Wie in Bild 2b zu sehen ist, hat die Verbindung eine L-Form mit einer langen und kurzen Schulter, die das „Andocken“ an Verbindung 17 ermöglicht. Die Simulation zeigte, dass die Verbindung 17 über zwei VP1-Blöcke und einen VP3-Block an der Protoprotomer-Schnittstelle in der Tasche verbunden ist. Aufgrund der ikosaedrischen Symmetrietyp des Virus können 60 solcher Regionen in einem Caspid vorhanden sein (
2c ).
Der betrachtete Bereich befindet sich in einem Abstand von 16 Å von der hydrophoben Tasche, auf die das Pleconaril abzielt. Somit wirkt Verbindung 17 nicht an der gleichen Stelle wie Pleconaril, dh ohne seine antivirale Aktivität zu beeinträchtigen, sondern es zu ergänzen.
Wissenschaftler haben Wechselwirkungen innerhalb von Proteinen, Grenzflächen, Strukturen und Verbindungen simuliert, die die Reste VP1 (73, 75–78, 155–157, 159–160, 219 und 234) und VP3 (233–236) zeigten, die eine Tasche bilden (
2d und
2e ). .
Eine Analyse der Konservierung dieser Taschenreste in den 56 Aminosäuresequenzen von CVB3 zeigte, dass 7 von 16 vollständig konserviert sind (d. H. Es befindet sich eine Verbindung 17 im Inneren), und etwa 14 Reste zeigten ein Ergebnis von 97% Konservierung. Die Taschenkonservierung tritt auch bei allen Enteroviren der Gruppe B auf.
Allerdings sind nicht alle Viren so leicht anfällig für eine Hemmung durch Verbindung 17. Daher war es notwendig zu verstehen, was sie so resistent macht. Zu diesem Zweck führten die Wissenschaftler eine klonale Selektion durch, wobei 4 Resistenzmutationen hervorgehoben wurden. Drei der vier Aminosäuremutationen befanden sich in unmittelbarer Nähe der Tasche (F76C, E78G und A98V), und eine weitere (D133G) war ziemlich weit entfernt.
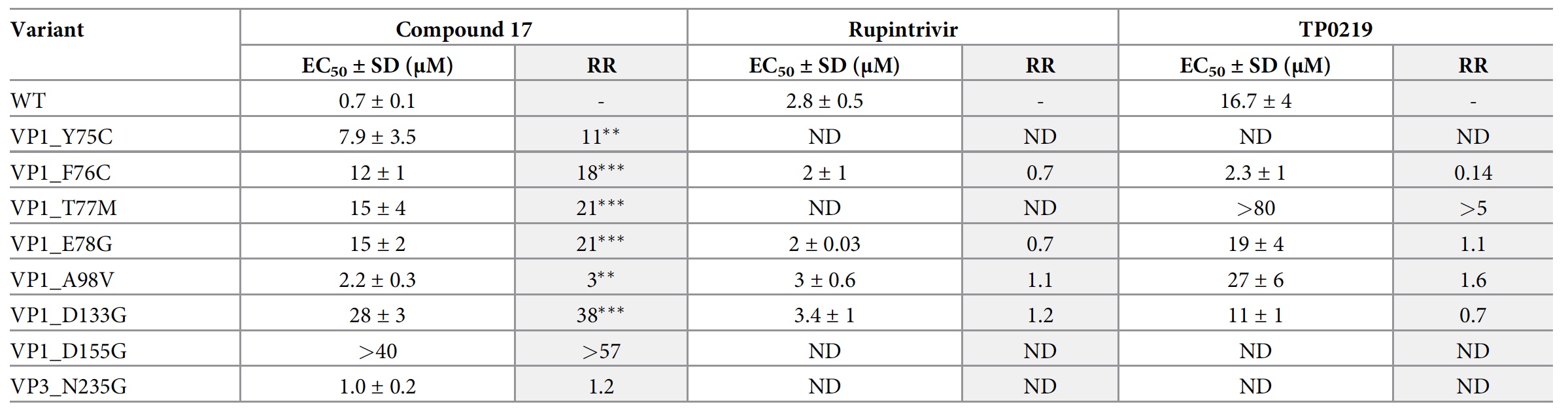 Ausmaß der Wirkung von Verbindung 17, Rupintrivir (3C-Proteaseinhibitor) und TP0219 (Glutathion-abbauende Verbindung) auf die CVB3-WT-Replikation und modifizierte CVB3-Varianten.
Ausmaß der Wirkung von Verbindung 17, Rupintrivir (3C-Proteaseinhibitor) und TP0219 (Glutathion-abbauende Verbindung) auf die CVB3-WT-Replikation und modifizierte CVB3-Varianten.Wissenschaftler haben 12 CVB3-Mutanten im CVB3-Klon durch Reverse Engineering hergestellt. Eine Glutathion-unabhängige Version von VPB1_T77M CVB3, die gegen die Glutathion-abbauende Verbindung TP0219 resistent ist, wurde ebenfalls hergestellt.
Nur acht der 12 Mutanten waren lebensfähig (
2d ), 7 von ihnen waren gegen Verbindung 17 resistent und reagierten gleichermaßen auf Rupintrivir.
Die Untersuchung der einzigen resistenten Mutation weit entfernt von der Tasche hat gezeigt, dass VP1_D133G hitzebeständiger als CVB3 Nancy ist und Verbindung 17 es immer noch stabilisieren kann. Das heißt, VP1_D133G ist eine kompensatorische Mutation und keine Mutation, die die Bindung von Verbindung 17 verhindert.
VP1_T77 war jedoch an der Bindung von Glutathion beteiligt. Die Analyse zeigte, dass die Glutathion-unabhängige Variante VP1_T77M CVB3 eine verringerte Empfindlichkeit gegenüber Verbindung 17 aufweist. Es wurde auch gefunden, dass Glutathionethylester selbst bei der höchsten getesteten Konzentration keinen Einfluss auf die antivirale Aktivität von Verbindung 17 hatte.
Als nächstes überprüften die Wissenschaftler den Grad der möglichen Wirkung von Verbindung 17 auf die Bindung von viralen Rezeptoren. Hierzu wurden das Protein des humanen Coxsackie-Virus und der in einer Kette verknüpfte Adenovirus-Rezeptor (hCAR) verwendet. Die Bindungsaffinität von CVB3 nahm in Gegenwart von Verbindung 17 selbst bei der höchsten getesteten Konzentration nicht ab. Zusätzlich war Verbindung 17 gegen
CD55-abhängiges * Enterovirus B (E-11-Virus) aktiv.
CD55 (Beschleunigungsfaktor für die Komplementzersetzung) * - Membranprotein, Inhibitor des Komplementsystems.
Die experimentellen Daten werden auch durch die Tatsache bestätigt, dass sich die Bindungsstellen des Coxsackie-Rezeptors + Adenovirus und CD55 + CVB3 nicht mit der Tasche schneiden.
So haben Wissenschaftler herausgefunden, dass Verbindung 17 perfekt in die Kapsidtasche verschiedener Viren integriert ist. Die nächste Stufe der Studie besteht darin, die Wirksamkeit des in diese Tasche eingeführten Arzneimittels zu überprüfen.
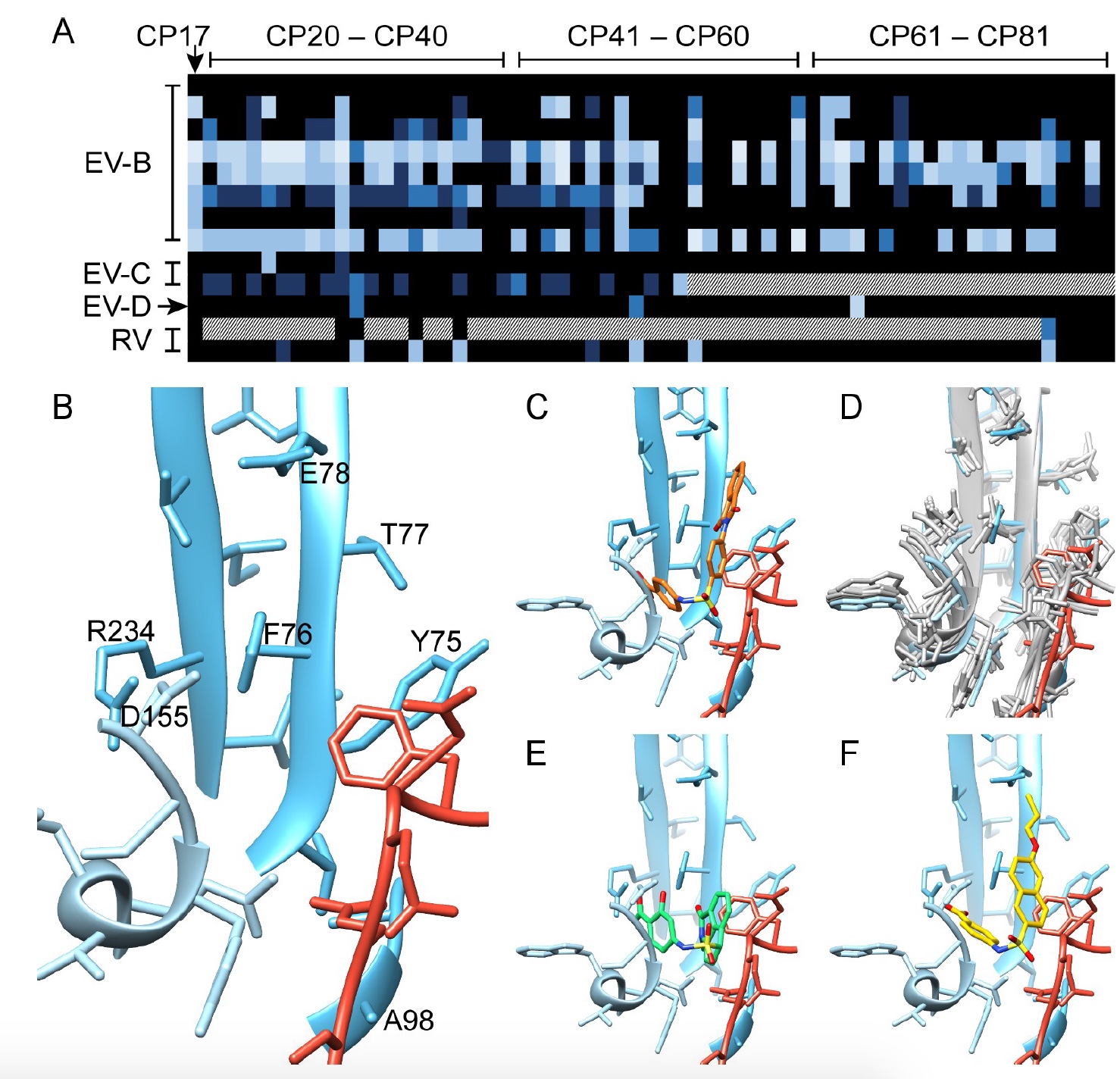 Bild Nr. 3
Bild Nr. 3Während dieses Tests wurden sowohl im Handel erhältliche Substanzen (Verbindungen 20–50) als auch im Labor hergestellte Modifikationen - Verbindungen 51–81 - verwendet.
Das Wissen über die Aktivität von Verbindung 17 ermöglichte es, die spezifischen Eigenschaften zu isolieren, die für die zukünftige Herstellung notwendig sind. Wissenschaftler analysierten Informationen aus antiviralen Assays und verwendeten sie zur Synthese aktiverer Analoga der Verbindung 17.
Die Synthese ergab Analoga, die gegen eine Reihe von Enteroviren aktiv waren: EV-B (CVB), EV-C (PV1 und CVA21), EV-D (EVD68), RV-A (RVA09, RVA59 und RVA63) und RV-B ( RVB14) (
3a ). Leider war keine der erzeugten Verbindungen gegen EVA-Viren (CVA16 und EVA71) wirksam.
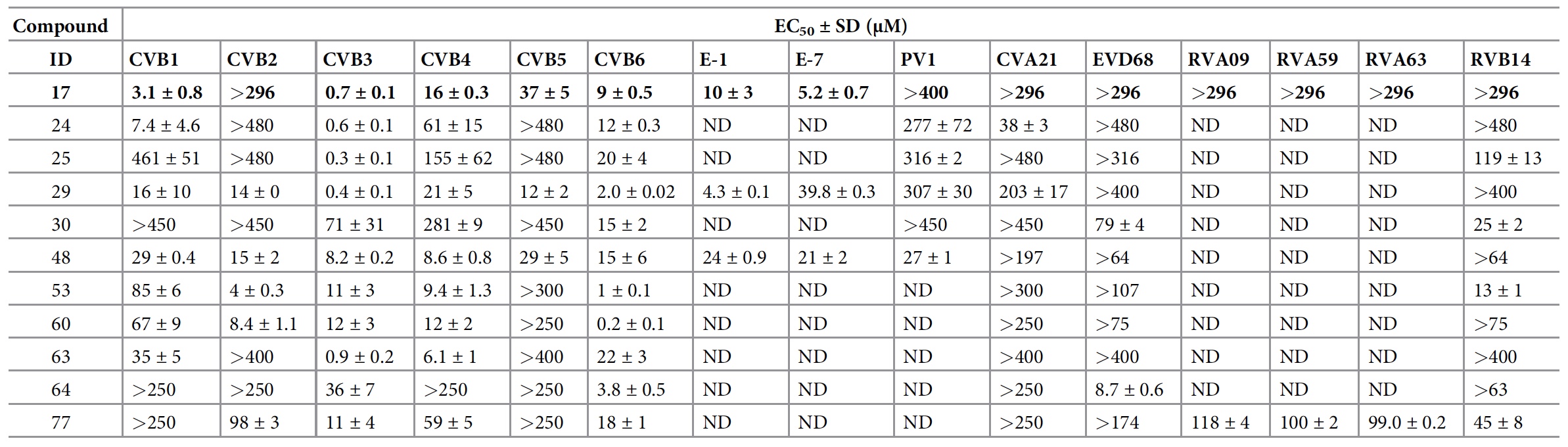 Verbindungen mit maximaler potentieller Aktivität in Bezug auf bestimmte Viren.
Verbindungen mit maximaler potentieller Aktivität in Bezug auf bestimmte Viren.Unter allen Analoga waren die Verbindungen 29 und 48 gegen alle 6 getesteten CVBs (Koskashi-Gruppe-B-Viren) aktiv. Verbindung 48 inhibierte die PV1-Replikation bei einer Konzentration von 144 uM vollständig. Verbindung 77 zeigte eine antivirale Aktivität gegen RV-A und RV-B.
Wie in Bild Nr. 3 zu sehen ist, ergänzt die Form der neuen Moleküle die Form der Tasche. Die Wissenschaftler konnten eine klare Struktur-Eigenschafts-Beziehung (die chemische Struktur des Moleküls zu seiner biologischen Aktivität) aus der Carboxylgruppe in Position R3 herstellen, wo das Wasserstoffatom für die antivirale Aktivität erforderlich ist, und in Position R2, wo die Hydroxylgruppe ihren Nutzen für eine breite antivirale Wirkung zeigt. Die Kryo-EM-Strukturierung zeigte, dass zwischen R3 und dem inhibierten Rest VP1_R234 eine Komplementarität der Ladung besteht.
Die Gesamtheit der Testergebnisse zeigt einen ziemlich hohen Grad an Implementierung der getesteten Verbindungen in die Taschen von Kapsidviren aus verschiedenen Gruppen.
Um die Nuancen der Studie genauer kennenzulernen, empfehle ich Ihnen, den Bericht von Wissenschaftlern (
hier oder
hier ) zu
lesen.Nachwort
Zusammenfassend haben Wissenschaftler Taschen in der Struktur von Enteroviren identifiziert, die mit Medikamenten gefüllt werden können, die die Ausbreitung des Virus verhindern oder es vollständig zerstören.
Die Hauptfigur war Verbindung 17 und ihre modifizierten Analoga, die einen hohen Aktivitätsgrad gegen CVB3 zeigten. Identifizierte Taschen sind sich in verschiedenen Gruppen von Viren sehr ähnlich, was die Weiterentwicklung von Arzneimitteln mit einem breiten Wirkungsspektrum ermöglicht.
Mit anderen Worten, Viren, die bisher noch niemand behandelt hat, können jetzt leicht überwunden werden. Natürlich ist es angesichts der Anzahl von Krankheiten und Anomalien, die seine Arbeit stören und die Türen zum menschlichen Körper für eine Vielzahl von Viren öffnen können, nicht die sinnvollste Idee, sich ausschließlich auf das menschliche Immunsystem zu verlassen. Diese Forschung und Entwicklung ist in unserer Zeit angesichts der Bevölkerung des Planeten und der Verstädterungsrate äußerst wichtig. Und diese Indikatoren beeinflussen die Ausbreitungsrate von Virusinfektionen stark. Darüber hinaus muss eine Person mit einem Medikament, das das Virus in der Wurzel überwinden kann, nicht jedes Symptom einzeln behandeln, dh eine Reihe anderer Medikamente (Tropfen, Sprays, Tabletten, Suspensionen usw. usw.) kaufen.
Die Wissenschaftler werden ihre Arbeit fortsetzen und sich darauf konzentrieren, Verbindungen zu finden, die gegen die größtmögliche Anzahl von Viren am wirksamsten sind. Wir können ihnen nur viel Glück wünschen und, bis sie den Job beendet haben, die Kälte alleine bekämpfen.
Freitag off-top:Nicht nur Menschen leiden unter Viren, sondern auch Computer und manchmal animierte Charaktere. ( Die zweite Serie ist hier.)Vielen Dank für Ihre Aufmerksamkeit, bleiben Sie neugierig, kümmern Sie sich um Ihre Gesundheit und haben Sie ein schönes Wochenende für alle. :) :)
Vielen Dank für Ihren Aufenthalt bei uns. Gefällt dir unser Artikel? Möchten Sie weitere interessante Materialien sehen? Unterstützen Sie uns, indem Sie eine Bestellung
aufgeben oder Ihren Freunden empfehlen, einen
Rabatt von 30% für Habr-Benutzer auf ein einzigartiges Analogon von Einstiegsservern, das wir für Sie erfunden haben: Die ganze Wahrheit über VPS (KVM) E5-2650 v4 (6 Kerne) 10 GB DDR4 240 GB SSD 1 Gbit / s von $ 20 oder wie teilt man den Server? (Optionen sind mit RAID1 und RAID10, bis zu 24 Kernen und bis zu 40 GB DDR4 verfügbar).
Dell R730xd 2 mal günstiger? Nur wir haben
2 x Intel TetraDeca-Core Xeon 2x E5-2697v3 2,6 GHz 14C 64 GB DDR4 4 x 960 GB SSD 1 Gbit / s 100 TV von 199 US-Dollar in den Niederlanden! Dell R420 - 2x E5-2430 2,2 GHz 6C 128 GB DDR3 2x960 GB SSD 1 Gbit / s 100 TB - ab 99 US-Dollar! Lesen Sie mehr über
den Aufbau eines Infrastrukturgebäudes. Klasse mit Dell R730xd E5-2650 v4 Servern für 9.000 Euro für einen Cent?