Methoden zur gezielten Medikamentenabgabe sind auf dem Höhepunkt der Beliebtheit - ein Punkteffekt auf die Läsionsherde ermöglicht es Ihnen, die Krankheit zu bekämpfen, fast ohne das gesunde Gewebe zu beeinträchtigen. Dennoch bleiben Fragen offen: Wie kann die Wirksamkeit einer solchen Therapie gesteigert, die Wirkung des Arzneimittels beschleunigt und seine Akkumulation im Körper minimiert werden? Wissenschaftler des Biological Nanomaterials Laboratory von NUST MISiS arbeiten seit mehreren Jahren in diese Richtung, und nach den neuesten Entdeckungen des Teams konnte die Effizienz der Arzneimittelabgabe an einen bösartigen Tumor unter Verwendung von Neutrophilen - Zellen des Immunsystems - um 30% gesteigert werden. Die Ergebnisse werden in der internationalen Fachzeitschrift
ACS Nano veröffentlicht .

Die Wissenschaftler führten eine intravital (an lebendem Gewebe) durchgeführte Studie über den Mechanismus der gezielten Arzneimittelabgabe an bösartige Tumoren unter Verwendung von Liposomen durch. Es stellte sich heraus, dass die Immunzellen von Neutrophilen die Effizienz der Arzneimittelabgabe an den Tumor um 30% steigern.
Liposomen - künstlich erzeugte Fettvesikel - dringen aufgrund des sogenannten EPR-Effekts (Enhanced Permeability and Retention) in den Tumor ein. In den Liposomen wird das Medikament „genäht“ und wenn es in das bösartige Gewebe gelangt, wird es freigesetzt.
Der EPR-Effekt ist auf das übermäßige Wachstum von Blutgefäßen zurückzuführen, das durch den abnormalen Bedarf des Tumors an Sauerstoff und Nahrung verursacht wird. Bei pathologischem Wachstum treten in den Wänden von Blutgefäßen mit einem Durchmesser von bis zu 200 nm große Poren auf. Das Wachstum des Tumors bewirkt auch eine Kompression der Lymphgefäße und verhindert den normalen Ausfluss von interzellulärer Flüssigkeit. Somit dringen Liposomen in den Tumor ein und können aufgrund einer gestörten Lymphdrainage nicht austreten.
Es wird angenommen, dass Liposomen aufgrund des EPR-Effekts nur in den Tumor eindringen können, nicht jedoch in gesundes Gewebe. Aber ist das wirklich so? Und was passiert im Schiff?
Im Verlauf der Studie beobachteten die Wissenschaftler die Abgabe des Arzneimittels an das Gewebe gesunder Mäuse und an verschiedene Arten von bösartigen Tumoren: Brustkrebs, Prostatakrebs und Melanom. Die Beobachtungen wurden mit einem Intravitalmikroskop durchgeführt, mit dem Sie Prozesse direkt in einem lebenden Organismus untersuchen können.
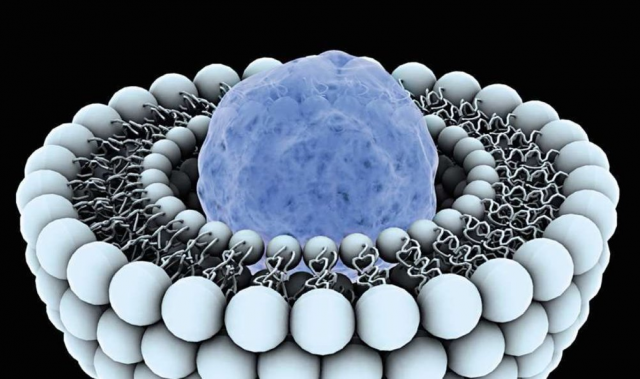 Liposomen "haften" an einer Krebszelle
Liposomen "haften" an einer Krebszelle„Die erste Schlussfolgerung, die wir als Ergebnis der Studie erhalten haben, ist, dass zwei Arten des Eindringens von Liposomen aus Blutgefäßen in Gewebe in lebenden Geweben auftreten. Ein Mikroleck ist eine kleine isolierte Ansammlung von Liposomen um ein Gefäß. Ein solches Verfahren ist für die Behandlung von Tumoren unbrauchbar, da es dem Arzneimittel nicht erlaubt, die Tumorzellen zu erreichen. Darüber hinaus wurden in gesunden Geweben Mikroleckagen festgestellt, was die Toxizität von Medikamenten auf Liposomenbasis in einer modernen Klinik erklärt “, sagt Viktor Naumenko , Autor der Arbeit, Forscher am Biomedical Nanomaterials Laboratory von NUST MISiS .
Das zweite, interessanteste Beobachtungsergebnis ist Neutrophil, eine Art weiße Blutkörperchen, und die Immunzelle des Körpers, die in das Tumorgewebe eindringt. Wenn der Neutrophile das Gefäß zusammen mit ihm durch die „angelehnte Tür“ in der Gefäßwand verlässt, können Liposomen in den Tumor eindringen. Nach den Ergebnissen des wissenschaftlichen Teams erhöhen Neutrophile die Penetrationseffizienz von Liposomen in den Tumor um ein Drittel.
Diese Entdeckung liefert ein klares Muster: Neutrophile erhöhen die Gefäßpermeabilität des Tumors für die gezielte Abgabe von liposomalen Arzneimitteln und erhöhen daher die Heilungschance. Darüber hinaus tritt dies nur bei einem Makroleak auf, bei dem es sich um eine große diffuse „Wolke“ von Liposomen handelt, die tief in den Tumor eindringt und so eine gezielte Arzneimittelabgabe gewährleistet.
„Die Unterscheidung zwischen den beiden Arten von Lecks ist wichtig, um den Mechanismus der Wirkungsweise von Medikamenten auf Liposomenbasis zu verstehen. Unsere Ergebnisse zeigen, dass Mikroleckagen nicht nur zur Abgabe von Arzneimitteln an Tumorzellen beitragen, sondern auch für die unerwünschte Anreicherung in gesunden Geweben verantwortlich sind. Die therapeutische Wirkung wird durch Makroleakings erzielt und durch Neutrophile verstärkt “, betonte Viktor Naumenko.
Das Team setzt derzeit Laborstudien fort, um die unerwünschten Nebenwirkungen der Liposomentherapie zu reduzieren. Die Entwicklung künstlicher Stimulationsmechanismen für die Produktion von Neutrophilen im Körper des Patienten zur Verbesserung der Onkotherapie ist eines der vielversprechenden Anwendungsgebiete der erhaltenen Daten.