A la luz de mis sueños de
terapia génica con la ayuda de los factores de Yamanaki , Liz Parrish decidió refrescar la memoria de los detalles del autoexperimento. ¿De repente, ella aceptará actuar como el primer paciente para la terapia Yamanova? No, estoy bromeando, por supuesto, pero hay cierta seriedad en este chiste. Realmente creo que la terapia génica para el contragolpe epigenético tiene potencial terapéutico. Y por unos $ 15-20 millones, este potencial puede ser llevado al comienzo de los ensayos clínicos o refutado.
De todos modos, volviendo del cielo a la tierra, ¿qué se presentó Liz Parrish? Según sus garantías, Liz se presentó a 2 terapias genéticas diferentes utilizando vectores virales adenoasociados (AAV): el gen de la telomerasa hTERT y el gen FS de la folistatina (diseñado para inhibir la miostatina).
Debe aclararse que, muy probablemente, no se trataba de dos variedades de AAV, sino mucho más, ya que Liz necesitaba preparar un AAV específico para cada tipo de tejido objetivo. Y luego tuvo que entregar este AAV particular a este tejido objetivo. Esto es lo que entendí de esta entrevista con Liz en Longecity Now:
http://www.longecity.org/media/Liz_Parrish_LongeCity_Now2016.mp3Vale la pena señalar que el AAV no se integra deliberadamente en el genoma; es decir, para las células que se dividen, las células hijas NO recibirán los genes que se entregaron a la célula original usando AAV. Pero tendrán telómeros alargados, siempre que el gen hTERT funcione según lo previsto en su célula madre:
https://www.addgene.org/viral-vectors/aav/aav-guide/El hecho de que Liz se inyectara algún tipo de inyección (sí, escépticos, te escucho) es confirmado por el director de un documental sobre ella que filmó este procedimiento en Colombia:
El MIT Technology Review trató de confirmar aspectos de la historia de Parrish hablando con Matthew Andrews, un director de cine de Los Ángeles, quien dijo que iba a suspender el tratamiento de Parrish en septiembre, un modesto consultorio médico con un médico y una enfermera que también realizaron análisis de sangre. . “Era una sala de tratamiento, no había dispositivos particularmente de alta tecnología. Se acostó en la cama sin anestesia, recibió inyecciones y se conectó a un gotero ”, dijo. “Era aburrido desde el punto de vista de un observador externo, aunque, por supuesto, no sé qué estaba pasando dentro del cuerpo.
https://www.technologyreview.com/s/542371/a-tale-of-do-it-yourself-gene-therapy/
Por cierto, según Liz, la terapia con AAV entregó con éxito el gen de la telomerasa hTERT en solo el 20% de sus células. Ella dijo esto en su presentación en Digital October en Moscú, 22 de junio de 2016 (aproximadamente a las 1:46:41 en este video):
¿Por qué Liz eligió estos tratamientos particulares? Michael Fossel y Bill Andrews han estado hablando sobre el potencial antienvejecimiento de la telomerasa durante muchos años. Maria Blasco confirmó un enfoque específico para el uso de la terapia TERT en ratones, donde extendió tanto la supervivencia promedio como la edad máxima de los ratones en dos grupos: uno recibió inyecciones de TERT a los 420 días de edad (un aumento en la supervivencia media del 24% y un aumento del 13% en el máximo esperanza de vida), y el otro a la edad de 720 días (aumento de la supervivencia media en un 20% y aumento de la esperanza de vida máxima en un 13%):
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3494070/Por cierto, Michael Fossel dijo que aconsejó a Liz varias veces, ya que estaba trabajando en el comienzo de ensayos clínicos de un enfoque muy similar a la terapia con hTERT para pacientes con enfermedad de Alzheimer:
Nuestra firma de biotecnología, Telocyte, tiene la intención de hacer casi lo mismo, pero con una serie de diferencias importantes: utilizaremos solo una terapia: terapia con el gen de la telomerasa (hTERT), y tenemos la intención de realizar ensayos humanos completos con la aprobación de la FDA, con el procedimiento armonización de IRB, así como el uso de estándares de producción de terapia GMP.
Al mismo tiempo, aplaudo el coraje de Liz al usar a sí misma como sujeto de investigación. Usarte a ti mismo como sujeto elimina muchas de las críticas éticas que serían más relevantes si Liz usara a otros pacientes. Como muchos otros, vemos la urgente necesidad de desarrollar e implementar intervenciones terapéuticas más efectivas: los pacientes no solo sufren, sino que también mueren mientras tratamos de avanzar. En el caso de la enfermedad de Alzheimer, por ejemplo (nuestro principal objetivo terapéutico para los telocitos), desafortunadamente, actualmente no hay tratamientos efectivos, y una gran población de pacientes se ve obligada a morir mientras desarrollamos un nuevo tratamiento para ellos. Un enfoque lento y equilibrado para buscar tratamiento apenas es bienvenido por ellos en tal situación.
Y aun así ...
Decidimos seguir un enfoque estándar, con la aprobación de la FDA de ensayos en humanos, por tres razones que consideramos importantes: 1) queremos garantizar la seguridad, 2) queremos garantizar la eficiencia y 3) queremos garantizar la confianza. La cuestión de la seguridad no es fácil: el Alzheimer es fatal, por lo que la seguridad aquí puede parecer menos importante que la efectividad. Y realmente creemos que no hay razón para no probar la terapia experimental para pacientes desesperados si los riesgos fácilmente eliminables se eliminan por adelantado (por ejemplo, utilizando procesos de producción seguros para vectores virales). La cuestión de la efectividad tampoco es fácil: alguien dice que necesita probar cualquier terupia, incluso remotamente efectiva. Pero no vemos ninguna razón para usar una terapia mínimamente efectiva si podemos proporcionar la terapia más efectiva usando solo un poco más de previsión y cuidado. La cuestión de la confianza tampoco es simple: alguien afirma que será suficiente para curar al menos a un paciente de la enfermedad de Alzheimer. Esto es así, pero solo con la condición de que nos crean que realmente lo curamos. Pero si nadie nos cree, el hecho de que hayamos curado a alguien solo no ayudará a millones de otros pacientes.
http://www.michaelfossel.com/blog/?p=139
En cuanto a la segunda terapia de Liz con el gen de la folistatina, según tengo entendido, este enfoque fue probado previamente en mí mismo por el socio de Liz y copropietario de BioViva, Jason Williams. Williams, por cierto, había desarrollado previamente varias otras terapias experimentales de AAV genéticas, y también tiene su propia clínica en Colombia, donde ofrece algunas de estas terapias a los pacientes (pero Liz no realizó sus procedimientos en su clínica):
http://www.neuralgene.com/technology-pipeline.cfmLa terapia específica de AAV con FS que Liz se presentó ya pasó con éxito la segunda fase de CI en Gran Bretaña, y ahora está pasando por la tercera:
http://www.nature.com/mt/journal/v23/n1/full/mt2014200a.htmlPregunta: ¿Por qué probar dos terapias tan diferentes al mismo tiempo? Liz dice que espera un efecto sinérgico, y que hay evidencia de que la terapia con FS puede agotar las células madre, y la terapia con hTERT debería ayudar a prevenir esto.
Los primeros resultados de la terapia informados por BioViva fueron que los telómeros de los linfocitos Lys se extendieron de 6,710 a 7,330 pares de bases después del tratamiento. La afirmación de que esto es equivalente a "retroceder 20 años de acortamiento de los telómeros", aunque parezca patético, tiene algún tipo de justificación científica, ya que la velocidad promedio del acortamiento de los telómeros de leucocitos es de aproximadamente 30 pares de bases por año:
Durante el envejecimiento normal, los telómeros se acortan en ayudantes T CD4 +, células T citotóxicas CD8 + y células B productoras de anticuerpos con una tasa anual de 19–35 pares de bases
http://www.ncbi.nlm.nih.gov/pubmed/10903716
http://www.ncbi.nlm.nih.gov/pubmed/12437664
Al mismo tiempo, algunas personas notan que la elongación de los telómeros en un 9% está dentro del 8-10% del error de medición de qPCR, pero de lo que leí sobre qPCR, el 8-10% es un error entre laboratorios o entre métodos, y no un error al usar El mismo equipo en el mismo laboratorio. Es decir, puede ver una diferencia del 10% en los resultados al analizar la misma muestra en dos laboratorios diferentes o al usar dos métodos diferentes. Pero Liz afirma que sus telómeros se midieron tanto antes como después de recibir tratamiento en el mismo laboratorio: los Laboratorios SpectraCell.
Además, Liz afirma que los resultados fueron confirmados por otras dos organizaciones científicas: la ONG belga HEALES y la Fundación Británica para la Investigación Biogerontológica. Por lo tanto, la probabilidad de que la diferencia del 9% se deba a un error de medición me parece mucho menor que la probabilidad de que esta diferencia se deba a cambios biológicos reales. Por supuesto, en aras de la confianza, sería necesario analizar todas las muestras de Liz utilizando otros métodos (no qPCR, sino TRF, por ejemplo), y en otros laboratorios. Espero que esto se haga.
Por cierto, debo señalar que la pregunta sigue siendo cuán independientes son las organizaciones científicas mencionadas anteriormente, ya que HEALES está asociado con ILA (International Longevity Alliance), donde Liz es miembro de la junta directiva, y la Fundación Británica para la Investigación Biogerontológica está dirigida por Avi Roy, quien también es Director de Ciencia, BioViva.
Por cierto, en una conferencia de prensa en Moscú, Liz dijo que envió algunas de sus muestras antes y después de la terapia al laboratorio de George Church en Harvard, que prometió llevar a cabo un análisis detallado de ellas, incluidas pruebas que evalúen el cambio de metilación (con la esperanza de ver " un "perfil más joven de
horas de
metilación identificado en las obras de Steve Horvath". Liz habla de esto en el mismo video (alrededor de 1:48:41):
George Church es, por supuesto, genial, porque es casi Einstein de la genética moderna, pero ... es miembro del Consejo Científico BioViva. Esperemos que con el tiempo haya un tercero completamente independiente que se comprometerá a confirmar los resultados de Liz, preferiblemente utilizando otro método para medir los telómeros. En la misma conferencia de prensa, Liz dijo que estaba lista para proporcionar sus muestras para su análisis en laboratorios independientes, siempre que tuvieran una buena reputación.
En marzo de 2017, Liz emitió un comunicado de prensa con sus últimos resultados de sus análisis:
https://bioviva-science.com/blog/2017/3/2/dual-gene-therapy-has-beneficial-effects-on-blood-biomarkers-and-muscle-compositionAllí, afirma que los datos de resonancia magnética de sus caderas muestran una disminución en el marmoleo de los músculos, es decir, una disminución en la cantidad de depósitos de grasa intramuscular, que puede considerarse como un efecto positivo de la terapia con folistatina:
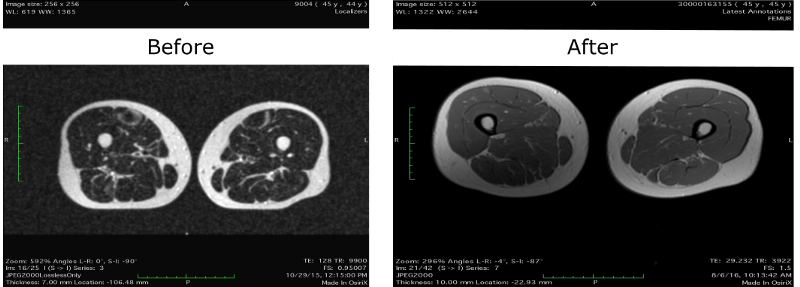
Pero, tal vez, la diferencia visual entre las imágenes se debe solo a una mejora en la resolución de la resonancia magnética: la imagen anterior se tomó en un dispositivo de 1 Tesla, y la nueva fue de 1,5 Tesla. Además, me parece que las imágenes se obtuvieron de lugares ligeramente diferentes en las caderas: las imágenes más recientes, a juzgar por la distancia entre las piernas, se tomaron de las rebanadas ligeramente más bajas de la pelvis que las viejas. Y cuanto más bajos son los sacerdotes, más bajo es el porcentaje de grasa en las piernas. Aunque, tal vez Liz solo separó las piernas un poco más en la última prueba.
Por cierto, en los datos recientes de Liz, fue interesante ver un nivel bastante alto (1.6) de proteína C reactiva antes de la introducción de la terapia génica y una disminución posterior de la PCR a 0.2 en febrero de 2016. Sería interesante saber cuál fue el valor de la PCR en la ronda de pruebas en 2016: Liz proporciona los valores de glucosa y triglicéridos de agosto de 2016, pero no la PCR.
En conclusión, mencionaré un par de críticas sobre el uso de la longitud de los telómeros de los linfocitos como marcadores de "rejuvenecimiento":
- (A) la medición de los telómeros de los linfocitos no es una buena métrica en principio, ya que tienen demasiada variación en la longitud de los telómeros
- (B) la longitud promedio de los telómeros, especialmente en los glóbulos blancos (WBC), puede fluctuar naturalmente durante un período de tiempo bastante corto (menos de 2 años)
Bajo el ítem (A), Michael Fossell escribió una publicación detallada en su blog, así que solo le daré un enlace:
http://www.michaelfossel.com/blog/?p=182Y de acuerdo con el ítem (B): sí, la longitud promedio de los telómeros puede, aparentemente, a veces aumentar espontáneamente, aunque no tanto como en el caso de Liz, y esto ocurre con poca frecuencia (en 10-15% de los casos). Aquí hay dos buenas obras sobre el tema:
http://www.clinsci.org/content/128/6/367.fullhttps://www.hindawi.com/journals/jir/2016/5371050/Este gráfico del último trabajo es especialmente indicativo: como podemos ver, durante 18 meses suficientes personas han alargado los telómeros (todos los puntos están por encima de cero):
Por cierto, algunos escépticos incondicionales requieren evidencia de que Liz realmente introdujo los genes reclamados. En principio, esto podría verificarse rápida y económicamente utilizando RT-qPCR en los linfocitos Lys antes y después de la terapia: si el AAV administraba sus genes, deberíamos ver la diferencia en las curvas. Quizás el laboratorio de George Church podría haber hecho tal análisis. Pero no creo que esto sea necesario, porque mentir francamente acerca de presentarte estos genes a ti mismo y luego enviar tus muestras a George Church sería el colmo de la idiotez.