Correlación no significa causalidad. Esta frase se encuentra en la cabeza de todos aquellos que estudian estadísticas de las primeras lecciones. Además, la correlación, por supuesto, insinúa esta misma causalidad, a menudo para dos parámetros de correlación, si no una relación causal directa, entonces al menos una causa externa común. Uno de mis ejemplos favoritos: las ventas de helados se correlacionan bien con la cantidad de personas ahogadas, pero ambas variables son independientes entre sí y se deben al tercer factor: el clima.
En la lucha contra el envejecimiento, surgen constantemente nuevas y nuevas hipótesis de alguna Gran Terapia, que ayudará a obtener una victoria decisiva en esta lucha, y rápidamente se ponen de moda. No hace mucho tiempo, era Su Majestad la Telomerasa, pero hace un par de años fue retirada del trono de la
Senolítica , un medio para combatir
las células senescentes . Estas son
células zombis que no solo no cumplen sus funciones y al mismo tiempo se niegan a morir, sino que también envenenan todo a su alrededor, destacando un cóctel de sustancias proinflamatorias llamadas "
fenotipo secretor asociado a la senescencia " o SASP.
Es cierto que, como ha sucedido a menudo, la correlación puede intentar mostrar su astucia y dirigirnos por el camino equivocado: el hecho de que el cuerpo se vuelva más células senescentes con el envejecimiento no significa que sean su conductor. Y es muy probable que resulten ser un rastro tan falso. Estudios recientes de Andrei Gudkov, profesor, doctor en ciencias biológicas, fundador y director científico de la compañía biotecnológica Cleveland BioLabs, y en general uno de los biólogos rusos más exitosos en el extranjero, cuyos resultados
presentó en la conferencia Scripps sobre biología del envejecimiento en enero de 2017, me hacen más para estar seguro de esto En general, para mí es muy interesante, incluso diría datos revolucionarios. Aquí está su presentación de video completa, mira, no te arrepentirás:
Observaciones experimentales
¿Qué dijo Andrei tan revolucionario? Y aquí está lo que:
- En ratones irradiados a las 10 semanas con una dosis de radiación "fatal" de 11 Gy (aparentemente esta dosis es fatal si la médula ósea del donante no se trasplanta inmediatamente después de los ratones, como se hizo en los experimentos de Gudkov), no se detectan células senescentes incluso a través de 30 semanas después de la exposición. Lo cual es muy extraño, porque la irradiación in vitro (en cultivos celulares) es una forma garantizada de enviar una parte significativa de las células a un estado senescente (aquí, en la foto a continuación, los racimos oscuros son células senescentes; tenga en cuenta cuántos hay al irradiar un cultivo celular con una dosis de 11 Gy ):

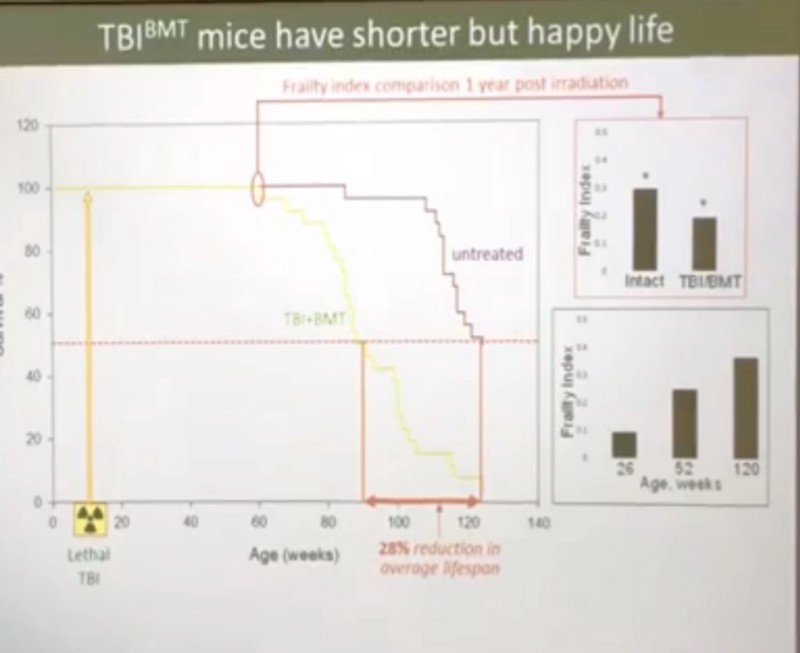
- Además, el índice de fragilidad en ratones irradiados un año después de la radiación fue mejor que en los ratones control que no recibieron irradiación, y los ratones irradiados vivieron no menos que los controles (RV promedio a las 90 semanas versus control 120, y el RV máximo de los ratones irradiados fue 120 semanas versus 135 semanas en otro experimento):
- Al mismo tiempo, no solo no se detectan células senescentes en ratones, sino que el perfil de citoquinas de la respuesta inflamatoria no difiere de los ratones control, lo que no se puede decir de los ratones irradiados viejos, cuya respuesta inflamatoria es mucho mayor (el mismo inflamatorio ). Es decir, el sistema inmunitario después de la irradiación funciona perfectamente al mismo nivel que el de los pares no irradiados. Aquí, sin embargo, es importante recordar que la médula ósea en ratones irradiados es donante, y que es él quien es la fuente de las células madre hematopoyéticas, los precursores de la gran mayoría de las células inmunes (los macrófagos tisulares y otros residentes inmunes tisulares son una excepción). Pero en cualquier caso, es muy extraño ver que la radiación no afecta ni la respuesta inflamatoria ni la cantidad de células senescentes. La siguiente diapositiva muestra ratones irradiados de 40 semanas (tercera fila), en comparación con ratones no irradiados de 40 semanas (primera fila) y 98 semanas (segunda fila). Se ve claramente que las células senescentes (manchas azules) están presentes solo en ratones no irradiados de 98 semanas de edad. La última columna a la derecha es el perfil de citoquinas de la respuesta inmune:

- Por cierto, la transcripción de ratones irradiados y no irradiados de 40 semanas de edad es casi idéntica, en contraste con el transcriptoma de ratones de 98 semanas de edad:
- Y la resistencia al cáncer en ratones irradiados es generalmente mayor. En el modelo de cáncer inducido, cuando los ratones fueron inyectados con células de melanoma (células de melanoma B16 ), los ratones irradiados vivieron más tiempo que los no irradiados, aunque tenían muchas más metástasis pulmonares:
- Y los tumores cancerosos en los ratones irradiados crecieron mucho más lentamente (curva roja versus verde), y la tasa de supervivencia promedio fue 3.5 veces mayor que la de los no irradiados (es decir, incluso mejor que la tasa de supervivencia promedio igual en el experimento anterior):
La hipótesis de Andrei Gudkov
¿Cuál es la hipótesis de Andrei Gudkov sobre este tema? ¿Qué, en su opinión, explica todas estas misteriosas observaciones resumidas en la siguiente diapositiva?
La hipótesis es la siguiente: a medida que se produce daño en el ADN, la mayoría de las células (no destruidas de inmediato por la apoptosis) en las que el cuerpo no puede repararse de inmediato no puede transformarse de inmediato en senescentes (como en opinión de Andrey, la hipótesis generalmente aceptada hoy en la diapositiva anterior ), y se congela en un cierto estado llamado DSPC (
Células propensas a la senescencia latentes, o "las células pro-senescentes latentes").
Es decir, estas células continúan viviendo y funcionando, y se vuelven senescentes solo si necesitan compartir, pero luego entra en juego el sistema inmune (innato), en el que la función de atrapar y matar las células senescentes se ajusta perfectamente: los macrófagos y las inmunoglobulinas son responsables de ello. M (IgM). Esquemáticamente, la nueva hipótesis de Andrei se ve así:
Es cierto, Andrei cree que todo lo anterior es cierto solo para
las células
mesenquimales , y las células epiteliales después de la irradiación siguen el camino más alto en la diapositiva anterior, es decir, las roturas de ADN se reparan en ellas de inmediato. En apoyo del hecho de que las células mesenquimales están llenas de descomposiciones, Andrei cita datos de que los ratones irradiados contienen
un orden de magnitud más roturas de ADN de doble cadena:
Si Andrei revisó las células epiteliales en busca de roturas bicatenarias para probar su hipótesis de que las roturas se repararon de inmediato, no lo sé. Pero sobre la base de datos experimentales sobre células mesenquimales, Andrei cree que después de la irradiación, casi el 100% de ellas se vuelven "pro-senescentes" (DSPC), como escribe en esta diapositiva:
Y el mismo hecho de que durante la división se vuelven senescentes y son destruidos por el sistema inmune, según Andrey, solo explica la mejor resistencia de los ratones irradiados al cáncer: el tumor no puede crecer rápidamente, ya que los nuevos vasos sanguíneos diseñados para suministrarle sangre crecen en tal los ratones son mucho más lentos porque las células progenitoras de estos vasos son todas pro-senescentes.
Andrei demostró la pro-senescencia de tales células experimentalmente: en el cultivo celular, las células de los ratones irradiados se convierten casi inmediatamente en senescentes y no crecen, en contraste con las células de los ratones de control:
Lo que, según Andrei, confirma esta hipótesis, es que en una dieta alta en calorías (o alta en
grasas , para ser precisos), los ratones irradiados mueren aún más rápido. Es cierto que en otros experimentos se demostró que una dieta rica en grasas en sí misma acorta la vida de los ratones, y el hecho de que el grupo de control no irradiado con una dieta rica en grasas también perdió alrededor del 10% de la población simultáneamente con el grupo irradiado, a mis ojos, genera algunas dudas. . Por lo tanto, me gustaría ver la curva de supervivencia completa para el control no irradiado con una dieta rica en grasas:
Sistema inmunitario - Lijadora forestal
¿Cómo demostró Andrei que el sistema inmunitario es responsable de controlar y eliminar las células senescentes? Muy hermosa Colocó las células senescentes en una construcción que se asemeja a una jaula de metal para buceadores de tiburones, e implantó estas estructuras en un ratón. Y luego miró a qué tipo de tiburones estaban navegando. Los macrófagos (con el entorno habitual de otras células inmunes, eosinófilos, etc.) resultaron ser tiburones.
Aquí en este gráfico se muestra que sin “células” protectoras, las células senescentes desaparecen muy rápidamente (la población disminuye 100 veces) después de la implantación en el ratón (curva verde), y cuando se colocan en una cápsula protectora, haciéndolas inaccesibles para cualquier otra célula, sus números prácticamente no disminuye (curva azul):
Y aquí están los tiburones: macrófagos. Y, sorprendentemente, estos macrófagos comienzan a expresar un marcador senescente de beta-galactosidasa, que anteriormente se consideraba un marcador de células exclusivamente senescentes. No entiendo por qué sucede esto, y Andrey, en mi opinión, también.
Además, Andrei demostró en otro experimento que una parte significativa de esas células que antes consideramos senescentes son macrófagos, que en sí mismos son apenas senescentes (es decir, no secretan
SASP , el cóctel de factores proinflamatorios ya mencionado), pero, muy probablemente, dispersos entre la población de células senescentes reales, como los luchadores en el campo de batalla:
La pregunta principal para mí y para Andrei es por qué estos luchadores hacen frente a las células senescentes tan bien antes de envejecer, y luego dejan de hacerlo abruptamente. Aquí nuestros puntos de vista divergen. Andrei cree que con la edad, cierto recurso del sistema inmune se agota, y es por eso que deja de lidiar con ellos. Y en ratones irradiados, este recurso se usa más rápido, porque hay muchas más células senescentes:
Por supuesto, no estoy de acuerdo con la hipótesis del recurso. No puedo imaginar que 11 Gy de radiación, que convierte el 100% de las células mesenquimales en células pro-senescentes, comience a agotar el recurso solo después de un año, e incluso entonces reduce el páncreas promedio en solo un 28% y el páncreas máximo en un 18-20%.
Al mismo tiempo, estoy muy interesado en por qué las células epiteliales, de acuerdo con la hipótesis de Andrew, se salvan de este destino. Me parece importante comprender qué sucedió exactamente en ratones irradiados con tejidos que se dividen rápidamente y cómo esto encaja con la hipótesis de las células pro senescentes. De hecho, en el cuerpo hay bastantes poblaciones que se renuevan rápidamente: intestinos, estómago, pulmones, sistema reproductivo (el sistema sanguíneo no cuenta, ya que está formado principalmente por la médula ósea, que se trasplantó de donantes intactos a ratones irradiados):
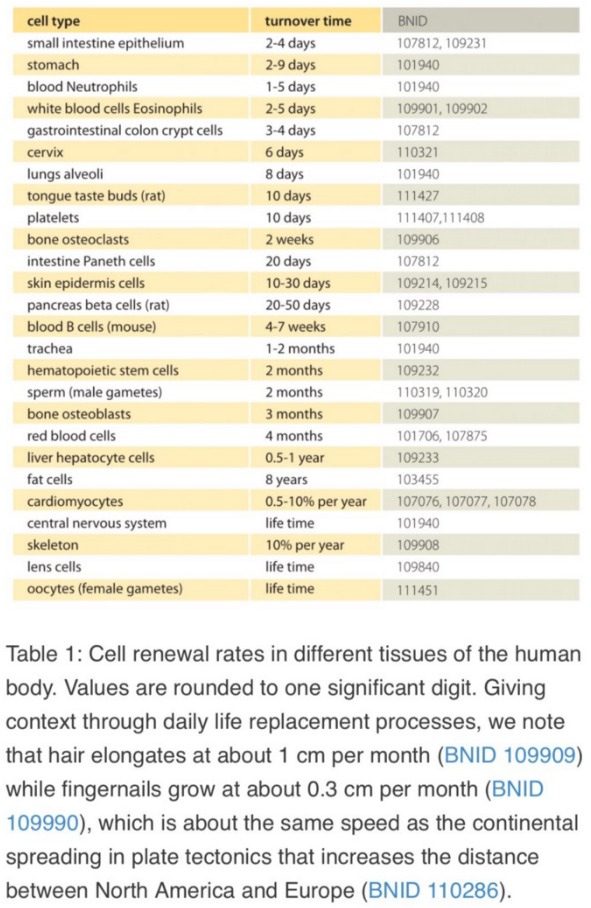
Además, no está muy claro para mí cómo las células mesenquimales de los ratones irradiados lograron continuar funcionando y sintetizar correctamente las proteínas correctas para su vida, si tenían muchas más rupturas de ADN (porque las proteínas están construidas a partir de ADN). Por cierto, este es otro excelente argumento en contra de la hipótesis del "envejecimiento por la acumulación de mutaciones" (después de todo, hay alguien más que cree en esta hipótesis ...). Si recuerdas, las roturas de ADN de doble cadena en ratones irradiados fueron
un orden de magnitud mayor.
En cualquier caso, veo un concepto mucho más plausible de una reducción programada en la calidad de los mecanismos de reparación, que en la juventud, incluso después de una megadosis de radiación, no permite la aparición de células senescentes, y en la vejez causan números similares en ratones de control.
Al mismo tiempo, una dieta rica en grasas es una señal para que el reloj interno acelere el envejecimiento. Y la restricción calórica es la señal opuesta, extendiendo significativamente la vida de los ratones comunes. Sí, las dosis subletales de radiación (25 a 50 veces más altas que el fondo), por cierto, también prolongaron la vida de los ratones en un 20%. Lo que, a mi entender, no encaja bien con ningún concepto de recursos. Por cierto, sería interesante ver el efecto de la restricción calórica en ratones irradiados.
Entonces, ¿qué pasa con el Senolítico?
Andrei tiene su propio senolítico,
EBS3899 (de
Everon Biosciences ), que funcionó muy bien en cultivos celulares, pero cuando se tradujo en un organismo vivo, fue, según Andrei, mucho menos efectivo: el efecto de un aumento de ALS en un 13% se observó solo en ratones machos, y solo si el senolítico se usó a las 89 semanas de vida (la aplicación anterior para aumentar el páncreas no condujo, ya que su uso en mujeres):
Por lo tanto, la conclusión principal de Andrei, como lo escuché, es que debemos buscar herramientas para influir en otros mecanismos de envejecimiento (llaves ajustables en la diapositiva) si queremos lograr un aumento mucho mayor en el páncreas:
Y es difícil estar en desacuerdo con Andrey.
Por cierto, quizás incluso Ned David, jefe de Unity Biotechnology, la startup más grande para el desarrollo de la senolítica, en la que invirtieron Peter Thiel y Jeff Bezos, está de acuerdo con él. David
ya se ha reunido dos veces con Juan Carlos Ispisua Belmonte, autor de
mi trabajo favorito , y en marzo de 2017 ya discutieron algunos posibles próximos pasos.
Bueno, con gran interés seguiremos el desarrollo de los eventos.