Durante las últimas décadas, la ciencia ha logrado avances significativos en el tratamiento del cáncer, y aunque todavía estamos lejos de derrotar por completo esta terrible enfermedad, los médicos tienen cada vez más herramientas para destruir tumores o limitar su crecimiento. Lo principal es que les dan a los pacientes con cáncer la oportunidad de vivir más tiempo.
Una de esas herramientas es la activación de la inmunidad de una persona para combatir las células cancerosas. Hay toda un área dedicada a esto: inmunooncología. Se concentra mucha atención en él, es en esta área donde se realiza la mayor cantidad de investigación hoy y se están desarrollando los medicamentos más prometedores.
En
Medicine 24/7 utilizamos activamente la inmunoterapia, y vemos que da buenos resultados. Es cierto que nos enfrentamos al hecho de que muchos pacientes no conocen este método de tratamiento o lo consideran todavía insuficientemente estudiado y no confiable.
En esta publicación, trataremos de aclarar las preguntas: qué es la inmunoterapia, cómo funciona y quién puede ayudar.
 Judy Perkins Tenía cáncer de mama terminal que se curó completamente con el último método de inmunoterapia.Amenaza oculta ¿Cómo funciona el cáncer?
Judy Perkins Tenía cáncer de mama terminal que se curó completamente con el último método de inmunoterapia.Amenaza oculta ¿Cómo funciona el cáncer?Las células cancerosas son rebeldes mutantes que han logrado burlar al sistema.
En el proceso de la vida, todas las células del cuerpo pasan por etapas de desarrollo estrictamente definidas, realizan funciones específicas, se multiplican de acuerdo con reglas estrictas y eventualmente envejecen y mueren. Este es un proceso natural. La muerte programada de células viejas que han acumulado mucho daño se llama apoptosis.
Sin embargo, bajo la influencia de la herencia o de factores externos adversos, algunas células acumulan errores genéticos y se “rebelan”: se niegan a vivir de acuerdo con el algoritmo establecido por la naturaleza, comienzan a multiplicarse sin control o no mueren a tiempo. Esto no es raro. Potencialmente, las células cancerosas pueden aparecer periódicamente en cada una, esto es normal. Casi siempre tales "advenedizos" son asesinados por el servicio de seguridad interno del cuerpo:
inmunidad .
Una de las funciones principales en este proceso es desempeñada por los linfocitos T o, más simplemente,
las células T. Responden a un
antígeno (una sustancia ajena al cuerpo), reconocen y destruyen enemigos potenciales: por ejemplo, microbios o material de donante inapropiado. Normalmente, los linfocitos T también matan las células del cuerpo, que comenzaron a mutar y no se comportan de acuerdo con las reglas. Por lo tanto, el cáncer no ocurre en todos: en la mayoría, la inmunidad hace frente a los trastornos antes de que se propaguen.
Pero el cáncer busca sobrevivir y las células tumorales están tratando de capturar tantos recursos como sea posible para ser "más exitosos". Se multiplican más rápido, secretan factor de crecimiento vascular (para atraer más sangre y nutrientes al tumor), desarrollan resistencia a los medicamentos, obligan a las células madre a aumentar el crecimiento de los tejidos tumorales (enviando señales engañosas con una solicitud de regeneración).
Las células cancerosas logran un éxito particular en el disfraz: algunas de ellas eliminan proteínas antigénicas especiales de su superficie por las cuales las células T pueden reconocerlas. Otros secretan moléculas especiales que suprimen el sistema inmunitario, y algunos incluso forman híbridos con macrófagos (uno de los tipos de células inmunes), ¡y se convierten literalmente en superpoderes!
Por un lado, el parentesco con las células normales del cuerpo les ayuda en esto, una especie de disfraz congénito. Por otro lado, la variabilidad genética de las células cancerosas les da una mayor adaptabilidad. Cuantas más mutaciones se hayan acumulado en el ADN de la célula en el momento de su malignidad (conversión a malignidad), mayores serán las posibilidades de que sobreviva a la respuesta inmune y desarrolle un plan de captura exitoso.
Despertar del poder. Historia de los descubrimientos NobelLa inmunidad humana es en realidad un verdadero ejército de asesinos despiadados, y después de cada "operación de combate" para neutralizar a otro enemigo, deben ser tranquilizados y transferidos de un ejército a una posición pacífica. Este mecanismo reduce la temperatura a valores normales y detiene la inflamación cuando el peligro ha pasado y la infección ha sido derrotada.
En 2018, el Premio Nobel de Fisiología o Medicina fue otorgado al estadounidense James Ellison y al japonés Tasuk Honjo por sus descubrimientos independientes en el mismo campo: ¿cómo ocurre exactamente este cambio del modo agresivo al silencioso?
Al principio, ninguno de los científicos pensó en el tratamiento del cáncer. Ambos querían entender más claramente el funcionamiento de la respuesta inmune. En ese momento, estaba claro que en la superficie de las células T y en la superficie de las células presentadoras de antígeno (
APC ) hay moléculas receptoras que actúan entre sí, provocando o ralentizando el sistema inmunitario. Se descubrió el
TCR, un receptor de células T por el cual las células T reconocen las proteínas "enemigas" expuestas en APC.
Encontramos el complejo principal de histocompatibilidad MHC (complejo principal de histocompatibilidad), con la ayuda de los cuales las APC presentan piezas de proteínas extrañas para la identificación de las células T. Peter Doherty y Rolf Zinkernagel recibieron su Premio Nobel por descubrir este escenario.
Los científicos entendieron que los receptores en la superficie de las células T funcionan en conjunto con los coestimuladores en la superficie de APC. La proteína
CD28 de la superficie de las células T se aisló en
1980 , pronto se encontró la molécula B7 en la superficie de APC. Durante los experimentos, los investigadores del grupo Ellison transfirieron el gen
B7 a las células cancerosas, y comenzaron a ser rechazados por el tejido sano. Resultó que B7 se une a CD28 en la célula T, y por lo tanto comienza su trabajo: la célula T destruye la célula tumoral, en cuya superficie sobresale la proteína B7.
En
1987 , Ellison descubrió el
antígeno 4 de los linfocitos T citotóxicos
CTLA-4 (antígeno 4 asociado a los linfocitos T citotóxicos) y descubrió que la estructura de esta proteína es similar a la conocida CD28, y también puede unirse a B7, sin embargo, con esto funciona exactamente de la manera opuesta: detiene la respuesta inmune.
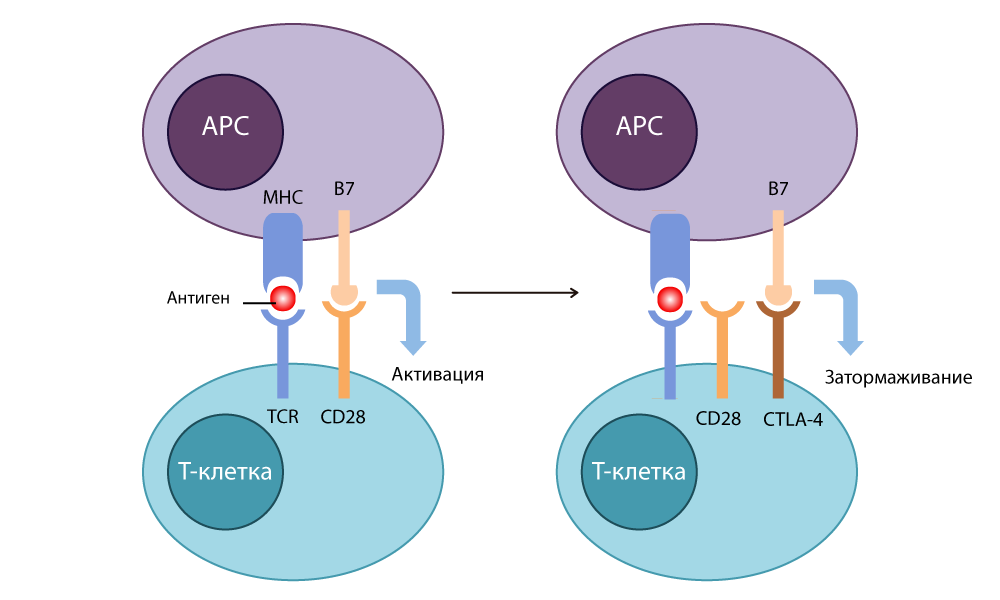 Acción CTLA-4
Acción CTLA-4Primero, los médicos iban a usar este "freno" para combatir las enfermedades autoinmunes (cuando la inmunidad comienza a atacar las células sanas del cuerpo). Pero a Allison se le ocurrió algo brillante: no ejerza presión sobre el freno, sino apáguelo.
Desarrolló un anticuerpo inhibidor (interruptor) que se une al CTLA-4 y evita que se cierre con B7 para apagar las respuestas inmunes. Moléculas B7 libres unidas a CD28, la célula T se activó y estaba lista para matar nuevamente. Cuando realizó experimentos en ratones con cáncer con cáncer en 1995, quedó claro que incluso las astutas células cancerosas no podían esconderse de esos linfocitos T sin frenos. En 2010, se realizaron estudios exitosos en pacientes sin esperanza. En algunos pacientes, el melanoma desapareció junto con las metástasis, ¡un resultado increíble!
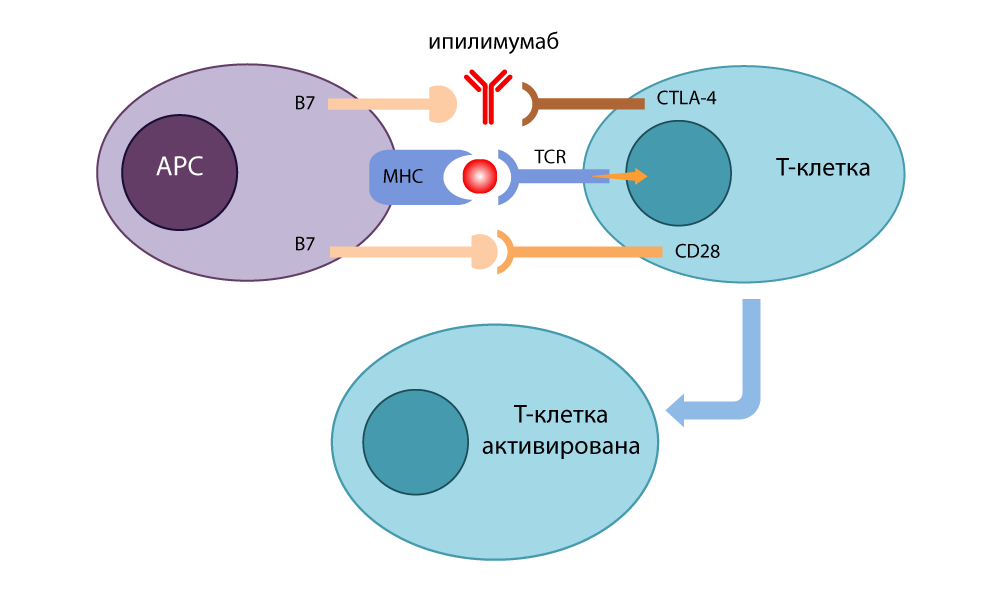 La acción del inhibidor de CTLA-4 - ipilimumab
La acción del inhibidor de CTLA-4 - ipilimumabAl mismo tiempo, en Kyoto,
Tasuku Honjo encontró otra molécula receptora en la superficie de la célula T:
PD-1 (proteína de muerte celular programada-1 , proteína de muerte celular programable-1). Durante los experimentos (nuevamente en ratones que sufren mucho tiempo), los japoneses descubrieron que la desactivación del gen que codifica esta proteína provoca síntomas de enfermedad autoinmune en ratones, es decir, la inhibición de PD-1 también apaga los "frenos" de los linfocitos T y los hace agresivos y activos.
Honjo descubrió que PD-1 pone a las células T en modo de suspensión cuando se une a la proteína PD-L1 / PD-L2 en la superficie de una célula presentadora de antígeno (APC). El inhibidor PD-1 abrió este enlace y activó las células T nuevamente. La acción de este "freno" fue similar a la acción de CTLA-4, pero tomó una ruta diferente.
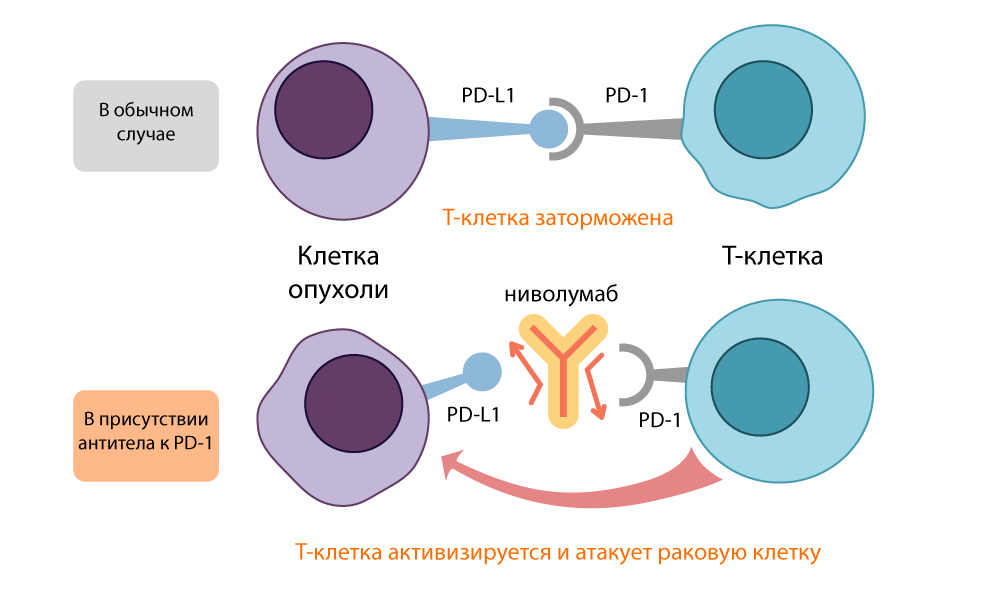 La acción del inhibidor PD-L1 - nivolumab
La acción del inhibidor PD-L1 - nivolumabAmbas moléculas "inhibidoras" abiertas, CTLA-4 y PD-1, se llamaron
puntos de control inmunitario (
puntos de control): es su número y actividad lo que hace que las células T tomen una decisión: calmarse o comenzar a luchar.
Resultó que los bloqueadores CTLA-4 activan la inmunidad en general, todas las células T, y el inhibidor PD-1 actúa más específicamente en los tumores, porque muchas células cancerosas llevan la "segunda pieza del rompecabezas", la molécula PD-L1 / PD-L2. Debido a esto, el tratamiento con inhibidores de PD-1 ofrece un menor riesgo de complicaciones.
La inmunidad contraataca. ¿Qué ayudan los inhibidores de punto de control?Allison y Honjo hicieron no solo una contribución seria a la comprensión de los procesos fisiológicos, sino que también lanzaron una ola de investigación práctica fundamentalmente nueva en medicina aplicada.
El descubrimiento de la inhibición de los puntos de control inmunitario (TIC) abre un área fundamentalmente nueva para encontrar soluciones. Antes de esto, los métodos para combatir el cáncer: cirugía, radiación y quimioterapia, estaban dirigidos directamente al tumor en sí, a la destrucción de las células cancerosas. Ahora los médicos tienen un campo enorme para la investigación en una dirección completamente diferente: cambiar la interacción de las células cancerosas con su entorno.
Por cierto, fue esta diferencia fundamental la que dio a los médicos un gran avance. Hasta ahora, el tumor se ha visto afectado según su ubicación. Para el cáncer de seno, un medicamento, para el cáncer de estómago, es completamente diferente. Y el inhibidor de las TIC pembrolizumab en 2017 se registró por primera vez en la historia de la oncología como un medicamento para el tratamiento de cualquier cáncer en cualquier órgano, si solo las pruebas confirman que el tumor tiene una propiedad especial: inestabilidad de microsatélites. Es decir, su ADN es especialmente propenso a las mutaciones. Anteriormente, nunca ha sido posible curar el cáncer para algún síntoma común. Este es un gran logro.
La revolución fue el resultado del uso de nuevos medicamentos contra los tipos de cáncer más agresivos: el melanoma metastásico en el estadio IV se consideraba incurable. Y los pacientes con dicho diagnóstico que se sometieron al curso del medicamento ipilimumab (bloqueador CTLA-4) en 2010, recibieron un año adicional de vida, por lo que el desarrollo del tumor se detuvo. En el 58% de ellos, el tumor disminuyó en un tercio.
En el tratamiento del cáncer de pulmón de células no pequeñas con nivolumab (inhibidor de PD-1), el riesgo de muerte de los pacientes disminuyó en un 40%.
El pembrolizumab (también un inhibidor de PD-1) mostró una disminución del 43% en el crecimiento tumoral en el grupo tratado por melanoma. El 74% de los pacientes vivieron sin deterioro durante el año, durante 18 meses hubo 71%. Es importante que el efecto de prescribir el medicamento supere los efectos secundarios en todas las etapas del desarrollo de la enfermedad.
Hoy en día, los inhibidores de CTLA-4 y PD-1 tratan el melanoma (incluido el inoperable), el cáncer de pulmón de células no pequeñas, el carcinoma de células escamosas de cabeza y cuello, el carcinoma de células renales, ciertos tipos de linfomas, cáncer de recto, vejiga y tumores con inestabilidad de microsatélites.
De particular interés son los estudios que muestran la efectividad de la
terapia combinada con fármacos anti-PD-1 y anti-CTLA-4.
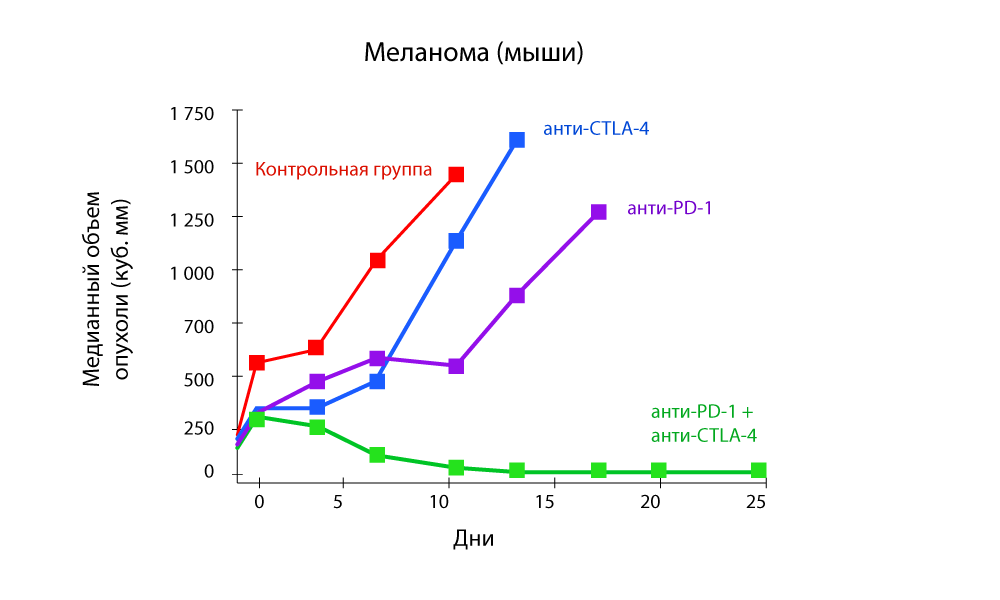 Cambio en el volumen tumoral: una fuerte disminución con la combinación de fármacos anti-PD-1 y anti-CTLA-4
Cambio en el volumen tumoral: una fuerte disminución con la combinación de fármacos anti-PD-1 y anti-CTLA-4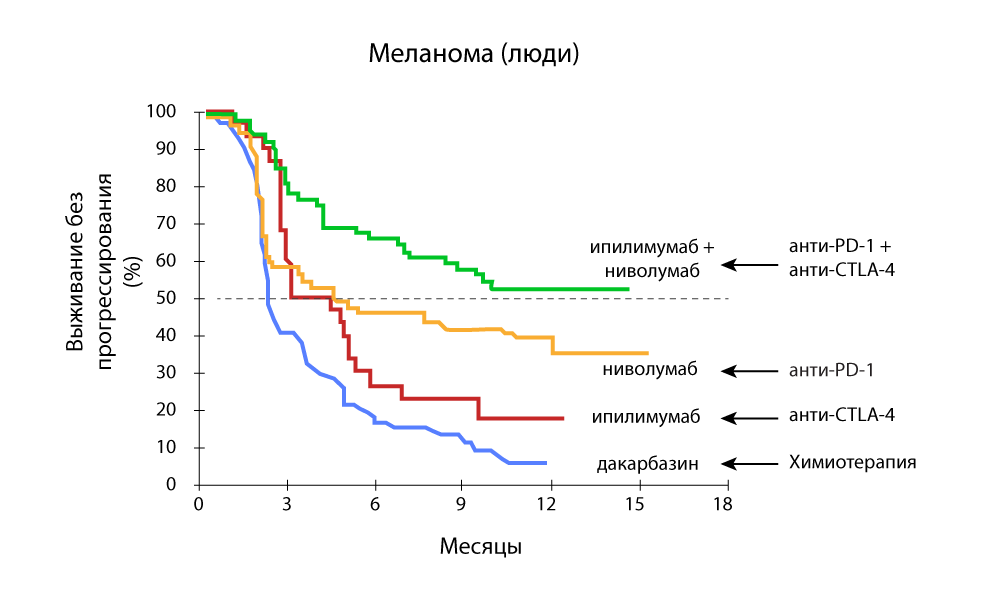 Supervivencia libre de progresión: la combinación de fármacos anti-PD-1 y anti-CTLA-4 es más efectiva
Supervivencia libre de progresión: la combinación de fármacos anti-PD-1 y anti-CTLA-4 es más efectivaEn Medicine 24/7, hemos estado usando con éxito pembrolizumab y nivolumab desde que se registraron en la Federación de Rusia. Seguimos toda la investigación extranjera y estábamos ansiosos por reponer el arsenal.
Ataque de los clones. Inmunidad Genéticamente ModificadaLos inhibidores de los puntos de control inmunitario están merecidamente en el centro de atención, pero este mecanismo aún no es perfecto y no puede curar ningún cáncer. Es bueno que en inmunoterapia las áreas de investigación relacionadas se desarrollen activamente. Una de las más prometedoras es la
terapia CAR-T .
La letra T en el nombre del método son las mismas células T inmutables de nuestra inmunidad. CAR (receptor de antígeno quimérico) es un receptor de antígeno quimérico. ¿Por qué el receptor se llama quimérico? Porque se ensambla a partir de varias partes tomadas de diferentes células, utilizando las habilidades de los ingenieros genéticos.
Las células T ordinarias tienen un receptor
TCR específico
( receptor
de células T) . Él "siente" todas las células del cuerpo a su paso y, si detecta alguna molécula extraña en la superficie de la célula, envía una señal de activación a la célula T. Eso, a su vez, se ocupa del propio alienígena no deseado o libera sustancias activas especiales (citocinas) y llama a otras células inmunes a "resolverlo". Mata las células T de manera muy eficiente.
Es cierto, no muy preciso. Tenemos muchas menos especies de TCR que antígenos. Por lo tanto, las células T pueden reconocer muchos antígenos por su TCR, pero solo aproximadamente. Las células cancerosas a menudo explotan esta debilidad de nuestro sistema de seguridad y fingen ser "propias".
La evolución resolvió el problema lo mejor que pudo: en el cuerpo humano hay otro mecanismo para identificar extraños: los
anticuerpos . Estas son proteínas especiales que son secretadas por otra clase de células inmunes: los linfocitos B. Las células B, a diferencia de las células T, tienen un enfoque individual para cada "cliente".
El anticuerpo es una estructura de proteína en la forma de la letra Y. En ambos extremos de este "tenedor" hay sitios que se unen al antígeno. Estas secciones pueden cambiar en cada próxima generación de anticuerpos para ajustarse más al antígeno, como la selección de piezas de rompecabezas. Cuando se detecta un antígeno extraño, las células B secretan miles de millones de anticuerpos, entre los cuales se realiza la selección para la coincidencia más exacta con el antígeno. El resultado es un anticuerpo de referencia, "entrenado" específicamente para el reconocimiento muy preciso de un antígeno "alienígena" específico.
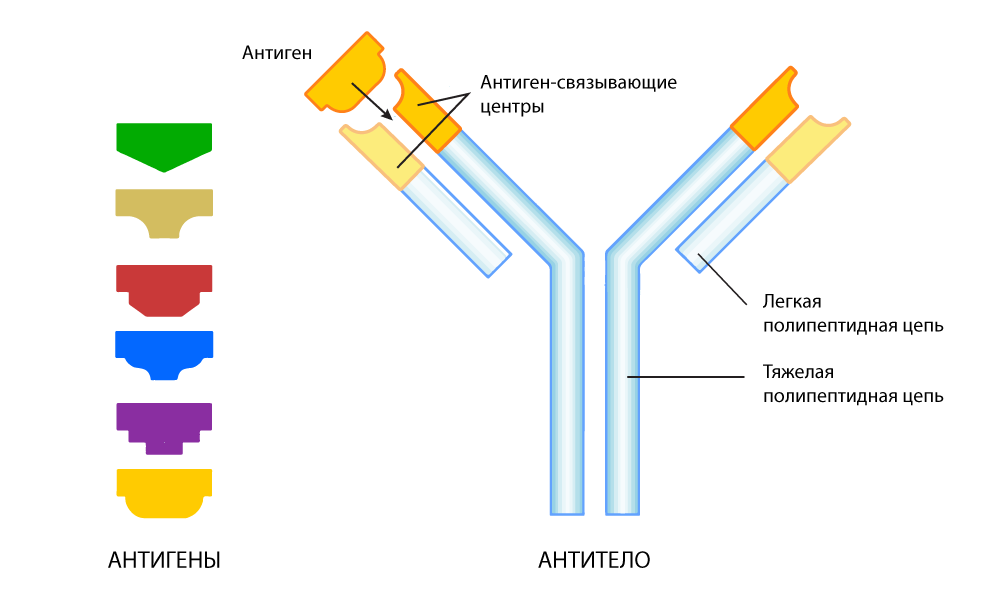 Un anticuerpo adaptado para encontrar un antígeno específico.
Un anticuerpo adaptado para encontrar un antígeno específico.Sin embargo, reconocer no siempre significa neutralizar. Con esto, los anticuerpos tienen dificultades: por sí solos pueden destruir lejos del "enemigo" de ninguna manera en todos los casos.
Entonces, en 1989, al químico e inmunólogo israelí Zelig Ashkhar se
le ocurrió
una combinación del poder mortal de las células T de ojos ciegos y el objetivo de los francotiradores de los anticuerpos. Aisló las secciones terminales de los anticuerpos proteicos que pueden unirse fuertemente al antígeno de ciertas células cancerosas, y las "trasplantó" a las células T, que reemplazaron la parte de TCR responsable del reconocimiento de los antígenos.
Posteriormente, comenzó a trabajar junto con un colega estadounidense, Stephen Rosenberg, lograron hacer del receptor quimérico un diseño más eficiente, tanto sensible como selectivo.
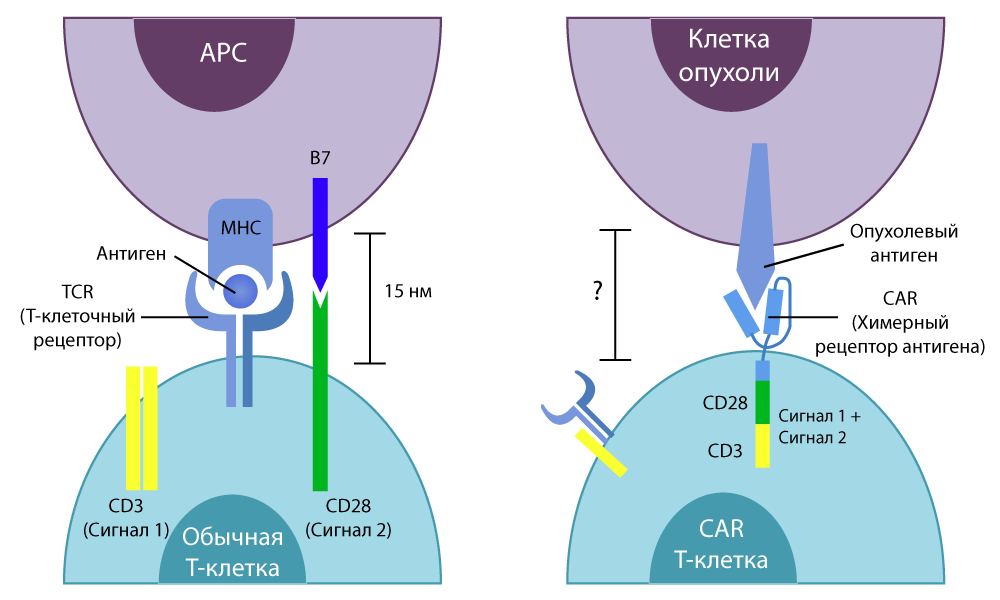 La diferencia entre las células T convencionales y las células CAR-T
La diferencia entre las células T convencionales y las células CAR-TLos estudios in vitro han mostrado buenos resultados. Luego, los científicos volvieron a tratar a los ratones, luego transfirieron minuciosamente la técnica a los humanos.
Con el tiempo, la terapia CAR-T ha dado un aspecto moderno.
- Primero, con la ayuda de las pruebas moleculares moleculares, se determinan mutaciones específicas en las células tumorales humanas, en las cuales los anticuerpos pueden "sintonizarse".
- Luego, una persona toma sus propias células T, cambia utilizando métodos de bioingeniería, en lugar de TCR "trasplante" CAR, sintonizado con las mutaciones identificadas.
- Luego, las células CAR-T modificadas se multiplican in vitro y se introducen nuevamente en el cuerpo humano, donde reconocen y eliminan con éxito las células cancerosas.
En los ensayos clínicos iniciados en 2010, se obtuvieron resultados alentadores de inmediato: en el tratamiento del linfoma, 12 de 13 pacientes mostraron mejoría y 4 comenzaron la remisión. En el tratamiento de la leucemia, la remisión ocurrió en 17 de 33 personas.
En 2018, apareció
un artículo de oncólogos estadounidenses en Nature Medicine, que informó que durante dos años han estado observando a un paciente que está completamente sano después de la terapia CAR-T. Ella se curó de cáncer de mama metastásico con metástasis. Esta foto de ella en un kayak se da al comienzo del artículo: después del tratamiento, regresó al trabajo y se fue de campamento.
Nueva esperanza ¿La inmunoterapia será una panacea?Al igual que otros tratamientos contra el cáncer, la inmunoterapia tiene sus limitaciones. A pesar del hecho de que en algunos casos los pacientes dan una muy buena respuesta a la terapia con inhibidores del punto de control inmunitario, en el 60% de los casos se desarrolla resistencia primaria o adquirida a los fármacos anti-PD-1 o anti-CTLA-4: el tumor simplemente no responde para tratamiento o se adapta rápidamente y aprende a "sortearlo".
Además de PD-1, PD-L1 / 2, CTLA-4, CD28 y B7, hay muchos otros co-receptores en las superficies de las células T y las células tumorales, cuyos efectos aún no se han estudiado, así como el trabajo de los puntos de control, pero también afectan a la respuesta inmune. Una de las áreas de trabajo es el efecto sobre estos co-receptores.
Además, la terapia de las TIC se complementa con la introducción de vacunas, citocinas, betabloqueantes, y este enfoque también funciona bien en
algunos casos .
La terapia con CAR-T sigue siendo extremadamente costosa y solo se encuentra en la etapa de uso comercial: se están desarrollando avances en los grupos científicos de Eshhar y Rosenberg, otros investigadores, cada uno de los grupos crea tipos especiales de CAR-T con una acción dirigida contra un tipo específico de cáncer. Pero hasta ahora esto es solo investigación, pruebas y pruebas. Pasarán varios años antes de que esto se convierta en un método de tratamiento masivo bien establecido, pero aun así no será posible ofrecer garantías del 100%.
Pero mientras los científicos realizan investigaciones, los médicos están introduciendo regímenes de tratamiento experimental utilizando los logros que ya existen. Y el efecto más notable es la combinación de inmunoterapia con los clásicos "tres pilares" de la oncología: radiación y quimioterapia, cirugía. Al combinar estos métodos, siempre se obtiene la sinergia: juntos funcionan de manera más eficiente que a su vez.
Si, hasta ahora, los medicamentos de inmunoterapia estándar se incluían en la tercera, quinta línea (es decir, el turno) de la terapia, ahora los médicos se están moviendo para prescribirlos de inmediato, junto con la quimioterapia y la terapia con anticuerpos monoclonales dirigidos: tales pacientes a menudo muestran una mejor dinámica y terminar viviendo más tiempo.En Rusia, todas las inmunopreparaciones importantes ya se han registrado. El problema, sin embargo, es que para cada uno de ellos el Ministerio de Salud estipula por separado la evidencia. Es decir, en las instrucciones originales para el medicamento se pueden recetar, por ejemplo, nueve tipos diferentes de cáncer, en los que se puede recetar el medicamento, y en nuestro país está registrado solo para seis de ellos. Y así con cada droga. Como resultado, mientras que alrededor del 50% de los tumores aún no están incluidos en esta lista. En consecuencia, como parte del tratamiento para el seguro médico obligatorio, un médico no puede recetar estos medicamentos a todos los pacientes.Además, los médicos de las clínicas de presupuesto estatal están estrictamente limitados a los protocolos de tratamiento. Y si en el protocolo los inhibidores del punto de control se prescriben solo en 3 líneas, en tercer lugar después de dos líneas de "química" estándar, entonces el médico simplemente no tiene el derecho de recetarlos, incluso si cree que esto ayudará al paciente.Bueno, un problema común es la falta de calificaciones. El método, aunque logró probarse, sigue siendo nuevo para muchos médicos en el país. Todos los medicamentos son occidentales y nos llegan con un retraso de 2-3 años. Y, dado que la inmunoterapia se ha utilizado activamente durante solo unos pocos años, muchos todavía no tienen experiencia con ellos. Además, el uso de inmunoterapia requiere un conocimiento específico.En medicina privada, no estamos limitados por el presupuesto. Si en "Medicina 24/7"el paciente se refiere a un tumor para el cual aún no se ha registrado un medicamento de inmunoterapia, le sugerimos que se someta a un estudio de genética molecular. Según los resultados, queda claro si su tumor responderá a la inmunoterapia. Si es así, el médico tiene todo el derecho de prescribirlo. Por lo tanto, en nuestro hospital usamos inmunoterapia para casi todos los tipos de cáncer, que da muy buenos resultados. Incluso los pacientes en estadio III-IV muestran mejoría. Las inmunopreparaciones nos dan la oportunidad de extender la vida de las personas, incluso en casos que se consideraron desesperados.Común en las clínicas públicas y privadas son los propios pacientes. No siempre entienden bien qué tipo de método es este, cómo funciona, de ahí la desconfianza. Esperamos que este artículo haya ayudado a comprender y comprender que la inmunoterapia de hoy está merecidamente en el centro de atención de los oncólogos. A juzgar por los resultados, ella ya está lista para pararse en un nivel con los métodos clásicos. La terrible enfermedad retrocederá un paso más.