El uso de la inteligencia artificial para hacer diagnósticos está a la vuelta de la esquina. E incluso más cerca de lo que parece. De hecho, inmediatamente dos equipos de investigación en ambos lados del Atlántico lograron resolver el problema de la "caja negra" de la IA en medicina.
El problema con el recuadro negro es que el sistema de IA cuando entrega los resultados, y en medicina está diagnosticando y recomendando más terapia, no proporciona la justificación que, en particular, requiere la Administración de Drogas y Alimentos de los Estados Unidos (FDA) .
En diciembre del año pasado, el Hospital General de Massachusetts (Hospital General de Massachusetts) informó que pudo enseñar a la IA a "explicar" el diagnóstico de sangrado intracraneal. Cinco meses antes, la compañía británica DeepMind, adquirida por Google en 2014, anunció un avance similar en el diagnóstico de enfermedades oculares.
La tarea principal de ambos equipos era enseñar al sistema a evaluar las imágenes de los escáneres y tomar decisiones como lo hace un médico especialista.
Atlas de signos
Los médicos del Departamento de Radiología del Hospital de Massachusetts, junto con estudiantes graduados de Ingeniería y Ciencias Aplicadas de Harvard, desarrollaron un modelo de IA que puede clasificar la hemorragia intracraneal, según un comunicado de prensa en el sitio web del hospital. Para entrenar el sistema, el equipo utilizó 904 tomografías computarizadas (tomografía computarizada), cada una de las cuales contenía alrededor de 40 imágenes individuales. Un equipo de cinco neurorradiólogos marcó cada una de las imágenes para detectar la presencia de uno de los cinco subtipos de hemorragia, según la ubicación, así como la ausencia de hemorragia per se. Para mejorar la precisión de este sistema de aprendizaje profundo, el equipo ha integrado acciones que imitan el proceso de análisis de imágenes por parte de un radiólogo, que incluye ajustar parámetros como el contraste y el brillo para revelar diferencias ocultas, y desplazarse por las secciones adyacentes de la tomografía computarizada para determinar si realmente apareció algo en una imagen, refleja un problema real o no se trata de distorsión alguna.
Inmediatamente después de crear el modelo del sistema, los investigadores lo probaron con dos conjuntos separados de tomografías computarizadas: 100 exploraciones con hemorragia intracraneal y 100 sin ella, tomadas antes del desarrollo del sistema, y 79 exploraciones con hemorragia y 117 sin ella, tomadas después de que se creó el modelo. En el caso del primer conjunto de datos tomado antes, el modelo fue preciso para determinar y clasificar el sangrado intracraneal a nivel de análisis realizado por el radiólogo. Al analizar el segundo conjunto, ella demostró que puede ser incluso mejor que una persona que no es experta en este campo.
Para resolver el problema de la "caja negra", el equipo hizo que el sistema verificara y guardara esas imágenes del conjunto de datos de entrenamiento que representan más claramente los síntomas característicos de cada uno de los cinco subtipos de hemorragia. Usando este atlas de características distintivas, el sistema puede representar un grupo de imágenes similares a las utilizadas en el análisis de tomografías computarizadas para explicar sobre qué bases se tomaron las decisiones.
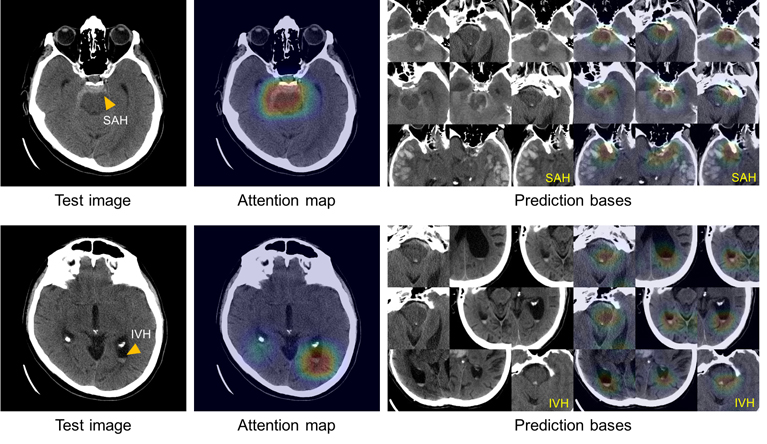
Esta ilustración muestra la capacidad del sistema para explicar el diagnóstico de hemorragias subaracnoideas (arriba a la izquierda) e intraventricular (abajo a la izquierda), mostrando imágenes con síntomas similares (derecha) del atlas de imágenes utilizadas para entrenar el sistema.
"El reconocimiento rápido de la hemorragia intracraneal, seguido de un tratamiento adecuado inmediato de los pacientes con síntomas de accidente cerebrovascular agudo, puede minimizar los efectos graves para la salud y prevenir la muerte", dijo el coautor del estudio, el radiólogo Michael Leo. - En muchos laboratorios no hay neurorradiólogos especialmente capacitados, especialmente por la noche o los fines de semana, lo que requiere que no especialistas decidan si los síntomas del paciente son causados por hemorragia o no. La disponibilidad de una "segunda opinión virtual" confiable, capacitada por neurorradiólogos, podría mejorar los resultados de los no especialistas y ayudar a garantizar que los pacientes reciban el tratamiento adecuado ".
Mapa de segmentación de tejidos
En agosto de 2018, la compañía británica DeepMind publicó un estudio sobre el recurso Nature Medicine en el que afirmó que había resuelto el problema de la "caja negra" mediante el desarrollo de un modelo de IA que podría funcionar a un nivel médico profesional, que, sin embargo, no excluye a las personas del proceso de tratamiento, sino que, por el contrario, ayuda a los médicos a ser más efectivos, como en el caso descrito anteriormente.
Según un estudio publicado , el equipo de DeepMind trabajó en el campo de las enfermedades oftálmicas junto con el centro de lucha contra las enfermedades oftálmicas del Hospital Moorfields Eye y desarrolló un modelo para el diagnóstico de imágenes 3D de tomografía óptica coherente (OCT). Fue posible abrir la "caja negra" creando dos redes neuronales separadas que trabajan juntas. El primero, segmentando con la arquitectura convolucional tridimensional (U-Net), transforma los escaneos OCT sin procesar en un mapa de segmentación del tejido ocular. Para el entrenamiento, se utilizaron 877 exámenes OCT clínicos, cada uno de los cuales tenía 128 secciones, solo tres representativas fueron segmentadas manualmente. La red de segmentación encuentra varios síntomas (hemorragias, lesiones focales, etc.) y crea un mapa. Según Mustafa Suleiman, jefe de IA Aplicada, en el blog de la compañía, esto ayuda a los optometristas a obtener acceso a cómo "piensa" el sistema.
La segunda red neuronal, que clasifica, analiza el mapa propuesto y proporciona diagnósticos y recomendaciones de tratamiento al personal tratante. Los desarrolladores consideran fundamentalmente importante que la red muestre recomendaciones como porcentajes, lo que permite a los médicos evaluar la "confianza" del sistema en su análisis. "Esta característica es crítica, ya que los optometristas juegan un papel clave en la decisión sobre el tratamiento que recibirán los pacientes", dice Mustafa Suleiman. Según él, la característica clave del sistema, que lo hace útil en la práctica, es la oportunidad para que los médicos estudien cuidadosamente las recomendaciones de la IA. El sistema está diseñado para ayudar a prevenir la pérdida completa de visión al acelerar el diagnóstico de enfermedades como la retinopatía diabética, la degeneración macular relacionada con la edad y varias docenas de otras enfermedades.

Descripción de la ilustración. Obtención de cálculos utilizando un complejo de segmentación y clasificación de redes. La ilustración muestra cómo un conjunto de 5 muestras de una red segmentada y 5 muestras de una red de clasificación se usan juntas para crear 25 pronósticos para una exploración. Cada muestra de red segmentada inicialmente proporciona un mapa segmentado de supuestos basados en la OCT que se está investigando. Para cada uno de los cinco supuestos, los patrones de la red de clasificación proporcionan probabilidad para cada marcador. Aquí, el marcador de la ubicación de la atrofia se presenta en detalle.
Ambos equipos de investigación expresan la esperanza de que los sistemas desarrollados por ellos no reemplazarán a los médicos, sino que los ayudarán a ser más efectivos en la toma de decisiones, lo que significa que ayudarán a ayudar a más pacientes en poco tiempo. El siguiente paso es utilizar los desarrollos directamente en los escáneres de hospitales.