Batteries au lithium-soufre pour les futurs programmes spatiaux
Aujourd'hui, les batteries dans les programmes spatiaux sont principalement utilisées comme sources d'alimentation de secours, lorsque les appareils sont à l'ombre et ne peuvent pas recevoir l'énergie des panneaux solaires, ou dans des combinaisons spatiales pour sortir dans l'espace. Mais les types de batteries utilisées aujourd'hui (Li-ion, Ni-H 2 ) ont un certain nombre de limitations. Premièrement, ils sont trop encombrants, car la préférence n'est pas donnée à l'intensité énergétique, mais à la sécurité, du fait de multiples mécanismes de protection pour réduire le volume ne contribue pas du tout. Et deuxièmement, les batteries modernes ont des limites de température, et dans les programmes futurs, selon l'emplacement, les températures peuvent varier de -150 ° C à +450 ° C.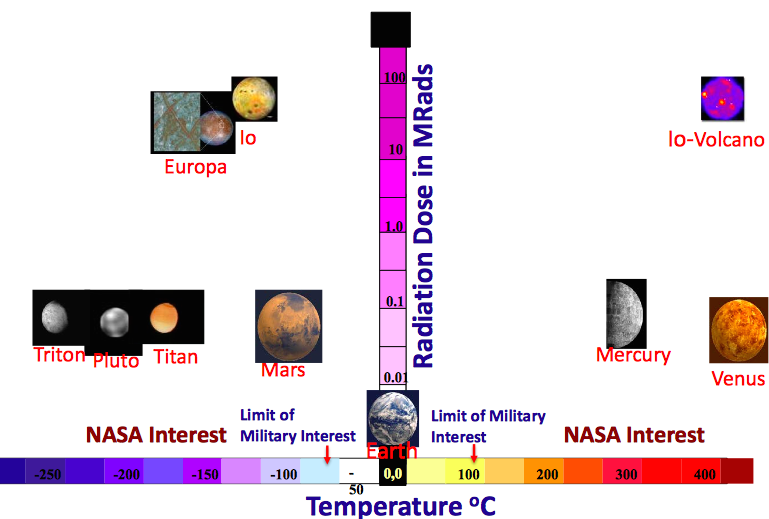 SourceDe plus, n'oubliez pas l'augmentation du rayonnement de fond. En général, les futures batteries pour l'industrie spatiale devraient non seulement être compactes, durables, sûres et énergivores, mais également fonctionner à des températures élevées ou basses, ainsi que dans des conditions de fond de rayonnement accru. Naturellement, aujourd'hui une telle technologie magique n'existe pas. Néanmoins, des développements scientifiques prometteurs tentent de se rapprocher des exigences des futurs programmes. En particulier, je voudrais parler d'une direction dans la recherche, qui est soutenue par la NASA dans le cadre du programme Game Changing Development (GCD).Étant donné que la combinaison de toutes les spécifications ci-dessus dans une seule batterie est une tâche difficile, l'objectif principal de la NASA aujourd'hui est d'obtenir des batteries plus compactes, énergivores et plus sûres. Comment atteindre cet objectif?Pour commencer, pour augmenter considérablement la consommation d'énergie par unité de volume, des batteries avec des matériaux fondamentalement nouveaux pour les électrodes sont nécessaires, car les capacités des batteries lithium-ion (Li-ion) sont limitées par les capacités des matériaux pour la cathode (environ 250 mAh / g pour les oxydes) et l'anode ( environ 370 mAh / g pour le graphite), ainsi que les limites de tension auxquelles l'électrolyte est stable. Et l'une des technologies qui permet d'augmenter la capacité en utilisant des réactions fondamentalement nouvelles au lieu de l'intercalation sur les électrodes est les batteries lithium-soufre (Li-S), dont l'anode contient du lithium métallique, et le soufre est utilisé comme matériau actif pour la cathode. Le fonctionnement d'une batterie lithium-soufre est quelque peu similaire au fonctionnement d'une batterie lithium-ion: les ions lithium sont impliqués dans le transfert de charge à la fois là et là. Mais contrairement au Li-ion, les ions du Li-S ne s'intègrent pas dans la structure en couches de la cathode,et entamez la réaction suivante avec lui:
SourceDe plus, n'oubliez pas l'augmentation du rayonnement de fond. En général, les futures batteries pour l'industrie spatiale devraient non seulement être compactes, durables, sûres et énergivores, mais également fonctionner à des températures élevées ou basses, ainsi que dans des conditions de fond de rayonnement accru. Naturellement, aujourd'hui une telle technologie magique n'existe pas. Néanmoins, des développements scientifiques prometteurs tentent de se rapprocher des exigences des futurs programmes. En particulier, je voudrais parler d'une direction dans la recherche, qui est soutenue par la NASA dans le cadre du programme Game Changing Development (GCD).Étant donné que la combinaison de toutes les spécifications ci-dessus dans une seule batterie est une tâche difficile, l'objectif principal de la NASA aujourd'hui est d'obtenir des batteries plus compactes, énergivores et plus sûres. Comment atteindre cet objectif?Pour commencer, pour augmenter considérablement la consommation d'énergie par unité de volume, des batteries avec des matériaux fondamentalement nouveaux pour les électrodes sont nécessaires, car les capacités des batteries lithium-ion (Li-ion) sont limitées par les capacités des matériaux pour la cathode (environ 250 mAh / g pour les oxydes) et l'anode ( environ 370 mAh / g pour le graphite), ainsi que les limites de tension auxquelles l'électrolyte est stable. Et l'une des technologies qui permet d'augmenter la capacité en utilisant des réactions fondamentalement nouvelles au lieu de l'intercalation sur les électrodes est les batteries lithium-soufre (Li-S), dont l'anode contient du lithium métallique, et le soufre est utilisé comme matériau actif pour la cathode. Le fonctionnement d'une batterie lithium-soufre est quelque peu similaire au fonctionnement d'une batterie lithium-ion: les ions lithium sont impliqués dans le transfert de charge à la fois là et là. Mais contrairement au Li-ion, les ions du Li-S ne s'intègrent pas dans la structure en couches de la cathode,et entamez la réaction suivante avec lui:2 Li + S -> Li 2 S
Bien qu'en pratique, la réaction à la cathode ressemble plutôt à ceci:S 8 -> Li 2 S 8 -> Li 2 S 6 -> Li 2 S 4 -> Li 2 S 2 -> Li 2 S
SourceLe principal avantage d'une telle batterie est sa grande capacité, qui est 2 à 3 fois supérieure à la capacité des batteries lithium-ion. Mais en pratique, tout n'est pas si rose. Lors de la recharge, les ions lithium se déposent sur l'anode comme horribles, formant des chaînes métalliques (dendrites), qui conduisent finalement à un court-circuit. De plus, les réactions entre le lithium et le soufre à la cathode entraînent de grands changements dans le volume du matériau (jusqu'à 80%), de sorte que l'électrode est rapidement détruite et que les composés soufrés eux-mêmes sont de mauvais conducteurs, de sorte que beaucoup de matériau de carbone doit être ajouté à la cathode. Enfin, et surtout, les produits de réaction intermédiaires (polysulfures) se dissolvent progressivement dans l'électrolyte organique et «voyagent» entre l'anode et la cathode, ce qui conduit à une très forte auto-décharge.Mais tous les problèmes ci-dessus tentent de résoudre un groupe de scientifiques de l'Université du Maryland (UMD), qui a remporté une subvention de la NASA. Alors, comment les scientifiques sont-ils parvenus à résoudre tous ces problèmes? Tout d'abord, ils ont décidé «d'attaquer» l'un des principaux problèmes des batteries lithium-soufre, à savoir l'autodécharge. Et au lieu d'un électrolyte organique liquide, qui, comme mentionné ci-dessus, dissout progressivement les matières actives, ils ont utilisé un électrolyte en céramique solide, ou plutôt Li 6 PS 5 Cl, qui conduit assez bien les ions lithium à travers son réseau cristallin.Mais si les électrolytes solides résolvent un problème, ils créent également des difficultés supplémentaires. Par exemple, de grands changements dans le volume de la cathode pendant la réaction peuvent entraîner une perte rapide de contact entre l'électrode solide et l'électrolyte et une forte diminution de la capacité de la batterie. Par conséquent, les scientifiques ont proposé une solution élégante: ils ont créé un nanocomposite composé de nanoparticules de matériau actif cathodique (LI 2 S) et d'électrolyte (Li 6 PS 5 Cl) enfermé dans une matrice de carbone.SourceCe nanocomposite présente les avantages suivants: d'une part, la répartition des nanoparticules d'un matériau qui change de volume lors de la réaction avec le lithium dans le carbone, dont le volume reste pratiquement inchangé, améliore les propriétés mécaniques du nanocomposite (ductilité et résistance) et réduit le risque de fissuration. De plus, le carbone améliore non seulement la conductivité, mais n'interfère pas non plus avec le mouvement des ions lithium, car il a également une bonne conductivité ionique. Et du fait que les matériaux actifs sont nanostructurés, le lithium n'a pas à parcourir de longues distances pour réagir et tout le volume du matériau est utilisé plus efficacement. Enfin, l'utilisation d'un tel composite améliore le contact entre l'électrolyte, la matière active et le carbone conducteur.En conséquence, les scientifiques ont obtenu une batterie entièrement solide d'une capacité d'environ 830 mAh / g. Bien sûr, il est trop tôt pour parler de lancer une telle batterie dans l'espace, car une telle batterie ne fonctionne que pour 60 cycles de charge / décharge. Mais en même temps, malgré une perte de capacité aussi rapide, 60 cycles constituent déjà une amélioration significative par rapport aux résultats précédents, car auparavant, les batteries lithium-soufre solides ne fonctionnaient pas pendant plus de 20 cycles. Il convient également de noter que ces électrolytes solides peuvent fonctionner dans une large plage de températures (en passant, ils fonctionnent mieux à des températures supérieures à 100 ° C), de sorte que les limites de température de ces batteries seront plus probablement dues aux matériaux actifs qu'à l'électrolyte, ce qui distingue ces systèmes. des batteries utilisant des solutions organiques comme électrolyte. Source: https://habr.com/ru/post/fr398529/
All Articles