Comment obtenir de la glace à une température de + 151 ° C
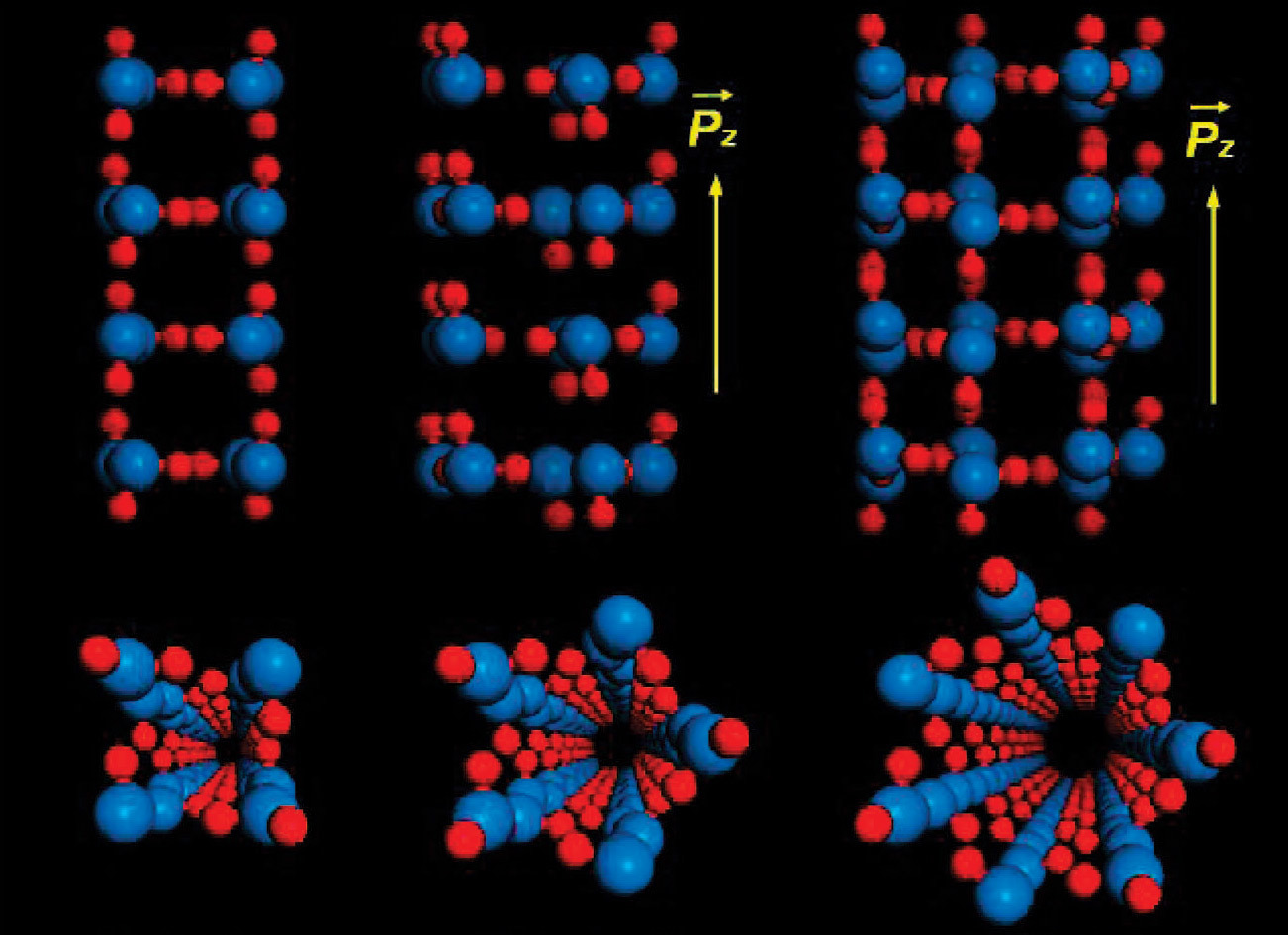 La structure d'un nanofeuille quadrangulaire, pentagonal et heptagonal à l'intérieur d'un nanotube à paroi simple. Les boules bleues et rouges correspondent aux atomes d'oxygène et d'hydrogène. Source: résultats de simulation 2008. Lespropriétés inhabituelles de l'eau font depuis longtemps l'objet d'un examen minutieux par les scientifiques. Il y a dix ans, il s'est avéré qu'à l'intérieur de nanotubes d'un diamètre inférieur à 2,5 nm, l'eau ne gèle pas, mais continue de couler même à des températures proches du zéro absolu (−273,15 ° C). Les bizarreries ne s'arrêtent pas là.Les transitions de phase de l'eau avec un changement de l'état d'agrégation à l'intérieur des nanotubes de carbone ne correspondent clairement pas à la théorie standard de la thermodynamique. Cela s'applique non seulement au point de congélation, mais également au point d'ébullition. Comme on le sait, à pression atmosphérique normale, le point d'ébullition de l'eau est d'environ 100 ° C. Avec l'augmentation de la pression dans le réservoir, la température d'ébullition augmente - ce principe est utilisé par les autocuiseurs pour cuire les aliments plus rapidement. Inversement, le point d'ébullition de l'eau peut être réduit en réduisant la pression. Par exemple, dans les montagnes à une altitude de 5 km, il est impossible de cuisiner certains produits, car là le point d'ébullition de l'eau n'est que de 83 ° C en raison de la basse pression atmosphérique.Les scientifiques savent également que la température des transitions de phase de l'eau dépend également de la forme et de la taille du récipient. Si la pression reste constante, le point d'ébullition ou le point de congélation peut être décalé d'environ 10 ° C en utilisant le volume du récipient. Mais dans les nanotubes de carbone, les choses sont bouleversées. Comme déjà mentionné, l'eau y conserve un état liquide à des températures proches du zéro absolu. Maintenant, les scientifiques du Massachusetts Institute of Technology (MIT) ont étudié en détail un autre phénomène intéressant - une transition de phase vers un état solide (nanotubes de glace) à haute température, lorsque l'eau devrait s'évaporer dans des conditions normales.Ce phénomène a été découvert en 2001.un groupe de scientifiques japonais et américains. Les nanotubes de glace sont particulièrement intéressants car ils se forment à des températures élevées et peuvent être utilisés dans divers nanodispositifs électroniques, y compris les nanoturbines à gaz , les nanocapteurs à écoulement et les membranes à haut flux. De plus, la capacité de l'eau à geler dans des nanotubes de glace à des températures bien supérieures à 0 ° C permet d' utiliser des nanotubes de glace dans des systèmes de transfert de chaleur . Des confirmations expérimentales de cette utilisation ont été obtenues, mais les tailles et paramètres exacts des nanotubes de carbone, nécessaires à la solidification de l'eau à température ambiante et au-dessus, n'ont pas encore été connus et étudiés.À ce jour, la plupart des expériences avec la transition de phase de l'eau dans les nanotubes de carbone se sont limitées à des simulations de la dynamique moléculaire sur ordinateur, plutôt qu'à de véritables expériences physiques. À la suite de la simulation, il s'est avéré que les propriétés de l'eau dépendent fortement du diamètre du nanotube de carbone. Par exemple, dans les pores d'un diamètre de 0,8 à 1,0 nm, l'eau se stabilise bien à l'état de vapeur, et quelque part entre les diamètres des tubes de 1,1 et 1,2 nm, les simulations montrent une stabilisation sous forme de glace, c'est-à-dire sous forme solide. Ensuite, avec une augmentation de diamètre supérieure à 1,4 nm, la stabilisation se produit à nouveau sous forme liquide. Tout cela est très intéressant - et par conséquent, le MIT a développé une méthodologie pour des expériences physiques afin de tester les propriétés de l'eau dans des nanotubes de carbone d'un diamètre de 1,05 à 1,52 nm avec des parois simples et doubles.Les auteurs de l'expérience ont également développé une technique de surveillance de l'eau dans les nanotubes par spectroscopie Raman (vibrations radiales, RBM).
La structure d'un nanofeuille quadrangulaire, pentagonal et heptagonal à l'intérieur d'un nanotube à paroi simple. Les boules bleues et rouges correspondent aux atomes d'oxygène et d'hydrogène. Source: résultats de simulation 2008. Lespropriétés inhabituelles de l'eau font depuis longtemps l'objet d'un examen minutieux par les scientifiques. Il y a dix ans, il s'est avéré qu'à l'intérieur de nanotubes d'un diamètre inférieur à 2,5 nm, l'eau ne gèle pas, mais continue de couler même à des températures proches du zéro absolu (−273,15 ° C). Les bizarreries ne s'arrêtent pas là.Les transitions de phase de l'eau avec un changement de l'état d'agrégation à l'intérieur des nanotubes de carbone ne correspondent clairement pas à la théorie standard de la thermodynamique. Cela s'applique non seulement au point de congélation, mais également au point d'ébullition. Comme on le sait, à pression atmosphérique normale, le point d'ébullition de l'eau est d'environ 100 ° C. Avec l'augmentation de la pression dans le réservoir, la température d'ébullition augmente - ce principe est utilisé par les autocuiseurs pour cuire les aliments plus rapidement. Inversement, le point d'ébullition de l'eau peut être réduit en réduisant la pression. Par exemple, dans les montagnes à une altitude de 5 km, il est impossible de cuisiner certains produits, car là le point d'ébullition de l'eau n'est que de 83 ° C en raison de la basse pression atmosphérique.Les scientifiques savent également que la température des transitions de phase de l'eau dépend également de la forme et de la taille du récipient. Si la pression reste constante, le point d'ébullition ou le point de congélation peut être décalé d'environ 10 ° C en utilisant le volume du récipient. Mais dans les nanotubes de carbone, les choses sont bouleversées. Comme déjà mentionné, l'eau y conserve un état liquide à des températures proches du zéro absolu. Maintenant, les scientifiques du Massachusetts Institute of Technology (MIT) ont étudié en détail un autre phénomène intéressant - une transition de phase vers un état solide (nanotubes de glace) à haute température, lorsque l'eau devrait s'évaporer dans des conditions normales.Ce phénomène a été découvert en 2001.un groupe de scientifiques japonais et américains. Les nanotubes de glace sont particulièrement intéressants car ils se forment à des températures élevées et peuvent être utilisés dans divers nanodispositifs électroniques, y compris les nanoturbines à gaz , les nanocapteurs à écoulement et les membranes à haut flux. De plus, la capacité de l'eau à geler dans des nanotubes de glace à des températures bien supérieures à 0 ° C permet d' utiliser des nanotubes de glace dans des systèmes de transfert de chaleur . Des confirmations expérimentales de cette utilisation ont été obtenues, mais les tailles et paramètres exacts des nanotubes de carbone, nécessaires à la solidification de l'eau à température ambiante et au-dessus, n'ont pas encore été connus et étudiés.À ce jour, la plupart des expériences avec la transition de phase de l'eau dans les nanotubes de carbone se sont limitées à des simulations de la dynamique moléculaire sur ordinateur, plutôt qu'à de véritables expériences physiques. À la suite de la simulation, il s'est avéré que les propriétés de l'eau dépendent fortement du diamètre du nanotube de carbone. Par exemple, dans les pores d'un diamètre de 0,8 à 1,0 nm, l'eau se stabilise bien à l'état de vapeur, et quelque part entre les diamètres des tubes de 1,1 et 1,2 nm, les simulations montrent une stabilisation sous forme de glace, c'est-à-dire sous forme solide. Ensuite, avec une augmentation de diamètre supérieure à 1,4 nm, la stabilisation se produit à nouveau sous forme liquide. Tout cela est très intéressant - et par conséquent, le MIT a développé une méthodologie pour des expériences physiques afin de tester les propriétés de l'eau dans des nanotubes de carbone d'un diamètre de 1,05 à 1,52 nm avec des parois simples et doubles.Les auteurs de l'expérience ont également développé une technique de surveillance de l'eau dans les nanotubes par spectroscopie Raman (vibrations radiales, RBM).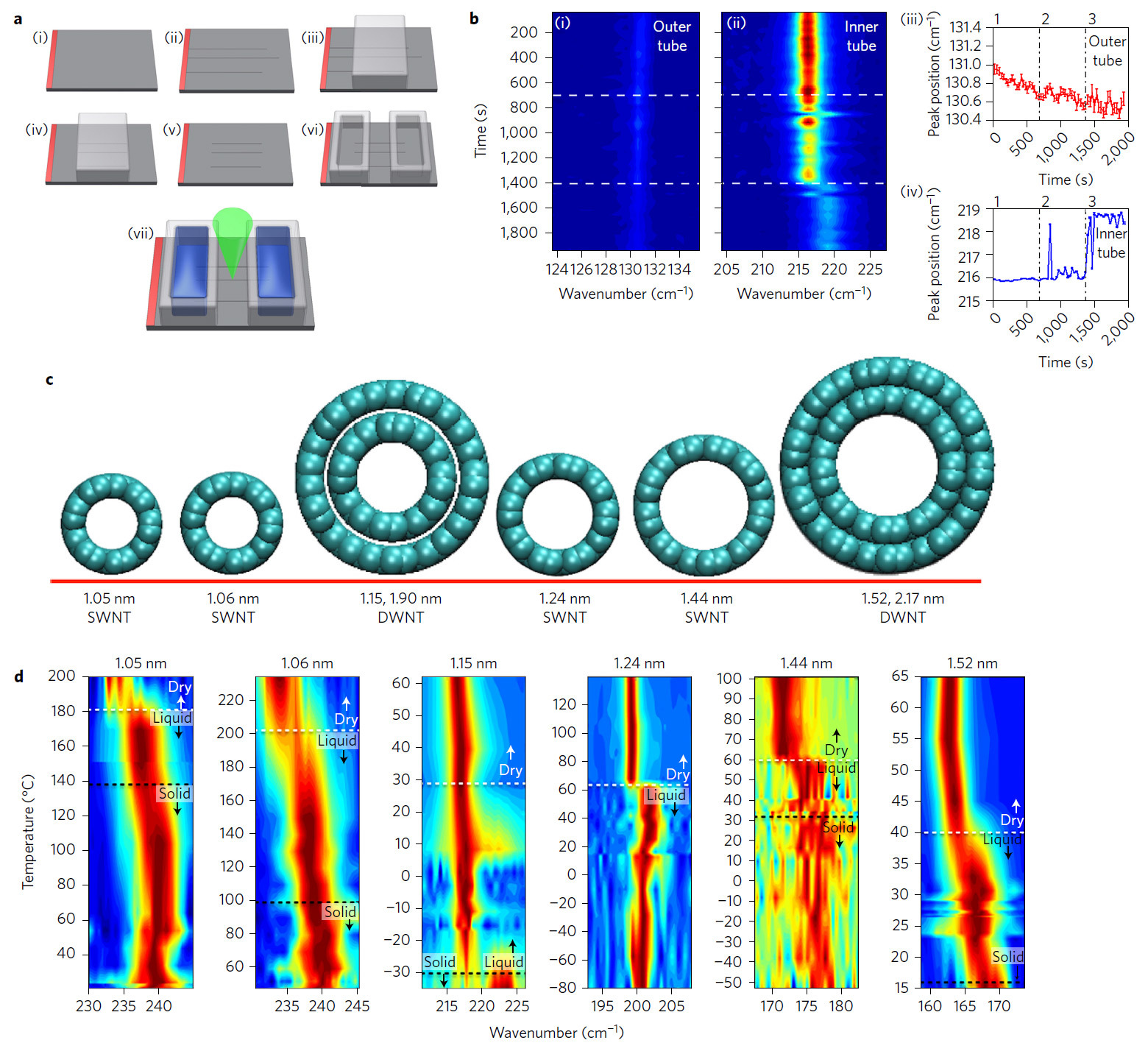 Une configuration expérimentale pour faire croître des nanotubes et les remplir d'eau (pourquoi les nanotubes hydrophobes font passer l'eau à l'intérieur - les scientifiques ne comprennent pas non plus complètement); modèles informatiques de nanotubes simple et double couche pour l'expérimentation; résultats de la spectroscopie RamanDes expériences ont montré qu'à certains diamètres de nanotubes, l'eau passe à l'état solide d'agrégation à des températures supérieures à 100 ° C. La température de transition de phase maximale enregistrée est de 105 ° C à 151 ° C (il n'a pas été possible de mesurer plus précisément) avec un diamètre de nanotube à paroi simple de 1,05 nm. C'est beaucoup plus élevé que la théorie ne l'avait prédit.. Dans certains cas, le point de congélation réel était presque 100 ° C plus élevé que prévu. Les expériences ont d'abord été menées dans des conditions réelles de laboratoire - il s'est avéré, pas en vain. Personne ne s'attendait à une aussi grande différence dans les propriétés de l'eau dans des nanotubes de 1,05 et 1,06 nm de diamètre.
Une configuration expérimentale pour faire croître des nanotubes et les remplir d'eau (pourquoi les nanotubes hydrophobes font passer l'eau à l'intérieur - les scientifiques ne comprennent pas non plus complètement); modèles informatiques de nanotubes simple et double couche pour l'expérimentation; résultats de la spectroscopie RamanDes expériences ont montré qu'à certains diamètres de nanotubes, l'eau passe à l'état solide d'agrégation à des températures supérieures à 100 ° C. La température de transition de phase maximale enregistrée est de 105 ° C à 151 ° C (il n'a pas été possible de mesurer plus précisément) avec un diamètre de nanotube à paroi simple de 1,05 nm. C'est beaucoup plus élevé que la théorie ne l'avait prédit.. Dans certains cas, le point de congélation réel était presque 100 ° C plus élevé que prévu. Les expériences ont d'abord été menées dans des conditions réelles de laboratoire - il s'est avéré, pas en vain. Personne ne s'attendait à une aussi grande différence dans les propriétés de l'eau dans des nanotubes de 1,05 et 1,06 nm de diamètre.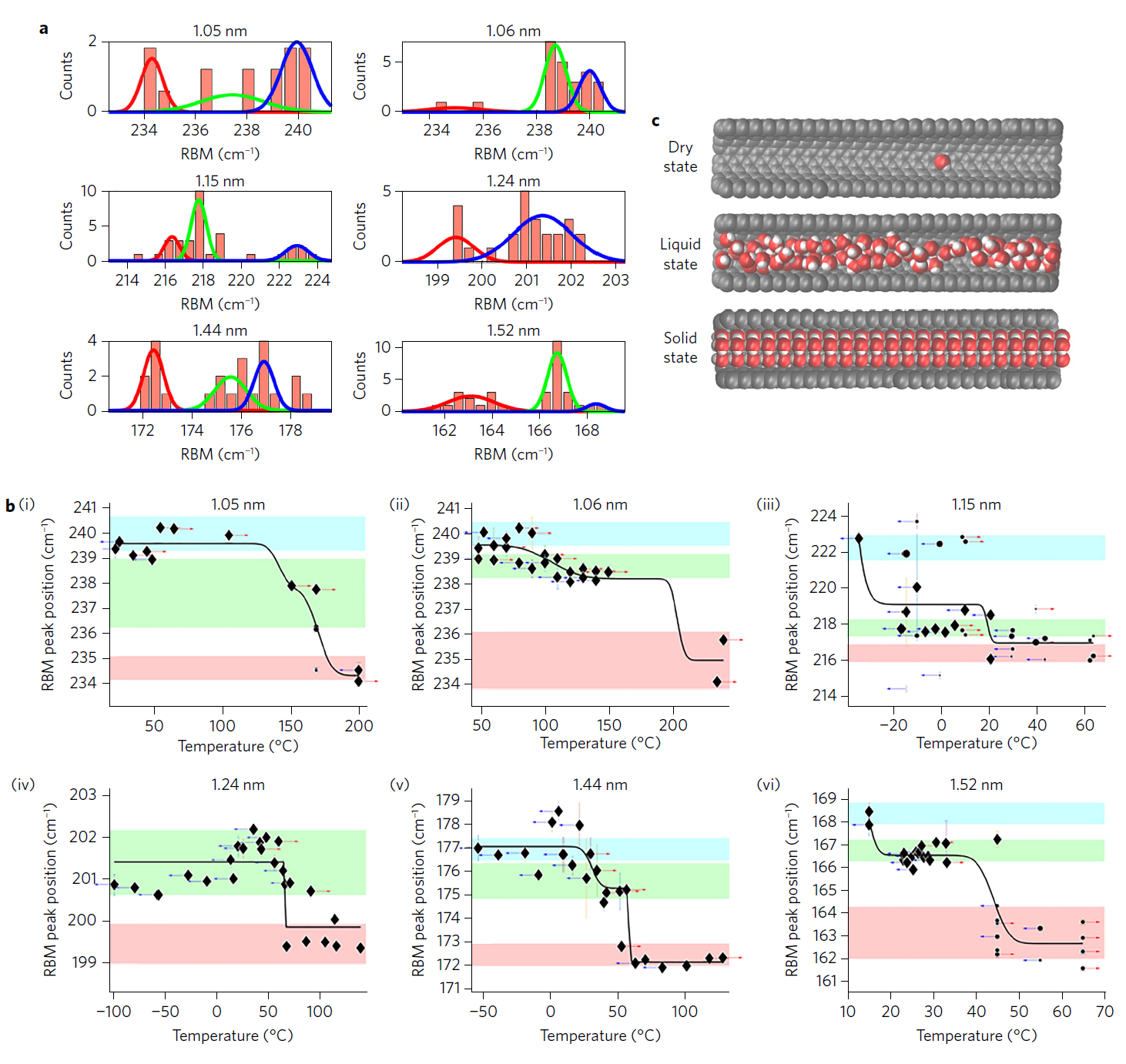 La couleur bleue dans le diagramme indique l'état solide de l'eau, le vert indique l'état liquide, le rouge indique des nanotubes vides (état sec)Après avoir traversé le point de congélation, les scientifiques ont abaissé la température et remis l'eau à l'état liquide, prouvant la réversibilité du processus. Dans les nanotubes d'un diamètre de 1,06 nm, la glace fondait à une température de 87–117 ° ; dans les nanotubes de 1,44 et 1,52 nm, le point de congélation se situe entre 15–49 ° et 3–30 ° , respectivement.La glace nanométrique possède une combinaison intéressante de propriétés électriques et thermiques. La présence de glace qui ne fond pas à des températures allant jusqu'à + 151 ° C peut intéresser les ingénieurs et les concepteurs. À température ambiante, cette glace sera absolument stable, elle peut être utilisée comme fil dans l'électronique et d'autres appareils (l'eau est l' un des meilleurs conducteurs de protons connus de la science ), qui ne chauffent pas jusqu'à + 151 ° C, sinon ce conducteur fondra.Les travaux scientifiques ont été publiés le 28 novembre 2016 dans la revue Nature Nanotechnology (doi: 10.1038 / nnano.2016.254, pdf ).
La couleur bleue dans le diagramme indique l'état solide de l'eau, le vert indique l'état liquide, le rouge indique des nanotubes vides (état sec)Après avoir traversé le point de congélation, les scientifiques ont abaissé la température et remis l'eau à l'état liquide, prouvant la réversibilité du processus. Dans les nanotubes d'un diamètre de 1,06 nm, la glace fondait à une température de 87–117 ° ; dans les nanotubes de 1,44 et 1,52 nm, le point de congélation se situe entre 15–49 ° et 3–30 ° , respectivement.La glace nanométrique possède une combinaison intéressante de propriétés électriques et thermiques. La présence de glace qui ne fond pas à des températures allant jusqu'à + 151 ° C peut intéresser les ingénieurs et les concepteurs. À température ambiante, cette glace sera absolument stable, elle peut être utilisée comme fil dans l'électronique et d'autres appareils (l'eau est l' un des meilleurs conducteurs de protons connus de la science ), qui ne chauffent pas jusqu'à + 151 ° C, sinon ce conducteur fondra.Les travaux scientifiques ont été publiés le 28 novembre 2016 dans la revue Nature Nanotechnology (doi: 10.1038 / nnano.2016.254, pdf ).Source: https://habr.com/ru/post/fr399679/
All Articles