À la lumière de mes rêves de
thérapie génique à l'aide des facteurs Yamanaki , Liz Parrish a décidé de rafraîchir la mémoire des détails de l'auto-expérience. Du coup, va-t-elle accepter d'être la première patiente de la thérapie Yamanova? Non, je plaisante, bien sûr, mais il y a du sérieux dans cette blague. Je pense vraiment que la thérapie génique pour le recul épigénétique a un potentiel thérapeutique. Et pour quelque 15 à 20 millions de dollars, ce potentiel peut être amené au début des essais cliniques ou réfuté.
Quoi qu'il en soit, en revenant du paradis sur terre - qu'est-ce que Liz Parrish s'est présentée? Selon ses assurances, Liz s'est présentée 2 thérapies géniques différentes en utilisant des vecteurs viraux adéno-associés (AAV): le gène hTERT telomerase et le gène follistatin FS (conçu pour inhiber la myostatine).
Il convient de préciser que, très probablement, il ne s'agissait pas de deux variétés d'AAV, mais bien plus, car Liz devait préparer un AAV spécifique pour chaque type de tissu cible. Et puis elle a dû délivrer cet AAV particulier à ce tissu cible. Voici ce que j'ai compris de cette interview avec Liz sur Longecity Now:
http://www.longecity.org/media/Liz_Parrish_LongeCity_Now2016.mp3Il convient de noter que l'AAV ne s'intègre pas délibérément dans le génome - c'est-à-dire que pour les cellules qui se divisent, les cellules filles NE recevront PAS les gènes qui ont été livrés à la cellule d'origine à l'aide de l'AAV. Mais ils auront des télomères allongés, à condition que le gène hTERT fonctionne comme prévu dans leur cellule mère:
https://www.addgene.org/viral-vectors/aav/aav-guide/Le fait que Liz se soit injecté une sorte d'injection (oui, sceptiques, je vous entends) est confirmé par le réalisateur d'un documentaire sur elle qui a filmé cette procédure en Colombie:
Le MIT Technology Review a tenté de confirmer certains aspects de l'histoire de Parrish en parlant à Matthew Andrews, un réalisateur de Los Angeles, qui a déclaré qu'il interrompait le traitement de Parrish en septembre - une modeste chambre de médecin avec un médecin et une infirmière qui ont également prélevé des analyses de sang. . «C'était une salle de traitement, il n'y avait pas de gadgets particulièrement high-tech. Elle était allongée sur le lit sans anesthésie, recevant des injections et connectée à un compte-gouttes », a-t-il déclaré. «C'était ennuyeux du point de vue d'un observateur extérieur, même si, bien sûr, je ne sais pas ce qui se passait à l'intérieur du corps.
https://www.technologyreview.com/s/542371/a-tale-of-do-it-yourself-gene-therapy/
Soit dit en passant, selon Liz, la thérapie AAV a réussi à délivrer le gène de la télomérase hTERT dans seulement 20% de ses cellules. Elle a déclaré cela lors de sa présentation à Digital October à Moscou, le 22 juin 2016 (vers 1:46:41 dans cette vidéo):
Pourquoi Liz a-t-elle choisi ces traitements particuliers? Michael Fossel et Bill Andrews parlent du potentiel anti-âge de la télomérase depuis de nombreuses années. Une approche spécifique de l'utilisation de la thérapie TERT a été confirmée par Maria Blasco chez la souris, où elle a prolongé à la fois la survie moyenne et l'âge maximum des souris dans deux groupes - une a reçu des injections TERT à l'âge de 420 jours (une augmentation de la survie médiane de 24% et une augmentation de 13% au maximum). l'espérance de vie), et l'autre à l'âge de 720 jours (augmentation de la survie médiane de 20% et augmentation de l'espérance de vie maximale de 13%):
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3494070/Soit dit en passant, Michael Fossel a déclaré avoir conseillé Liz à plusieurs reprises, car il travaillait au début d'essais cliniques d'une approche très similaire à la thérapie hTERT pour les patients atteints de la maladie d'Alzheimer:
Notre entreprise de biotechnologie, Telocyte, a l'intention de faire presque la même chose, mais avec un certain nombre de différences importantes: nous n'utiliserons qu'une seule thérapie - la thérapie avec le gène de la télomérase (hTERT), et nous avons l'intention de mener des essais humains à part entière avec l'approbation de la FDA, avec la procédure l'harmonisation de l'IRB, ainsi que l'utilisation des normes de production de thérapie GMP.
En même temps, j'applaudis le courage de Liz à se servir d'elle-même comme sujet de recherche. Vous utiliser comme sujet élimine une grande partie des critiques éthiques qui seraient plus pertinentes si Liz utilisait d'autres patients. Comme beaucoup d'autres, nous constatons le besoin urgent de développer et de mettre en œuvre des interventions thérapeutiques plus efficaces: les patients non seulement souffrent, mais meurent également pendant que nous essayons d'avancer. Dans le cas de la maladie d'Alzheimer, par exemple (notre principale cible thérapeutique pour Telocyte), malheureusement, il n'existe actuellement aucun traitement efficace, et une énorme population de patients est obligée de mourir pendant que nous développons un nouveau traitement pour eux. Une approche lente et équilibrée de la recherche d'un traitement n'est guère saluée par eux dans une telle situation.
Et pourtant ...
Nous avons décidé de suivre une approche standard - avec l'approbation de la FDA des essais sur l'homme - pour trois raisons que nous considérons importantes: 1) nous voulons assurer la sécurité, 2) nous voulons garantir l'efficacité et 3) nous voulons assurer la confiance. La question de la sécurité n'est pas facile: la maladie d'Alzheimer est mortelle, donc la sécurité ici peut sembler moins importante que l'efficacité. Et nous pensons vraiment qu'il n'y a aucune raison de ne pas essayer de thérapie expérimentale pour les patients désespérés si les risques facilement amovibles sont éliminés à l'avance (par exemple, en utilisant des processus de production sûrs pour les vecteurs viraux). La question de l'efficacité n'est pas non plus facile: quelqu'un dit que vous devez essayer n'importe quelle terupie, même à distance efficace. Mais nous ne voyons aucune raison d'utiliser une thérapie peu efficace si nous pouvons fournir la thérapie la plus efficace en utilisant seulement un peu plus de prévoyance et de soins. La question de la confiance n'est pas non plus simple: quelqu'un prétend qu'il suffira de guérir au moins un patient atteint de la maladie d'Alzheimer. Il en est ainsi, mais à condition qu'ils nous croient que nous l'avons vraiment guéri. Mais si personne ne nous croit, le fait que nous ayons guéri quelqu'un seul n'aidera pas des millions d'autres patients.
http://www.michaelfossel.com/blog/?p=139
Quant à la deuxième thérapie de Liz utilisant le gène de la follistatine, si je comprends bien, cette approche a déjà été testée sur moi-même par le partenaire de Liz et copropriétaire de BioViva, Jason Williams. Williams, soit dit en passant, avait précédemment développé plusieurs autres thérapies génétiques expérimentales par AAV, et possède également sa propre clinique en Colombie, où il propose certaines de ces thérapies aux patients (mais Liz n'a pas suivi ses procédures dans sa clinique):
http://www.neuralgene.com/technology-pipeline.cfmLa thérapie FS AAV spécifique que Liz a introduite elle-même a déjà passé avec succès la deuxième phase de l'IC en Grande-Bretagne, et est actuellement en cours de troisième:
http://www.nature.com/mt/journal/v23/n1/full/mt2014200a.htmlQuestion: Pourquoi tester deux thérapies aussi différentes en même temps? Liz dit qu'elle s'attend à un effet synergique et qu'il existe des preuves que la thérapie FS peut épuiser les cellules souches, et la thérapie hTERT devrait aider à prévenir cela.
Les premiers résultats de la thérapie rapportés par BioViva ont été que les télomères des lymphocytes Lys sont passés de 6 710 à 7 330 paires de bases après le traitement. L'affirmation selon laquelle cela équivaut à «reculer de 20 ans le raccourcissement des télomères», bien que cela semble pathétique, a une justification scientifique, car la vitesse moyenne du raccourcissement des télomères leucocytaires est d'environ 30 paires de bases par an:
Pendant le vieillissement normal, les télomères sont raccourcis en CD4 + T-helpers, CD8 + cytotoxic T-cells et anticorps-product B-cells à un taux annuel de 19–35 paires de bases
http://www.ncbi.nlm.nih.gov/pubmed/10903716
http://www.ncbi.nlm.nih.gov/pubmed/12437664
Dans le même temps, certaines personnes notent que l'allongement des télomères de 9% se situe entre 8 et 10% de l'erreur de mesure qPCR, mais d'après ce que j'ai lu sur qPCR, 8-10% est une erreur interlaboratoires ou inter-méthodes, et non une erreur lors de l'utilisation le même équipement dans le même laboratoire. Autrement dit, vous pouvez voir une différence de 10% dans les résultats lorsque vous testez le même échantillon dans deux laboratoires différents ou en utilisant deux méthodes différentes. Mais Liz affirme que ses télomères ont été mesurés avant et après avoir reçu un traitement dans le même laboratoire - SpectraCell Laboratories.
En outre, Liz affirme que les résultats ont été confirmés par deux autres organisations scientifiques: l'ONG belge HEALES et la British Foundation for Biogerontological Research. Par conséquent, la probabilité que la différence de 9% soit due à une erreur de mesure me semble bien inférieure à la probabilité que cette différence soit due à de réels changements biologiques. Bien sûr, par souci de confiance, il serait nécessaire d'analyser tous les échantillons de Liz en utilisant d'autres méthodes (pas qPCR, mais TRF, par exemple), et dans d'autres laboratoires. J'espère que cela sera fait.
Soit dit en passant, je dois noter que la question demeure de savoir à quel point les organisations scientifiques ci-dessus sont indépendantes, car HEALES est associé à ILA (International Longevity Alliance), où Liz est membre du conseil d'administration, et la British Foundation for Biogerontological Research est dirigée par Avi Roy, qui est également Directeur des sciences, BioViva.
Soit dit en passant, lors d'une conférence de presse à Moscou, Liz a déclaré qu'elle avait envoyé certains de ses échantillons avant et après la thérapie au laboratoire de George Church à Harvard, qui a promis d'en effectuer une analyse détaillée, y compris des tests évaluant le changement de méthylation (dans l'espoir de voir " un profil "plus jeune" d'
heures de
méthylation identifié dans les travaux de Steve Horvath). Liz en parle dans la même vidéo (vers 1:48:41):
George Church est, bien sûr, cool, car il est presque Einstein de la génétique moderne, mais ... il est membre du Conseil scientifique de BioViva. Espérons qu'avec le temps, un tiers complètement indépendant se chargera de confirmer les résultats de Liz, de préférence en utilisant une autre méthode de mesure des télomères. Lors de la même conférence de presse, Liz a déclaré qu'elle était prête à fournir ses échantillons pour des tests dans des laboratoires indépendants, à condition qu'ils soient vraiment fiables.
En mars 2017, Liz a publié un communiqué de presse avec ses derniers résultats de ses analyses:
https://bioviva-science.com/blog/2017/3/2/dual-gene-therapy-has-beneficial-effects-on-blood-biomarkers-and-muscle-compositionLà, elle affirme que les données IRM de ses hanches montrent une diminution du persillage des muscles, c'est-à-dire une diminution de la quantité de dépôts graisseux intramusculaires, qui peut être considérée comme un effet positif du traitement par follistatine:
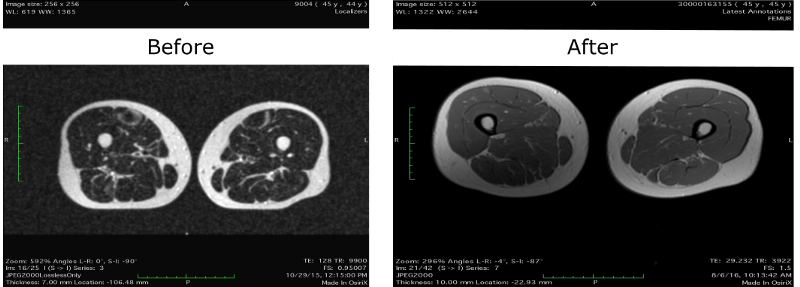
Mais, peut-être, la différence visuelle entre les images n'est due qu'à une amélioration de la résolution de l'IRM: l'ancienne image a été prise sur un appareil Tesla, et la nouvelle était de 1,5 Tesla. De plus, il me semble que les images ont été obtenues à des endroits légèrement différents des hanches - des images plus récentes, à en juger par la distance entre les jambes, ont été prises à partir des tranches légèrement plus basses du bassin que les anciennes. Et plus les prêtres sont bas, plus le pourcentage de graisse dans les jambes est faible. Bien que Liz ait peut-être simplement écarté ses jambes un peu plus lors du dernier test.
Soit dit en passant, dans les données récentes de Liz, il était intéressant de voir un niveau plutôt élevé (1,6) de protéine C-réactive avant l'introduction de la thérapie génique et une diminution ultérieure du CRP à 0,2 en février 2016. Il serait intéressant de savoir quelle était la valeur de CRP dans le cycle de tests en 2016 - Liz donne des valeurs de glucose et de triglycérides d'août 2016, mais pas de CRP.
En conclusion, je mentionnerai quelques critiques concernant l'utilisation de la longueur des télomères des lymphocytes comme marqueurs de «rajeunissement»:
- (A) la mesure des télomères des lymphocytes n'est pas une bonne métrique en principe, car ils ont trop de variations dans la longueur des télomères
- (B) la longueur moyenne des télomères, en particulier dans les globules blancs (WBC), peut fluctuer naturellement pendant une période de temps assez courte (moins de 2 ans)
Sous le point (A), Michael Fossell a écrit un article détaillé sur son blog, je vais donc juste lui donner un lien:
http://www.michaelfossel.com/blog/?p=182Et selon le point (B) - oui, la longueur moyenne des télomères peut, apparemment, parfois augmenter spontanément, mais pas autant que dans le cas de Liz, et cela se produit rarement (dans 10 à 15% des cas). Voici deux bons travaux sur le sujet:
http://www.clinsci.org/content/128/6/367.fullhttps://www.hindawi.com/journals/jir/2016/5371050/Ce graphique du dernier travail est particulièrement indicatif - comme nous pouvons le voir, pendant 18 mois, suffisamment de personnes ont allongé les télomères (tous les points sont supérieurs à zéro):
Soit dit en passant, certains sceptiques inconditionnels exigent des preuves que Liz a vraiment introduit les gènes revendiqués. En principe, cela pourrait être vérifié à moindre coût et rapidement en utilisant RT-qPCR sur les lymphocytes Lys avant et après la thérapie: si l'AAV a délivré ses gènes, nous devrions voir la différence dans les courbes. Peut-être que le laboratoire de George Church aurait pu faire une telle analyse. Mais je ne pense pas que ce soit nécessaire, parce que mentir franchement à l'idée de vous présenter ces gènes, puis d'envoyer vos échantillons à George Church serait le comble de l'idiotie.