Une tumeur maligne diffère des autres types de tumeurs et de maladies en ce que ses cellules sont similaires aux cellules saines du corps. Par conséquent, les scientifiques sont confrontés à une tâche difficile: faire la distinction entre les cellules et détruire uniquement les cellules infectées. Tout au long de l'histoire, les médecins ont eu différentes idées sur la façon de procéder. Aujourd'hui, l'
Atlas expliquera comment l'oncologie s'est développée et comment le cancer est traité aujourd'hui.
 Illustrations: Michael Kowalski
Illustrations: Michael KowalskiThéorie humorale hippocratique
Jusqu'au XVIIIe siècle, les maladies oncologiques étaient difficiles à étudier: le matériel adéquat n'avait pas encore été inventé, l'église interdisait l'autopsie, et la peste et la variole ont coûté la vie et attiré l'attention. Par conséquent, depuis les temps anciens, peu de cas de tumeurs malignes nous sont parvenus, mais ils le sont néanmoins.

La première mention du cancer se trouve dans le papyrus d'Edwin Smith - le texte médical de l'Égypte ancienne, qui remonte au 16ème siècle avant JC. Ce
papyrus peut être parcouru et lu. Le cas n ° 45 décrit des tumeurs malignes. Il note également qu'il n'y a pas de méthode de traitement.
Hippocrate (400 avant JC) a été le premier à distinguer les tumeurs bénignes des tumeurs malignes. Il croyait que le corps humain contient quatre humeurs ou liquides - sang, mucus, bile jaune et noire - et tout déséquilibre mène à la maladie. On pensait que la cause des tumeurs malignes était l'accumulation de bile noire à un certain endroit. Hippocrate a noté que sans traitement, les patients peuvent vivre plus longtemps: la bile noire s'est déjà propagée dans tout le corps et ne peut pas être retirée.
Bien sûr, il n'y a pas de bile noire dans le corps humain, mais l'idée de la propagation de la tumeur dans tout le corps était correcte. Les cellules malignes finissent par se séparer de la tumeur et donner des métastases.
Les médecins et les guérisseurs utilisent la théorie humorale depuis plus de 1300 ans. Pendant cette période, les autopsies ont été interdites pour des raisons religieuses, ce qui a limité l'étude des tumeurs. Les traitements disponibles dans les temps anciens et au Moyen Âge étaient la chirurgie, la moxibustion, la saignée et les rituels.
Première chirurgie
La chirurgie est l'une des plus anciennes branches de la médecine. Cependant, à l'époque médiévale, les interventions n'ont pas toujours conduit aux résultats escomptés en raison de la grande perte de sang, d'un risque élevé d'infection après la chirurgie et de l'absence d'antiseptiques.
GalenLe médecin romain Galen (130-200 AD) a écrit sur le traitement chirurgical du cancer du sein à un stade précoce, mais n'a pas considéré cette méthode efficace pour traiter les tumeurs volumineuses et "cachées". Il a adhéré à la théorie humorale et a suggéré que la bile noire ne peut pas être complètement retirée du corps. Cette approche a sauvé la vie de nombreuses personnes: au Moyen Âge, les patients sont souvent décédés pendant la chirurgie ou en raison de complications postérieures.
Annulation de la théorie humoraleAprès la levée de l'interdiction de l'autopsie au XVIe siècle, Andreas Vesalius a compilé le premier guide anatomique du corps humain et, un siècle plus tard, Matthew Bailey a décrit la structure de diverses pathologies. La théorie humorale a dû être révisée, car les scientifiques n'ont trouvé aucune bile noire.

Au 17ème siècle, les méthodes chirurgicales pour enlever les tumeurs ont commencé à se développer. Le chirurgien allemand Wilhelm Fabry lors d'une opération pour retirer le cancer du sein a excisé une tumeur ainsi que des ganglions lymphatiques élargis, et le chirurgien néerlandais Adrian Helvetius a effectué une mastectomie, une ablation complète du sein. Quelques années plus tard, il a écrit sur l'un des cas: «Depuis, le patient s'est complètement rétabli. Les douleurs ont complètement cessé, les cicatrices ont guéri et elle jouit du même état de santé qu'avant le cancer. »
Dans les années 1850, le scientifique allemand Rudolf Virchow a découvert une division cellulaire incontrôlée dans les tumeurs. Il a appelé ce phénomène néoplasie, et son travail principal, Pathologie cellulaire, est devenu la base pour comprendre les causes du cancer.
Anesthésie et antiseptiqueEn 1846, l'anesthésie a été inventée. Cela a résolu le problème de la douleur, car auparavant, les gens devaient subir une intervention chirurgicale dans leur esprit. Et en 1867, le médecin français Joseph Lister a découvert que la pommade à l'acide carbolique agit comme un antiseptique et aide à guérir les plaies après la chirurgie.
L'anesthésie et le premier antiseptique ont élargi les possibilités de la chirurgie et les opérations ont commencé à être effectuées partout. Cependant, dans certains cas, les tumeurs ont réapparu. Ensuite, les chirurgiens ont commencé à augmenter le volume des interventions, ce qui a finalement conduit à l'émergence d'une méthode de chirurgie radicale.
Chirurgie radicaleLe chirurgien William Halstead pensait que plus il y aurait de tissus prélevés pendant la chirurgie, moins il y aurait de risques de rechute. La conclusion n'est pas entièrement correcte, car les cellules malignes pourraient même se propager dans tout le corps et se métastaser dans d'autres tissus avant la chirurgie.

Ce n'est que dans les années 1970 lors d'essais cliniques qu'il a été prouvé que des opérations moins étendues sont aussi efficaces que des opérations radicales. Malheureusement, à cette époque, la mastectomie radicale a gagné en popularité et était considérée comme la seule véritable méthode de traitement du cancer du sein.
ModernitéDans les années 1990, les chirurgiens ont minimisé les interventions dans les tissus humains sains. Aujourd'hui, les opérations sont divisées en deux types: ouvertes et peu invasives. Pour une chirurgie ouverte, le médecin fait une grande incision pour retirer la tumeur, les tissus malsains et éventuellement les ganglions lymphatiques.
Pour effectuer une opération mini-invasive, le médecin fait plusieurs petites incisions, trouve la tumeur à l'aide d'un tube mince avec une caméra (laparoscope) et retire la tumeur par une autre incision avec des instruments. Après cette opération, le patient récupère plus rapidement.
Radiothérapie
À la fin du 19e siècle, les scientifiques ont attiré l'attention sur la capacité des rayons X à tuer les cellules malignes. Ensuite, personne ne savait non plus comment le rayonnement destructeur affecte les tissus sains.
Tubes à rayons XLes rayons X ont été découverts en 1895, simultanément avec le développement de la chirurgie radicale. Un an plus tard, un jeune médecin Emil Grubbe a remarqué comment la peau et les ongles des personnes qui travaillaient avec des sources de rayonnement ont été détruits. Il a suggéré que les rayons tuent également les cellules tumorales et a été le premier à utiliser la radiothérapie pour traiter l'oncologie.
La méthode a rapidement gagné en popularité: en Europe et aux États-Unis ont ouvert de nouvelles cliniques offrant une radiothérapie. Il était efficace dans les cas où la tumeur n'avait pas le temps de se propager à d'autres organes.
L'idée d'utiliser le rayonnement était excellente, mais elle ne tenait pas compte de deux inconvénients importants du tube à rayons X: un flux de rayonnement inhomogène et un pouvoir de pénétration insuffisant. La majeure partie de la dose est absorbée par d'autres tissus ou dispersée. Ainsi, les rayons X augmentent le nombre de mutations dans les cellules saines, ce qui conduit à la formation de nouvelles tumeurs. Cette option ne peut pas être considérée comme un traitement approprié.
RadiumEn 1902, les scientifiques Pierre et Marie Curie ont découvert les propriétés radioactives du radium. À première vue, cette substance pénétrait plus profondément que les rayons X et offrait plus de possibilités de traitement. Au cours des 10 années qui ont suivi la découverte du radium, de nombreux médecins et scientifiques qui ne sont pas conscients des dangers de l'exposition ont développé diverses maladies malignes. Cela s'est poursuivi jusqu'à l'apparition des premiers dosimètres et étalons de mesure du rayonnement radioactif.
Accélérateur d'électrons et cobalt radioactifEn 1940, Donald Kerst a assemblé un bétatron, un accélérateur cyclique d'électrons. L'appareil émet des particules à haute énergie et capacité de pénétration, donc lorsqu'il est utilisé, il y a peu de rayons diffusés. En 1951, le neurochirurgien suédois Lars Lexell a développé le Gamma Knife. Il a plusieurs sources de rayonnement de cobalt radioactif et donne un faisceau uniforme de haute énergie. Le Betatron et le gamma knife sont utilisés avec succès pour traiter les tumeurs aujourd'hui.

Le rayonnement détruit l'ADN des cellules directement ou indirectement. Dans le deuxième cas, l'eau contenue dans les cellules se transforme en radicaux libres - particules chargées qui endommagent l'ADN. Le rayonnement ne comprend pas quelles cellules détruire, saines ou malignes, par conséquent, les appareils nécessitent un ajustement minutieux afin que le pic de dose tombe à la profondeur souhaitée.
ModernitéAujourd'hui, l'oncologie utilise des rayons X, des rayons gamma et des particules chargées. Ils peuvent pénétrer dans le corps et agir sur les cellules malignes grâce à un appareil spécial ou provenir de matières radioactives placées dans le corps du patient à côté de la tumeur (curiethérapie).
Il existe également un troisième type de radiothérapie - systémique. Un patient reçoit une injection d'un liquide radioactif, tel que l'iode, qui trouve et tue les cellules tumorales. Mais dans ce cas, il est difficile de prendre en compte la quantité exacte d'isotope que le corps absorbe, et la dose peut être nocive.
Chimiothérapie
La chirurgie et la radiothérapie ont été utilisées pour traiter les tumeurs solides qui ne se développent pas à partir des cellules du système hématopoïétique. Personne ne savait comment traiter le lymphome et la leucémie.
Gaz moutardeL'idée d'utiliser des substances toxiques pour traiter ces maladies est née après la Première Guerre mondiale. À cette époque, le gaz moutarde, le gaz moutarde, était utilisé comme arme chimique. Il a brûlé la peau et les muqueuses et a également tué des globules blancs: ils étaient pratiquement absents chez les blessés.
Les scientifiques se sont demandé si le gaz moutarde pouvait guérir le lymphome, une tumeur du tissu lymphatique. Avec cette maladie, les lymphocytes se divisent et perturbent de façon incontrôlable le fonctionnement des ganglions lymphatiques et d'autres organes, de sorte que la réduction des lymphocytes semblait être la bonne décision. En 1942, après des études animales, un patient atteint de lymphome a reçu par voie intraveineuse 10 doses de gaz moutarde. Le nombre de lymphocytes a chuté rapidement et la tumeur a diminué, mais a ensuite recommencé à se développer. Cela signifiait que la thérapie fonctionnait, mais la dose n'était pas suffisante pour récupérer complètement.
La rémission s'est produite parce que le gaz moutarde était inclus dans le groupe des agents alkylants qui détruisent l'ADN des cellules et les empêchent de se diviser. Mais alors, ils ne savaient toujours rien.
 Précurseur du méthotrexate
Précurseur du méthotrexateEn 1947, le docteur Sidney Farber a montré qu'un dérivé d'acide folique, l'améthoptérine, inhibe le développement de la leucémie aiguë chez les enfants, caractérisée par une division incontrôlée des globules blancs. Ce médicament était le précurseur du méthotrexate, qui est toujours utilisé aujourd'hui.
Les résultats d'une biopsie de moelle osseuse de patients après un traitement à l'améthoptérine étaient normaux. La chimiothérapie a prolongé la vie des enfants jusqu'à 6 mois, mais la maladie est revenue. Farber a déployé toutes ses forces pour trouver un remède qui pourrait guérir complètement la leucémie. Il était alors difficile de supposer qu'il était nécessaire d'utiliser plusieurs substances toxiques à la fois, et pas une.
En 1950, Gertrude Elion a développé le médicament 6-mercaptopurine (6-MP), qui a rapidement été approuvé pour une utilisation chez les enfants atteints de leucémie. Après lui, les médecins ont de nouveau observé une courte rémission.
Chimiothérapie combinéePlus tard, des essais cliniques randomisés ont été menés, au cours desquels il est devenu clair que l'utilisation de deux médicaments au lieu d'un prolonge la rémission et améliore le pronostic.
En 1956, le Dr Min Chiu Lee a confirmé cliniquement qu'une combinaison de quatre médicaments guérissait le choriocarcinome métastatique chez les femmes enceintes. L'Institut national d'oncologie a d'abord considéré ces actions comme un traitement agressif et inutile des patients, et le scientifique a été suspendu de ses fonctions. Ce n'est que plus tard qu'il est devenu clair que seules les femmes qui avaient suivi le traitement complet de Lee ont survécu. Ce fut la première cure complète avec chimiothérapie.
Chimiothérapie adjuvanteDans les années 60 et 70, les scientifiques ont essayé d'utiliser la chimiothérapie comme traitement supplémentaire pour le cancer du sein après la chirurgie. Les chirurgiens hésitaient à entreprendre des essais cliniques: personne ne voulait faire face à des effets secondaires supplémentaires chez les patients. Mais ils avaient tort.
En fait, toute tumeur est une maladie systémique. Les cellules malignes se propagent dans tout le corps même aux premiers stades sous forme de micrométastases. Ils restent dans le corps même après l'ablation de la tumeur, les méthodes de traitement locales ne sont donc pas suffisantes. Il est nécessaire d'affecter systématiquement la maladie à l'aide d'un traitement médicamenteux. Par exemple, un traitement adjuvant (chimiothérapie après chirurgie) peut réduire le risque de rechute et de décès.
Plusieurs études ont montré l'intérêt de la chimiothérapie adjuvante pour le traitement du cancer du sein et du cancer colorectal. Toujours en 1974, un effet positif a été prouvé dans le cas du cancer du testicule métastatique, et la chimiothérapie a été utilisée pour traiter les tumeurs solides.
Les médicaments de chimiothérapie arrêtent et ralentissent la division cellulaire. Au cours du traitement, les cellules qui se divisent meurent rapidement. Ce ne sont pas seulement des cellules malignes, mais aussi des cellules saines, ce qui entraîne des effets secondaires: perte de cheveux, nausées et sensibilité aux infections.
Immunothérapie
L'immunothérapie est un type de traitement du cancer relativement nouveau. Il est basé sur l’utilisation de médicaments qui entraînent les cellules immunitaires du patient. Cela a été rendu possible grâce à la découverte de la structure de l'ADN, à l'étude des caractéristiques des cellules malignes et des cellules du système immunitaire.
Vaccin coliEn 1891, William Coley a noté que les patients atteints de cancer qui avaient la scarlatine ou une maladie érysipélateuse avaient une rémission. Après cela, il a commencé à administrer des bactéries streptococciques à des patients atteints d'un cancer avancé. La tumeur a diminué, mais les patients sont décédés d'une infection. Puis Kolya a chauffé le vaccin et a introduit des streptocoques morts aux patients.
Le résultat pour l'époque était impressionnant: les patients se sont rétablis et ont vécu plusieurs années. Cependant, le vaccin Kolya n'est pas répandu. Les scientifiques n'ont pas pu expliquer le mécanisme de l'action des bactéries sur la tumeur et le risque d'infection était élevé. Tout le monde était beaucoup plus intéressé par la chimiothérapie et la radiothérapie.
En 1976, le vaccin BCG, utilisé pour prévenir la tuberculose, a été utilisé avec succès pour traiter le cancer de la vessie. Il active le système immunitaire et aide le corps à combattre ce type de cancer.
Anticorps monoclonauxEn 1975, Georges Köller et Cesar Milstein ont publié un article sur une méthode de production d'un hybride cellulaire d'une cellule tumorale et d'un lymphocyte. La technologie des hybridomes permet de détecter des antigènes caractéristiques des tumeurs de certains tissus, d'obtenir des anticorps contre ces derniers et de les utiliser pour le diagnostic et le typage des tumeurs. Ces anticorps sont appelés monoclonaux: ils sont produits par des cellules immunitaires clones qui proviennent de la même cellule mère.
D'autres types d'anticorps marquent les cellules cancéreuses pour faciliter la détection et la destruction du système immunitaire.
À la fin des années 1990, la FDA a approuvé les premiers anticorps monoclonaux thérapeutiques, le rituximab et le trastuzumab. Le premier est destiné au traitement du lymphome et le second au cancer du sein.
En 2010, Stephen Rosenberg a annoncé le succès de la thérapie par les récepteurs d'antigènes chimériques. Il est basé sur une modification génétique des cellules T du patient pour le traitement d'une tumeur maligne.
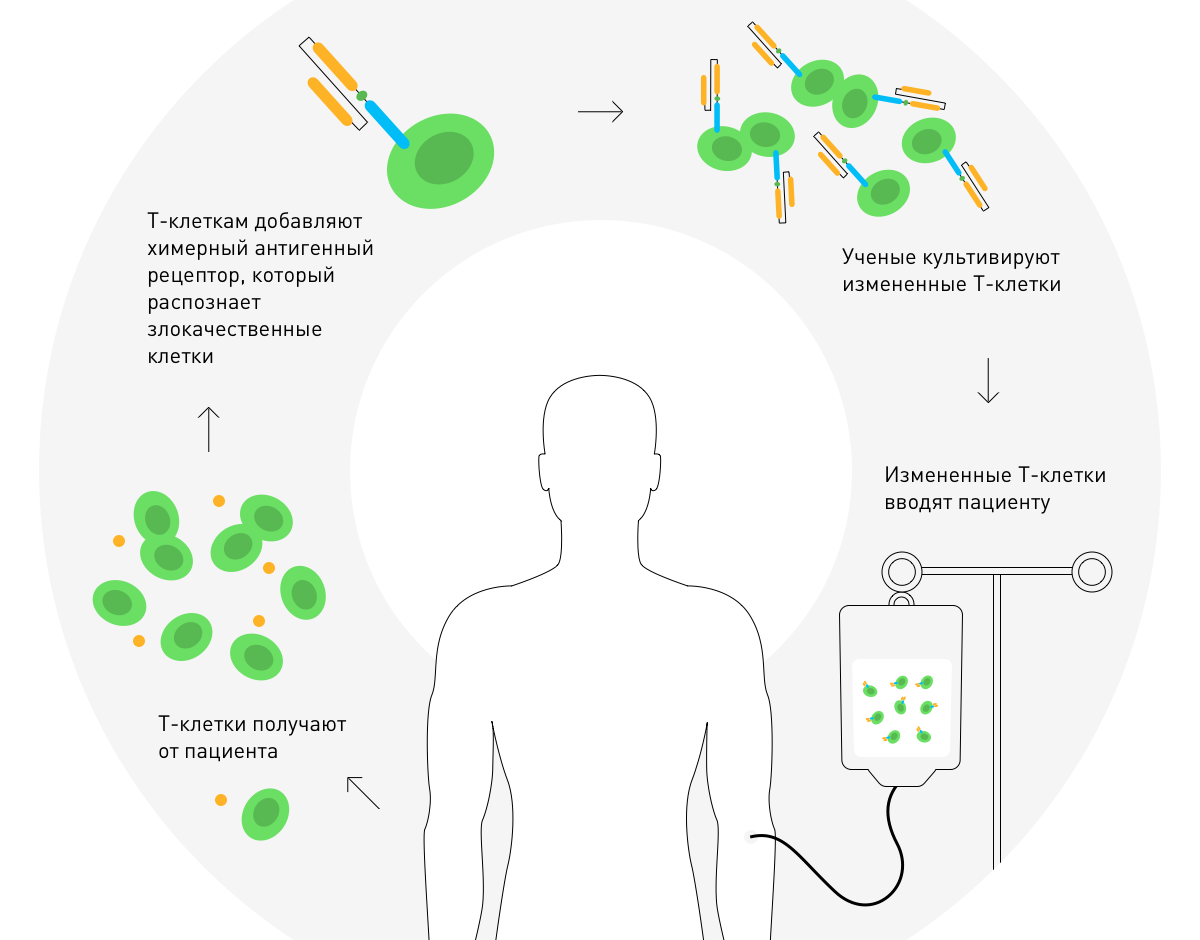 Cytokines
CytokinesUne autre méthode d'immunothérapie est l'introduction dans le muscle ou la veine de cytokines, des protéines biologiquement actives qui régulent la réponse immunitaire. L'interleukine-2 aide les cellules du système immunitaire à se diviser plus rapidement et l'interféron - à lutter contre les infections virales et les tumeurs malignes.
Points de contrôleUn autre domaine prometteur est l'effet sur les points de contrôle immunitaire, qui suppriment la réponse du système immunitaire. Les scientifiques ont appris à bloquer les points de contrôle des cellules T, ce qui aide le système immunitaire à reconnaître et à attaquer les cellules malignes. Cette méthode a déjà été approuvée par la FDA pour le traitement du cancer.
Le traitement optimal peut être sélectionné à l'aide de diagnostics moléculaires. Les scientifiques examinent le matériel chirurgical ou la biopsie du patient pour identifier les mutations des proto-oncogènes et des gènes suppresseurs. L'ensemble des mutations est individuel pour chaque tumeur, le traitement doit donc être personnalisé. La prochaine fois, l'
Atlas parlera en détail du diagnostic moléculaire.