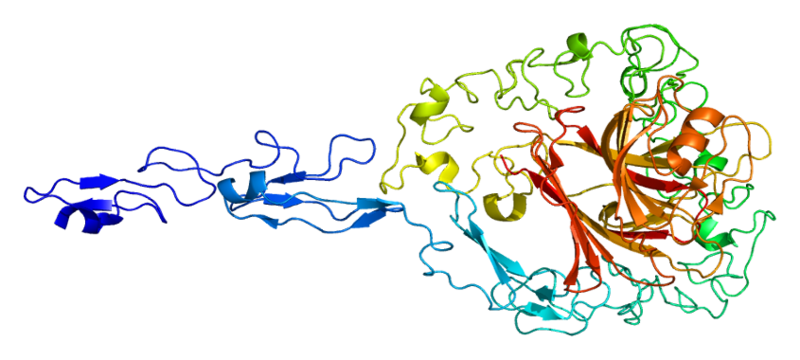
 Structure de la protéine thrombospondine-2
Structure de la protéine thrombospondine-2Fin juillet de cette année, une
grande étude d'un groupe international de chercheurs consacré à la recherche de biomarqueurs efficaces du vieillissement dans le cadre du concept de
fragilité (fragilité ou asthénie sénile) a été publiée.
Le terme «fragilité» a été introduit dans la diffusion scientifique de JH Friend en 1954, d'abord retenu dans l'article Science
«Hélas pour les fragilités humaines! . Le concept même de
fragilité se définit aujourd'hui comme la présence de tels signes chez une personne âgée: perte de poids (sarcopénie), réduction dynamiquement prouvée de la force des brosses, faiblesse sévère et fatigue accrue, diminution de la vitesse de déplacement, diminution significative de l'activité physique. Il est généralement admis que la
fragilité (asthénie sénile) survient lorsqu'il y a trois symptômes ou plus, mais s'il y a un ou deux symptômes, il s'agit d'un inconfort sénile.
États-Unis Le Conseil fédéral sur le vieillissement a inventé le terme «fragilité» pour un groupe spécial de personnes âgées atteintes de
«déficiences physiques, cognitives et émotionnelles importantes qui nécessitent une attention supplémentaire» . Selon les estimations modernes, le nombre de personnes âgées pouvant être classées comme
fragiles est aujourd'hui de 12,9%, l'invalidité sénile est de 48,9%, qui, en l'absence de traitement adéquat et de mesures de réadaptation, prend une forme détaillée dans les 4 à 5 ans.
Les auteurs de cette étude définissent la
fragilité comme
«le phénotype principal du vieillissement accéléré qui décrit la dysfonction multi-organes ou la multi- morbidité (c'est-à-dire la présence de 2 maladies chroniques ou plus, sans lien étiologique et pathogène),
ainsi qu'une vulnérabilité accrue aux maladies supplémentaires chez les personnes âgées» .
Comme base de leur travail, les scientifiques ont utilisé des bases de données d'expression génique (http://genomics.senescence.info/genes, y compris GenAge, AnAge, LongevityMap, CellAge, DrugAge, Digital Aging Atlas) pour identifier les gènes qui sont régulés pendant le vieillissement, la longévité et maladies liées à l'âge. Dans le même temps, ils ont accordé une attention particulière aux facteurs et molécules sécrétés trouvés dans les fluides biologiques en tant que biomarqueurs potentiels.
Lors de la première étape des travaux, des facteurs ont été identifiés qui ont été largement exprimés et associés à plusieurs voies de «signes distinctifs du vieillissement», ainsi que ceux déjà utilisés comme biomarqueurs dans le diagnostic des pathologies liées à l'âge. Ensuite, cet ensemble de biomarqueurs a été élargi conformément à l'expérience des auteurs de l'étude.
La recherche de biomarqueurs a été menée dans six directions, six «signes de vieillissement»:
1. Inflammation
2. Mitochondries et apoptose
3. Homéostasie calcique,
4. Fibrose
5. NMJ (jonction neuromusculaire) et neurones
6. Le cytosquelette et les hormones.
44 biomarqueurs potentiels ont été analysés, dont 19 ont reçu un score de haute priorité, 22 ont été identifiés comme étant de priorité moyenne.
En conséquence, les chercheurs ont identifié un panel de biomarqueurs de
fragilité principal et élargi en six points.
L'inflammation Les changements généraux du système immunitaire, affectant les réponses immunitaires adaptatives et innées, sont devenus l'un des «signes de vieillissement» les plus importants, et les facteurs immunologiques ont été parmi les premiers marqueurs décrits pour l'asthénie sénile. Le processus de vieillissement est étroitement lié à l'augmentation systémique des médiateurs pro-inflammatoires de diverses natures. Cette augmentation peut être soit directement liée à l'exposition soutenue aux agents infectieux tout au long de la vie, soit à des changements liés à l'âge dans le microbiote intestinal.
La raison peut en être le dysfonctionnement métabolique observé dans l'obésité, ainsi que la sécrétion d'antigènes causée par la mort cellulaire et l'accumulation subséquente de débris cellulaires. En général, l'inflammation entraîne une stimulation chronique des cellules immunitaires, ce qui se traduit par une inflammation de bas grade et à long terme, qui affecte les réponses immunitaires innées et adaptatives.
De plus, le vieillissement entraîne des changements notables dans les phénotypes et les fonctions des cellules immunitaires. En général, ce phénotype, appelé «immunogénicité», favorise l'accumulation de lésions cellulaires et moléculaires dans les tissus vieillissants, potentialise de nombreux troubles liés à l'âge (par exemple, l'athérosclérose, le diabète et les maladies neurodégénératives) et, surtout, réduit la réponse efficace aux infections, au cancer et à d'autres lésions tissulaires. .
En relation avec l'inflammation, les biomarqueurs suivants ont été identifiés:
- Antigène CD14 . Il s'agit d'une glycoprotéine qui s'exprime principalement par les monocytes et les macrophages. En tant que partie du complexe TLR 4 - CD14, il participe à la réponse immunitaire de l'organisme - la liaison des lipopolysaccharides bactériens.
- Fractalkin (CX3CL1) . La fractalkine est produite surtout dans les cellules endothéliales activées, les cellules musculaires lisses et les macrophages. Il améliore la migration des leucocytes de la circulation sanguine dans les tissus en augmentant la liaison médiée par la sélectine, provoquant l'adhésion et, finalement, la migration des leucocytes à travers la couche endothéliale. CX3CL1 possède également des propriétés anti-apoptotiques.
- Pentraxine (PTX3) . La pentraxine agit comme un composant de l'immunité innée humorale et est induite par diverses cytokines inflammatoires dans les leucocytes du sang périphérique et les cellules dendritiques myéloïdes.
La pentraxine est également sécrétée par les cellules endothéliales, les cellules musculaires lisses vasculaires, les fibroblastes et les adipocytes, favorisant la différenciation des fibrocytes et jouant un rôle dans l'angiogenèse et le remodelage des tissus. - Molécules d' adhésion SVCAM / sICAM (molécule d'adhésion intercellulaire de type 1, molécule d'adhésion endothéliale vasculaire de type 1). Ils appartiennent à la superfamille des immunogolobulines. ICAM-1 est exprimé sur les cellules épithéliales et dendritiques, les fibroblastes, les macrophages tissulaires et VCAM-1 - sur les macrophages tissulaires, les cellules dendritiques, les fibroblastes osseux, les myoblastes et les fibres musculaires.
- Interleukine 6 (IL-6) . C'est l'un des médiateurs les plus importants de la phase aiguë de l'inflammation. Exprimé dans divers tissus, y compris le muscle squelettique, la vessie, la vésicule biliaire, l'appendice, l'œsophage, la moelle osseuse, les poumons, les glandes surrénales, la prostate et le tissu adipeux. L'IL-6 est principalement produite aux sites d'inflammation et induit une réponse inflammatoire transcriptionnelle par l'IL-6RA (récepteur alpha-IL-6).
- L'interféron γ est une protéine inductible (IP-10) , une autre désignation est la chimiokine 10 du motif CXCL10 CXC. C'est une chimiokine induite par l'IFN de la sous-famille CXC et un ligand pour le récepteur CXCR3, qui est principalement exprimé par les lymphocytes T activés et les fibroblastes.
La liaison de CXCL10 à CXCR3 entraîne la migration des cellules T, la stimulation des monocytes et des cellules NK, ainsi que la modulation de l'expression de la molécule d'adhésion et l'induction de l'apoptose
Mitochondries et apoptose . Les mitochondries jouent un rôle central dans la production d'ATP, ainsi que dans la réduction du taux métabolique basal et des performances physiques. Les dysfonctionnements des mitochondries liés à l'âge comprennent une diminution du taux de transfert d'électrons, une perméabilité accrue par rapport à H + de la membrane interne et une altération de la synthèse d'ATP.
De plus, les mutations de l'ADN mitochondrial s'accumulent au cours du vieillissement. Toutes les cellules, en particulier les neurones et les cellules musculaires, sont très sensibles au dysfonctionnement mitochondrial associé aux dommages oxydatifs, car de grandes quantités d'ATP sont nécessaires pour maintenir les processus neuronaux et la fonction contractile.
Dans le cadre de la dysfonction mitochondriale, les biomarqueurs suivants ont été identifiés:
Facteur de différenciation de croissance
-15 (facteur de différenciation de croissance 15, GDF15). Cytokine pléiotrope, une protéine de la superfamille du facteur de croissance transformant bêta. Impliqué dans la réponse inflammatoire et la régulation de l'apoptose en cas de lésion et lors de différents processus pathologiques.
Irizine (domaine de la fibronectine de type III contenant 5, FNDC5). Protéine membranaire, précurseur de l'hormone peptidique irisine. Il régule positivement la différenciation des graisses brunes, favorise la biogenèse mitochondriale, préserve la fonction des mitochondries dans des conditions d'hypoxie, protège contre l'apoptose et possède une activité anti-inflammatoire.
Vimentine (VIM) . Une protéine qui joue un rôle important dans le maintien de l'intégrité cellulaire. Impliqué dans les processus d'apoptose.
Homéostasie du calcium .
Le calcium joue un rôle important dans de nombreux processus physiologiques et physiopathologiques, extracellulaires et intracellulaires. Les niveaux physiologiques de calcium ont des limites assez étroites, et même de petits changements peuvent entraîner d'énormes dysfonctionnements.
Le calcium est absorbé dans les intestins, excrété par les reins et ses niveaux sont principalement régulés par les hormones parathyroïdiennes. Le calcium se trouve principalement dans les muscles, le cœur et les os. Au sein de la cellule, le réticulum endoplasmique (ER) et les mitochondries sont le principal réservoir et, dans des conditions homéostatiques, des concentrations relativement faibles de calcium sont présentes dans le cytoplasme.
La viabilité cellulaire et l'activité d'un grand nombre d'enzymes dépendent du calcium. Ainsi, il n'est pas surprenant que les troubles de l'homéostasie du calcium soient associés à des dysfonctionnements d'organes, à la vieillesse et à de nombreuses maladies.
Les biomarqueurs suivants ont été identifiés ici:
S100 calcium binding protein B (S100 calcium binding protein B, S100B). Appartient au groupe des protéines de liaison au calcium S100, elle est produite dans les cellules gliales, principalement les astrocytes, ainsi que dans les adipocytes. Participe à la signalisation intracellulaire et extracellulaire du calcium. Le S100B est impliqué dans la régulation d'un certain nombre de processus cellulaires, tels que la progression et la différenciation du cycle cellulaire.
Regucalcin (Regucalcin, RGN) . Également connu sous le nom de protéine marqueur de vieillissement-30 (protéine marqueur de sénescence-30, SMP30). Exprimé principalement dans le foie et les reins. Il joue un rôle important dans l'homéostasie calcique, est impliqué dans le stress oxydatif induit par le calcium.
Calréticuline (calréticuline, CALR) . Une protéine multifonctionnelle qui se lie aux ions Ca 2+. Il agit dans les mitochondries, à la surface des cellules proapoptotiques et dans le réticulum endoplasmique, où il se lie aux protéines mal repliées pour empêcher leur exportation. Il a un certain nombre de fonctions dans l'apoptose et dans la réponse immunitaire.
Fibrose .
La fibrose est le processus de formation de tissu fibreux, qui peut faire partie du processus normal de cicatrisation après une blessure. Dans le même temps, le tissu fibreux peut également remplacer de façon permanente les tissus fonctionnels en raison du vieillissement.
En conséquence, les tissus fibreux s'accumulent dans des organes tels que le cœur, les poumons, les reins, le foie et interfèrent avec le fonctionnement normal des organes. Cela entraîne une hyperprolifération et une inflammation accrue en raison de la présence de diverses cellules inflammatoires (neutrophiles et macrophages).
De plus, l'activité non contrôlée de la protéase interfère avec les mécanismes de réparation normaux, ce qui peut entraîner une augmentation du tissu fibreux. De nombreuses cytokines, telles que l'IL-13 (interleukine 13), l'IL-21 (interleukine-21), le TGF-bêta et les chimiokines, telles que MCP-1 et MIP-1 bêta, sont impliquées dans la fibrose.
De plus, les facteurs angiogéniques (par exemple, VEGF (facteur de croissance endothélial vasculaire)), les facteurs de croissance (par exemple, PDGF (facteur de croissance dérivé des plaquettes)) et les composants du système rénine-angiotensine-aldostérone ont été identifiés comme d'importants régulateurs de la fibrose et sont à l'étude comme cibles potentielles. médicaments anti-fibreux.
Dans le cadre de la fibrose, les biomarqueurs suivants ont été identifiés:
- Transforming Growth Factor Beta (TGF-beta) . Une protéine qui contrôle la prolifération, la différenciation cellulaire et d'autres fonctions dans la plupart des cellules. Un représentant des cytokines, est impliqué dans la réponse immunitaire, le cancer, les maladies cardiovasculaires, le diabète et de nombreuses autres pathologies.
- Inhibiteur 1 de l'activateur du plasminogène (PAI-1 ou Serpine E1). Il inhibe l'activité de l'activateur tissulaire du plasminogène et de l'urokinase, qui, à leur tour, activent la transition du plasminogène en plasmine, qui décompose la fibrine du caillot sanguin. Ainsi, le PAI-1 affecte négativement la fibrinolyse et empêche la dissolution des caillots sanguins, ce qui augmente le risque de complications vasculaires, diverses thromboembolies.
- Activateur de plasminogène urokinase ( activateur de plasminogène urokinase, uPA). Il s'agit d'une sérine protéase sécrétée qui convertit le plasminogène en plasmine. Elle est fonctionnellement associée à l'inhibiteur d'activateur du plasminogène décrit ci-dessus 1. L'activation de la plasmine provoque une cascade protéolytique qui, selon l'environnement physiologique, est impliquée dans la thrombolyse ou la dégradation de la matrice extracellulaire. Cette cascade est impliquée dans les maladies vasculaires et la progression du cancer.
- Matrilysine, métalloprotéinase matricielle-7 (MMP-7) . La MMP-7 est exprimée dans divers organes et tissus, notamment le foie, les poumons, le cœur, la glande mammaire, la rate, le cerveau, la moelle épinière et l'hypophyse. Les fonctions de MMP-7 sont étroitement liées à des processus tels que la morphogenèse, l'angiogenèse et la réparation tissulaire. La dérégulation de son action est associée à la fibrose, la production de cytokines inflammatoires et les déséquilibres endocriniens. Impliqué dans un certain nombre de pathologies, telles que la cirrhose, la polyarthrite rhumatoïde et le cancer.
- Transglutaminase 2 (TGM2) . C'est le membre le plus répandu de la famille des transglutaminases et il est exprimé à des degrés divers dans presque tous les types de cellules. Il joue un rôle modulateur dans le développement du système nerveux, ainsi qu'un effet régulateur sur la mort des cellules neuronales. Impliqué dans divers processus physiopathologiques, tels que la cicatrisation des plaies, la croissance et la survie des cellules, l'apoptose et l'autophagie.
- Thrombospondine-2 (THBS2) . Une partie de la famille des protéines de thrombospondine est présente dans divers tissus, tels que l'épithélium et l'endothélium, le tissu conjonctif. Il active le TGF-beta latent et joue un rôle important dans la régulation de la prolifération cellulaire, de l'apoptose et de l'angiogenèse.
- Angiotensinogène (angiotensinogène, AGT). Le précurseur de l'angiotensine est produit dans le foie et est transformé en angiotensine I par l'action de la rénine. Les niveaux d'angiotensinogène augmentent avec les corticostéroïdes plasmatiques, les œstrogènes, l'hormone thyroïdienne et l'angiotensine II. Il joue un rôle clé dans la régulation de la pression artérielle systémique, de la vasoconstriction, de la prise d'eau et de la rétention de sodium, dans les processus pro-inflammatoires, prothrombotiques et profibrotiques.
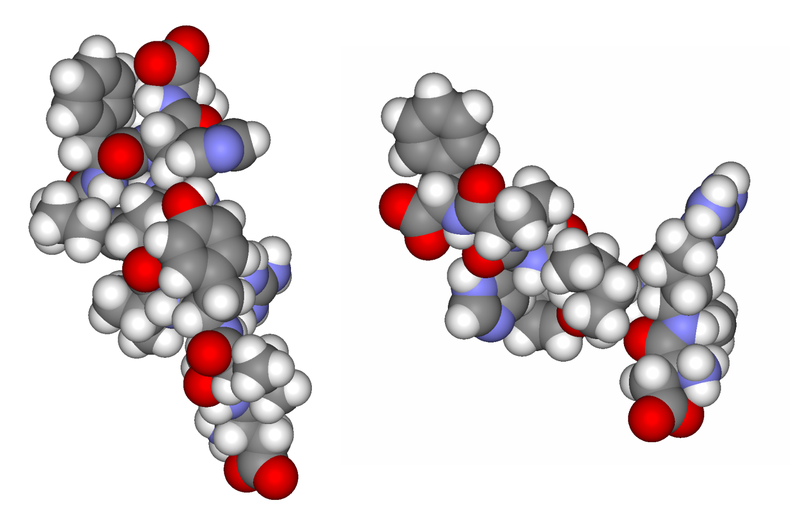 Angiotensine I et II
Angiotensine I et IIPréparé par Alexey Rzheshevsky