 Porcs légers dans un bioréacteur
Porcs légers dans un bioréacteurLa culture d'organes commencera à sauver la vie des patients dans un délai de cinq ans, après que les scientifiques ont transplanté avec succès un poumon de porc bio-conçu.
Un groupe de l'
École de
médecine de l'
Université du Texas (UTMB) a montré que les poumons, cultivés en laboratoire, prenaient facilement racine chez les porcs et, en deux semaines, un réseau de vaisseaux sanguins s'y est développé.
Les tentatives précédentes ont échoué, car les organes ne formaient pas un réseau complexe de vaisseaux nécessaires à l'approvisionnement correct en oxygène et en circulation sanguine.
Mais de nouvelles expériences ont montré que deux mois après l'implantation, les poumons fonctionnaient toujours et que les porcs avaient une saturation en oxygène à 100%, ce qui signifiait que tous leurs globules rouges transportaient l'oxygène à travers le corps.
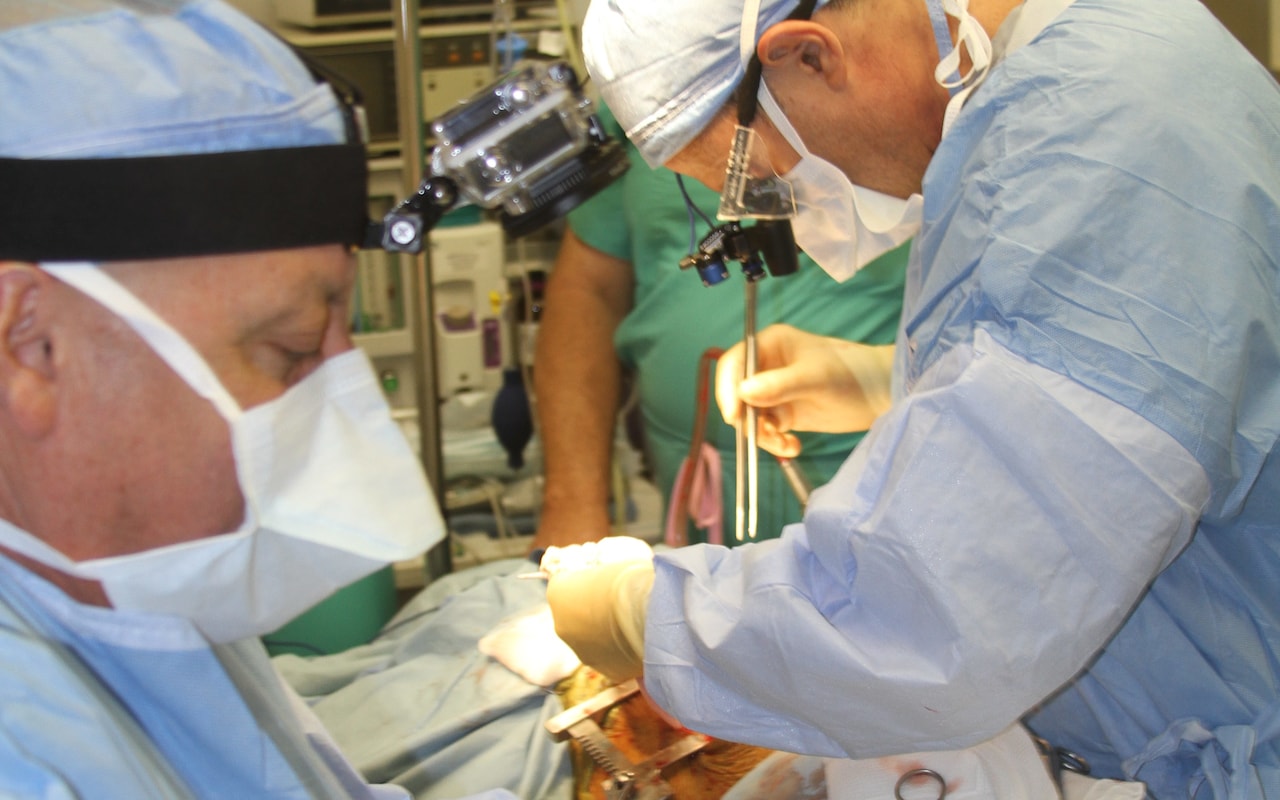 Transplantation en temps réel de poumons de porc bio-modifiés
Transplantation en temps réel de poumons de porc bio-modifiésLa méthode aidera à résoudre la
crise du don d'organes au Royaume-Uni. La liste d'attente compte environ 7 000 personnes, dont 350 ont besoin d'une transplantation pulmonaire en raison de la fibrose kystique et de l'emphysème, mais un quart mourra sans recevoir l'organe souhaité.
«Notre objectif ultime est d'offrir de nouvelles opportunités à de nombreuses personnes en attente d'une greffe», a déclaré Joan Nichols, professeur de médecine à l'UTMB.
"Dans le futur, nous allons prélever des cellules souches humaines et développer un organe qui sera leur organe, sans immunosuppression, et qui fonctionnera comme leurs propres poumons."
Wakin Cortiella, directeur du Laboratoire de génie tissulaire et de régénération d'organes de l'UTMB, a déclaré: "Je dirais que dans cinq à dix ans, nous recevrons des patients avec des poumons bio-conçus."
 Joan Nichols et Wakin Cortiella en laboratoire
Joan Nichols et Wakin Cortiella en laboratoirePour faire croître des organes en laboratoire, les scientifiques ont pris des porcs légers et les ont privés de sang et de cellules à l'aide d'un mélange spécial, de sorte qu'il ne restait qu'un cadre.
Ensuite, ils ont créé un cocktail de nutriments et de cellules pulmonaires du porc qui recevra la greffe et l'ont placé dans un réservoir avec un squelette d'organe.
Les poumons ont été cultivés pendant 30 jours et implantés dans quatre porcs qui ont été maintenus en vie pendant 10 heures, deux semaines, un mois et deux mois pour voir comment les vaisseaux sanguins se développent.
Tous les porcs qui ont reçu des poumons issus de la bio-ingénierie sont restés en bonne santé.
Deux semaines après la transplantation, les poumons issus de la bio-ingénierie ont formé un réseau de vaisseaux sanguins nécessaires à la vie pulmonaire. Et il n'y avait aucun œdème pulmonaire pouvant entraîner une insuffisance respiratoire.
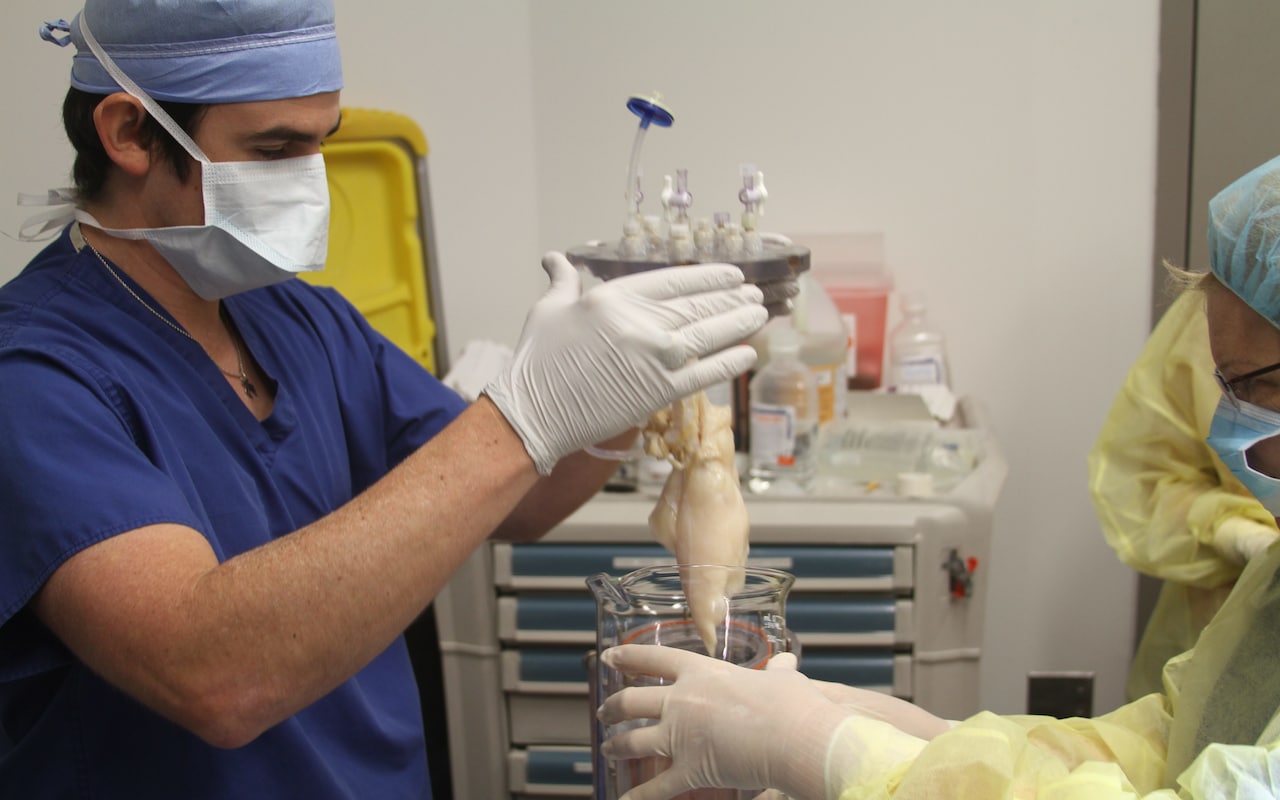 Poumons de bio-ingénierie à la veille de la transplantation
Poumons de bio-ingénierie à la veille de la transplantationActuellement, les poumons donnés doivent être ajustés en fonction de la taille des poumons du patient, et le receveur doit prendre des immunosuppresseurs pour réduire le risque de rejet d'organe. Mais si vous semez la structure d'un organe avec ses cellules, il n'y aura pas de réponse immunitaire.
Dans un avenir proche, des cadres pulmonaires seront reçus d'organes donnés, mais il est possible qu'à l'avenir ils soient imprimés sur une bioprinter.
"Nous avons développé un bien meilleur réseau vasculaire dans les poumons que nous n'avions pas auparavant", a déclaré le Dr Cortiella.
«Nous sommes également passés de petits animaux à de grands animaux avec de gros poumons.»
«Les poumons issus de la bio-ingénierie peuvent être développés à tout moment, de sorte qu'une personne n'a pas besoin d'attendre qu'un bon organe soit trouvé. Vous pouvez les cultiver à la fois comme un enfant et comme un adulte. "
La prochaine étape consiste à garder les porcs en vie aussi longtemps que possible afin que les poumons issus de la bio-ingénierie parviennent à maturité et prennent racine, mais les chercheurs disent qu'ils commenceront les tests chez les patients en phase terminale au cours des cinq à dix prochaines années.
«Tout le travail a nécessité 15 ans de recherche, notre équipe a fait des choses incroyables avec un budget minimal et un groupe de personnes incroyablement dévoué», a déclaré le professeur Nichols.
Publication dans la revue
Science Translational Medicine .