Les chercheurs ont tendance à accorder de plus en plus d'attention aux processus inflammatoires dans le cerveau dans les maladies dégénératives, à la fois dans le rôle de la cause racine et dans le rôle du facteur secondaire causé par les dommages aux tissus nerveux. La neuroinflammation peut s'avérer être le processus central du vieillissement de l'organisme.
Il est très difficile de déterminer la neuroinflammation dans le contexte de maladies neurodégénératives, bien que, par exemple, avec la sclérose en plaques (une maladie auto-immune qui n'a rien à voir avec la sclérose domestique), cela ne soit pas difficile. Dans ce dernier cas, les lymphocytes et les monocytes en excès pénètrent au-delà de la barrière séparant le tissu nerveux de la circulation sanguine, provoquant un dysfonctionnement.
Avec des pathologies qui incluent la maladie d'Alzheimer, que vous connaissez probablement de l'état de l'écrivain Terry Pratchett avant sa mort, la maladie de Parkinson, dont le peintre Salvador Dali a souffert au cours de ses dernières années, la sclérose latérale amyotrophique, qui est devenue connue en lien avec l'état du physicien Stephen Hawking, la description est effectuée en fonction de la réaction, exprimée par un changement dans la forme et la structure des cellules gliales - astrocytes et microglies. Beaucoup de ces maladies se manifestent à un âge avancé, elles sont associées au vieillissement et éventuellement provoquées par celui-ci. Comprendre la neuroinflammation, ses causes et ses conséquences, peut potentiellement améliorer le traitement de nombreuses maladies, dont certaines ne sont traitées que de manière symptomatique.
Afin de comprendre le phénomène de neuroinflammation, vous devez d'abord comprendre ce qu'est l'inflammation. La question proposée remonte à plus de 2000 ans, mais la définition de l'inflammation, qui conduirait les scientifiques et les médecins du monde entier à un consensus, n'a pas encore été proposée.
Qu'est-ce que l'inflammation?
"Rubor, et tumeur, cum calore et dolore." Rougeur, gonflement avec fièvre et douleur - c'est ainsi que l'ancien médecin romain Cornelius Celsus décrit l'inflammation. Cette définition manque de détails importants qui sont clarifiés par son collègue, le chirurgien Galen, environ 100 ans après son prédécesseur - functio laesa ou fonction altérée.
Ensemble, ces cinq signes décrits transmettent brièvement l'essence des manifestations de l'inflammation et, sous une forme presque inchangée, atteignent nos jours. Les étudiants en médecine sont toujours la première chose dont ils se souviennent du twister de langue latine lorsqu'ils ont répondu à l'examen.
Mais une telle définition ne nous convient pas catégoriquement, car elle ne dit rien sur les mécanismes du développement de la pathologie et de son étiologie. Avec la divulgation des détails de ce dernier, les physiologistes ont dû bricoler. L'histoire se souvient de nombreuses théories qui concernaient principalement le rôle des vaisseaux sanguins dans le développement de l'inflammation, cependant, une compréhension plus significative est apparue après qu'Ilya Mechnikov a attiré l'attention sur les cellules et dérivé sa définition:
«L'inflammation dans son ensemble doit être considérée comme une réaction phagocytaire du corps contre des figures ennuyeuses; cette réaction s'effectue soit en déplaçant les phagocytes seuls, soit sous l'action des phagocytes vasculaires ou du système nerveux. »
Les phagocytes, cellules capables d'absorber et de détruire les particules étrangères nocives, étaient au centre des travaux de Mechnikov. En conséquence, la principale raison de critiquer sa définition était le manque de reconnaissance du rôle des protéines dissoutes dans les fluides corporels, qui, comme on le sait maintenant, ont un effet significatif sur le processus. Nous sommes impressionnés par cette définition en raison de la mention du système nerveux, laissez Mechnikov et ajoutez-la uniquement pour reconnaître la régulation nerveuse de la paroi vasculaire, qui module également le cours de l'inflammation.
Avec une définition de la neuroinflammation, les choses vont vraiment mal. Si vous ouvrez Wikipedia, vous pouvez découvrir que «la neuroinflammation est une inflammation du tissu nerveux». Voici un tel circulus in definiendo, une erreur logique dans laquelle l'énoncé se déduit de lui-même.
LienUne définition intéressante peut être trouvée dans la colonne éditoriale ACS sur les neurosciences chimiques, qui définit la neuroinflammation comme des processus cellulaires non autonomes qui provoquent la mort cellulaire, un dysfonctionnement ou la restauration des neurones et des oligodendrocytes lors d'une maladie neurodégénérative.
"Processus non cellulaires autonomes qui dictent la mort, le dysfonctionnement ou la récupération des cellules du SNC pour les neurones et les oligodendrocytes au cours d'une maladie neurodégénérative."
LienIl s'agit d'une très bonne définition, qui décrit les bons et les mauvais côtés de la neuroinflammation, néanmoins elle limite ce processus à la portée d'une maladie neurodégénérative. Alors, que se passe-t-il avant qu'une personne n'ait pas remarqué Alzheimer ou Parkinson, elle ne peut pas avoir d'inflammation dans son cerveau?
Pour cela, la question de la définition reste ouverte. Tenez compte des faits et de l'interprétation de la recherche dans ce domaine.
Pourquoi l'inflammation est-elle nécessaire?
S'il n'y avait pas de régénération, la vie serait impossible.
Si tout se régénérait, la mort serait impossible.
"S'il n'y avait pas de régénération, il ne pourrait pas y avoir de vie.
Si tout se régénérait, il n'y aurait pas de mort. »
- Richard Goss
Quelle est l'essence de l'inflammation? Ami ou ennemi? - ami ou ennemi? - comme l'écrivent des publications scientifiques internationales et des portails de vulgarisation scientifique dans leur désir de transmettre au lecteur la complexité des processus en cours du phénomène décrit.
L'objectif principal d'un processus tel que l'inflammation est d'informer le corps de tout dommage ou rupture. Et l'organisme "doit déjà prendre une décision et agir en conséquence". Le plus souvent, cette décision est prise par une coopérative de cellules immunitaires locales et systémiques, qui éliminent d'abord le facteur dommageable, puis rétablissent collectivement l'homéostasie du tissu affecté dans la mesure où elles réussissent.
Les événements prennent une telle tournure, par exemple, avec des dommages traumatiques aux tissus nerveux. Dans les premiers moments après un ensemble malheureux de circonstances ou l'action de laboratoire prévue chez les vertébrés, il y a une mort massive de cellules affectées par le traumatisme.
La première vague de mort cellulaire due à la nécrose et à l'apoptose (un suicide cellulaire programmé qui a subi des blessures incompatibles avec la vie) disparaît après quelques heures, après quoi une deuxième vague plus longue s'ensuit, probablement causée par l'action de produits de décomposition sur les tissus environnants. Dans ce cas, l'interaction du tissu nerveux et vasculaire peut être perturbée, ce qui entraîne des interruptions dans l'approvisionnement en énergie, en ions et en substances nécessaires.
L'activation de la microglie en réponse aux dommages se produit immédiatement. Les cellules microgliales, ces minuscules macrophages, effectuent directement la «réaction phagocytaire du corps contre des figures ennuyeuses», comme décrit par Mechnikov.
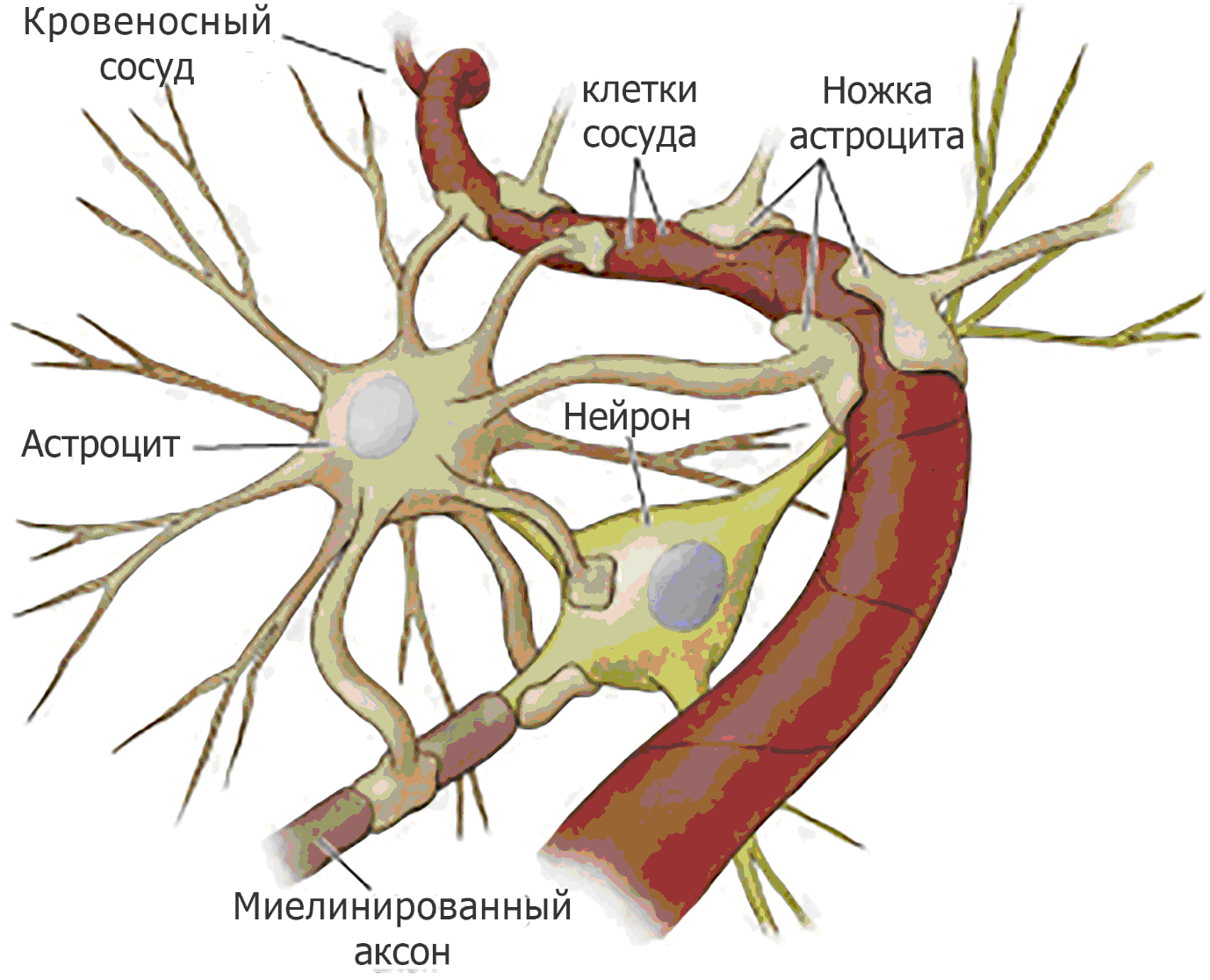 Représentation schématique d'un astrocyte et d'un neurone près d'un vaisseau sanguin
Représentation schématique d'un astrocyte et d'un neurone près d'un vaisseau sanguinIls sondent constamment la zone environnante à la recherche de substances pouvant indiquer des dommages aux neurones ou menacer leur intégrité. En l'absence de tels signaux de danger, l'activité des macrophages dans le tissu nerveux est supprimée par les peptides sécrétés par les neurones, qu'elle ne menace pas. Sinon - lorsqu'une blessure survient - la microglie est activée en quelques minutes! Cela se reflète dans leur forme et leur fonction. Les cellules deviennent plus mobiles, peuvent commencer à se diviser, afficher de nombreux récepteurs sur la membrane externe pour une évaluation plus précise de la situation. Lorsqu'elles sont activées, elles éjectent des protéines et des chimiokines complémentaires dans l'espace intercellulaire, qui attirent davantage de cellules immunitaires, des cytokines qui font réagir les voisins à la situation, des enzymes protéolytiques pour décomposer les protéines de la matrice extracellulaire, augmentant ainsi l'espace de manœuvre ainsi que les formes actives l'oxygène et l'azote afin de diffuser un signal de danger.
LienLes astrocytes ne sont pas loin derrière leurs homologues gliaux. Étant représentés par la classe la plus importante en nombre de cellules du système nerveux central, ils occupent une position stratégique entre les cellules endothéliales des vaisseaux sanguins et des neurones, régulant le travail de la barrière entre le sang et le cerveau. Après une blessure, ils répondent soit aux signaux de danger provenant des neurones, soit aux substances libérées par la microglie activée. Ensuite, les astrocytes augmentent de taille, hypertrophiant, libérant des peptides neurorégulateurs, par exemple, le BDNF (facteur neurotrophique dérivé du cerveau) ou le facteur neurotrophique cérébral, qui contribue à la survie des neurones endommagés. Ils produisent et sécrètent également des protéines fibrillaires qui restaurent la matrice extracellulaire et forment une cicatrice gliale. D'une part, c'est une bonne chose, car le site des dommages est isolé, d'autre part, dans cette zone, la régénération des neurones sera difficile.
 Migration des globules blancs vers le site de la blessure
Migration des globules blancs vers le site de la blessureLa microglie et les astrocytes jouent un rôle de premier plan dans les blessures traumatiques, cependant, ce scénario a une scène de foule étendue. Dans les plus brefs délais après les dommages, les leucocytes roulent littéralement dans le lieu d'action (c'est leur forme normale de mouvement le long de l'endothélium avec inflammation). De tout l'hôte de leucocytes, les neutrophiles sont les premiers à arriver, qui commencent à sécréter activement des cytokines pro-inflammatoires, des espèces réactives de l'oxygène et des peptides qui provoquent l'apoptose des cellules. Leur séjour sur le lieu de la blessure est temporaire, après 48 heures ils ne sont plus observés, néanmoins, leur apparition est l'un des premiers événements importants.
Derrière eux, les microglies sont activées, les lymphocytes T et B sont recrutés, qui répondent aux changements protéiques causés par les dommages. Aux premiers stades, les globules rouges et les plaquettes sont également parfois endommagés. Ils sont également très activement impliqués dans la régulation de la neuroinflammation, bien que cela ne se produise que lorsque la paroi vasculaire est endommagée. Ces cellules produisent un facteur d'activation plaquettaire, qui est impliqué dans la régulation de l'activation microgliale, et en plus de ce qui peut sembler inattendu, elles sont une source supplémentaire de sérotonine (elle est produite non seulement dans le système nerveux, mais aussi bien au-delà). Dans ce cas, la sérotonine aide à arrêter le flux sanguin des vaisseaux sanguins, la survie des neurones et la préservation de leur plasticité.
www.sciencedirect.com/science/article/pii/S0889159118305786?via%3DihubLes cellules nerveuses ne sont pas restaurées?
Comme Santiago Ramon-i-Cahal, le fondateur de la neurobiologie moderne, postulé au début du 20e siècle, les cellules nerveuses du corps d'un adulte ne sont pas restaurées. Vous devez avoir entendu cette déclaration plus d'une fois sous la forme de l'expression "les nerfs perdus ne sont pas restaurés". Cependant, dans les années 60 du siècle dernier, Joseph Altman a annoncé la découverte de la division des neurones dans les hippocampes de cobayes matures.
LienCette évidence de neurogenèse adulte n'a été prise au sérieux que dans les années 90 du siècle dernier. Les données accumulées sur la neurogenèse de diverses espèces, y compris les primates, ont conduit à un changement de paradigme.
LienLes chercheurs ont confirmé que la neurogenèse se produit réellement dans le cerveau de divers animaux adultes et ont finalement trouvé des traces de neurones nouvellement formés dans le cerveau d'un adulte. On estime que des centaines de ces cellules sont produites chaque jour dans l'hippocampe, où elles contribuent à façonner la mémoire et de nouvelles compétences. Ce concept est largement accepté par les scientifiques, et vous pouvez même trouver des régimes et des exercices spéciaux qui le renforcent soi-disant. On pouvait s'y attendre, vous pouvez même trouver TED parler de ce phénomène.
C'est juste le problème: un tel renouvellement des neurones ne l'est peut-être pas. Des études qui réfutent l'existence de la neurogenèse adulte continuent d'apparaître jusqu'à aujourd'hui. La dernière grande étude de ce type a été publiée le 15 mars de cette année dans la revue Nature. Dans ce document, des scientifiques du California Institute de San Francisco concluent qu'ils n'ont pas pu détecter au moins quelques traces dans plusieurs dizaines d'hippocampes obtenus à partir du cerveau d'adultes qui ont légué leur corps à la science. Selon les chercheurs, ils n'ont trouvé aucun signe, même dans les spécimens les mieux conservés.
LienComme d'habitude, il est très difficile de prouver que quelque chose manque réellement, et de nombreux scientifiques sont sceptiques quant aux résultats des travaux. Beaucoup indiquent que le comptage a été effectué indirectement - par la présence de protéines qui sont généralement produites par de jeunes cellules récemment divisées. Ces protéines pourraient facilement se dégrader peu de temps après la mort du corps.
Il est très probable que le débat se poursuive, et le dernier mot dans cette affaire ne sera prononcé que lorsque des méthodes d'observation des neurones dans le cerveau des êtres vivants seront développées.
Dans le cerveau d'un poisson zèbre, les neurones de la paroi ventriculaire latérale peuvent se diviser, puis se déplacer vers la zone affectée, formant de jeunes neurones pour remplacer les morts. Les cellules correspondantes des souris les plus proches de nous ne sont plus capables d'un tel foyer, bien que placées in vitro, la capacité soit restaurée. On pense que c'est le microenvironnement au site de la blessure chez ces animaux très développés qui empêche le développement de nouveaux neurones.
LienEn cas de lésion tissulaire, le microenvironnement se forme en raison des produits de dégradation des protéines et autres macromolécules dont il est composé, ainsi que des substances sécrétées par les cellules environnantes. Les actions spécifiques des cellules gliales et leur rôle dans la restauration dépendent fortement de la nature de la blessure. Avec une activation excessive et constante de la microglie, les substances sécrétées par elle à des concentrations élevées deviennent toxiques pour les cellules environnantes, les cytokines produites perturbent le travail des neurones; les protéines fibrillaires sécrétées par les astrocytes inhibent la formation de liaisons fonctionnelles.
Une quantité élevée d'interleukine 1, l'un des principaux médiateurs de l'inflammation, en particulier sa forme bêta, ainsi que le facteur de nécrose tumorale, les interleukines 6 et 10 produites dans le système nerveux central lorsqu'elles sont endommagées, peuvent entraîner des maux de tête et des migraines.
Il ne faut pas oublier que ces cytokines pro-inflammatoires sont nécessaires à la restauration des tissus affectés, bien qu'elles puissent à leur tour provoquer la mort cellulaire et provoquer des lésions tissulaires secondaires. Par exemple, le facteur alpha de nécrose tumorale est toxique pour les neurones aux stades initiaux de l'inflammation, mais il favorise la régénération aux stades ultérieurs.
Neuroinflammation dans la maladie d'Alzheimer
Comme il résulte évidemment de la définition donnée ci-dessus, la neuroinflammation est un compagnon fréquent des maladies neurodégénératives. Ces maladies se caractérisent par une perte de structure, de fonction et de nombre de neurones.
La maladie, décrite pour la première fois par le psychiatre allemand Alois Alzheimer, affecte généralement les personnes de plus de 65 ans, bien que d'autres formes soient parfois trouvées. Avec le développement de la maladie, les patients perdent la capacité de se souvenir des informations et, dans le cas extrême, ils perdent leur mémoire à long terme, la capacité de parler, de naviguer et de prendre soin d'eux-mêmes. La cause de nombreuses déficiences cognitives dans cette pathologie est la dégénérescence des neurones et des synapses, conduisant à une atrophie du cortex cérébral.
La microglie en tant que l'un des principaux participants à la neuroinflammation devient active après exposition à l'un des nombreux stimuli, à savoir l'hypoxie, les traumatismes, les accidents vasculaires cérébraux et des facteurs tels que les virus, les bactéries et les toxines. Les cellules sont également activées lorsque des plaques amyloïdes et des amas de protéines tau apparaissent. Ces deux facteurs - les enchevêtrements neurofibrillaires de la protéine tau et la neuroinflammation - sont des signes clés de la maladie d'Alzheimer.
LienLa microglie activée est observée en excès dans le cerveau du patient lorsqu'elle est examinée par un pathologiste post-mortem. Apparemment, en présence de cytokines pro-inflammatoires, les macrophages du cerveau perdent la capacité de phagocyter les accumulations extracellulaires de bêta-amyloïde, un groupe de peptides qui forment une plaque caractéristique. De plus, une concentration accrue de cytokines, telles que l'interleukine 1 bêta, empêche la formation de synapses, ce qui explique leur perte dans le processus pathologique.
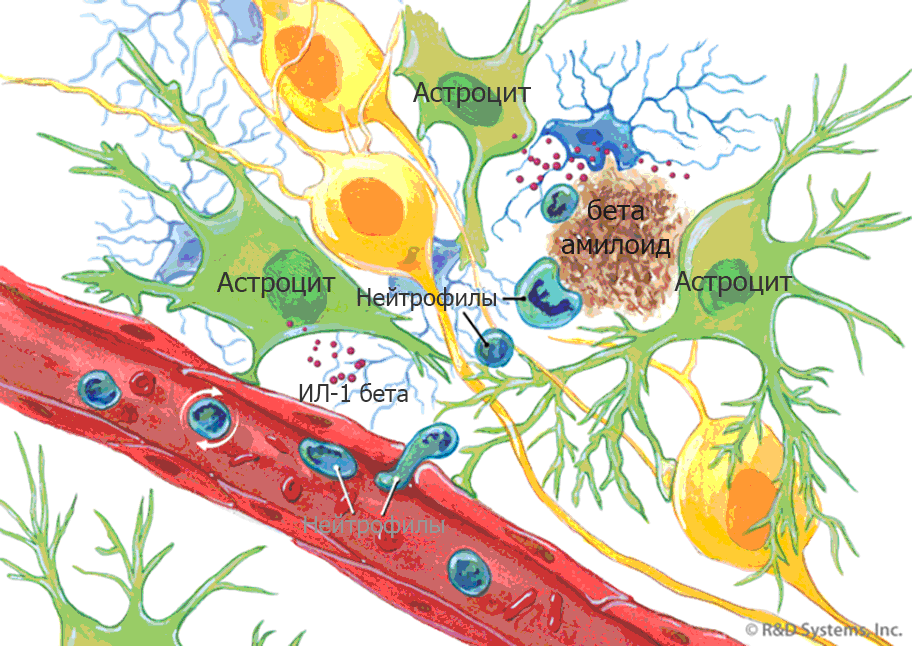 Neuroinflammation dans la maladie d'Alzheimer
Neuroinflammation dans la maladie d'AlzheimerCompte tenu des énormes dommages causés au cerveau par l'inflammation chronique, il a été suggéré que les substances qui suppriment l'inflammation peuvent traiter la maladie ou au moins réduire la probabilité de son développement. Il existe des preuves que les anti-inflammatoires non stéroïdiens (AINS), tels que l'ibuprofène, peuvent réduire l'inflammation causée par les plaques amyloïdes, mais les essais cliniques n'ont pas été achevés en raison du risque élevé d'effets secondaires. Les AINS ne sont actuellement pas considérés comme utiles dans le traitement de la maladie d'Alzheimer, et aucun des essais cliniques visant à prouver la capacité des AINS à prévenir ou à réduire le risque de développer la maladie n'est achevé.
Des études récentes ont généralement mis en doute les avantages de la prise quotidienne de faibles doses d'aspirine et potentiellement d'autres AINS. Une étude publiée dans l'une des revues médicales les plus influentes de Lancet, où les médecins et les scientifiques ont suivi plus de 12000 patients présentant un risque modéré de développer une maladie cardiaque, n'a confirmé aucun avantage de la prise de ce médicament.
LienNeuroinflammation de la maladie de Parkinson
Mais quant aux autres maladies neurodégénératives?
Dans la maladie de Parkinson, caractérisée par la mort massive de neurones des noyaux gris centraux sécrétant de la dopamine, la neuroinflammation est presque la principale composante de la maladie.Les personnes atteintes de la maladie de Parkinson perdent le contrôle de leurs mouvements, leurs mains commencent à trembler, leur écriture empire. Les patients commencent à marcher plus lentement, ils ont du mal à marcher. Ce sont toutes des manifestations précoces de la maladie. Au fil du temps, la pensée abstraite et le contrôle de l'attention se détériorent et des hallucinations apparaissent. Près de 50% des personnes diagnostiquées en sont atteintes.post mortem , 1, 2, 6, , . . , .
Cependant, malgré les grands succès dans l'étude de la pathologie présentée, les chercheurs ont du mal à dire avec certitude si la neuroinflammation est la cause ou la conséquence de la maladie. Une chose est sûre: dès que l'inflammation est impliquée dans le jeu, elle devient un acteur clé. Ceci est confirmé par des études épidémiologiques. Contrairement à la maladie d'Alzheimer, les AINS, à l'exception de l'aspirine, peuvent réduire le risque de développer la maladie de Parkinson selon une méta-analyse réalisée en 2010.LienUne caractéristique de nombreuses maladies neurodégénératives est que le risque de développement augmente avec l'âge. De cela, on peut supposer que la neuroinflammation et le vieillissement sont également en quelque sorte liés.Neuroinflammation dans le vieillissement
Les cellules cérébrales vivent et meurent, c'est un cycle de vie normal. Les neurones sont progressivement remplacés par des astrocytes et les cytokines éjectées lors de leur mort contrôlent l'inflammation et la récupération. Ainsi, à tout moment sélectionné, un certain niveau de cytokines pro-inflammatoires est présent dans le cerveau. Cependant, avec l'âge, les marqueurs de l'inflammation de la glie deviennent plus grands et contribuent en outre à une réponse immunitaire excessive lors de la stimulation. La microglie devient hyperactive.Avec le vieillissement, il existe également des troubles des fonctions cognitives - mémoire, parole, pensée abstraite - bien que dans une moindre mesure qu'avec les maladies neurodégénératives. En général, le vieillissement peut être considéré comme un risque majeur de déficience cognitive légère.Les personnes âgées présentent souvent des signes de déficience cognitive pendant ou après une infection ou un stress. Ces observations sont confirmées dans des expériences de laboratoire sur des souris, dont les troubles cognitifs peuvent être causés par l'administration de lipopolysaccharide (un composant de la paroi bactérienne sur lequel se développe la réponse immunitaire), mais qui peuvent être atténués en utilisant du resvératrol, un puissant agent anti-inflammatoire.LienVieillissement d'hippocampe
Toute description du vieillissement du SNC commence invariablement par l'hippocampe, la zone du cerveau responsable de la formation des souvenirs. Il est affecté à la fois dans le vieillissement normal et dans la maladie d'Alzheimer. En plus de la mémoire, l'hippocampe intrigue les chercheurs avec les effets du stress. Étant donné que l'hippocampe est un élément de rétroaction important responsable de l'arrêt de la production de glucocorticoïdes, l'effet du stress chronique sur son vieillissement est étroitement surveillé.Dans les premières études sur le vieillissement hippocampique, il a été montré que chez les personnes âgées, il y a une perte significative du nombre de neurones. Cependant, dans des études ultérieures utilisant des techniques précises, les physiologistes ont trouvé des différences minimes entre le nombre de neurones dans les hippocampes des jeunes et des personnes âgées.Une situation très similaire s'est développée avec le volume de l'hippocampe, mesuré par imagerie par résonance magnétique. On sait de manière fiable que plus le volume de l'hippocampe est petit, pire sera la mémoire d'une personne âgée. Heureusement, des études montrent que l'entraînement aérobie modéré aide à maintenir le volume de l'hippocampe. Les effets du cortisol sur des parties du cerveau soumises au stressÉtant donné que les neurones hippocampiques possèdent une quantité importante de récepteurs des glucocorticoïdes, ils sont vulnérables à un stress prolongé. Chez les personnes qui souffrent d'un stress traumatique sévère et à long terme, l'hippocampe s'atrophie plus rapidement que le reste du cerveau.Des effets similaires sont observés dans le trouble de stress post-traumatique, la schizophrénie et la dépression. Fait intéressant, l'atrophie dans la dépression peut être ralentie en prenant des antidépresseurs même s'ils ne permettent pas de faire face à d'autres symptômes.
Les effets du cortisol sur des parties du cerveau soumises au stressÉtant donné que les neurones hippocampiques possèdent une quantité importante de récepteurs des glucocorticoïdes, ils sont vulnérables à un stress prolongé. Chez les personnes qui souffrent d'un stress traumatique sévère et à long terme, l'hippocampe s'atrophie plus rapidement que le reste du cerveau.Des effets similaires sont observés dans le trouble de stress post-traumatique, la schizophrénie et la dépression. Fait intéressant, l'atrophie dans la dépression peut être ralentie en prenant des antidépresseurs même s'ils ne permettent pas de faire face à d'autres symptômes.Neuroinflammation dans les troubles mentaux
. ; . . , , , , . 10 . 1 , , , . , , .
La perturbation du sommeil décrite dans des conditions expérimentales provoque l'activation des mêmes récepteurs d'immunité innée que le stress social.LienDu fait que la neuroinflammation peut jouer un rôle clé dans les maladies psychiatriques - dépression, schizophrénie, trouble bipolaire - ce phénomène devient extrêmement curieux, car les résultats de ces expériences suggèrent que ces maladies peuvent être prévenues bien avant d'être corrigées par le mode de vie , régime alimentaire et habitudes de sommeil.LienVieillissement de l'hypothalamus
Contrairement à l'hippocampe, dont les changements expliquent la survenue de troubles cognitifs avec l'âge, l'hypothalamus contrôle éventuellement le vieillissement.Cette structure dans le cerveau, semblable à l'amygdale, est un pont entre les systèmes nerveux et endocrinien du corps humain. Il aide à réguler le comportement et de nombreux besoins fondamentaux, tels que la faim, le sommeil, la peur et l'agression. En conséquence, avec l'âge, l'homéostasie des cellules nerveuses sécrétantes qui composent l'hypothalamus est perturbée et les manifestations associées au vieillissement se manifestent.Les premières recherches dans ce sens ont concerné la mise en place de chaînes de rétroaction de différentes hormones, souvent sexuelles. Cependant, les perturbations de la rétroaction et l'émergence d'une résistance aux œstrogènes, à l'insuline, à l'hormone de croissance et à d'autres molécules régulatrices sont une conséquence et non une cause. Les mécanismes cellulaires et moléculaires qui expliquent la perte de l'homéostasie ne sont toujours pas bien compris.Au cours des dernières années, plusieurs voies moléculaires et gènes ont été examinés qui sont associés à l'apparition et à la progression de processus dégénératifs liés à l'âge. Parmi eux étaient désormais très populaires parmi les chercheurs sirtuines, SIRT, protéine cible de rapamycine de mammifère, mTOR, facteur de transcription NF-kB et autres.mTOR est une enzyme appartenant à la famille des protéines kinases, qui est la cible de la rapamycine, un médicament anticancéreux. À la suite d'études sur les tremblements, les vers, les mouches et certains mammifères, il a été démontré que la rapamycine est capable de prolonger la vie de ces organismes modèles. MTOR a donc acquis une réputation de déterminant central, évolutif et conservateur de l'espérance de vie.mTOR est très sensible à l'insuline et aux facteurs de croissance; il contrôle le métabolisme de la cellule, sa croissance et sa survie. Cependant, avec une stimulation chronique élevée, un travail excessif de mTOR entraîne un stress oxydatif, une accumulation de dommages et un vieillissement de la cellule - tous signes de la réponse inflammatoire de la cellule.L'activation du facteur de transcription NF-kB contribue au développement ultérieur de la réponse inflammatoire, car elle contrôle les gènes responsables de son maintien. Des travaux scientifiques récents ont montré qu'un excès constant de calories dans les aliments peut contribuer au développement de réponses inflammatoires dans l'hypothalamus.Excès de neuroinflammation
« ». – , , : , , . , NF-kB. , 1 .
NF-kB , , , , .
Au fil du temps, cela affaiblit l'homéostasie hypothalamique. Cette dérégulation est associée au vieillissement systémique et au développement de pathologies liées à l'âge - diabète, obésité, maladies cardiovasculaires, démence et dysfonctionnement reproductif.www.ncbi.nlm.nih.gov/pmc/articles/PMC2586330www.ncbi.nlm.nih.gov/pmc/articles/PMC3756938www.ncbi.nlm.nih.gov/pubmed/23636330www.ncbi.nlm.nih .gov / pmc / articles / PMC4313775Cellules souches et neuroinflammation
En 2013, des chercheurs de l'Albert Einstein College of Medicine ont découvert des cellules souches de l'hypothalamus, qui à leur avis sont également capables de contrôler le vieillissement de l'organisme. Ils rapportent que le nombre de cellules souches hypothalamiques diminue avec le temps chez les souris qui ont fait l'objet de l'étude. À deux ans - l'âge des souris âgées - la plupart de ces cellules ne sont plus présentes.Les expérimentateurs ont transplanté des cellules souches à des souris normales, ainsi qu'à des souris auxquelles elles avaient précédemment détruit les cellules souches hypothalamiques. Les deux groupes ont montré des signes de retard de vieillissement. Il s'est avéré que des miARN spécifiques étaient l'effecteur clé de ce phénomène. Ce groupe de molécules diffère des ARN ordinaires en ce qu'ils ne participent pas au processus de synthèse des protéines, mais participent plutôt à la régulation de l'expression d'autres gènes dans les cellules. Une cellule peut sécréter des microARN dans des conteneurs spéciaux - des exosomes., . : – , , .
, , miR-107, miR-155 miR-223, , .
Les études sur les microARN ne sont encore qu'au début du voyage, et des idées sur la façon dont elles peuvent être utilisées pour augmenter l'espérance de vie en bonne santé pourraient nous attendre dans un proche avenir.Conclusion
Comme vous pouvez le voir maintenant, la neuroinflammation est un processus extrêmement complexe. Avec elle, il n'y a pas de manifestations classiques de l'inflammation décrites par Celsus, à savoir une rougeur, un gonflement par la chaleur et la douleur. Cependant, dans la neuroinflammation, les mécanismes moléculaires et cellulaires sont partiellement les mêmes que dans l'inflammation. Dans les deux cas, des molécules de signalisation ou des cytokines, telles que les interleukines, les chimiokines et le facteur de nécrose tumorale, sont impliquées. L'un et l'autre processus ont des côtés positifs et négatifs.
La clé de ces processus est la tentative du corps de réparer les tissus endommagés de la manière dont il dispose. Il y a des différences. Les macrophages résidents dans le tissu cérébral sont des cellules microgliales. Ils ne se trouvent pas dans d'autres tissus du corps. Au lieu de la cicatrice habituelle, le tissu nerveux se forme glial en raison de l'activation des astrocytes.
Il n'est pas surprenant que l'inflammation dans le tissu nerveux, en particulier le système nerveux central, ait des conséquences profondes. La neuroinflammation est impliquée dans le vieillissement, les pathologies liées à l'âge, l'obésité et certains types de démence.
Malgré le fait que la santé dépend en grande partie de la génétique, notre comportement détermine également en partie comment nous vivons et vieillissons. Une activité physique modérée et, encore une fois, une alimentation modérée, saine et variée, un sommeil sain peuvent réduire la neuroinflammation, ainsi que prolonger la santé du cerveau et du corps. Il est également nécessaire de demander l'aide des médecins à temps, même s'il s'agit d'une «sorte de dépression» et qu'elle passera d'elle-même. Et aussi ne vous impliquez pas dans l'automédication et la bonne aventure par pubmed, qui est venu dans notre société pour remplacer le diagnostic de Google.
www.ncbi.nlm.nih.gov/pmc/articles/PMC4588685www.ncbi.nlm.nih.gov/pubmed/25527485Auteur Vasily Tsvetkov