Au cours des dernières décennies, la science a fait des progrès importants dans le traitement du cancer, et bien que nous soyons encore loin de vaincre complètement cette terrible maladie, les médecins ont de plus en plus d'outils pour détruire les tumeurs ou limiter leur croissance. L'essentiel est qu'ils donnent aux patients atteints de cancer la possibilité de vivre plus longtemps.
L’un de ces outils est l’activation de l’immunité d’une personne pour lutter contre les cellules cancéreuses. Il y a tout un domaine dédié à cela - l'immuno-oncologie. Une grande attention y est portée, c'est dans ce domaine que se font le plus de recherches aujourd'hui et que les médicaments les plus prometteurs se développent.
Chez
Medicine 24/7, nous utilisons activement l'immunothérapie - et nous voyons qu'elle donne de bons résultats. Certes, nous sommes confrontés au fait que de nombreux patients ne connaissent pas du tout cette méthode de traitement ou la considèrent comme encore insuffisamment étudiée et non fiable.
Dans cette publication, nous essaierons de clarifier les questions: qu'est-ce que l'immunothérapie, comment ça marche et qui peut aider.
 Judy Perkins. Elle avait un cancer du sein en phase terminale qui était complètement guéri avec la dernière méthode d'immunothérapie.Menace cachée. Comment fonctionne le cancer
Judy Perkins. Elle avait un cancer du sein en phase terminale qui était complètement guéri avec la dernière méthode d'immunothérapie.Menace cachée. Comment fonctionne le cancerLes cellules cancéreuses sont des rebelles mutants qui ont réussi à déjouer le système.
Au cours de la vie, toutes les cellules du corps passent par des stades de développement strictement définis, remplissent des fonctions spécifiées, se multiplient selon des règles strictes et finissent par vieillir et mourir. C'est un processus naturel. La mort programmée de vieilles cellules qui ont accumulé beaucoup de dégâts est appelée apoptose.
Cependant, sous l'influence de l'hérédité ou de facteurs externes défavorables, certaines cellules accumulent des erreurs génétiques et se «rebellent»: elles refusent de vivre selon l'algorithme fixé par la nature, commencent à se multiplier de façon incontrôlable ou ne meurent pas à temps. Ce n'est pas rare. Potentiellement, des cellules cancéreuses peuvent apparaître périodiquement dans chacune - c'est normal. Presque toujours, ces «parvenus» sont tués par le service de sécurité intérieure du corps - l'
immunité .
L'un des rôles principaux dans ce processus est joué par les lymphocytes T ou, plus simplement,
les cellules T. Ils répondent à un
antigène (une substance étrangère au corps), reconnaissent et détruisent les ennemis potentiels: par exemple, les microbes ou le matériel donneur inapproprié. Normalement, les lymphocytes T tuent également les cellules du corps, qui ont commencé à muter et à ne pas se comporter conformément aux règles. Par conséquent, le cancer ne survient pas chez tout le monde - dans la majorité, l'immunité résout les troubles avant de se propager.
Mais le cancer cherche à survivre et les cellules tumorales tentent de capturer autant de ressources que possible, pour devenir "plus performantes". Ils se multiplient plus rapidement, sécrètent un facteur de croissance vasculaire (pour attirer plus de sang et de nutriments vers la tumeur), développent une résistance aux médicaments, forcent les cellules souches à augmenter la croissance des tissus tumoraux (envoi de signaux trompeurs avec une demande de régénération).
Les cellules cancéreuses obtiennent un succès déguisé particulier: certaines d'entre elles éliminent de leur surface des protéines antigéniques spéciales grâce auxquelles les cellules T peuvent les reconnaître. D'autres sécrètent des molécules spéciales qui suppriment l'immunité, et certains forment même des hybrides avec des macrophages (l'un des types de cellules immunitaires) - et acquièrent littéralement des superpuissances!
D'une part, la parenté avec les cellules normales du corps les aide à cela - une sorte de déguisement congénital. D'un autre côté, la variabilité génétique des cellules cancéreuses leur confère une adaptabilité accrue. Plus il y a de mutations accumulées dans l'ADN de la cellule au moment de sa malignité (conversion en malignité), plus elle a de chances de survivre à la réponse immunitaire et d'élaborer un plan de capture réussi.
Éveil du pouvoir. Histoire des découvertes NobelL'immunité humaine est en fait une véritable armée de tueurs impitoyables, et après chaque «opération de combat» pour neutraliser un autre ennemi, ils doivent être rassurés et transférés d'une position militaire à une position pacifique. Ce mécanisme réduit la température à des valeurs normales et arrête l'inflammation lorsque le danger est passé et que l'infection a été vaincue.
En 2018, le prix Nobel de physiologie ou médecine a été décerné à l'américain James Ellison et au japonais Tasuk Honjo pour leurs découvertes indépendantes dans le même domaine: comment se produit exactement ce passage du mode agressif au mode silencieux.
Aucun des scientifiques n'a d'abord pensé au traitement du cancer. Tous deux voulaient une compréhension plus claire du fonctionnement de la réponse immunitaire. À ce moment-là, il était clair qu'à la surface des cellules T et à la surface des cellules présentatrices d'antigène (
APC ), il y avait des molécules réceptrices qui agissaient les unes sur les autres, provoquant ou ralentissant le système immunitaire.
TCR a été découvert
- un récepteur des cellules T par lequel les cellules T reconnaissent les protéines "ennemies" exposées à APC.
Nous avons trouvé le principal complexe d'histocompatibilité MHC (complexe majeur d'histocompatibilité), à l'aide duquel les CPA présentent des morceaux de protéines étrangères pour l'identification des lymphocytes T. Peter Doherty et Rolf Zinkernagel ont reçu leur prix Nobel pour avoir découvert ce scénario.
Les scientifiques ont compris que les récepteurs à la surface des cellules T fonctionnent en conjonction avec des co-stimulateurs à la surface de l'APC. La protéine
CD28 de la surface des cellules T a été isolée en
1980 , bientôt la molécule B7 a été trouvée à la surface de l'APC. Au cours des expériences, les chercheurs du groupe Ellison ont transféré le gène
B7 aux cellules cancéreuses et ils ont commencé à être rejetés par les tissus sains. Il s'est avéré que B7 se lie au CD28 sur la cellule T, et commence ainsi son travail: la cellule T détruit la cellule tumorale, à la surface de laquelle la protéine B7 "ressort".
En
1987 , Ellison a découvert l'
antigène-4 des lymphocytes T cytotoxiques
CTLA-4 (antigène-4 associé aux lymphocytes T cytotoxiques) - et a constaté que la structure de cette protéine est similaire au CD28 connu depuis longtemps, et est également capable de se lier à B7 - cependant, avec cela fonctionne exactement à l'opposé: il arrête la réponse immunitaire.
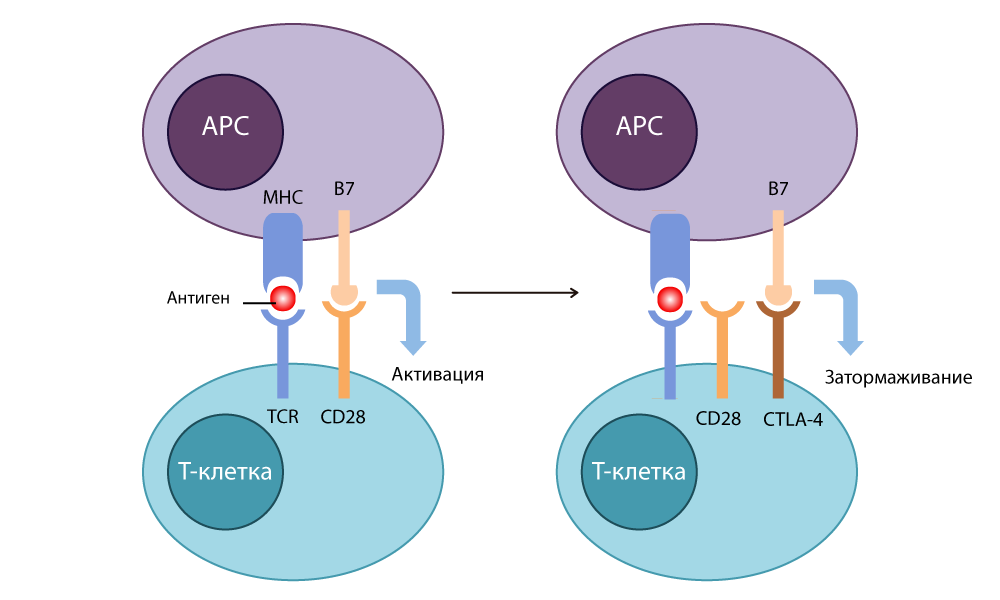 Action CTLA-4
Action CTLA-4Tout d'abord, les médecins allaient utiliser ce «frein» pour lutter contre les maladies auto-immunes (lorsque l'immunité commence à attaquer les cellules saines du corps). Mais Allison a trouvé une chose brillante: n'appuyez pas sur le frein, mais coupez-le.
Il a développé un anticorps inhibiteur (interrupteur) qui se lie à CTLA-4 et l'empêche de se fermer avec B7 pour arrêter les réponses immunitaires. Des molécules B7 libres liées à CD28, la cellule T activée et était prête à tuer à nouveau. Quand il a mené des expériences sur des souris cancéreuses en 1995, il est devenu clair que même les cellules cancéreuses rusées ne pouvaient pas se cacher de ces lymphocytes T avec les freins désactivés. En 2010, des études réussies ont été menées sur des patients désespérés. Chez certains patients, le mélanome a disparu avec les métastases - un résultat incroyable!
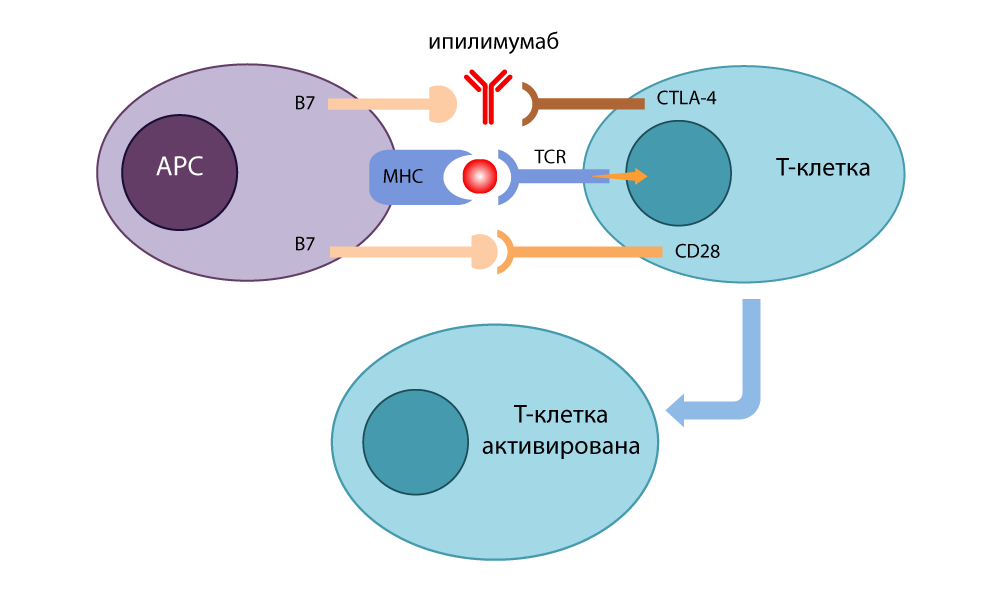 L'action de l'inhibiteur de CTLA-4 - ipilimumab
L'action de l'inhibiteur de CTLA-4 - ipilimumabDans le même temps, à Kyoto,
Tasuku Honjo a trouvé une autre molécule réceptrice à la surface du lymphocyte T:
PD-1 (Programmed cell Death protein-1 , Programmable Cellular Death Protein-1). Au cours des expériences (toujours sur des souris souffrant longtemps), les Japonais ont découvert que la désactivation du gène codant pour cette protéine provoque des symptômes de maladie auto-immune chez la souris - c'est-à-dire que l'inhibition de PD-1 a également désactivé les «freins» des lymphocytes T et les a rendus agressifs et actifs.
Honjo a découvert que PD-1 met la cellule T en mode veille lorsqu'elle se lie à la protéine PD-L1 / PD-L2 à la surface d'une cellule présentatrice d'antigène (APC). L'inhibiteur PD-1 a ouvert ce lien et a de nouveau activé les cellules T. L'action de ce «frein» était similaire à l'action de CTLA-4, mais elle a pris une voie différente.
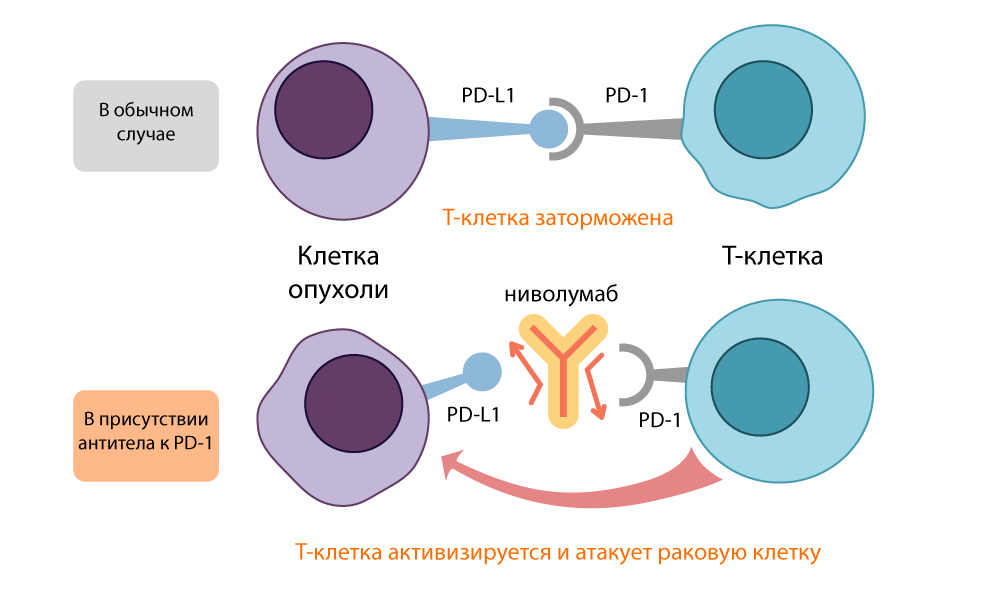 L'action de l'inhibiteur PD-L1 - nivolumab
L'action de l'inhibiteur PD-L1 - nivolumabLes deux molécules "inhibitrices" ouvertes, CTLA-4 et PD-1, ont été appelées
points de contrôle immunitaire (
points de contrôle) - c'est leur nombre et leur activité qui font que les lymphocytes T prennent une décision: se calmer ou commencer à se battre.
Il s'est avéré que les bloqueurs de CTLA-4 activent l'immunité en général, toutes les cellules T, et l'inhibiteur PD-1 agit plus spécifiquement sur les tumeurs, car de nombreuses cellules cancéreuses portent la «deuxième pièce du puzzle», la molécule PD-L1 / PD-L2. Pour cette raison, le traitement avec des inhibiteurs de PD-1 réduit le risque de complications.
L'immunité contre-attaque. Qu'est-ce que les inhibiteurs de point de contrôle aidentAllison et Honjo ont non seulement apporté une contribution sérieuse à la compréhension des processus physiologiques, mais ont également lancé une vague de recherches pratiques fondamentalement nouvelles en médecine appliquée.
La découverte de l'inhibition des points de contrôle immunitaire (TIC) ouvre un domaine fondamentalement nouveau pour trouver des solutions. Auparavant, les méthodes de lutte contre le cancer: chirurgie, radiothérapie et chimiothérapie - visaient directement la tumeur elle-même, la destruction des cellules cancéreuses. Les médecins ont désormais un immense champ de recherche dans une direction complètement différente: changer l'interaction des cellules cancéreuses avec leur environnement.
Soit dit en passant, c'est cette différence fondamentale qui a donné aux médecins une véritable percée. Jusqu'à présent, la tumeur a été affectée en fonction de sa localisation. Pour le cancer du sein, un médicament, pour le cancer de l'estomac, est complètement différent. Et l'inhibiteur des TIC pembrolizumab en 2017 a été enregistré pour la première fois dans l'histoire de l'oncologie en tant que médicament pour le traitement de tout cancer dans n'importe quel organe - si seulement les tests confirment que la tumeur a une propriété particulière: l'instabilité des microsatellites. Autrement dit, son ADN est particulièrement sujet aux mutations. Auparavant, il n'a jamais été possible de guérir le cancer d'un symptôme courant. C'est une grande réussite.
La révolution a été le résultat de l'utilisation de nouveaux médicaments contre les types de cancer les plus agressifs: le mélanome métastatique au stade IV était considéré comme incurable. Et les patients avec un tel diagnostic qui ont subi le traitement par le médicament ipilimumab (bloqueur de CTLA-4) en 2010 - ont reçu une année de vie supplémentaire - donc le développement de la tumeur s'est arrêté. Dans 58% d'entre eux, la tumeur a diminué d'un tiers.
Dans le traitement du cancer du poumon non à petites cellules avec nivolumab (inhibiteur de PD-1), le risque de décès des patients a diminué de 40%.
Le pembrolizumab (également un inhibiteur de PD-1) a montré une diminution de 43% de la croissance tumorale dans le groupe traité pour le mélanome. 74% des patients ont vécu sans détérioration au cours de l'année, contre 18% pendant 18 mois. Il est important que l'effet de la prescription du médicament l'emporte sur les effets secondaires à tous les stades du développement de la maladie.
Aujourd'hui, les inhibiteurs de CTLA-4 et PD-1 traitent le mélanome (y compris inopérable), le cancer du poumon non à petites cellules, le carcinome épidermoïde de la tête et du cou, le carcinome à cellules rénales, certains types de lymphomes, le cancer du rectum, de la vessie et des tumeurs avec instabilité des microsatellites.
Les études qui montrent l’efficacité d’
une thérapie combinée avec des médicaments anti-PD-1 et anti-CTLA-4 sont particulièrement intéressantes.
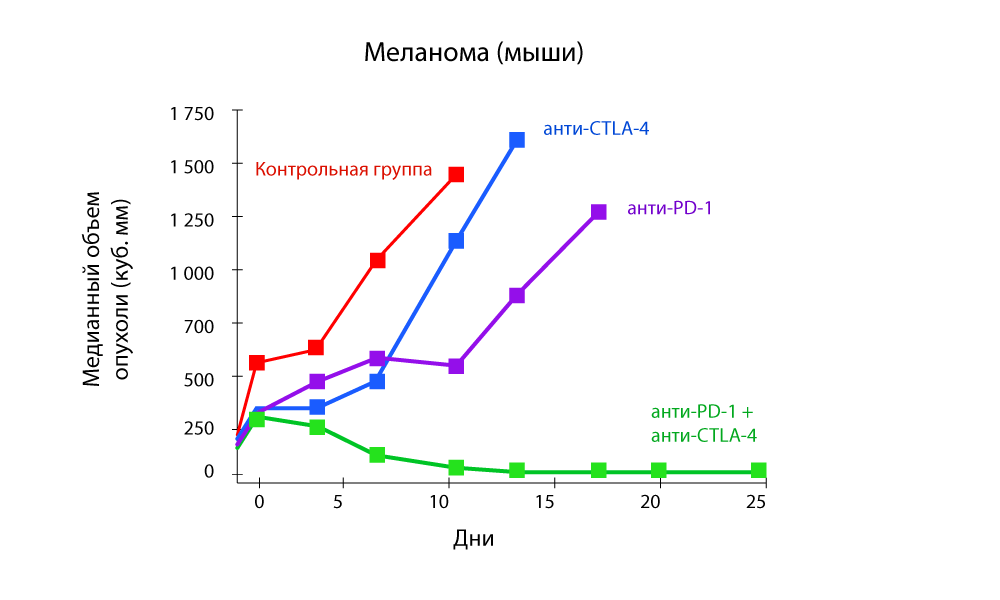 Changement du volume tumoral - une forte diminution avec la combinaison de médicaments anti-PD-1 et anti-CTLA-4
Changement du volume tumoral - une forte diminution avec la combinaison de médicaments anti-PD-1 et anti-CTLA-4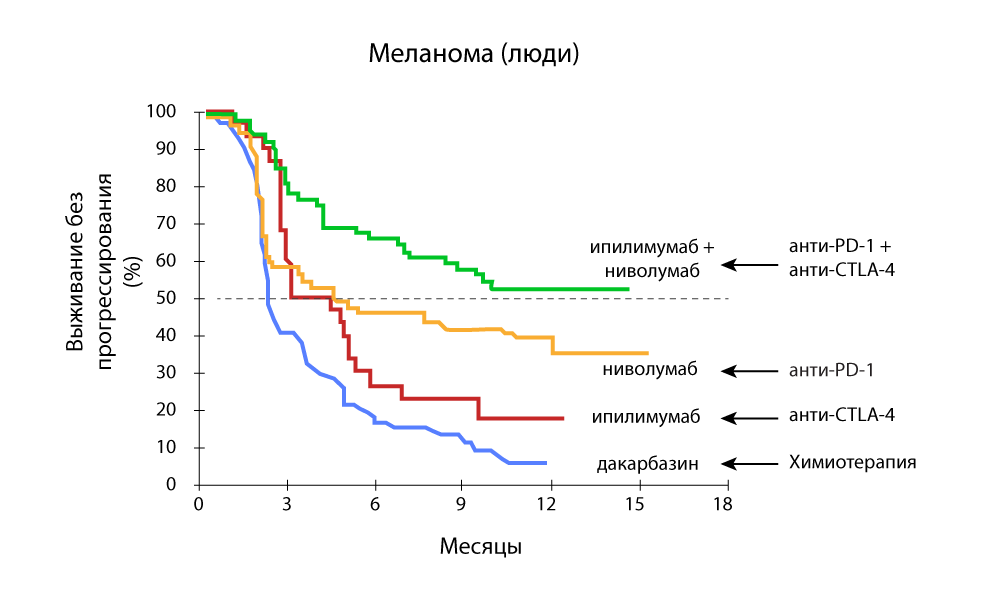 Survie sans progression - la combinaison de médicaments anti-PD-1 et anti-CTLA-4 est plus efficace
Survie sans progression - la combinaison de médicaments anti-PD-1 et anti-CTLA-4 est plus efficaceChez Medicine 24/7, nous utilisons avec succès le pembrolizumab et le nivolumab depuis leur enregistrement en Fédération de Russie. Nous avons suivi toutes les recherches étrangères et nous nous réjouissions de reconstituer l'arsenal.
Attaque des clones. Immunité génétiquement modifiéeLes inhibiteurs des points de contrôle immunitaire sont à juste titre à l'honneur, mais ce mécanisme n'est toujours pas parfait et ne peut guérir aucun cancer. Il est bon que les domaines de recherche liés à l'immunothérapie se développent activement. L'une des plus prometteuses est la
thérapie CAR-T .
La lettre T au nom de la méthode est tout de même des cellules T immuables de notre immunité. CAR (Chimeric antigen receptor) est un récepteur chimérique d'antigène. Pourquoi le récepteur est-il appelé chimérique? Parce qu'il est assemblé à partir de plusieurs pièces provenant de différentes cellules - en utilisant les compétences des ingénieurs génétiques.
Les cellules T ordinaires ont un récepteur
TCR spécifique
( récepteur
des cellules T) . Il "sent" toutes les cellules du corps sur son chemin et, s'il détecte une molécule étrangère à la surface de la cellule, envoie un signal d'activation à la cellule T. Cela, à son tour, traite soit de l'extraterrestre indésirable lui-même, soit libère des substances actives spéciales (cytokines) et appelle les autres cellules immunitaires à «les régler». Tuez les cellules T très efficacement.
C'est vrai, pas très précis. Nous avons beaucoup moins d'espèces TCR qu'il n'y a d'antigènes. Par conséquent, les cellules T peuvent reconnaître de nombreux antigènes par leur TCR, mais seulement approximativement. Les cellules cancéreuses exploitent souvent cette faiblesse de notre système de sécurité et prétendent être «la leur».
L'évolution a résolu le problème du mieux qu'elle pouvait: dans le corps humain, il existe un autre mécanisme d'identification des étrangers: les
anticorps . Ce sont des protéines spéciales qui sont sécrétées par une autre classe de cellules immunitaires: les lymphocytes B. Les cellules B, contrairement aux cellules T, ont une approche individuelle de chaque «client».
L'anticorps est une structure protéique sous la forme de la lettre Y. Aux deux extrémités de cette «fourchette», il existe des sites qui se lient à l'antigène. Ces sections peuvent changer dans chaque prochaine génération d'anticorps pour s'adapter plus étroitement à l'antigène - comme la sélection de pièces de puzzle. Lorsqu'un antigène étranger est détecté, les lymphocytes B sécrètent des milliards d'anticorps, parmi lesquels une sélection est effectuée pour la correspondance la plus exacte avec l'antigène. Le résultat est un anticorps de référence, «entraîné» spécifiquement pour la reconnaissance très précise d'un antigène «étranger» spécifique.
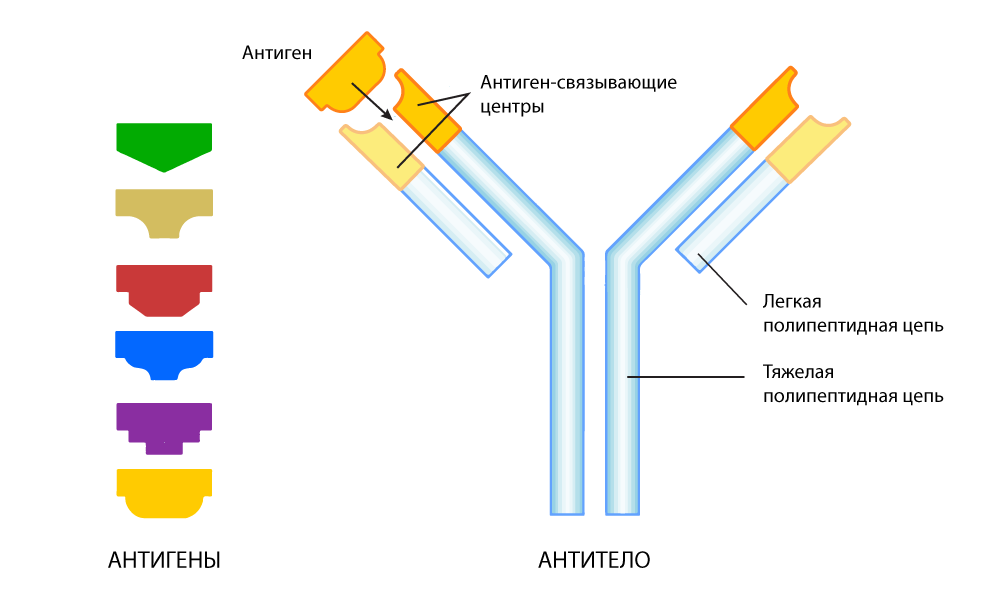 Un anticorps adapté pour trouver un antigène spécifique
Un anticorps adapté pour trouver un antigène spécifiqueCependant, reconnaître ne signifie pas toujours neutraliser. Avec cela, les anticorps ont des difficultés - à eux seuls, ils peuvent détruire loin de «l'ennemi» en aucun cas dans tous les cas.
Ainsi, en 1989, un chimiste et immunologiste israélien Zelig Ashkhar a
trouvé une combinaison de la puissance mortelle des cellules T aux yeux aveugles et du tireur d'élite visant des anticorps. Il a isolé les sections terminales d'anticorps protéiques capables de se lier étroitement à l'antigène de certaines cellules cancéreuses, et les a "transplantées" dans les cellules T - elles ont remplacé la partie du TCR responsable de la reconnaissance des antigènes.
Par la suite, il a commencé à travailler avec un collègue américain, Stephen Rosenberg, ils ont réussi à faire du récepteur chimérique une conception plus efficace, à la fois sensible et sélective.
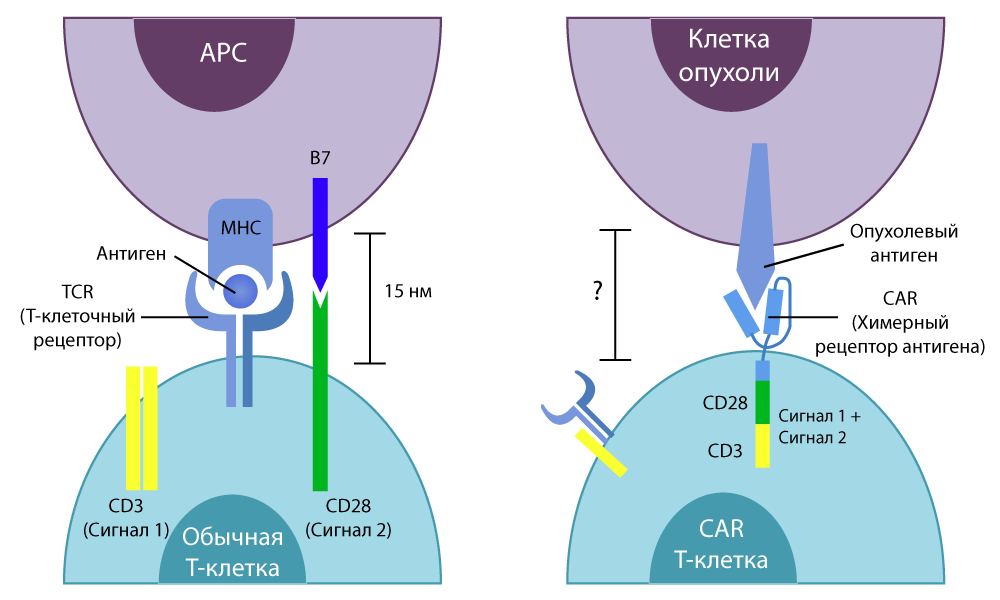 La différence entre les cellules T conventionnelles et les cellules CAR-T
La différence entre les cellules T conventionnelles et les cellules CAR-TDes études in vitro ont montré de bons résultats. Ensuite, les scientifiques ont de nouveau traité les souris, puis ont minutieusement transféré la technique aux humains.
Au fil du temps, la thérapie CAR-T a conduit à un look moderne.
- Premièrement, à l'aide de tests moléculaires et moléculaires, des mutations spécifiques dans les cellules tumorales humaines sont déterminées, sur lesquelles les anticorps peuvent être «accordés».
- Ensuite, une personne prend ses propres cellules T, change en utilisant des méthodes de bio-ingénierie, au lieu de TCR "transplanter" CAR, à l'écoute des mutations identifiées.
- Ensuite, les cellules CAR-T modifiées se multiplient in vitro et sont réintroduites dans le corps humain, où elles reconnaissent et tuent avec succès les cellules cancéreuses.
Dans les essais cliniques commencés en 2010, des résultats encourageants ont été immédiatement obtenus: dans le traitement du lymphome, 12 patients sur 13 ont montré une amélioration et 4 ont commencé une rémission. Dans le traitement de la leucémie, une rémission s'est produite chez 17 des 33 personnes.
En 2018,
un article d' oncologues américains est paru dans Nature Medicine, qui rapporte que depuis deux ans, ils observent un patient en parfaite santé après un traitement CAR-T. Elle a été guérie d'un cancer du sein métastatique avec métastases. Cette photo d'elle en kayak est donnée au début de l'article: après le traitement, elle est retournée au travail et fait du camping.
Nouvel espoir. L'immunothérapie sera-t-elle une panacée?Comme d'autres traitements contre le cancer, l'immunothérapie a ses limites. Malgré le fait que dans certains cas, les patients donnent une très bonne réponse au traitement avec des inhibiteurs du point de contrôle immunitaire, dans 60% des cas, une résistance acquise ou primaire aux médicaments anti-PD-1 ou anti-CTLA-4 se développe: la tumeur ne répond tout simplement pas pour le traitement ou s’adapte rapidement et apprend à le "contourner".
En plus de PD-1, PD-L1 / 2, CTLA-4, CD28 et B7, il existe de nombreux autres co-récepteurs à la surface des cellules T et des cellules tumorales, dont les effets n'ont pas encore été étudiés ainsi que le travail des points de contrôle, mais ils affectent également à la réponse immunitaire. L'un des domaines de travail est l'effet sur ces co-récepteurs.
En outre, la thérapie par les TIC est complétée par l'introduction de vaccins, de cytokines, de bêta-bloquants - et cette approche fonctionne également bien dans
certains cas .
La thérapie CAR-T est toujours extrêmement coûteuse et n'en est qu'au stade de l'utilisation commerciale: des développements sont en cours dans les groupes scientifiques d'Eshhar et Rosenberg, d'autres chercheurs - chacun des groupes crée des types spéciaux de CAR-T avec une action dirigée contre un type spécifique de cancer. Mais jusqu'à présent, ce n'est que de la recherche, des tests et des tests. Il faudra plusieurs années avant que cela ne devienne une méthode de traitement de masse bien établie - mais même dans ce cas, il ne sera pas possible de donner des garanties à 100%.
Mais pendant que les scientifiques mènent des recherches, les médecins introduisent des schémas thérapeutiques expérimentaux en utilisant les réalisations qui existent déjà. Et l'effet le plus notable est la combinaison de l'immunothérapie avec les «trois piliers» classiques de l'oncologie: la radiothérapie et la chimiothérapie, la chirurgie. En combinant ces méthodes, une synergie est toujours obtenue: ensemble, elles fonctionnent plus efficacement que tour à tour.
Si, jusqu'à présent, les médicaments d'immunothérapie standard ont été inclus dans la troisième, cinquième ligne (c'est-à-dire le tour) de la thérapie, maintenant les médecins se déplacent pour les prescrire immédiatement, ainsi que la chimiothérapie et la thérapie avec des anticorps monoclonaux ciblés: ces patients présentent souvent une meilleure dynamique et finissent par vivre plus longtemps.En Russie, toutes les immunopréparations majeures ont déjà été enregistrées. Le problème, cependant, est que pour chacun d'eux, le ministère de la Santé stipule séparément. Autrement dit, dans les instructions d'origine pour le médicament peut être prescrit, par exemple, neuf types de cancer différents, dans lesquels le médicament peut être prescrit, et dans notre pays, il n'est enregistré que pour six d'entre eux. Et donc avec chaque médicament. En conséquence, alors qu'environ 50% des tumeurs ne sont pas encore incluses dans cette liste. Par conséquent, dans le cadre du traitement de l'assurance médicale obligatoire, un médecin ne peut pas prescrire ces médicaments à tous les patients.En outre, les médecins des cliniques du budget de l'État sont strictement limités aux protocoles de traitement. Et si dans le protocole, les inhibiteurs du point de contrôle ne sont prescrits que sur 3 lignes, à la 3ème place après deux lignes de «chimie» standard, le médecin n'a tout simplement pas le droit de les écrire en premier, même s'il pense que cela aidera le patient.Eh bien, un problème commun est le manque de qualifications. La méthode, bien qu'elle ait réussi à faire ses preuves, est encore nouvelle pour de nombreux médecins du pays. Les médicaments sont tous occidentaux et nous parviennent avec un retard de 2-3 ans. Et, étant donné que l'immunothérapie n'est utilisée activement que depuis quelques années, beaucoup n'ont toujours pas d'expérience avec eux. De plus, l'utilisation de l'immunothérapie nécessite des connaissances spécifiques.En médecine privée, nous ne sommes pas limités par le budget. Si dans "Médecine 24/7"le patient fait référence à une tumeur pour laquelle un médicament d'immunothérapie n'a pas encore été enregistré, nous suggérons qu'il subisse une étude de génétique moléculaire. Selon les résultats, il devient clair si sa tumeur répondra à l'immunothérapie. Si c'est le cas, le médecin a le droit de le prescrire. Par conséquent, dans notre hôpital, nous utilisons l'immunothérapie pour presque tous les types de cancer - cela donne de très bons résultats. Même les patients de stade III-IV montrent une amélioration. Les préparations immunitaires nous donnent la possibilité de prolonger la vie des gens, même dans des cas considérés comme désespérés.Les patients eux-mêmes sont courants dans les cliniques privées et publiques. Ils ne comprennent pas toujours bien de quel type de méthode il s'agit, comment cela fonctionne, d'où la méfiance. Nous espérons que cet article a aidé à comprendre et à comprendre que l'immunothérapie est à juste titre au centre d'une attention particulière des oncologues. À en juger par les résultats, elle est déjà prête à se tenir sur un seul niveau avec les méthodes classiques. La terrible maladie reculera encore un peu.