
L'un des super-héros Marvel les plus célèbres a toujours été et sera considéré comme Logan, alias Wolverine. Et quelle caractéristique de son corps vient à l'esprit en premier, outre la régénération avec la vitesse du flash? En un mot - adamantium. Ce métal rare possède des propriétés uniques, il est presque impossible de le détruire et son traitement demande beaucoup d'efforts. Cette substance fictive a plusieurs équivalents dans notre réalité, qui ont également des propriétés très spécifiques. Parmi eux, l'iridium méritait une attention particulière des scientifiques. Ce métal ne peut guère faire un super-héros d'une simple personne, mais il sait comment détruire les cellules cancéreuses (Deadpool ne refuserait pas une telle chose). Comment les scientifiques en sont-ils arrivés à cette conclusion: quelle est l'efficacité de l'iridium dans la lutte contre le cancer et quel est son avenir en oncologie? Plongez dans le rapport du groupe d'étude pour obtenir des réponses. Allons-y.
Science des métauxL'iridium (Ir) est un métal de transition extrêmement solide du groupe du platine. Comme l'adamantium fictif, l'iridium est très résistant à la corrosion même à des températures de 2000 ° C. Autre similitude de ces deux métaux dans leur origine extraterrestre. Plus précisément, l'iridium sur notre planète est très petit, par conséquent, en forte concentration, il se trouve dans des endroits où tombent des météorites.
 Iridium (Ir)
Iridium (Ir)L'iridium est un métal assez jeune dans le monde scientifique, puisqu'il a été découvert en 1803 par le chimiste Smithson Tennant. Il a travaillé sur le platine avec un mélange d'acides nitrique et chlorhydrique, qui a un nom très inhabituel - aqua regia. Et comme il ressort de la composition de cette solution, après l'avoir utilisée, vous ne deviendrez pas un «maître ivre», comme Jackie Chan dans le film du même nom, mais plutôt un maître mort. Pour le mot «vodka» signifiait à l'origine de l'eau ordinaire et seulement après le XIVe siècle, il a commencé à être utilisé pour signifier une boisson alcoolisée.
Avec l'aide de la vodka royale, M. Tennant a pu obtenir sous forme pure les impuretés qui étaient dans le platine, à savoir l'osmium et l'iridium.
Comme mentionné précédemment, il y a très peu d'iridium - environ 3 tonnes de ce métal sont extraites par an. A titre de comparaison, l'extraction de l'argent, selon certaines sources, dépasse la barre des 27 000 tonnes par an.
Base d'étudeL'étude est basée sur la méthode déjà appliquée de traitement du cancer (et de certains autres également) - la thérapie photodynamique (PDT). Les personnages principaux de cette méthode sont les photosensibilisateurs et la lumière.
Photosensibilisateurs * - substances qui augmentent la sensibilité à l'exposition à la lumière dans les tissus biologiques.
Les sensibilisateurs sont assez pointilleux, c'est-à-dire qu'ils s'accumulent uniquement dans les tissus qui doivent être changés pour la procédure ultérieure d'irradiation avec de la lumière.
Lorsque la lumière pénètre dans le tissu cible, une réaction photochimique se produit - l'oxygène du triplet moléculaire (
3 O
2 ) est converti en oxygène singulet. De plus, des radicaux hautement actifs se forment. Ensemble, cela conduit à la mort des cellules cancéreuses.
Les scientifiques citent la photofrine et l'acide aminolévulinique comme les photosensibilisateurs les plus courants en thérapie PDT. Cependant, ces dernières années, de plus en plus d'attention a été portée aux métaux à haut coefficient de luminescence, car ils ont des propriétés photochimiques et photophysiques inhabituelles et utiles. Par exemple, TLD1433 (ruthénium) pour le traitement PDT pour la vessie et WST11 (palladium) pour le traitement des vaisseaux sanguins.
Résultats de rechercheAlors pourquoi ne pas utiliser l'iridium, pensaient les scientifiques. Mais d'abord, vous avez besoin d'un mécanisme qui permettra d'utiliser ce métal. Le patient ne prendra pas d'iridium par voie orale, comme les comprimés ordinaires. Et ici, l'albumine sérique humaine (
HSA ) est liée au travail qui, en raison de ses propriétés et de sa quantité (environ 55% de toutes les protéines sanguines), est un excellent porteur de diverses substances (dans notre cas, médicinales). En termes simples, le HSA peut être utilisé pour administrer des médicaments anticancéreux à la zone souhaitée du corps du patient, ce qui a déjà été démontré dans des études antérieures utilisant l'osmium, le ruthénium et le palladium.
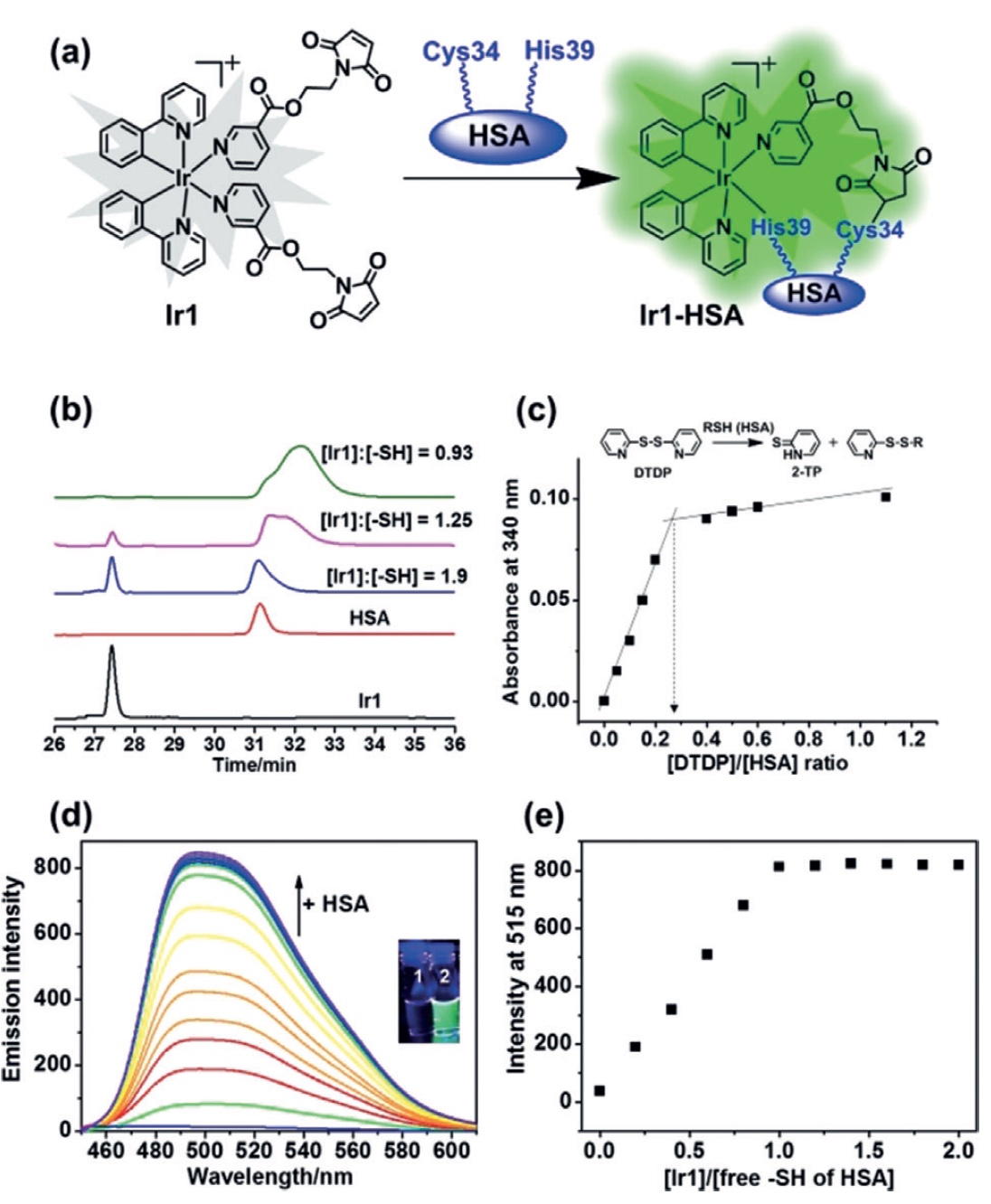 Image n ° 1
Image n ° 1Dans notre étude, les scientifiques ont créé un complexe organo-iridium (III) octaédrique fonctionnalisé au maléimide Ir1 (
1a ) en combinaison avec le HSA. Ce complexe (Ir1-HSA) s'est avéré beaucoup plus efficace pour augmenter la phosphorescence par rapport à Ir1 «pur», c'est-à-dire sans HSA.
Dans l'obscurité, Ir1-HSA est en grande partie non toxique pour les cellules ordinaires, mais présente une forte photo-cytotoxicité envers les cellules cancéreuses et leurs sphéroïdes (formations cellulaires).
L'Ir1 synthétisé était stable pendant 12 heures dans l'obscurité et après 1 heure d'exposition à la lumière bleue. Il a fallu vérifier la liaison carbone-carbone (C = C). Pour cela, un complexe de Ir1 et de cystéine (Cys) a été mis à réagir dans un rapport molaire Cys: Ir1 - 2: 1 dans [D
6 ] DMSO / D
2 O à une température de 298 K pendant 30 minutes. À la suite de la résonance magnétique des protons, les scientifiques ont trouvé la valeur maximale des protons vinyliques des groupes maléimide à environ 6,62 ppm (millionièmes de part). Avec l'ajout de cystéine, les pics ont disparu, mais ils ont réapparu déjà dans la plage de 2,9 ... 3,9 ppm. Les scientifiques attribuent cela à la conjugaison de la cystéine.
Ensuite, les scientifiques ont vérifié si le thiol libre Cys34 de HSA pouvait réagir avec C = C. Pour cela, 30 μM (micromole) Ir1 ont été incubés avec du HSA (0-120 μM) pendant 1 heure. De plus, les produits de réaction résultants ont été séparés en utilisant une chromatographie liquide haute performance en phase inverse (RP-HPLC).
Lorsque le HSA a atteint 120 μM, le pic de Ir1 a complètement disparu (rapport HSA: Ir1 = 4: 1). Ainsi, la teneur en thiol (SH) était de 0,27 ± 0,1 mole SH pour 1 mole de HSA (
1 s ). Par conséquent, la concentration de groupes SH libres de 120 μM de HSA est de 32,4 ± 1,2 μM. Avec cet indicateur, une réaction se produit avec 30 μM d'Ir1, conduisant à l'apparition d'un adduit (connexion directe des molécules) Ir1 et HSA dans un rapport 1: 1.
L'Ir1 pur n'a pas présenté de rayonnement puissant en solution aqueuse, contrairement au complexe Ir1-HSA (
1d ). Plus la concentration de HSA est élevée, plus la phosphorescence de Ir1 elle-même est forte (
1e ).
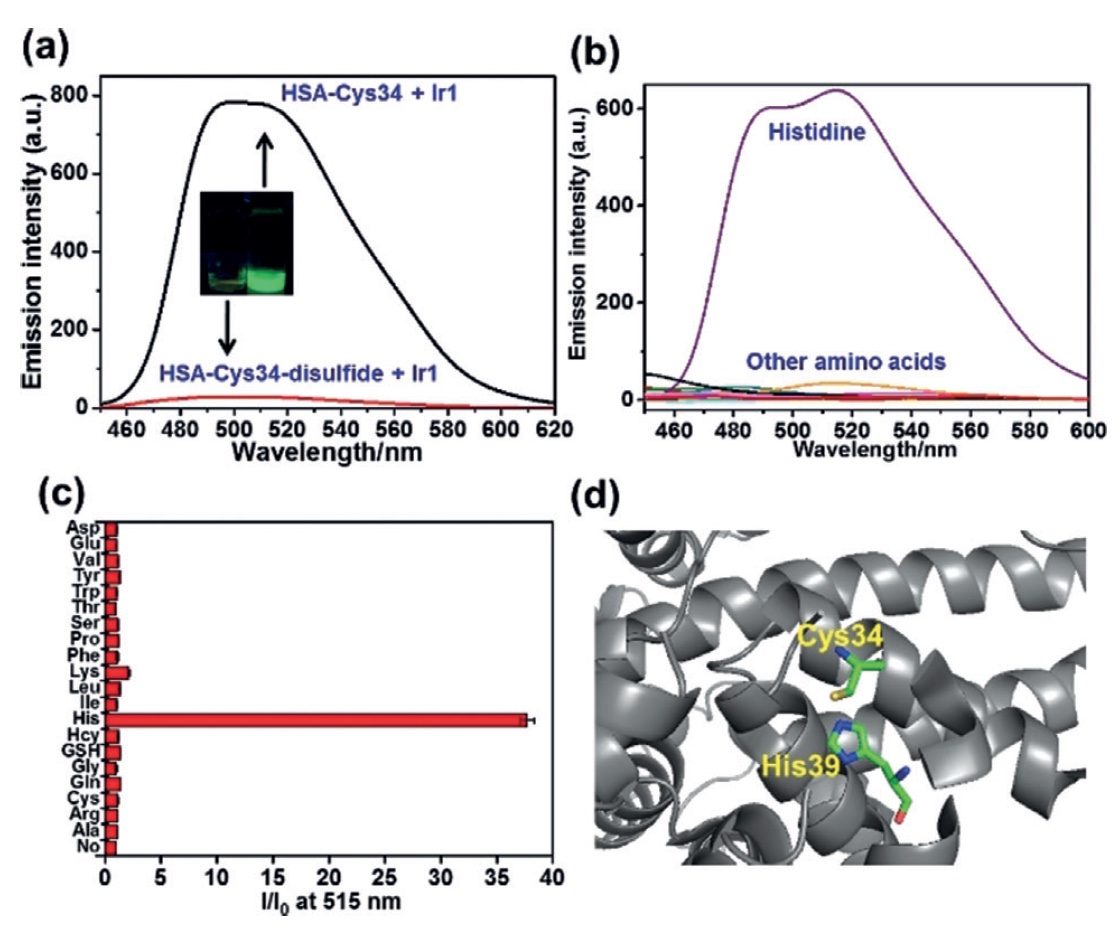 Image n ° 2
Image n ° 2Afin d'éliminer les groupes thiol libres de HSA, 100 uM de cystine par jour ont été ajoutés à la solution à une température de 277 K. Le produit résultant a été combiné avec Ir1 pendant 30 minutes. Les observations ont montré une diminution significative de la phosphorescence. Dans le cas du conjugué HSA-Cys34 et Ir1 (
2a ), la situation était opposée, ce qui suggère que c'est le Thysol Cys34 libre qui est le lien de connexion (plus précisément, le domaine de liaison) pour Ir1.
Il était maintenant nécessaire d'étudier la CSA plus en détail, en l'analysant dans ses composants. L'albumine sérique humaine possède une chaîne de 585 résidus d'acides aminés, parmi lesquels les scientifiques devaient trouver exactement ceux qui améliorent la luminescence de Ir1. Pour cela, une analyse luminescente de l'interaction de Ir1 avec divers acides aminés (
2b et
2c ) a été réalisée. Et comme nous pouvons le voir sur le graphique
2b , l'histidine (His), qui augmente la luminescence de Ir1 de 37 fois, est devenue le leader parmi les acides aminés avec une énorme marge.
Ayant un peu de compréhension de quoi et comment cela fonctionne à l'intérieur des composants du complexe Ir1-HSA, les scientifiques sont passés à une application pratique, c'est-à-dire à des expériences.
Tout d'abord, 0,4 millimole de Ir1 a été diluée dans 20 ml de MeOH: H2O, 0,4 millimole de HSA a été ajoutée et agitée pendant 1 heure. La microscopie confocale a ensuite été utilisée pour étudier la distribution de Ir1-HSA dans les cellules cancéreuses pulmonaires vivantes (A549).
Déjà après 30 minutes, Ir1-HSA était principalement concentré dans le cytoplasme des cellules cancéreuses. À 60-120 minutes du début de l'incubation, le complexe a pénétré dans les noyaux des cellules cancéreuses.
 Image 3: Microscopie confocale des cellules cancéreuses du poumon A549.
Image 3: Microscopie confocale des cellules cancéreuses du poumon A549.Cependant, il convient de noter que ce n'est pas l'ensemble du complexe qui a pénétré dans les noyaux des cellules cancéreuses, mais seulement Ir1. Un test d'immunofluorescence a montré que le HSA était simplement absent dans les noyaux des cellules exposées à Ir1.
 Image n ° 4: analyse par immunofluorescence de la présence de HSA dans les cellules cancéreuses du poumon.
Image n ° 4: analyse par immunofluorescence de la présence de HSA dans les cellules cancéreuses du poumon.Mais l'HSA ne disparaît pas sans laisser de trace, il reste simplement dans le cytoplasme et dans la membrane du noyau de la cellule cancéreuse. Il s'avère que le HSA remplit pleinement sa fonction: il a livré Ir au noyau cellulaire, et il est resté à l'extérieur.
 Image n ° 5: rendement quantique et durée de vie de la phosphorescence Ir1 et du complexe Ir1-HSA.
Image n ° 5: rendement quantique et durée de vie de la phosphorescence Ir1 et du complexe Ir1-HSA.Les scientifiques ont également vérifié le rendement quantique (exagéré, la force) et la durée de vie de la phosphorescence Ir1 (par lui-même) et du complexe Ir1-HSA.
Le rendement quantique de Ir1 était très faible (seulement 0,001) et la durée de vie à une température de 298 K était de 182,7 nanosecondes (
5a ). Mais le rendement quantique Ir1-CSA était déjà de 0,036 et la durée de vie était de 871,8 ns. Cette durée de phosphorescence contribue à la génération d'oxygène singulet (
1 O
2 ).
La spectroscopie de résonance paramagnétique électronique utilisant la 2,2,6,6-tétraméthylpipéridine comme piège à spin a permis de détecter la génération de 1O2 dans Ir1 pur et dans le complexe Ir1-HSA lors d'une irradiation à 465 nm pendant 20 minutes (
5b ). Comme prévu, le rendement quantique de 1O2 de Ir1-HSA était significativement plus élevé (0,83) que celui de Ir1 (0,06).
Il était également nécessaire de vérifier le degré d'effet de Ir1-HSA et Ir1 sur les cellules cancéreuses et sur les cellules saines. Trois options ont été utilisées comme cellules cancéreuses: le cancer du poumon A549, l'hépatome Hep-G2 et le cancer du poumon résistant au cisplatine A549R. En tant que cellules saines, MRC-5 (poumons) et LO2 (foie) ont été utilisés. L'expérience a été réalisée en deux variantes d'éclairage: l'obscurité totale tout au long de l'expérience et la lumière bleue.
Les cellules ont été incubées avec Ir1 ou Ir1-HSA pendant 2 heures, lavées avec du perborate de sodium et irradiées avec de la lumière bleue pendant 20 minutes ou laissées dans l'obscurité (deuxième expérience). Après cela, les cellules ont été restaurées en 46 heures.
L'effet de Ir1 sur les cellules A549 dans l'obscurité (89,6 μM) et sous illumination (53,3 μM) était pratiquement absent.
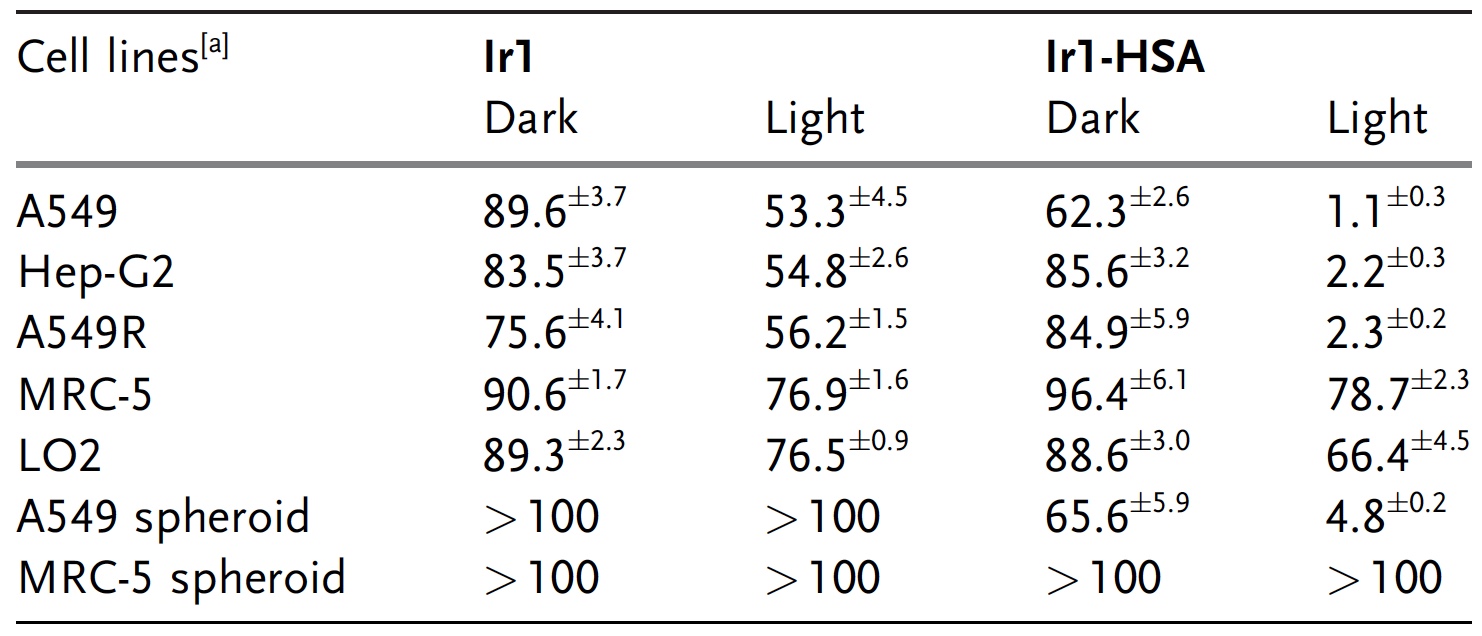 Tableau des effets de Ir1 et Ir1-HSA sur les cellules cancéreuses: plus le nombre est élevé, moins l'exposition (c.-à-d. Plus de cellules cancéreuses est restée indemne).
Tableau des effets de Ir1 et Ir1-HSA sur les cellules cancéreuses: plus le nombre est élevé, moins l'exposition (c.-à-d. Plus de cellules cancéreuses est restée indemne).Mais Ir1-CSA a montré des résultats très différents. Dans l'obscurité, le complexe de test n'affecte en rien les cellules cancéreuses, mais lorsqu'il est illuminé, sa cytotoxicité augmente considérablement. Des résultats similaires, comme nous le voyons dans le tableau ci-dessus, Ir1 et Ir1-HSA ont montré par rapport à d'autres cellules cancéreuses. Dans le même temps, les cellules saines dans l'obscurité et sous éclairage n'ont pas été affectées par Ir1 et Ir1-HSA.
Enfin, les scientifiques ont effectué une analyse des espèces réactives de l'oxygène (ROS) à l'intérieur des cellules après une exposition à la lumière. Dans l'obscurité, comme prévu, aucun ROS n'a été détecté. Mais dans les cellules qui ont subi une irradiation lumineuse après l'application de Ir1-HSA, des ROS ont été détectés (
5c ).
Pour une connaissance plus détaillée de l'étude, je vous recommande fortement de consulter le
rapport des scientifiques et
les documents supplémentaires .
ÉpilogueAvec cette étude, les scientifiques n'ont pas essayé d'inventer un vélo sous la forme de l'utilisation de métaux rares dans la thérapie photodynamique, car cela avait déjà été fait plus tôt avec l'osmium et le palladium. Cependant, personne n'a encore essayé d'utiliser l'iridium, que les chercheurs ont décidé de corriger. Leur travail n'a pas été inutile, car l'iridium a montré d'excellents résultats dans la lutte contre les cellules cancéreuses de différents types, tout en n'affectant pas les cellules saines.
Les maladies oncologiques sont l'une des plus courantes, faisant des millions de morts chaque année. L'invention de nouvelles méthodes pour combattre cette maladie et l'amélioration de celles existantes devraient et continueront. Bien sûr, nous sommes encore loin d'une victoire totale sur le cancer, mais les scientifiques du monde entier continuent leur combat dans les laboratoires, comme des millions de patients dans les services.
N'oubliez pas non plus les facteurs qui conduisent à la survenue d'un cancer. Certains d'entre eux (écologie, mauvaises habitudes, etc.) peuvent être complètement éliminés par une personne.
Vendredi hors sujet:
Personne sain d'esprit ne se réjouira de l'oncologie. De tels diagnostics vous font abandonner et tout oublier. Mais vous ne devez jamais abandonner. Si vous ne vous battez pas, le diagnostic prévaudra certainement. Mais si vous combattez la maladie, il y a toujours une chance de la vaincre. Alors pourquoi ne pas tenter cette chance?
Merci d'avoir regardé, restez curieux et passez un excellent week-end à tous, les gars.
Merci de rester avec nous. Aimez-vous nos articles? Vous voulez voir des matériaux plus intéressants? Soutenez-nous en passant une commande ou en le recommandant à vos amis, une
réduction de 30% pour les utilisateurs Habr sur un analogue unique de serveurs d'entrée de gamme que nous avons inventés pour vous: Toute la vérité sur VPS (KVM) E5-2650 v4 (6 cœurs) 10 Go DDR4 240 Go SSD 1 Gbps à partir de 20 $ ou comment diviser le serveur? (les options sont disponibles avec RAID1 et RAID10, jusqu'à 24 cœurs et jusqu'à 40 Go de DDR4).
VPS (KVM) E5-2650 v4 (6 cœurs) 10 Go DDR4 240 Go SSD 1 Gbit / s jusqu'au printemps gratuitement lors du paiement pendant
six mois, vous pouvez commander
ici .
Dell R730xd 2 fois moins cher? Nous avons seulement
2 x Intel Dodeca-Core Xeon E5-2650v4 128 Go DDR4 6x480 Go SSD 1 Gbps 100 TV à partir de 249 $ aux Pays-Bas et aux États-Unis! Pour en savoir plus sur la
création d'un bâtiment d'infrastructure. classe utilisant des serveurs Dell R730xd E5-2650 v4 coûtant 9 000 euros pour un sou?