
Avant de commencer la lecture, calculez le nombre d'appareils dotés de piles se trouvant à côté de vous dans un rayon de plusieurs mètres. Vous verrez sûrement un smartphone, une tablette, une montre intelligente, un tracker de fitness, un ordinateur portable, une souris sans fil? Tous ces appareils sont équipés de batteries lithium-ion - leur invention peut être considérée comme l'un des événements les plus importants dans le domaine de l'énergie.
Les batteries lithium-ion légères, spacieuses et compactes ont contribué à l'essor de l'électronique portable, dont l'existence était auparavant impossible. Seuls les gadgets au cours des 30 dernières années ont fait un saut technologique fantastique, et les batteries lithium-ion modernes ne sont presque pas différentes des premiers modèles de production du début des années 1990. Qui et comment ont inventé les piles rechargeables lithium-ion, quelles compositions y sont utilisées et y a-t-il un complot mondial contre les piles «éternelles»? Nous disons.
La légende de la première batterie
Entre la première tentative de produire chimiquement de l'électricité et la création de batteries lithium-ion, peut-être deux millénaires se sont écoulés. Il y a une supposition non confirmée que le premier élément galvanique créé par l'homme dans l'histoire de l'humanité était la "batterie de Bagdad", trouvée en 1936 près de Bagdad par l'archéologue Wilhelm Koenig. La découverte, datée du II-IV siècle avant JC. e., est un vase d'argile dans lequel se trouve un cylindre en cuivre et une tige de fer, l'espace entre lesquels pourrait être rempli "d'électrolyte" - acide ou alcalin. La reconstruction moderne de la découverte a montré que lorsque le récipient est rempli de jus de citron, il est possible d'atteindre une tension allant jusqu'à 0,4 volt.
 La batterie de Bagdad est assez similaire à une batterie portable. Ou un étui en papyrus? Source: Ironie / Wikimedia
La batterie de Bagdad est assez similaire à une batterie portable. Ou un étui en papyrus? Source: Ironie / Wikimedia
Pourquoi la «batterie de Bagdad» pourrait-elle être utilisée s'il restait quelques milliers d'années avant la découverte de l'électricité? Peut-être qu'il a été utilisé pour le dépôt précis d'or sur des figurines par la méthode de galvanisation - le courant et la tension de la "batterie" sont tout à fait suffisants pour cela. Cependant, ce n'est qu'une théorie, car les anciens peuples n'atteignaient aucune preuve de l'utilisation de l'électricité et de cette même «batterie»: la dorure était appliquée par fusion à cette époque, et le récipient inhabituel lui-même pouvait tout aussi bien être un conteneur protégé pour les rouleaux.
The Little Bang Theory
Le proverbe russe «Il n'y aurait pas de bonheur, mais le malheur a aidé» illustre le mieux possible le déroulement des travaux sur les batteries lithium-ion. Sans un incident inattendu et désagréable, la création de nouvelles batteries pourrait être retardée de plusieurs années.
Dans les années 1970, le Britannique Stanley Whittingham, qui travaillait chez Exxon Energy Company, a utilisé une anode au sulfure de titane et une cathode au lithium pour créer une batterie au lithium rechargeable. La première batterie au lithium rechargeable a montré des indicateurs de courant et de tension tolérables, elle n'a explosé que périodiquement et a empoisonné les gens autour d'elle avec du gaz: du disulfure de titane a libéré du sulfure d'hydrogène au contact de l'air, ce qui est au moins désagréable à respirer, mais au plus dangereux. De plus, le titane a toujours été très cher à tout moment, et dans les années 1970, le prix du disulfure de titane était d'environ 1 000 $ le kilogramme (l'équivalent de 5 000 $ de nos jours). Sans parler du fait que le lithium métallique brûle dans l'air. Exxon a donc détourné le projet de Whittingham du péché.
En 1978, Koichi Mizushima, qui a soutenu son doctorat en physique, était engagé dans la recherche à l'Université de Tokyo lorsqu'il a reçu une invitation d'Oxford pour rejoindre le groupe de John Goodenough, qui cherchait de nouveaux matériaux pour les anodes de batterie. C'était un projet très prometteur, car le potentiel des sources d'énergie au lithium était déjà connu, mais elles ne pouvaient pas vraiment apprivoiser le métal capricieux - les récentes expériences de Whittingham ont montré que le début de la production de masse des batteries lithium-ion convoitées était encore loin.
Les batteries expérimentales utilisaient une cathode au lithium et une anode au sulfure. La supériorité des sulfures sur les autres matériaux des anodes a donné à Mizushima et à ses collègues une direction à suivre. Les scientifiques ont commandé un four au sulfure dans leur laboratoire sur place pour expérimenter plus rapidement différents composés. Le travail avec le poêle ne s'est pas très bien terminé: un jour, il a explosé et provoqué un incendie. L'incident a contraint une équipe de chercheurs à reconsidérer leurs plans: peut-être que les sulfures, malgré leur efficacité, n'étaient pas le meilleur choix. Les scientifiques ont tourné leur attention vers les oxydes, qui étaient beaucoup plus sûrs à synthétiser.
Après de nombreux tests avec divers métaux, dont le fer et le manganèse, Mizushima a constaté que l'oxyde de lithium-cobalt donne les meilleurs résultats. Il suffit de ne pas l'utiliser de la même manière que l'équipe de Gudenaf l'avait supposé auparavant - pour rechercher non pas un matériau qui absorbe les ions lithium, mais un matériau qui donne le plus facilement des ions lithium. Le cobalt était également meilleur que d'autres car il répond à toutes les exigences de sécurité et augmente également la tension de la cellule à 4 volts, soit deux fois plus que les options de batterie précédentes.
L'utilisation du cobalt a été la plus importante, mais pas la dernière étape de la création de batteries lithium-ion. Après avoir résolu un problème, les scientifiques se sont confrontés à un autre: la densité actuelle était trop faible pour que l'utilisation de cellules lithium-ion soit économiquement viable. Et l'équipe qui a fait une percée a fait la seconde: en réduisant l'épaisseur des électrodes à 100 microns, il a été possible d'augmenter la force du courant au niveau d'autres types de batteries, avec une tension et une capacité doubles.
Premiers pas commerciaux
L'histoire de l'invention des batteries lithium-ion ne s'arrête pas là. Malgré la découverte de Mizushima, l'équipe de Gudenaf n'avait pas encore d'échantillon prêt pour la production de masse. En raison de l'utilisation de lithium métallique dans la cathode pendant la charge de la batterie, les ions lithium sont retournés à l'anode non pas en couche uniforme, mais par des dendrites - des chaînes en relief qui, en se développant, ont provoqué un court-circuit et des feux d'artifice.
En 1980, le scientifique marocain Rachid Yazami a découvert que le graphite remplit le rôle d'une cathode et qu'il est absolument ignifuge. Les électrolytes organiques existant à cette époque se sont rapidement décomposés au contact du graphite, alors Yazami les a remplacés par de l'électrolyte solide. La cathode en graphite de Yazami a été inspirée par la découverte de la conductivité des polymères par le professeur Hideki Shirakawa, pour laquelle il a reçu le prix Nobel de chimie. Et la cathode en graphite Yazami est toujours utilisée dans la plupart des batteries lithium-ion.
Lancement en production? Et encore non! 11 autres années se sont écoulées, les chercheurs ont amélioré la sécurité des batteries, augmenté la tension, expérimenté différents matériaux de cathode avant la mise en vente de la première batterie lithium-ion.
L'échantillon commercial a été développé par Sony et le géant chimique japonais Asahi Kasei. Il est devenu la batterie du caméscope amateur Sony CCD-TR1. Il a résisté à 1000 cycles de charge et la capacité résiduelle après une telle usure était quatre fois supérieure à celle d'un type similaire de batterie au nickel-cadmium.
Pierre d'achoppement en cobalt
Avant la découverte de l'oxyde de lithium et de cobalt Koichi Mizushima, le cobalt n'était pas un métal très recherché. Ses principaux gisements ont été découverts sur le territoire de l'Afrique dans l'État désormais connu sous le nom de République démocratique du Congo. Le Congo est le plus grand fournisseur de cobalt - 54% de ce métal est extrait ici. En raison de bouleversements politiques dans le pays dans les années 1970, le prix du cobalt a grimpé de 2000%, mais est ensuite revenu à ses valeurs antérieures.
Une demande élevée crée des prix élevés. Ni dans les années 90, ni dans les années 2000, le cobalt n'était l'un des principaux métaux de la planète. Mais ce qui a commencé avec la popularisation des smartphones dans les années 2010! En 2000, la demande de métal était d'environ 2 700 tonnes par an. En 2010, lorsque les smartphones iPhone et Android marchaient triomphalement autour de la planète, la demande a bondi à 25 000 tonnes et a continué de croître d'année en année. Désormais, le nombre de commandes dépasse de 5 fois le volume de cobalt vendu. Pour référence: plus de la moitié du cobalt extrait dans le monde est destiné à la production de batteries.
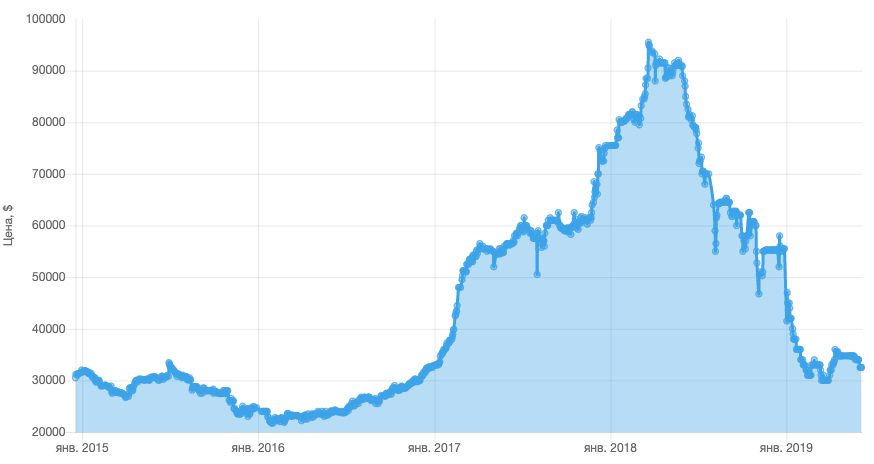 Tableau des prix du cobalt pour les 4 dernières années. Les commentaires sont redondants. Source: Elec.ru
Tableau des prix du cobalt pour les 4 dernières années. Les commentaires sont redondants. Source: Elec.ru
Si en 2017 le prix de la tonne de cobalt était en moyenne de 24000 $, alors depuis 2017, il a fortement augmenté, atteignant en 2018 un pic à environ 95500 $. Bien que les smartphones n'utilisent que 5 à 10 grammes de cobalt, la hausse des prix des métaux a affecté le coût des appareils.
Et c'est l'une des raisons pour lesquelles les constructeurs de voitures électriques s'inquiètent de la diminution de la part de cobalt dans les batteries des voitures. Par exemple, Tesla a réduit la masse de métal rare de 11 à 4,5 kg par machine, et prévoit à l'avenir de trouver des composés efficaces sans cobalt. En 2019, le prix du cobalt a augmenté anormalement et est tombé aux valeurs de 2015, mais les développeurs de batteries ont intensifié leurs efforts pour refuser ou réduire la part de cobalt.
Dans les batteries lithium-ion traditionnelles, le cobalt représente environ 60% de la masse totale. La composition lithium-nickel-manganèse utilisée dans les automobiles comprend de 10% à 30% de cobalt, selon les caractéristiques souhaitées de la batterie. La composition lithium-nickel-aluminium n'est que de 9%. Cependant, ces mélanges ne remplacent pas complètement l'oxyde de lithium-cobalt.
Problèmes de Li-ion
À ce jour, différents types de batteries lithium-ion sont les meilleures batteries pour la plupart des consommateurs. Capacieux, puissants, compacts et peu coûteux, ils présentent encore de sérieux inconvénients qui limitent le domaine d'utilisation.
Risque d'incendie. Pour un fonctionnement normal, une batterie au lithium-ion a besoin d'un contrôleur de puissance pour éviter une surcharge et une surchauffe. Sinon, la batterie se transforme en une chose très inflammable, s'efforçant de gonfler et d'exploser sous la chaleur ou lors de la charge à partir d'un adaptateur de mauvaise qualité. Le risque d'explosion est peut-être le principal inconvénient des batteries lithium-ion. Pour augmenter la capacité à l'intérieur des batteries, l'agencement est compacté, en raison duquel même de légers dommages à la coque entraînent instantanément un incendie. Tout le monde se souvient de l'histoire sensationnelle avec le Samsung Galaxy Note 7, dans lequel, en raison de l'étanchéité à l'intérieur du boîtier, la coque de la batterie a frotté au fil du temps, de l'oxygène a pénétré à l'intérieur et le smartphone a soudainement clignoté. Depuis lors, certaines compagnies aériennes ont demandé que les batteries lithium-ion soient transportées uniquement dans les bagages à main, et sur les vols cargo, un grand autocollant d'avertissement est apposé sur l'emballage des batteries.
La dépressurisation est une explosion. La recharge est une explosion. Vous devez payer le potentiel énergétique du lithium avec précautions.Le vieillissement Les batteries au lithium-ion sont sujettes au vieillissement, même si elles ne sont pas utilisées. Par conséquent, acheté en tant que smartphone de collection déballé il y a 10 ans, par exemple, le tout premier iPhone, tiendra une charge beaucoup moins due au très vieillissement de la batterie. Soit dit en passant, les recommandations visant à maintenir les batteries chargées jusqu'à la moitié de la capacité sont justifiées - lorsqu'elle est complètement chargée pendant un long stockage, la batterie perd sa capacité maximale beaucoup plus rapidement.
Auto-décharge. Accumuler de l'énergie dans des batteries lithium-ion et la stocker pendant de nombreuses années est une mauvaise idée. En principe, toutes les batteries perdent leur charge, mais le lithium-ion le fait particulièrement rapidement. Si les cellules NiMH perdent de 0,08 à 0,33% par mois, les cellules Li-Ion perdent de 2 à 3% par mois. Ainsi, dans un an, la batterie lithium-ion perdra un tiers de la charge et, après trois ans, elle se "reposera" à zéro. Pour être honnête, disons que les piles au nickel-cadmium sont encore pires - 10% par mois. Mais c'est une histoire complètement différente.
Sensibilité à la température. Le refroidissement et la surchauffe affectent fortement les paramètres d'une telle batterie: +20 ° C sont considérés comme la température ambiante idéale pour les batteries lithium-ion, si elle est réduite à +5 ° C, la batterie donnera à l'appareil 10% d'énergie en moins. Un refroidissement en dessous de zéro prend des dizaines de pour cent de la capacité et affecte également la santé de la batterie: si vous essayez de la charger, par exemple, à partir d'une batterie externe, un "effet mémoire" apparaîtra et la batterie perdra irrévocablement sa capacité en raison de la formation de lithium métal sur l'anode. À des températures hivernales moyennes en Russie, la cellule lithium-ion n'est pas fonctionnelle - laissez le téléphone en janvier dans la rue pendant une demi-heure pour le vérifier.
Pour faire face aux problèmes décrits, les scientifiques expérimentent des matériaux provenant d'anodes et de cathodes. Lors du remplacement de la composition des électrodes, un gros problème est remplacé par des problèmes plus petits - la sécurité incendie conduit à une diminution du cycle de vie et un courant de décharge élevé réduit la consommation d'énergie spécifique. Par conséquent, la composition des électrodes est sélectionnée en fonction de l'application de la batterie.
Qui a volé la révolution?
Chaque année, sur les fils d'actualité, des informations font état d'une autre percée dans la création de batteries extrêmement spacieuses et durables - il semble que les smartphones fonctionneront pendant un an sans se recharger et se rechargeront en dix secondes. Et où est la révolution de la batterie que les scientifiques promettent à tout le monde?
Souvent dans de tels reportages, les journalistes déforment les faits, omettant tout détail très important. Par exemple, une batterie à chargement instantané peut avoir une très faible capacité, adaptée uniquement pour alimenter un réveil de chevet. Ou la tension n'atteint pas un volt, bien que les smartphones aient besoin de 3,6 V. Et pour obtenir un ticket pour la vie, la batterie doit avoir un faible coût et une sécurité incendie élevée. Malheureusement, la grande majorité des développements étaient inférieurs dans au moins un paramètre, à cause de quoi les batteries "révolutionnaires" ne sont jamais allées au-delà du laboratoire.
 À la fin des années 2000, Toshiba a expérimenté des piles à combustible au méthanol rechargeables (faisant le plein de méthanol sur la photo), mais les batteries lithium-ion étaient toujours plus pratiques. Source: Toshiba
À la fin des années 2000, Toshiba a expérimenté des piles à combustible au méthanol rechargeables (faisant le plein de méthanol sur la photo), mais les batteries lithium-ion étaient toujours plus pratiques. Source: Toshiba
Et, bien sûr, nous laissons de côté la théorie du complot «les batteries sans fin ne sont pas rentables pour les fabricants». De nos jours, les piles des appareils grand public sont irremplaçables (ou plutôt, elles peuvent être changées, mais difficiles). Il y a 10 à 15 ans, remplacer une batterie endommagée dans un téléphone portable était simple, mais les sources d'alimentation ont vraiment perdu beaucoup de capacité en un an ou deux d'utilisation active. Les batteries lithium-ion modernes durent plus longtemps que le cycle de vie moyen de l'appareil. Dans les smartphones, vous pouvez penser à remplacer la batterie au plus tôt après 500 cycles de charge lorsqu'elle perd 10 à 15% de sa capacité. Et plutôt, le téléphone lui-même perdra de sa pertinence avant que la batterie ne tombe finalement en panne. Autrement dit, les fabricants de batteries ne gagnent pas sur le remplacement, mais sur la vente de batteries pour de nouveaux appareils. Ainsi, la batterie «éternelle» d'un téléphone de dix ans ne nuira pas aux affaires.
L'équipe de Goodenough reprend ses activités
Mais qu'est-il arrivé aux scientifiques du groupe John Goodenough, qui ont découvert l'oxyde de lithium-cobalt et ont ainsi donné vie à des batteries lithium-ion efficaces?
En 2017, Goodenough, âgé de 94 ans, a annoncé qu'en collaboration avec des scientifiques de l'Université du Texas, il avait développé un nouveau type de batterie à semi-conducteurs qui pouvait stocker 5 à 10 fois plus d'énergie que les batteries lithium-ion précédentes. Pour cela, les électrodes étaient en lithium et en sodium purs. Prix promis et bas. Mais il n'y a toujours pas de détails et de prévisions sur le début de la production de masse. Compte tenu du long chemin entre l'ouverture du groupe Gudenaf et le démarrage de la production de masse des batteries lithium-ion, de vrais échantillons sont attendus dans 8 à 10 ans.
Koichi Mizushima poursuit ses recherches chez Toshiba Research Consulting Corporation. «Avec le recul, je suis surpris que personne avant nous n'ait deviné utiliser un matériau aussi simple que l'oxyde de lithium-cobalt sur l'anode. À ce moment-là, de nombreux autres oxydes avaient été essayés, donc probablement sans nous, quelqu'un d'autre aurait fait cette découverte en quelques mois », a-t-il déclaré.
 Koichi Mizushima a reçu un prix de la Royal Chemical Society de Grande-Bretagne pour sa participation à la création de batteries lithium-ion. Source: Toshiba
Koichi Mizushima a reçu un prix de la Royal Chemical Society de Grande-Bretagne pour sa participation à la création de batteries lithium-ion. Source: Toshiba
L'histoire ne tolère pas les humeurs subjonctives, d'autant plus que M. Mizushima lui-même admet qu'une percée dans la création de batteries lithium-ion était inévitable. Mais il est toujours intéressant d'imaginer à quoi ressemblerait le monde de l'électronique mobile sans batteries compactes et volumineuses: des ordinateurs portables d'une épaisseur de quelques centimètres, d'énormes smartphones qui doivent être rechargés deux fois par jour, et pas de montres intelligentes, de bracelets de fitness, de caméras d'action, de quadcoptères et même des véhicules électriques. Chaque jour, les scientifiques du monde entier se rapprochent d'une nouvelle révolution énergétique, qui nous donnera des batteries plus puissantes et plus compactes, et avec elles une électronique incroyable, dont nous ne pouvons que rêver.