
À l'extérieur de la fenêtre, le soleil brillant brille, l'air est rempli d'humidité chaude et la brise fraîche a décidé de prendre des vacances, nous laissant à la chaleur déchirée. Je veux changer mon jean en short, un ordinateur portable en volley-ball et un bureau à la plage. L'été est associé aux vacances et aux vacances, mais parfois un invité que nous attendons habituellement pendant les mois d'hiver, à savoir un rhume, est coincé dans cette liste inactive. Il n'y a rien de pire que la température lorsque la température de l'air est d'environ 30. En été, les infections virales respiratoires aiguës transforment une personne en escargot, tissant lentement le long de l'asphalte chaud, laissant une traînée mucileuse.
La science de sauvetage peut-elle nous aider à combattre les rhinovirus, demandez-vous? Bien sûr, peut-être que les scientifiques vous répondront s'ils découvrent une nouvelle façon de lutter contre les rhinocéros / entérovirus cachés dans la «poche» du virus jusque-là inexplorée. De quel type de poche s'agit-il, que veulent les scientifiques et comment cela aidera-t-il à vaincre les rhinovirus? Nous trouverons les réponses dans le rapport du groupe de recherche.
Base d'étude
Pour commencer, nous nous rappelons rapidement de ce que nous avons ARVI et de ce que c'est vraiment.
 Visualisation du rhinovirus.
Visualisation du rhinovirus.L'ARVI, c'est-à-dire une infection virale respiratoire aiguë, est le résultat de l'activité active du virus dans le corps humain, à savoir dans son système respiratoire. Ces virus comprennent les rhinovirus du genre entérovirus. L'une des principales caractéristiques structurelles du rhinovirus est le virion ouvert, c'est-à-dire une particule virale sans coque.
Chez l'homme, les rhinovirus provoquent une inflammation des voies respiratoires supérieures, car ils préfèrent se multiplier dans la muqueuse qui recouvre le nasopharynx. Les symptômes en cas d'infection sont assez courants et familiers à tout le monde - température, écoulement nasal, douleur dans le larynx. En l'absence de traitement et d'une diminution de la réponse immunitaire du corps, les infections virales respiratoires aiguës peuvent évoluer en bronchite, sinusite ou otite moyenne.
Les rhinovirus peuvent-ils être traités et / ou vaccinés? Théoriquement possible, mais presque impossible, car le nombre de variantes sérologiques du pathogène est très important. Les infections à rhinovirus sont traitées en atténuant les symptômes, et le virus lui-même détruit le système immunitaire.
Si nous parlons du traitement d'une infection virale en tant que telle, il vaut la peine de comprendre le processus de destruction du virus lui-même. En règle générale, cela se fait en y introduisant un médicament, en gros. À l'heure actuelle, les inhibiteurs les plus étudiés sont les liants de capside, qui sont placés dans la poche hydrophobe de la capside virale.
Dans l'étude que nous envisageons aujourd'hui, les scientifiques ont identifié une poche auparavant inconnue qui est formée par les protéines virales VP1 et VP3 et est une caractéristique commune à différents types d'entéro-rhinovirus. L'introduction de médicaments dans cette poche stabilisera la région clé du virion, ce qui empêchera l'expansion conformationnelle nécessaire à la libération d'ARN viral. Par conséquent, pas de morve, de toux et de fièvre. D'accord, cela semble très inspirant.
Résultats de recherche
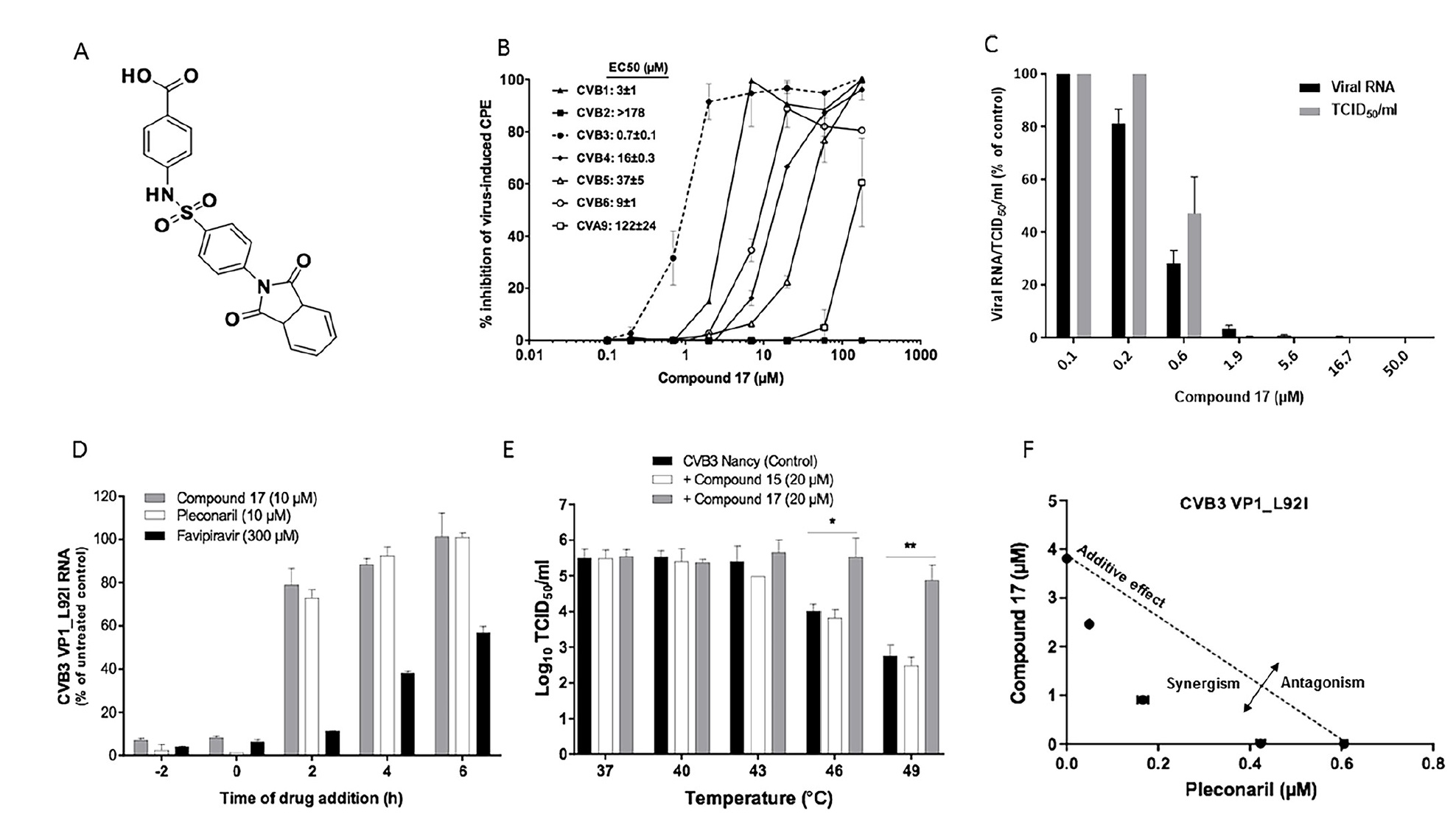 Image n ° 1
Image n ° 1Les scientifiques ont découvert que le
composé 17 (
1a ), qui est un dérivé du benzènesulfonamide, est un puissant inhibiteur de la souche B3 du virus Coxsackie. La concentration efficace demi-maximale (CE50) est de 0,7 ± 0,1 μM (
1b ).
Le composé 17 inhibe également la réplication de CVB1 et CVB6, présente une activité modérée contre CVB4, CVB5 et le virus Coxsackie A9 (CVA9), mais ne réagit pas contre CVB2 même à la concentration la plus élevée testée (
1b ). De plus, ce composé n'est pas inhibé dans CVA16 et EVA71 (groupe EV-A), CVA21 et PV1 (groupe EV-C), EVD68 (groupe EV-D) et le rhinovirus B14 (RVB14, RV-B).
L'activité antivirale du composé 17 a en outre été confirmée dans une analyse de la charge virale, dans laquelle il a réduit la manière dose-dépendante de la formation d'ARN du virus CVB3 et CVB3 avec des valeurs CE50 de 0,4 ± 0,01 μM et 1,1 ± 0,3 μM, respectivement (
1 s ).
Le composé 17, comme le pléconaril (un médicament antiviral), cible la réplication de CVB3 aux premiers stades du cycle viral. Dans le cas de l'introduction du composé 17, 2 heures après l'infection, l'activité antivirale est fortement réduite (
1d ).
Les scientifiques nous rappellent que les inhibiteurs des entérovirus à un stade précoce (par exemple le pléconaril) interagissent avec les capsides virales et augmentent leur résistance à l'inactivation thermique. Le composé 17 a augmenté la stabilité thermique du CVB3 de 1,5 à une température de 46 ° C et de 2,1 à 49 ° C (
1e ).
Si le composé 17 et le pléconaril sont combinés, une activité antivirale synergique sera observée. Autrement dit, ces deux substances ont des mécanismes d'action antivirale différents (
1f ).
Les données d'observation nous permettent de conclure que le composé 17 est bien adapté aux tests liés à la poche détectée dans la capside virale.
Afin de mieux prendre en compte le processus d'interaction du composé 17 et de la capside virale CVB3, les scientifiques ont réalisé une microscopie cryoélectronique.
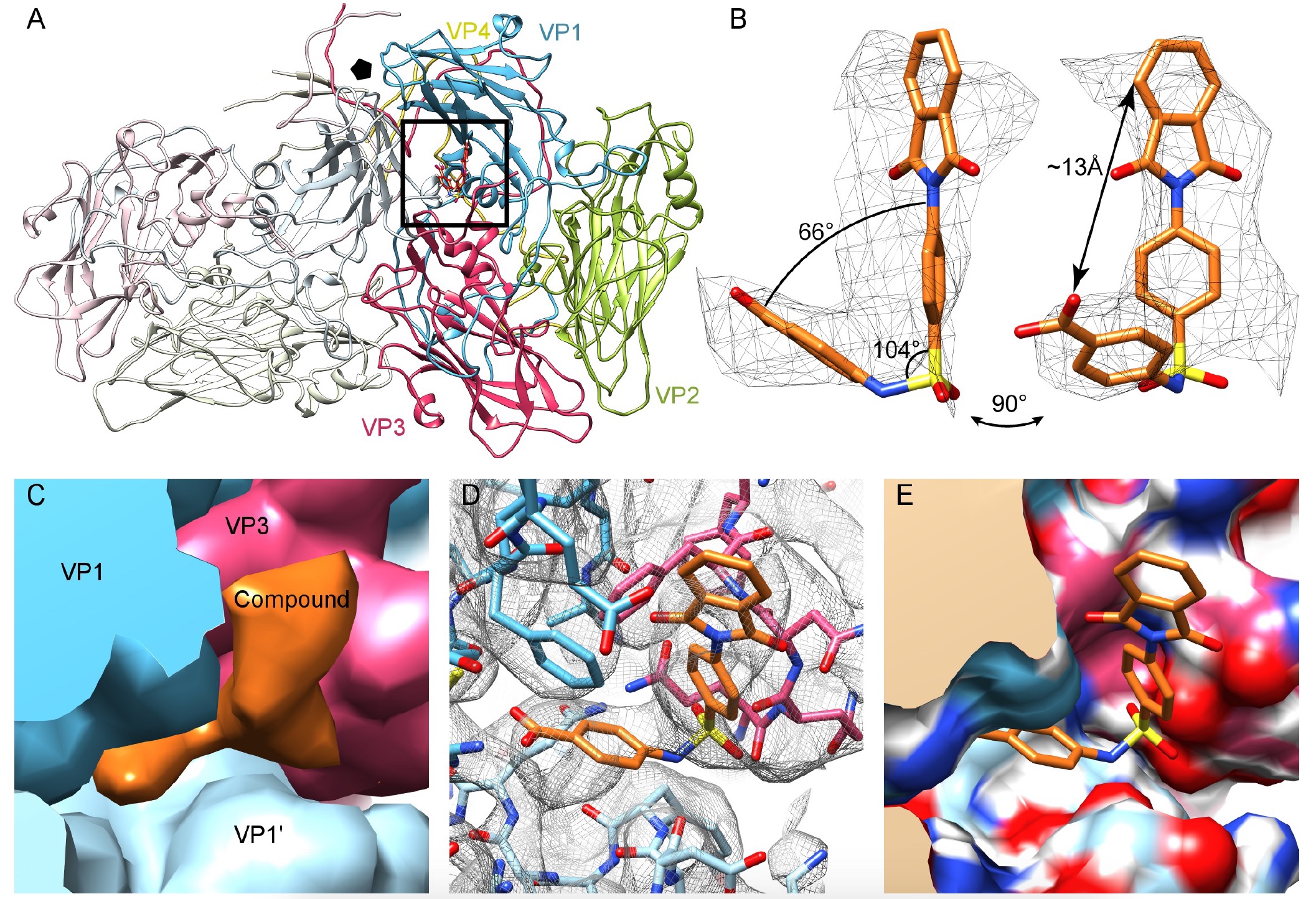 Image n ° 2
Image n ° 2Les chaînes latérales de la protéine de capside ont été facilement identifiées et le modèle d'homologie Nancy CVB3 pourrait facilement s'intégrer dans la carte du phoque. De plus, la souche cryo-EM de Nancy a montré un manque de compactage du facteur lipidique dans la poche hydrophobe de VP1. Cependant, une analyse des différences a révélé un compactage supplémentaire, qui peut être associé au modèle atomique du composé 17 (
2a ,
2c ).
Comme on peut le voir sur l'image 2b, le composé a une forme en L avec une épaule longue et courte, ce qui permet un «amarrage» avec la connexion 17. La simulation a montré que la connexion 17 est connectée dans la poche au moyen de deux blocs VP1 et d'un bloc VP3 sur l'interface du protoprotomère. En raison du type de symétrie icosaédrique du virus, il peut y avoir 60 régions de ce type dans une caspide (
2c ).
La région considérée est située à une distance de 16 Å de la poche hydrophobe visée par le pléconarile. Ainsi, le composé 17 ne fonctionne pas au même endroit que le pléconaril, c'est-à-dire sans interférer avec son activité antivirale, mais en le complétant.
Les scientifiques ont simulé les interactions au sein des protéines, des interfaces, des structures et des composés, qui ont montré les résidus VP1 (73, 75–78, 155–157,159–160, 219 et 234) et VP3 (233–236), qui forment une poche (
2d et
2e ) .
Une analyse de la conservation de ces résidus de poche dans les 56 séquences d'acides aminés de CVB3 a montré que 7 sur 16 sont complètement préservés (c'est-à-dire qu'il y a un composé 17 à l'intérieur), et environ 14 résidus ont montré un résultat de conservation de 97%. La conservation des poches se produit également dans tous les entérovirus du groupe B.
Cependant, tous les virus ne sont pas si facilement sensibles à l'inhibition par le composé 17. Par conséquent, il était nécessaire de comprendre ce qui les rend si résistants. Pour ce faire, les scientifiques ont procédé à une sélection clonale, mettant en évidence 4 mutations de résistance. Trois des quatre mutations d'acides aminés étaient situées à proximité immédiate de la poche (F76C, E78G et A98V), et une autre (D133G) était assez éloignée.
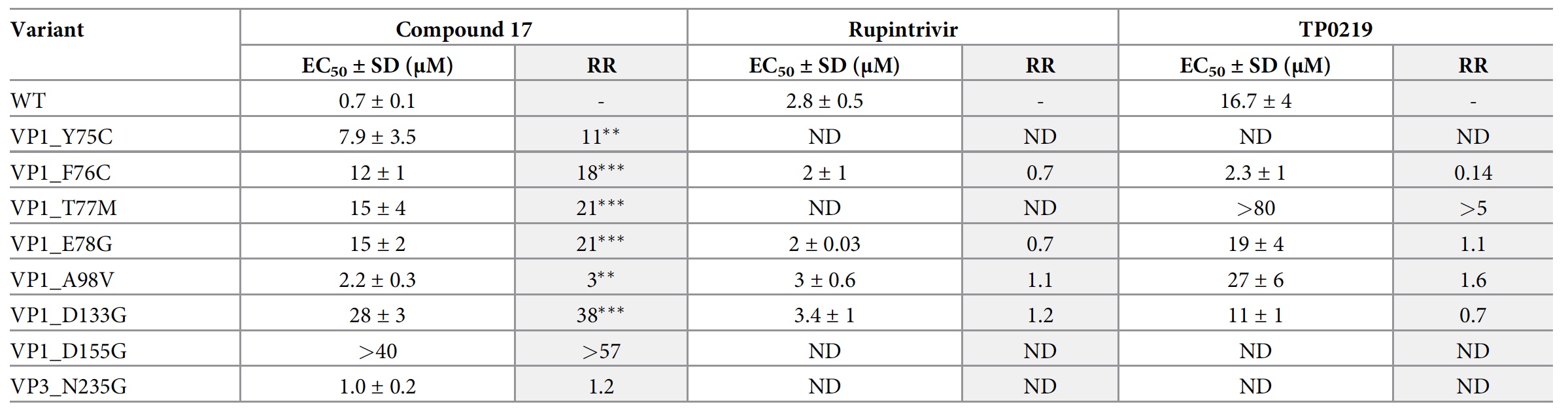 Étendue de l'effet du composé 17, du rupintrivir (inhibiteur de la protéase 3C) et du TP0219 (composé appauvrissant le glutathion) sur la réplication du CVB3 WT et les variantes modifiées du CVB3.
Étendue de l'effet du composé 17, du rupintrivir (inhibiteur de la protéase 3C) et du TP0219 (composé appauvrissant le glutathion) sur la réplication du CVB3 WT et les variantes modifiées du CVB3.Les scientifiques ont préparé 12 mutants CVB3 dans le clone CVB3 par rétro-ingénierie. Une variante indépendante du glutathion VPB1_T77M CVB3 a également été créée qui résiste au composé appauvrissant le glutathion TP0219.
Seuls huit des 12 mutants étaient viables (
2d ), 7 d'entre eux étaient résistants au composé 17 et réagissaient également au rupintrivir.
L'examen de la seule mutation résistante loin de la poche a montré que VP1_D133G est plus résistant à la chaleur que CVB3 Nancy, et le composé 17 peut encore le stabiliser. Autrement dit, VP1_D133G est une mutation compensatoire, et non une mutation qui empêche la liaison du composé 17.
Mais VP1_T77 a été impliqué dans la liaison du glutathion. L'analyse a montré que la variante VP1_T77M CVB3 indépendante du glutathion a une sensibilité réduite au composé 17. Il a également été constaté que l'ester éthylique du glutathion n'avait aucun effet sur l'activité antivirale du composé 17 même à la concentration la plus élevée testée.
Ensuite, les scientifiques ont vérifié le degré d'effet potentiel du composé 17 sur la liaison des récepteurs viraux. Pour cela, la protéine du virus Coxsackie humain et le récepteur d'adénovirus (hCAR) liés en chaîne ont été utilisés. L'affinité de liaison de CVB3 n'a pas diminué en présence du composé 17 même à la concentration la plus élevée testée. De plus, le composé 17 était actif contre l'entérovirus B
CD55-dépendant (virus E-11).
CD55 (facteur d'accélération de la décomposition du complément) * - protéine membranaire, inhibiteur du système du complément.
Les données expérimentales sont également confirmées par le fait que les sites de liaison du récepteur Coxsackie + adénovirus et CD55 + CVB3 ne se croisent pas avec la poche.
Ainsi, les scientifiques ont découvert que le composé 17 s'intègre parfaitement dans la poche de capside de divers virus. La prochaine étape de l'étude consiste à vérifier l'efficacité du médicament introduit dans cette poche.
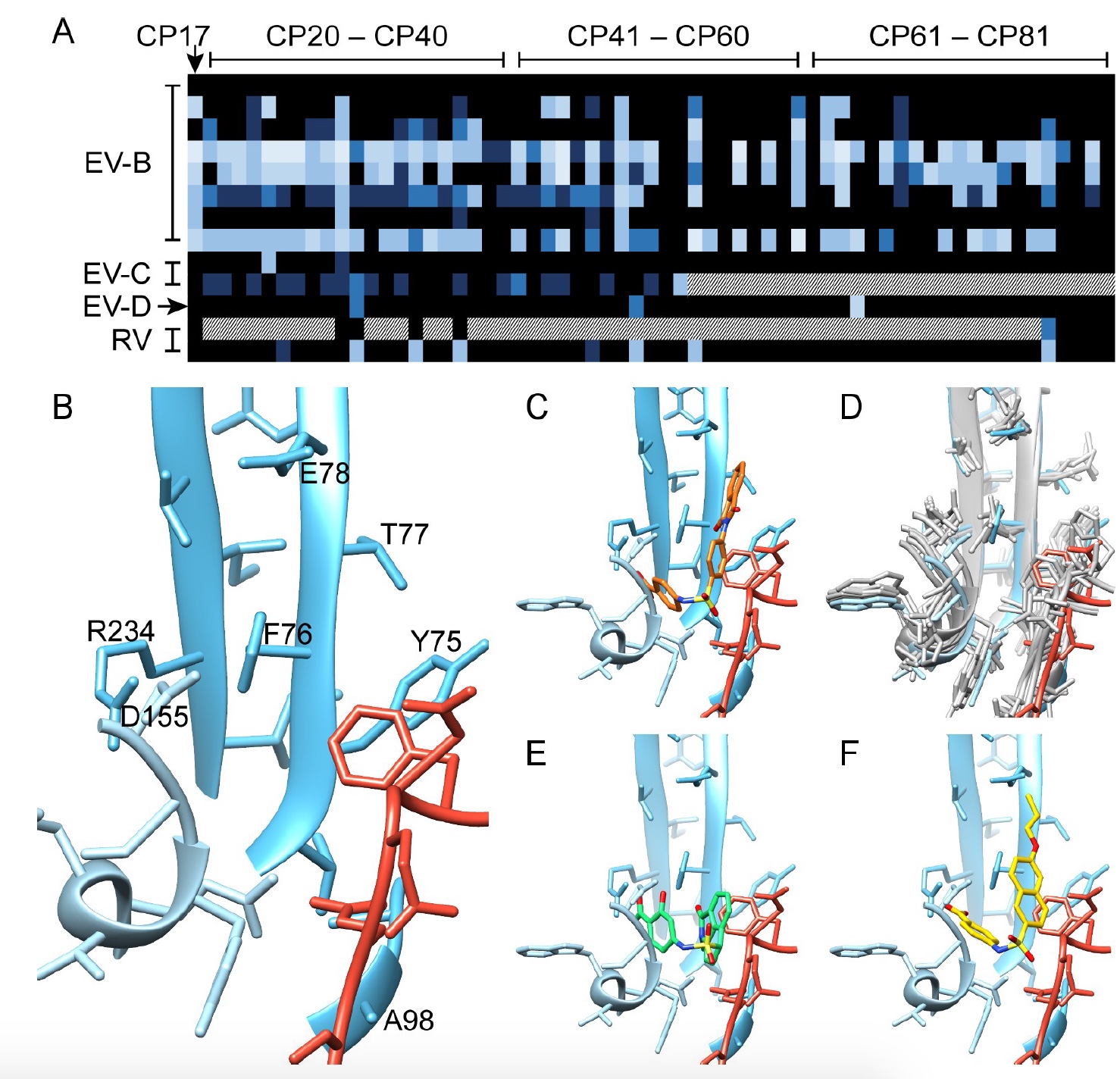 Image n ° 3
Image n ° 3Au cours de cet essai, des substances disponibles dans le commerce (composés 20 à 50) et des modifications apportées en laboratoire - composés 51 à 81 - ont été utilisées.
La connaissance de l'activité du composé 17 a permis d'isoler les caractéristiques spécifiques nécessaires à la préparation future. Les scientifiques ont analysé les informations provenant d'essais antiviraux et les ont utilisées dans la synthèse d'analogues plus actifs du composé 17.
La synthèse a abouti à des analogues actifs contre un certain nombre d'entérovirus: EV-B (CVB), EV-C (PV1 et CVA21), EV-D (EVD68), RV-A (RVA09, RVA59 et RVA63) et RV-B ( RVB14) (
3a ). Malheureusement, aucun des composés créés n'était actif contre les virus EVA (CVA16 et EVA71).
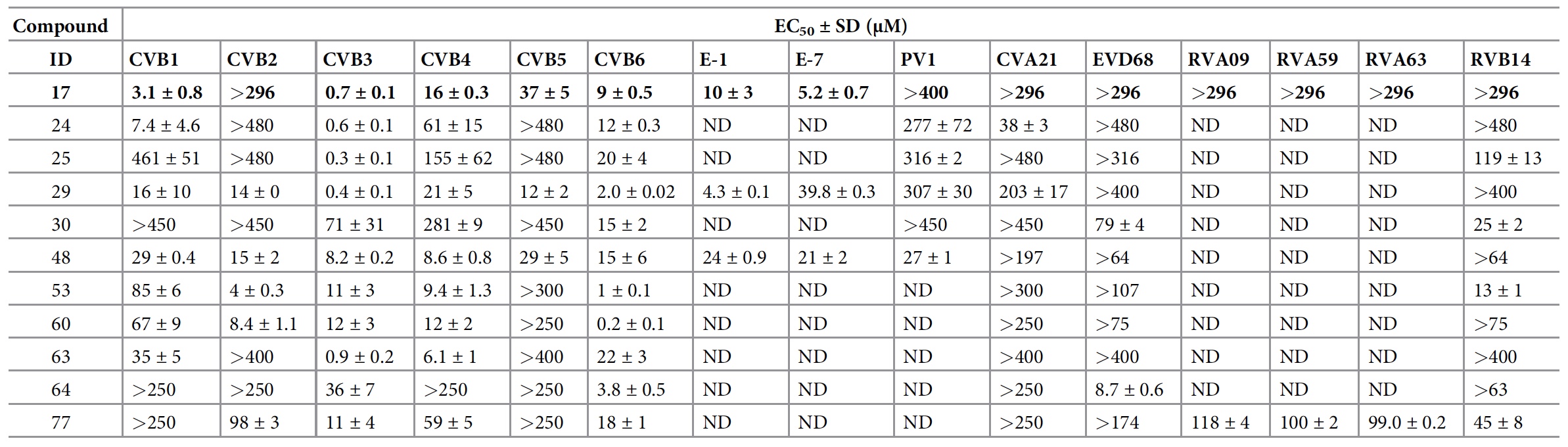 Composés ayant une activité potentielle maximale vis-à-vis de certains virus.
Composés ayant une activité potentielle maximale vis-à-vis de certains virus.Parmi tous les analogues, les composés 29 et 48 étaient actifs contre les 6 CVB testés (virus Koskashi du groupe B). Le composé 48 a complètement inhibé la réplication de PV1 à une concentration de 144 uM. Le composé 77 a montré une activité antivirale contre RV-A et RV-B.
Comme le montre l'image n ° 3, la forme des nouvelles molécules complète la forme de la poche. Les scientifiques ont pu établir une relation structure-propriété claire (la structure chimique de la molécule à son activité biologique) à partir du groupe carboxyle en position R3, où l'atome d'hydrogène est nécessaire pour l'activité antivirale, et en position R2, où le groupe hydroxyle démontre son avantage pour un large effet antiviral. La structuration cryogénique a montré qu'il existe une complémentarité de charge entre R3 et le résidu inhibé VP1_R234.
La totalité des résultats des tests indique un degré assez élevé de mise en œuvre des composés testés dans les poches des virus de la capside de différents groupes.
Pour une connaissance plus détaillée des nuances de l'étude, je vous recommande de consulter le rapport des scientifiques (
ici ou
ici )
Épilogue
En résumé, les scientifiques ont révélé des poches dans la structure des entérovirus qui peuvent être remplies de médicaments qui empêchent la propagation du virus ou le détruisent complètement.
Le caractère principal était le composé 17 et ses analogues modifiés, qui montraient un haut degré d'activité contre CVB3. Les poches identifiées sont assez similaires les unes aux autres dans différents groupes de virus, ce qui permet le développement ultérieur de médicaments avec un large spectre d'action.
En d'autres termes, les virus que personne n'a précédemment traités peuvent désormais être facilement surmontés. Bien sûr, s'appuyer uniquement sur le système immunitaire humain n'est pas l'idée la plus sensée, étant donné le nombre de maladies et d'anomalies qui peuvent perturber son travail, ouvrant les portes du corps humain à une variété de virus. Ces recherches et développements sont extrêmement importants à notre époque, compte tenu de la population de la planète et du taux d'urbanisation. Et ces indicateurs affectent considérablement le taux de propagation des infections virales. De plus, ayant un médicament qui peut vaincre le virus dans la racine, une personne n'a pas besoin de traiter chaque symptôme individuellement, c'est-à-dire d'acheter un tas d'autres médicaments (gouttes, sprays, comprimés, suspensions, etc., etc.).
Les scientifiques poursuivront leur travail, en se concentrant sur la recherche de composés qui seront les plus efficaces contre le nombre maximal possible de virus. Nous ne pouvons que leur souhaiter bonne chance et, jusqu'à ce qu'ils aient terminé leur travail, lutter seuls contre le froid.
Vendredi hors-dessus:Non seulement les gens souffrent de virus, mais aussi d'ordinateurs et parfois de personnages animés. ( La deuxième série est ici.)Merci de votre attention, restez curieux, prenez soin de votre santé et passez un excellent week-end pour tout le monde. :)
Merci de rester avec nous. Aimez-vous nos articles? Vous voulez voir des matériaux plus intéressants? Soutenez-nous en passant une commande ou en le recommandant à vos amis, une
réduction de 30% pour les utilisateurs Habr sur un analogue unique de serveurs d'entrée de gamme que nous avons inventés pour vous: Toute la vérité sur VPS (KVM) E5-2650 v4 (6 cœurs) 10 Go DDR4 240 Go SSD 1 Gbps à partir de 20 $ ou comment diviser le serveur? (les options sont disponibles avec RAID1 et RAID10, jusqu'à 24 cœurs et jusqu'à 40 Go de DDR4).
Dell R730xd 2 fois moins cher? Nous avons seulement
2 x Intel TetraDeca-Core Xeon 2x E5-2697v3 2.6GHz 14C 64GB DDR4 4x960GB SSD 1Gbps 100 TV à partir de 199 $ aux Pays-Bas! Dell R420 - 2x E5-2430 2.2Ghz 6C 128GB DDR3 2x960GB SSD 1Gbps 100TB - à partir de 99 $! Pour en savoir plus sur la
création d'un bâtiment d'infrastructure. classe utilisant des serveurs Dell R730xd E5-2650 v4 coûtant 9 000 euros pour un sou?