
Apa yang kita ingat dengan frasa "fiksi ilmiah"? Tentu saja, robot, mobil terbang, studi tentang sudut-sudut Semesta yang sebelumnya belum dijelajahi, alien, dan serangkaian plot. Di antara mereka, sebuah tempat khusus selalu dihuni oleh tema menetap planet lain, baik dari kepercayaan pada kematian yang tak terhindarkan dari seseorang sendiri, atau dari keinginan untuk secara radikal mengubah situasi. Pesaing pertama untuk judul Earth 2.0 selalu Mars, dingin dan tak bernyawa. Saat ini, masih belum memungkinkan untuk mengemas tas Anda dan terbang ke Mars berlibur selama dua minggu, tetapi ini benar-benar realistis dan layak, pertanyaannya adalah seberapa cepat. Minus Mars yang paling mencolok (dengan pengecualian kurangnya internet normal) adalah kurangnya atmosfer yang dapat diterima untuk kehidupan. Untuk terbang ke tujuan, keluar dari pesawat dan bernafas dalam-dalam, rasakan semua kesegaran udara lokal - ini bukan tentang Mars. Tapi ini tidak selalu terjadi.
Hari ini kami akan bertemu dengan Anda sebuah studi yang menjelaskan metode baru untuk menghasilkan oksigen melalui reaksi kimia yang tidak biasa. Bagaimana para ilmuwan menghasilkan oksigen molekuler dari CO
2 , seberapa efektif metode ini, dan di mana dapat digunakan selain perjalanan antarplanet? Kami akan mencari jawaban atas pertanyaan-pertanyaan ini dalam laporan para ilmuwan. Ayo pergi.
Dasar studi
Seseorang hanya membutuhkan tiga hal untuk hidup: makanan, air dan udara, di mana akan ada cukup oksigen. Ini adalah kebutuhan utama kami (ya, Internet tidak ada dalam daftar ini). Tetapi oksigen tidak terletak di jalan, terutama di luar planet kita yang tercinta. Karena itu, jika kita ingin pergi ke suatu tempat, kita perlu membawanya dan menggunakan berbagai perangkat untuk membersihkan udara dan menggunakannya kembali. Semua kegembiraan ini terjadi di banyak tempat, dan cepat atau lambat oksigen akan habis. Dan mengisi kembali cadangan di ruang angkasa atau di Mars akan, secara sederhana, bermasalah.
Namun, relatif baru-baru ini, para ilmuwan menemukan sejumlah besar oksigen dalam komet 67P / CG6, yang mendorong mereka untuk mengajukan pertanyaan yang sangat jelas - dari mana asalnya? Oksigen dalam tubuh seperti komet adalah hasil dari reaksi abiotik yang terjadi pada kondisi ekstrem, di mana dari H
2 O, CO
2 , CO, dll. O
2 (oksigen) dilepaskan. Para ilmuwan mengklaim bahwa reaksi semacam itu dapat menjelaskan keberadaan oksigen di komet, atmosfer atas Mars, dan atmosfer awal Bumi. Seseorang dapat menggunakan reaksi kimia semacam itu untuk menghasilkan O
2 dari CO
2 , yang akan membuat Mars cocok untuk kehidupan.
Jika sangat berlebihan dan singkat, maka reaksi yang disebutkan di atas adalah dekomposisi CO
2 menjadi komponen: C + O
2 . Dengan kata lain, disosiasi.
Pemisahan CO
2 dapat terjadi dalam beberapa skenario tergantung pada energi yang tersedia untuk reaksi. Disosiasi parsial CO
2 → CO + O (5.43 atau 7.56 eV) membutuhkan energi paling sedikit. Ada juga disosiasi lengkap CO
2 → C + O + O, membutuhkan 16,46 eV. Dan, disosiasi yang paling aneh dan eksotis adalah ketika CO
2 terurai menjadi C dan O
2 . Perhitungan menunjukkan bahwa reaksi serupa terjadi pada permukaan energi potensial dari keadaan dasar, mula-mula membentuk senyawa CO
2 perantara siklik [c-CO
2 (
1 A
1 )], yang kemudian berubah menjadi COO menengah antara (
1 Σ
+ ) dalam perjalanan menuju disosiasi dalam C + O
2 .
Reaksi semacam itu mungkin terjadi jika molekul "bengkok" sehingga kedua atom O menjadi sedekat mungkin satu sama lain. Ini membutuhkan 6 eV energi internal. Dan, Anda harus mengakui, tidak peduli seberapa kuat pria menekuk batang logam, akan jauh lebih sulit untuk menekuk molekul.
Transisi ke keadaan anionik yang tereksitasi secara elektronik dan CO
2 dapat membantu menekuk molekul. Para ilmuwan ingat bahwa percobaan terbaru oleh rekan-rekan mereka telah menunjukkan bahwa penggunaan photoexcitation VUV (ultraviolet vakum) dan lampiran elektron memungkinkan pemisahan CO
2 ke C (
3 P) + O
2 (X
3 Σ
g -). Namun, belum ada yang sebelumnya mempelajari proses eksotis ini pada tingkat yang cukup rinci. Dan semua karena sebagai hasil dari percobaan tersebut tidak ada produk O
2 terionisasi ditemukan. Tetapi, seperti yang kita ketahui, tidak menemukan sesuatu tidak berarti bahwa itu tidak sama sekali.
Oleh karena itu, dalam penelitian yang kami teliti hari ini, para ilmuwan menerapkan metode hamburan berkas ion bersama dengan pemodelan matematika untuk menunjukkan cara baru untuk mengaktifkan reduksi langsung CO
2 ke O
2 dengan mendeteksi produk O
2 terionisasi. Proses ini mengandung jalur reaksi intramolekul yang sebelumnya tidak diketahui yang terjadi selama tumbukan ion aktif dan permukaan CO
2 . Yang paling mengejutkan adalah tidak adanya ketergantungan reaksi ini pada sifat dan suhu permukaan.
Hasil penelitian
Pertama-tama, para ilmuwan menunjukkan pembentukan O
2 dalam tumbukan hipertermik CO
2 + / Au dengan merencanakan distribusi energi kinetik dari tiga produk ion molekul yang tersebar (CO
2 + , O
2 + dan O
2 - ) untuk energi CO
2 + kejadian yang berbeda (E
0 ) . Pada E
0 <80 eV, sinyal yang sangat lemah dari CO
2 + tersebar terdeteksi (
1a , grafik di sebelah kiri).
 Gambar No. 1
Gambar No. 1Energi puncak CO
2 + yang keluar sebanding dengan E
0 , yaitu, ada kenaikan balistik atau berdenyut dari permukaan, yang tidak termasuk sputtering fisik. Para ilmuwan percaya bahwa mengamati sinyal CO
2 + "dinamis" sangat penting karena bukti bahwa beberapa CO
2 selamat dari tabrakan permukaan. Selain itu, seseorang dapat menentukan urutan tumbukan atom penyusunnya. Selain CO
2 + , sinyal ion O
2 yang tersebar juga diamati (
1b ,
1c / grafik di tengah dan di sebelah kanan). Dalam hal ini, energi dari O
2 + dan O
2 yang dilepaskan
- mewakili sebagian besar energi dari partikel-partikel insiden (57%) dan secara seragam meningkatkan paralel dengan E
0 dalam rentang yang lebih luas daripada CO
2 + yang tersebar. Sinyal maksimum ion O
2 diamati pada E
0 ~ 100 eV.
Para peneliti menyebut penemuan produk ion O
2 mengejutkan, karena atomisasi permukaan O
2 maupun abstraksi atom O tidak dapat menjelaskan pembentukan ion-ion ini. Dan semua karena kedua mekanisme ini akan menghasilkan O
2 pada energi output yang jauh lebih rendah daripada yang diamati. Adalah logis untuk berasumsi bahwa disosiasi CO
2 sangat terlibat di sini.
Disosiasi CO
2 secara parsial dan komplit sesuai dengan produk ionik lain yang terdeteksi (CO
+ , CO
- , O
+ , O
- dan C
+ ). Dan energi dari CO
+ , CO
- dan O
- berubah secara paralel dengan energi dari partikel-partikel yang terjadi, yang konsisten dengan formasi dinamis dalam tumbukan permukaan.
Tetapi puncak O
+ dan C
+ menunjukkan ketergantungan yang sangat kecil pada E
0 , yang menunjukkan asal yang berbeda, yaitu penyemprotan. Konfirmasi disosiasi lengkap tersebar produk C
+ , yang memanifestasikan diri pada E
0 > 80 eV.
Selanjutnya, para ilmuwan menggunakan kinematika untuk menggambarkan mekanisme hamburan.
Teori tabrakan biner (BPS) memungkinkan kita untuk menghitung faktor kinematik, yang didefinisikan sebagai fraksi energi dari partikel-partikel kejadian, yang dipegang oleh produk yang tersebar keluar dari permukaan. Dalam model paling sederhana, CO
2 + tersebar sebagai satu molekul utuh, mis. sebagai bola padat dengan massa atom 44 Da. Dalam hal ini, BPS memprediksi koefisien kinematik 0,6349, yang berkorelasi agak lemah dengan data (
2a ).
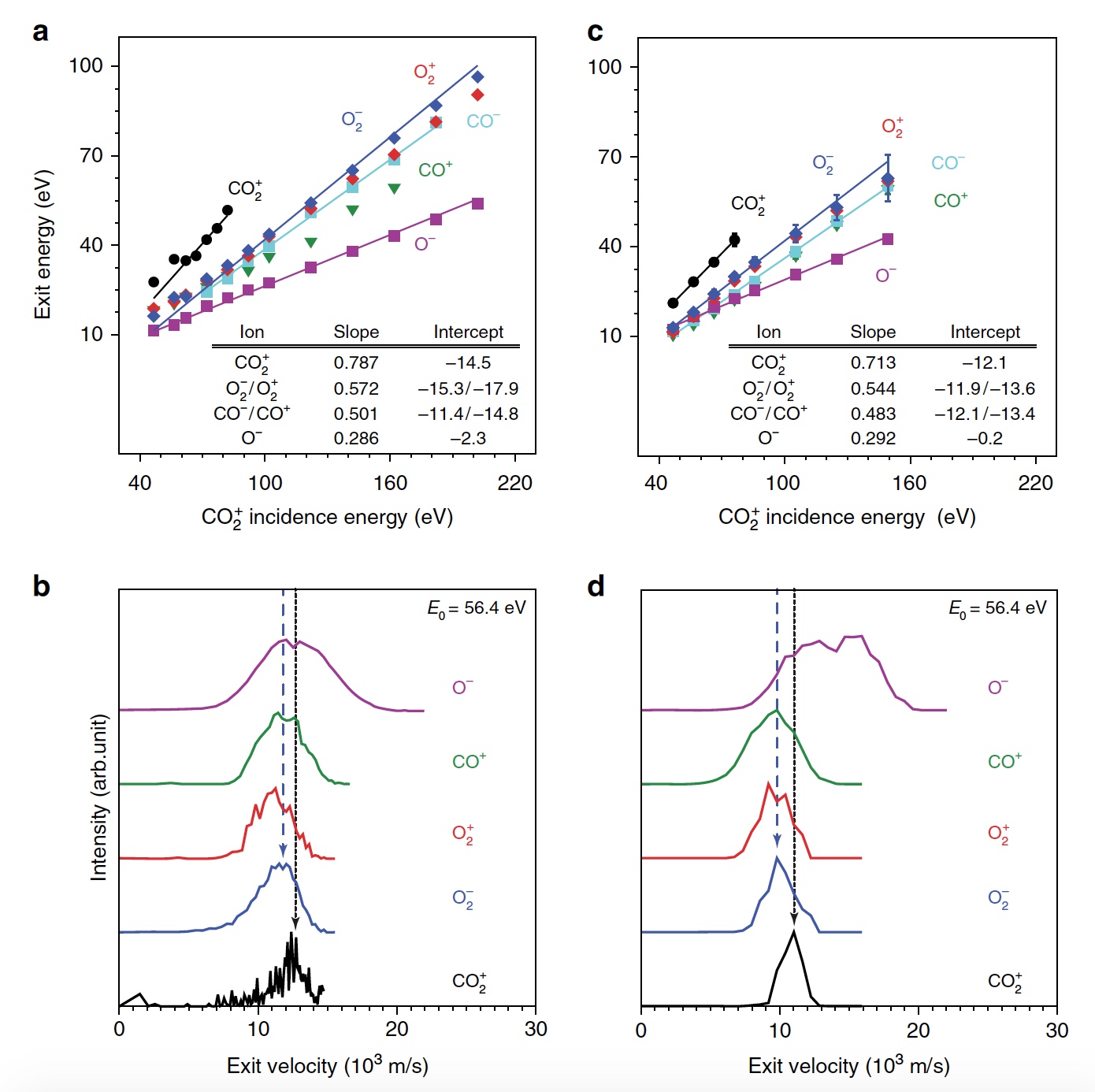 Gambar No. 2
Gambar No. 2Setelah itu, para ilmuwan menerapkan model di mana atom O pertama kali bertabrakan dengan permukaan atom Au, dan kemudian tumbukan kedua dari fragmen CO terjadi tanpa pemisahan cepat dari molekul CO
2 . Penerapan BPS pada model tabrakan berturut-turut ini memberikan koefisien kinematik 0,7870, yang sangat sesuai dengan data energi CO
2+ yang keluar (garis hitam pada
2a ). Grafik
2a juga menunjukkan energi dari produk ionik tersebar lainnya.
Sumber potensial utama dari produk tersebut dapat disebut disosiasi sebagian atau seluruhnya dari CO
2 dan penyemprotan permukaan dari fragmen-fragmen CO
2 yang teradsorpsi. Terlepas dari kenyataan bahwa beberapa pemercikan memang diamati pada nilai E0 yang tinggi (> 140 eV), analisis kinematik data tentang energi partikel yang keluar memberikan bukti yang meyakinkan tentang adanya disosiasi berdenyut yang tepat dari molekul CO
2 .
Selanjutnya, para ilmuwan melakukan analisis terhadap kecepatan partikel yang terpencar yang diamati.
Gambar
2b menunjukkan perbandingan puncak distribusi ion pada E
0 = 56,4 eV. Seperti yang dapat kita lihat, laju keluar dari CO
+ yang tersebar, O
2 + , O
2 - dan bagian yang lebih lambat dari tumpang tindih distribusi O, yang menunjukkan asal yang sama. Namun, distribusi O terasa lebih luas, meluas ke kecepatan output yang lebih tinggi, yang dapat menunjukkan asal alternatif. Produk ion O
2 keluar pada tingkat yang lebih rendah dari CO
2 + karena ketidak elastisan karena pecahnya ikatan kimia dan ionisasi permukaan non-resonansi.
Analisis kinematik di atas, kata para ilmuwan, telah memberikan bukti konklusif bahwa beberapa molekul CO
2 tersebar utuh setelah dua langkah tabrakan berurutan dari fragmen O dan CO. Namun, masih ada pertanyaan mengenai berbagai aspek mekanisme pembentukan O
2 .
Setelah percobaan, sejumlah pertanyaan tetap ada. Pertama, masih belum jelas apakah O
2 diproduksi oleh mekanisme adiabatik elektronik atau non-adiabatik. Kedua, jalur tumbukan yang mendasari distribusi kecepatan pada saat keluarnya fragmen ionik tidak diketahui. Ketiga, tidak diketahui berapa banyak O2 netral
terbentuk .
Dalam hal ini, pemodelan dapat memperjelas situasi, yaitu, metode dinamika molekul klasik (metode MD).
Untuk mensimulasikan lintasan hamburan CO
2 pada Au (111), hamburan geometri yang diamati dalam percobaan diterapkan. Diasumsikan bahwa CO
2 dilepaskan pada permukaan energi potensial dari elektron singlet dalam kasus netralisasi ion CO
2 + yang masuk sebelum tabrakan yang keras.
Netralisasi cepat terjadi melalui tunneling resonansi elektron dari permukaan logam ke kation molekul, karena tingkat molekul CO
2 (-13,8 eV) berada dalam zona Au yang diduduki (dari -5,3 ke -15,3 eV). Dalam simulasi, transfer elektron dari / ke permukaan juga diperhitungkan untuk memperhitungkan ionisasi produk tumbukan netral.
Gambar
2c menunjukkan nilai energi yang dihitung dari partikel yang keluar.
Ditemukan bahwa sejumlah kecil CO
2 mempertahankan integritas pada E
0 > 80 eV, yang konsisten dengan tidak adanya sinyal pada energi ini selama percobaan praktis. Data yang diperoleh melalui pemodelan sangat sesuai dengan data eksperimen, yang mudah dilihat dengan membandingkan grafik
2a (percobaan) dan
2c (simulasi).
Selain perjanjian antara eksperimen dan pemodelan ini, ia juga memanifestasikan dirinya dalam perbandingan laju ion keluaran pada E
0 = 56,4 eV (
2d ). Baik model dan percobaan menunjukkan perluasan distribusi kecepatan CO
+ dan O
- . Juga telah dikonfirmasi bahwa distribusi O2
+ dan O2
- mirip dengan kation yang meninggalkan lebih lambat daripada anion. Selain itu, dalam kedua kasus, ditemukan bahwa CO
2 + muncul pada tingkat yang lebih tinggi daripada produk O
2 terionisasi.
Oleh karena itu, penggunaan teknik pemodelan ini dapat memberikan data yang cukup akurat mengenai mekanisme reaksi konversi langsung CO
2 menjadi O
2 .
Selama tahap utama simulasi, 20.000 lintasan tabrakan CO
2 -on-Au diciptakan kembali pada energi yang berbeda dari partikel yang keluar. Akibatnya, beberapa varian produk disosiasi diperoleh, termasuk O
2 (
3a ).
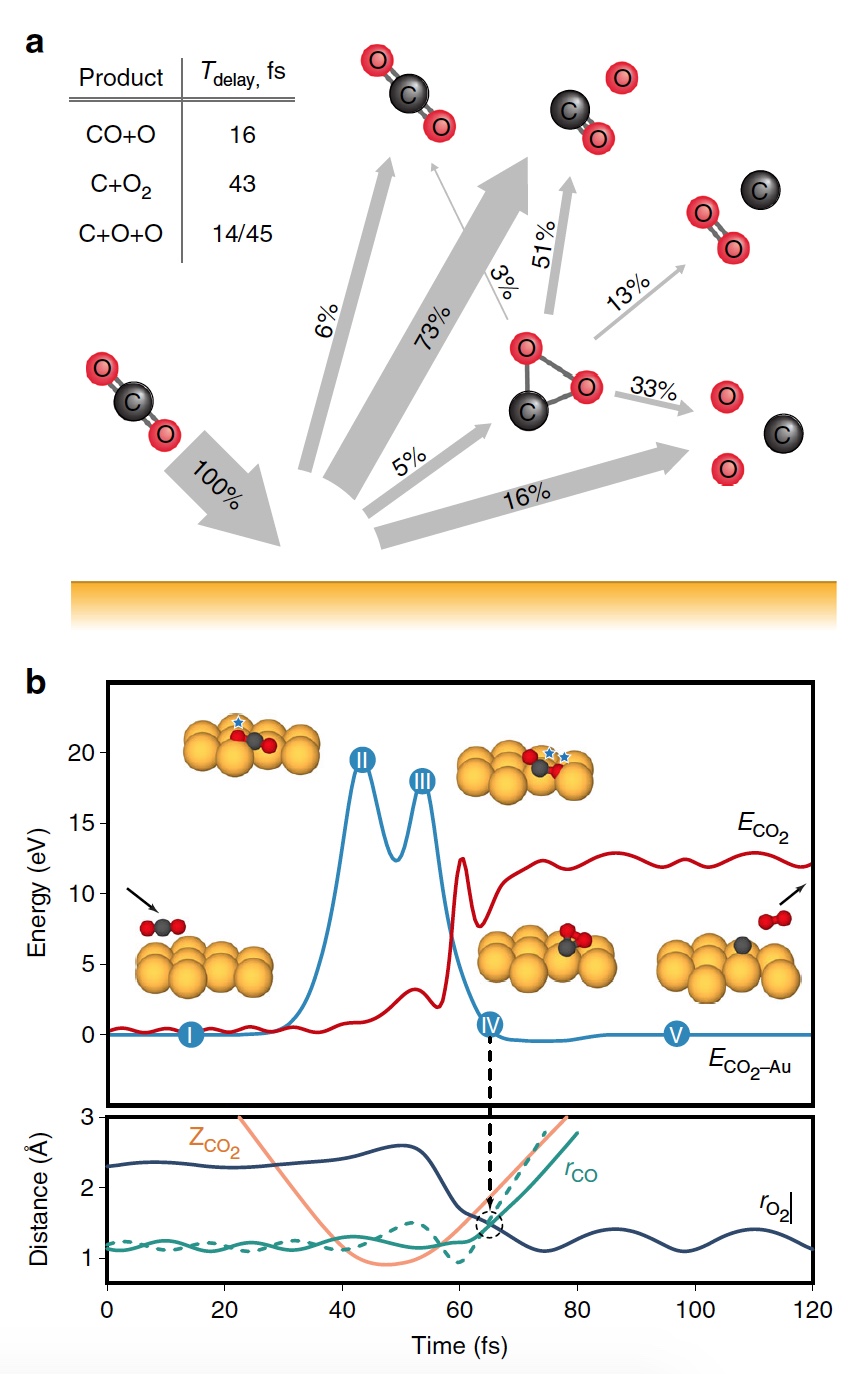 Gambar No. 3
Gambar No. 3Gambar
3b menunjukkan lintasan representatif yang menghasilkan pembentukan O
2 . Sebagai hasil dari transfer energi berdenyut selama tabrakan, penataan ulang intramolekul yang signifikan terjadi di dalam bouncing CO
2 . Jarak O - O menurun, dan jarak C - O meningkat, mencapai puncaknya ketika CO
2 memperoleh konfigurasi segitiga dengan panjang ikatan yang hampir sama. Produk CO
2 antara yang sangat bengkok seperti itu memiliki jumlah energi internal yang besar dan cepat terdisosiasi, menghasilkan pembentukan atom C bebas dan molekul O
2 yang bergetar secara panas.
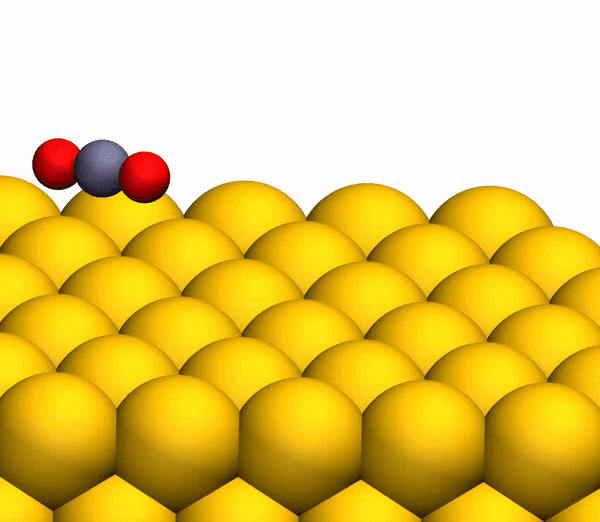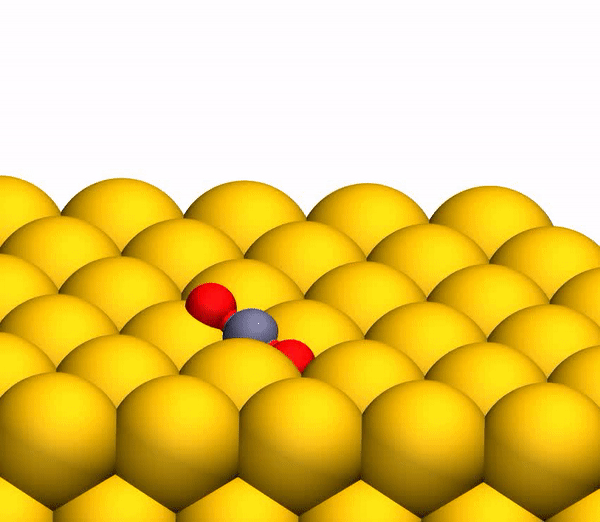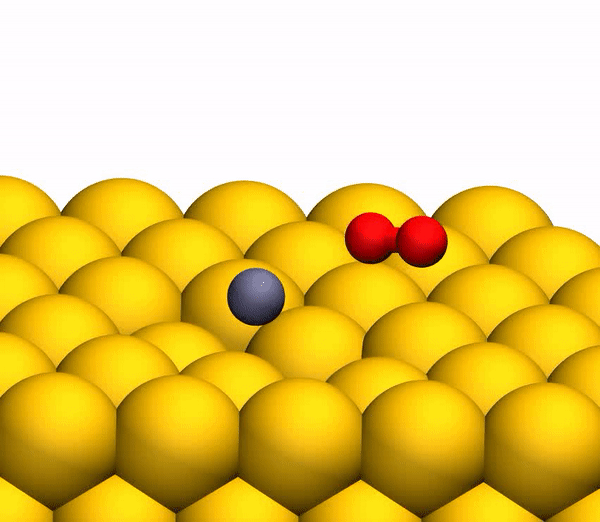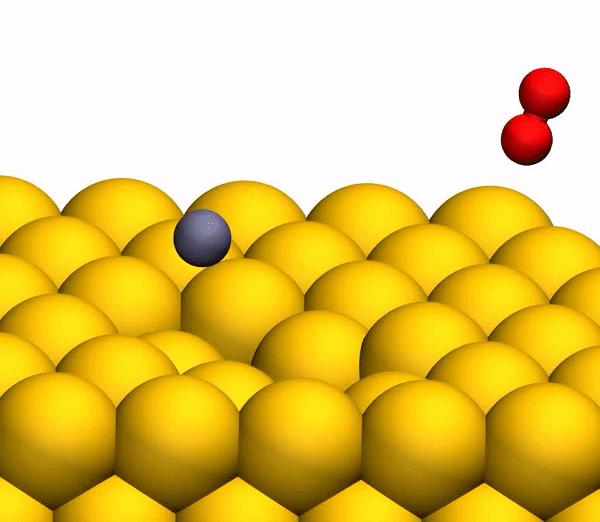 Proses pemisahan CO 2 menjadi atom C bebas dan molekul O 2 yang bergetar secara panas.
Proses pemisahan CO 2 menjadi atom C bebas dan molekul O 2 yang bergetar secara panas.Perlu dicatat bahwa mekanisme pemisahan yang dijelaskan di atas sepenuhnya konsisten dengan kesimpulan model kinematik yang digunakan sebelumnya.
Perhitungan menunjukkan bahwa sekitar 5% dari semua lintasan mengarah ke keadaan menengah CO
2 yang sangat bengkok, yang merupakan salah satu tahap ekstraksi O
2 . Kondisi ini terfragmentasi terutama melalui disosiasi parsial (51%), setelah disosiasi lengkap terjadi lagi, tetapi dengan hasil yang lebih tinggi (33%).
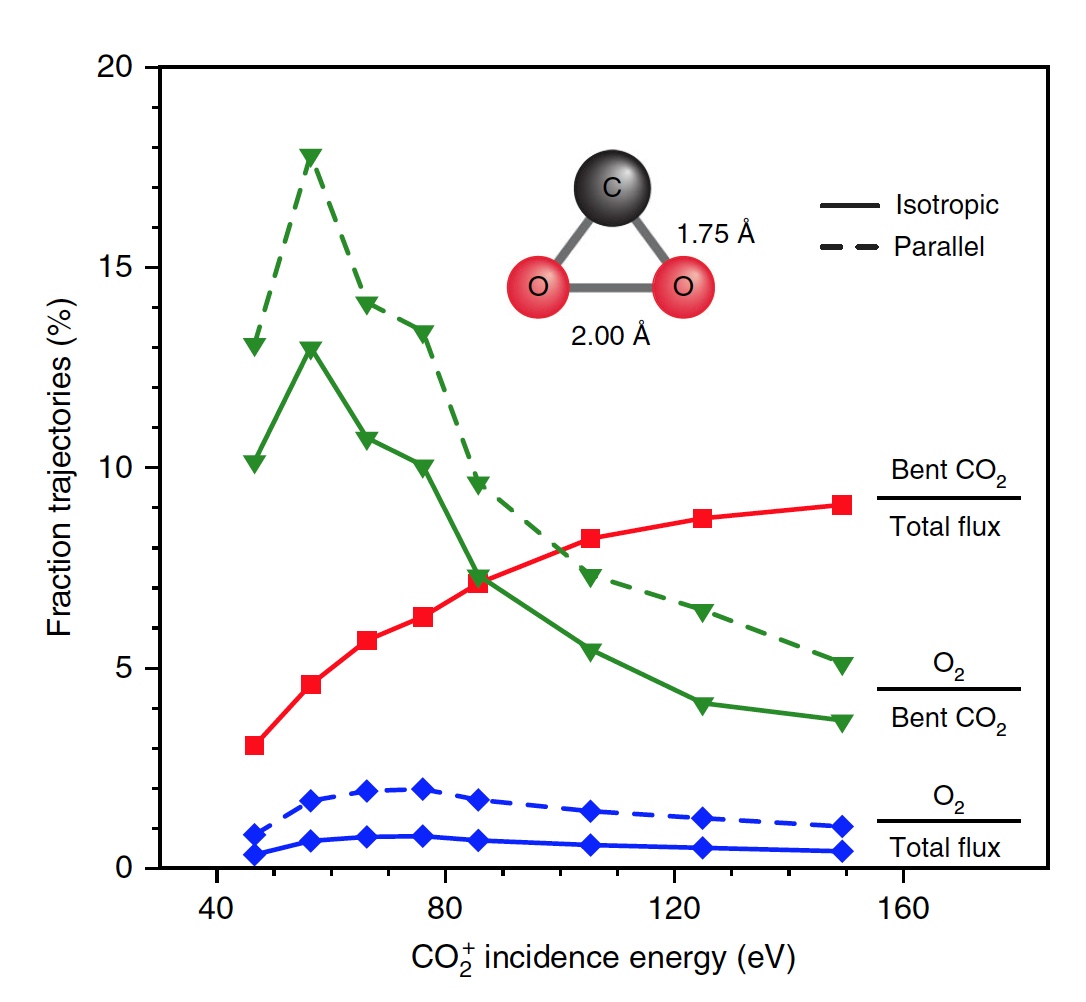 Gambar No. 4
Gambar No. 4Para ilmuwan mencatat bahwa dari semua molekul CO
2 yang melengkung, hanya 13 persen yang menghasilkan oksigen. Yaitu, hasil keseluruhan dari disosiasi CO
2 → C + O
2 adalah 0,6% pada E
0 = 56,4 eV. Jika Anda meningkatkan energi partikel yang terjadi, maka Anda bisa mendapatkan O
2 hingga 0,8 ± 0,2% pada E
0 ~ 70 ± 15 eV (garis biru pada gambar No. 4).
Selain itu, fraksi lintasan pembentukan O
2 meningkat secara signifikan ketika keadaan menengah CO
2 (garis hijau) yang ditekuk kuat tercapai, mencapai maksimum 13% pada E
0 ~ 55 ± 10 eV. Hasil total yang lebih rendah dari O2 netral disebabkan oleh kenyataan bahwa hanya sebagian kecil molekul CO
2 linier mencapai keadaan bengkok kuat (garis merah). Jika Anda secara spesifik mengubah orientasi molekul CO
2 yang masuk (poros sejajar dengan permukaan), maka sebagai hasilnya, Anda bisa mendapatkan 2% lebih banyak O
2 (garis hijau putus-putus).
Untuk seorang kenalan yang lebih mendetail dengan nuansa penelitian, saya sarankan Anda membaca
laporan para ilmuwan .
Epilog
Pekerjaan ini telah menunjukkan bahwa melalui reaksi kimia non-standar dimungkinkan untuk mendapatkan oksigen dari karbon dioksida. Tidak seorang pun akan berpendapat bahwa teknik seperti itu membutuhkan penyempurnaan dan peningkatan lebih lanjut. Namun, fakta bahwa karya ini benar-benar membuka kemungkinan baru untuk perjalanan antarplanet, penjajahan Mars, dan tidak hanya tidak dapat disangkal. Ada juga masalah dengan oksigen dan karbon dioksida di planet rumah kita. Sebaliknya, dengan yang terakhir, volumenya telah meningkat secara signifikan sejak industrialisasi. Dan mengingat bahwa CO
2 adalah salah satu penyebab utama pemanasan global, mengurangi jumlahnya dan mendapatkan oksigen dari kedengarannya seperti ide yang sangat menggoda. Karena kita masih tidak dapat melakukannya tanpa pabrik, pabrik, mobil dengan mesin pembakaran internal dan hal-hal lain, metode baru untuk membersihkan atmosfer kita tidak hanya diperlukan, tetapi juga sangat diperlukan. Untuk melakukan perjalanan ke planet yang jauh tentu saja keren, tetapi sebelum perpindahan besar-besaran ke Mars masih sangat, sangat jauh, oleh karena itu lebih baik memikirkan lebih banyak tentang Bumi tempat kita hidup daripada tentang Mars, tentang yang kita impikan.
Terima kasih atas perhatian Anda, tetap ingin tahu dan selamat bekerja, kawan! :)
Terima kasih telah tinggal bersama kami. Apakah Anda suka artikel kami? Ingin melihat materi yang lebih menarik? Dukung kami dengan melakukan pemesanan atau merekomendasikannya kepada teman-teman Anda,
diskon 30% untuk pengguna Habr pada analog unik dari server entry-level yang kami temukan untuk Anda: Seluruh kebenaran tentang VPS (KVM) E5-2650 v4 (6 Cores) 10GB DDR4 240GB SSD 1Gbps dari $ 20 atau bagaimana membagi server? (opsi tersedia dengan RAID1 dan RAID10, hingga 24 core dan hingga 40GB DDR4).
Dell R730xd 2 kali lebih murah? Hanya kami yang memiliki
2 x Intel TetraDeca-Core Xeon 2x E5-2697v3 2.6GHz 14C 64GB DDR4 4x960GB SSD 1Gbps 100 TV dari $ 199 di Belanda! Dell R420 - 2x E5-2430 2.2Ghz 6C 128GB DDR3 2x960GB SSD 1Gbps 100TB - mulai dari $ 99! Baca tentang
Cara Membangun Infrastruktur Bldg. kelas menggunakan server Dell R730xd E5-2650 v4 seharga 9.000 euro untuk satu sen?