[
* Judul artikel ini merujuk pada nama album studio pertama Fatboy Slim, "Better Living Through Chemistry" / approx. perev. ]

Baterai timbal-asam tidak bisa disebut keajaiban teknik modern. Ini sangat andal dan mudah digunakan, dan untuk mengisi daya, Anda hanya perlu menerapkan tegangan tetap dan menunggu sedikit; akibatnya, baterai terisi dan tetap terisi penuh - itu saja. Di sisi lain kesederhanaan ini adalah ukuran, berat, kepadatan energi, dan toksisitas bahan.
Baterai lithium adalah hit modern, namun, kepadatan energi yang tinggi mengarah pada fakta bahwa kasing kecilnya dapat menjadi marah dan menjadi sangat berbahaya jika dianiaya. Para ilmuwan sedang mencari opsi baterai yang lebih aman, sistem pengisian yang ditingkatkan, formula untuk memperpanjang masa pakai baterai yang dapat diisi ulang ribuan kali, dan satu publikasi baru-baru ini telah menyebabkan banyak tanggapan yang antusias.
Pertimbangkan persyaratan untuk sel baterai di dalam kendaraan listrik:
- Kepadatan energi tinggi (sejumlah besar energi dalam baterai kecil).
- Kemungkinan pengisian cepat.
- Kemungkinan debit cepat.
- BANYAK siklus pengisian / pengosongan.
- Debit diri rendah.
- Keamanan
Saat ini, baterai lithium-ion adalah pilihan terbaik, tetapi ada banyak reaksi kimia dengan lithium, dan tergantung pada rencana penggunaan, keseimbangan dan pengisian, dimungkinkan untuk mengoptimalkan berbagai varian reaksi untuk karakteristik operasi yang berbeda. Meskipun tidak ada baterai yang sempurna, dan permintaan yang saling bertentangan menjamin ketersediaan beberapa opsi di pasar.
Cara kerja ion lithium +
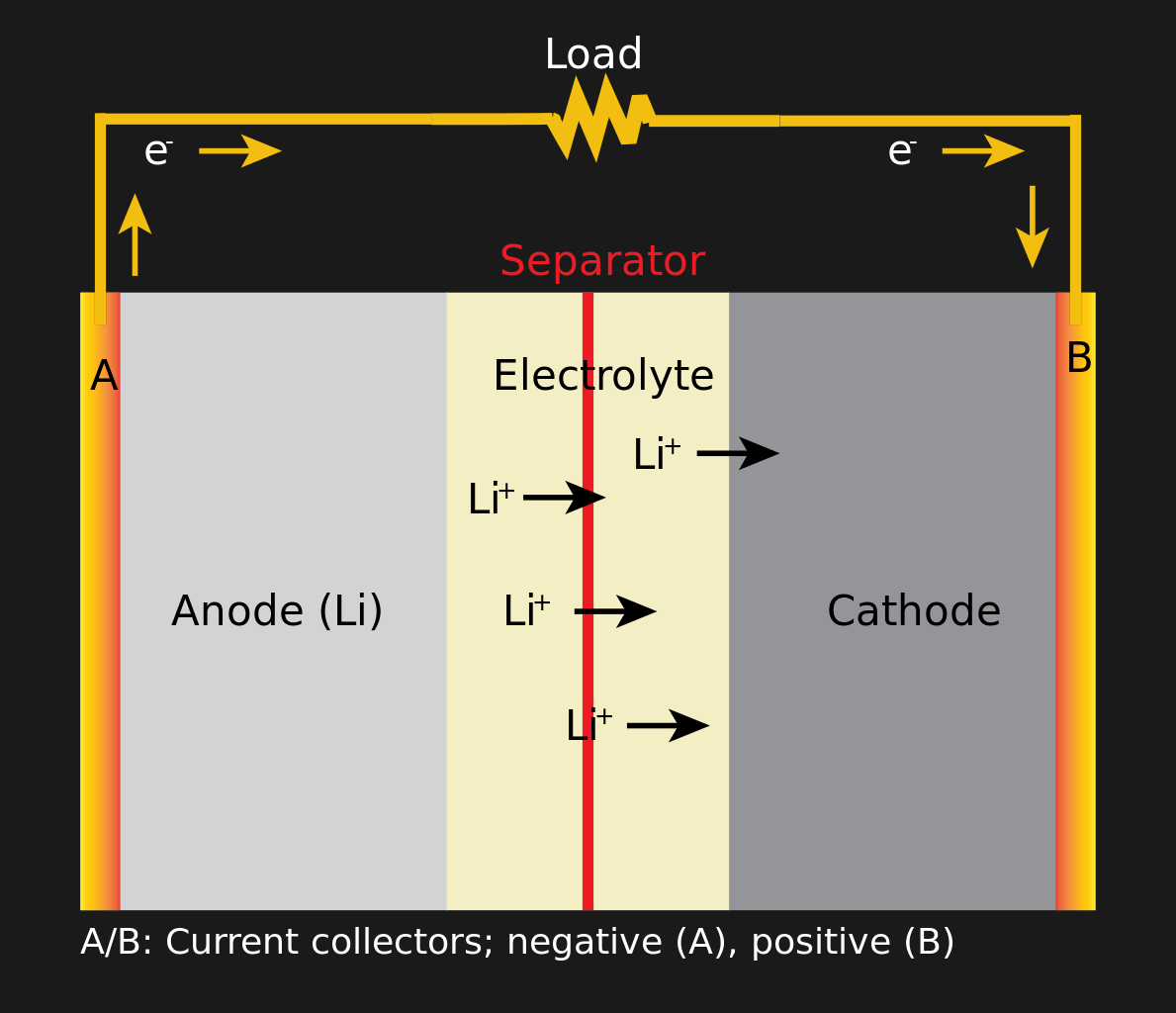 Mengosongkan Baterai Li-ion
Mengosongkan Baterai Li-ionSemua baterai bekerja sama. Ada tiga komponen: anoda, katoda, dan elektrolit. Reaksi kimia antara elektrolit dan elektroda (anoda dan katoda) menciptakan ion di dekat satu elektroda dan elektron di sebelah yang lain, menghasilkan perbedaan potensial. Pasang elektroda terbuat dari bahan yang berbeda. Anoda adalah grafit yang terikat pada tembaga, dan katoda adalah kristal lithium yang terikat pada aluminium. Elektrolit berfungsi seperti isolator, sehingga lebih mudah bagi elektron untuk berpindah dari satu elektroda ke elektroda lain melalui sirkuit daripada di dalam baterai. Pada akhir reaksi, baterai habis, dan reaksi tidak akan lagi pergi jika elektron tidak punya tempat untuk pergi. Untuk mengisi daya baterai, proses berbalik, dan tegangan yang dipasok ke elektrolit memulai reaksi berlawanan arah. Tidak semua elektrolit dibuat sama; Kimiawi baterai, yang tidak dapat diisi ulang, memungkinkannya untuk menyimpan lebih banyak energi, tetapi penerapan tegangan balik di dalamnya tidak memulai reaksi kimia kembali.
Kemampuan baterai paling baik diungkapkan dengan meningkatkan luas permukaan elektroda, jadi lebih baik membuat sandwich dari anoda, elektrolit dan katoda setipis mungkin dan dengan area kontak yang lebih besar. Sandwich ini juga mencakup beberapa irisan bahan berpori lainnya yang memungkinkan ion untuk melewatinya tetapi mencegah bahan bermigrasi. Ambil beberapa sandwich baterai Anda dan susun menjadi satu, bergantian dengan pembagi. Hasilnya adalah baterai datar (sel murah dalam casing perak), atau baterai prismatik (baterai modis yang tidak akan Anda temukan di laptop), atau jika Anda memutar semuanya menjadi tabung - baterai silinder (misalnya, 18650, atau AA) .
Baterai Juta Mil
Anda mungkin sudah membaca berita bahwa Tesla berjanji untuk melepaskan baterai yang bertahan jutaan kilometer. Pekerjaan nyata dilakukan oleh sekelompok peneliti dari University of Dalhousie di Halifax (Kanada) berdasarkan kontrak dengan Tesla, namun, mereka melakukan banyak pengujian pada berbagai baterai Li-ion untuk menemukan kombinasi terbaik dari unsur-unsur kimia, serta penggunaan dan pengisian profil. A Million Mile Battery hanyalah jebakan pemasaran yang menggambarkan penelitian yang mengoptimalkan formula kimia baterai untuk meningkatkan masa pakai baterai mereka.
Pekerjaan itu sendiri dipenuhi dengan jargon teknis , jadi saya mempelajari masalah baterai sepanjang akhir pekan untuk membuat pilihan.
Hal pertama yang perlu diperhatikan mengenai formula "satu juta mil" mereka - itu tidak khas untuk perilaku sebagian besar pengemudi saat ini, rata-rata pemilik mobil yang berkendara ke tempat kerja dan rumah. Para ilmuwan telah mengarahkan penggunaan mobil seperti itu, yang melibatkan perjalanan konstan dan pengisian baterai setelah pelepasan yang hampir sempurna. Situasi ini cocok untuk truk, taksi, dan bus. Mereka menggunakan istilah 100% DOD, mis. "Debit kedalaman" adalah ketika baterai digunakan hingga berhenti, dan hanya kemudian diisi, tidak seperti, misalnya, smartphone yang dikenakan biaya setiap malam, terlepas dari kondisi baterai.
Apa yang muncul: baterai seperti dingin; formula baru yang panas
Mereka menemukan bahwa suhu sangat penting. Baterai yang telah bekerja sebagian besar hidupnya pada 20 ºC akan bertahan lebih lama dari yang bekerja pada 40 ºC; namun, baterai yang beroperasi pada suhu tinggi, dan kemudian jatuh ke kondisi rendah, kehilangan kapasitas pada kecepatan yang sama dengan baterai yang selalu beroperasi pada suhu rendah. Dengan kata lain, pada suhu tinggi baterai kehilangan kapasitas lebih cepat, dan pada suhu rendah kehilangannya tidak begitu cepat, dan baterai apa pun dapat bergerak di sana-sini pada grafik ini tanpa efek memori. Suhu yang lebih rendah memberikan tingkat degradasi yang lebih rendah pada tingkat molekul - lebih sedikit retakan, dendrit, kantong gas, dll. Mereka sangat bertumpu pada betapa pentingnya menjaga segala sesuatu pada suhu rendah.
Dalam percobaan sebelumnya, para peneliti menghabiskan banyak waktu mempelajari kombinasi elemen kimia lainnya, tetapi menetap di elektroda grafit NMC532 (seperti kebanyakan komunitas ilmiah). Dalam kimia, NMC532 adalah nama lain untuk LiNi
0,5 Mn
0,3 Co
0,2 O
2 . Secara sederhana, ini berarti bahwa katoda terutama terdiri dari kristal litium, dengan penambahan sejumlah kecil nikel, mangan, kobalt dan oksigen, dan anoda terdiri dari grafit (meskipun studi tentang graphene terlihat menjanjikan).
Namun, karakteristik NMC532 / grafit tidak lengkap untuk baterai. Juga diperlukan untuk menunjukkan elektrolit. Elektrolit adalah campuran
LiPF 6 , pelarut dan aditif, dengan nama yang terlalu lucu untuk diucapkan dengan keras - seperti dimetil karbonat atau etilen sulfat. Dalam karya ini, mereka menguji beberapa kombinasi pelarut. Aditif juga dapat mempengaruhi kinerja sel dengan meningkatkan tingkat pengisian / pengosongan dengan memperpendek masa hidup, atau sebaliknya. Berdasarkan penelitian sebelumnya, mereka benar-benar menyukai dua formula suplemen (2% FEC + 1% LFO, dan 2% VC + 1% DTD), meskipun mereka menemukan bahwa mereka berperilaku berbeda pada suhu yang berbeda, dan menyarankan memilih aditif sesuai dengan yang diinginkan. aplikasi. Dalam pembuatan baterai, komponen kering biasanya dibuat terlebih dahulu, yang kemudian ditambahkan cairan elektrolit (Sparkfun melakukan
artikel rinci yang menjelaskan proses produksi).
Dengan memilih formula khusus dan mempertahankan suhu operasi yang rendah, para peneliti dapat meminimalkan dua penyebab utama degradasi baterai; kehilangan lithium dan peningkatan impedansi. Rata-rata, seiring waktu, ion lithium, bergerak ke sana-sini, naik ke tempat-tempat yang tidak memungkinkan mereka untuk bekerja. Mereka dapat menjadi terisolasi secara elektrik, dikelompokkan menjadi pelat, dendrit dan film permukaan, bereaksi dengan komponen sel lainnya, dan tidak berpartisipasi dalam pengisian dan pemakaian. Dendrit sangat berbahaya - kristal-kristal ini dalam bentuk jarum lithium yang tajam dapat menembus pemisah dan membuat hubungan arus pendek sel, yang kemudian memanas dan mengarah ke reaksi mandiri, dan akhirnya menjadi ledakan. Impedansi meningkat karena korosi elektroda dan hilangnya luas permukaan yang berguna, karena reaksi kimia, keretakan, atau pembentukan lapisan permukaan resistif yang menghalangi elektroda.
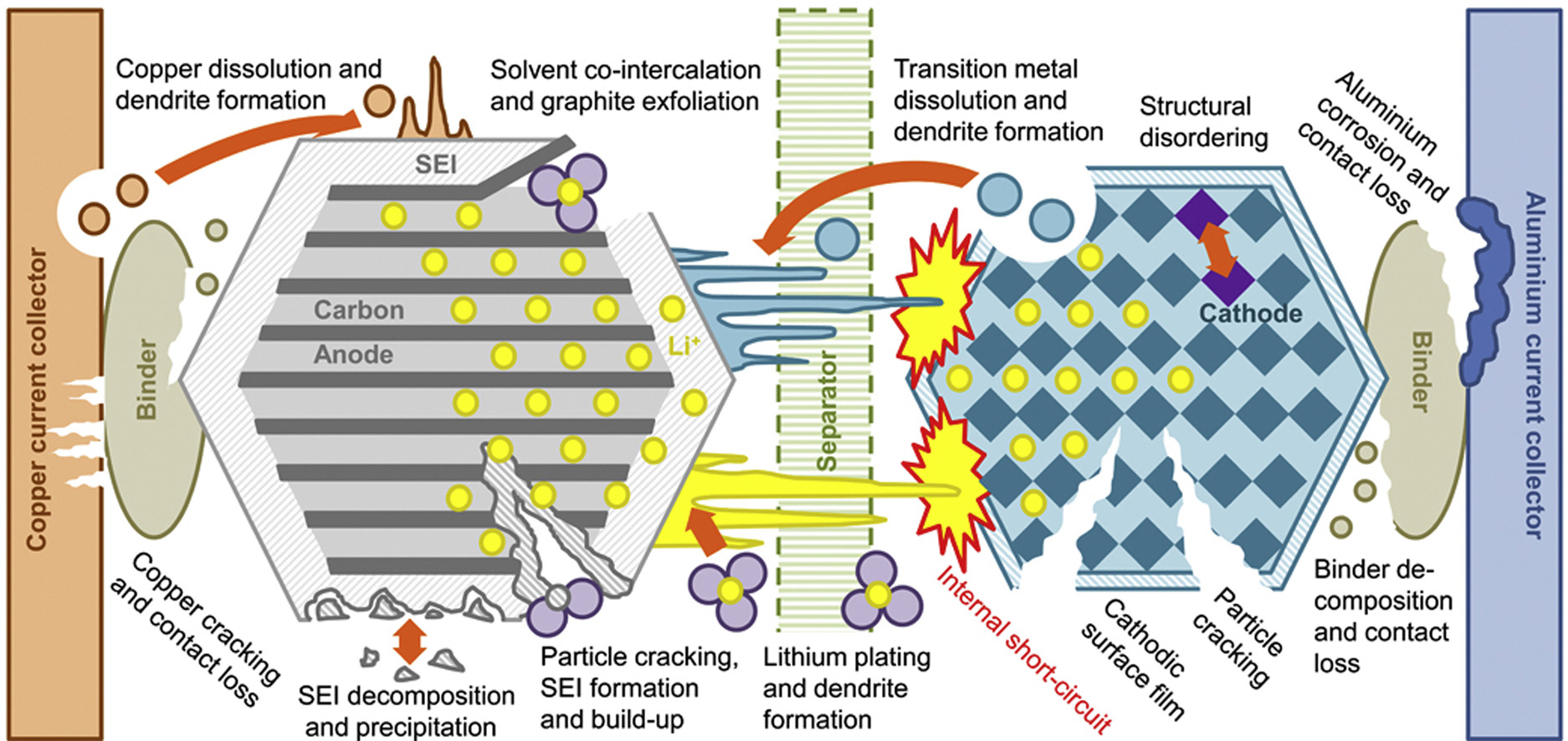 Metode degradasi baterai. Ada banyak dari mereka, tetapi pada dasarnya mereka sampai pada kenyataan bahwa "atom bergerak ke tempat yang tidak mereka butuhkan"
Metode degradasi baterai. Ada banyak dari mereka, tetapi pada dasarnya mereka sampai pada kenyataan bahwa "atom bergerak ke tempat yang tidak mereka butuhkan"Salah satu alasan mengapa penelitian mereka menarik perhatian yang meningkat adalah karena penelitian ini teliti dan terbuka. Butuh tiga tahun, butuh dia untuk menjalankan setiap baterai melalui ribuan siklus pengisian dan pemakaian menggunakan perangkat pengisian dan pemakaian yang sangat akurat yang mencatat kapasitas baterai - dan semuanya untuk mendapatkan data paling lengkap. Biasanya cukup sulit untuk mengukur siklus masa pakai baterai dalam mode akselerasi; Baterai dikenakan kecepatan pengisian / pemakaian yang lebih tinggi daripada yang dibutuhkan dalam kehidupan normal, dan menerima waktu pemulihan yang lebih sedikit. Fakta bahwa para peneliti menghabiskan begitu banyak waktu untuk pekerjaan mereka menunjukkan hasil yang lebih realistis. Mereka juga secara eksplisit menunjukkan:
Tidak seperti laporan yang menggambarkan penggunaan sel komersial, kami memasukkan deskripsi lengkap dari semua detail baterai kami, termasuk komposisi elektroda, komposisi elektrolit, aditif yang digunakan, dll. Ini dilakukan agar orang lain dapat mereproduksi sel-sel ini dan menggunakannya untuk pemeriksaan mereka sendiri.
Sangat menyenangkan bagi perubahan untuk melihat studi dengan dukungan komersial, diposting di domain publik, dan bahkan di bawah lisensi Creative Commons.
Terlepas dari keterbukaan pekerjaan, kami mungkin tidak akan melihat baterai Li-ion buatan sendiri dalam waktu dekat. Mungkin kita akan melihat transisi bertahap ke formula yang diusulkan, dan kami ingin lebih banyak pengaruh diberikan pada pendinginan, karena ini secara signifikan meningkatkan masa pakai baterai. Kami yakin bahwa jika Anda memerlukan baterai, Tesla akan segera dapat menjualnya kepada Anda dari salah satu gigafactories-nya.