É possível produzir uma fonte de energia comestível ou o princípio de operação de uma célula a combustível abiótica. Parte 1: Teoria
Na Internet, existem muitas instruções sobre como fabricar baterias "comestíveis" a partir de limões, etc. Mas a comestibilidade de tais dispositivos está em questão, já que os eletrodos, em regra, são placas de metal (geralmente zinco e cobre), e apenas o eletrólito, cujo papel é o limão, é comestível. Recentemente, perguntei-me, é possível criar uma bateria totalmente comestível?Explicarei imediatamente que a bateria não deve ser de componentes biocompatíveis, mas de componentes comestíveis. Obviamente, seria fácil criar um supercapacitor comestível a partir de carvão ativado, mas, como você sabe, o consumo de energia dos supercapacitores é muito baixo comparado às baterias.A principal dificuldade dessa idéia é encontrar eletrodos / coletores de corrente adequados. Primeiro, é necessário que o material comestível possua boa condutividade e, em segundo lugar, participe de reações eletroquímicas. E a primeira coisa que vem à mente quando você pensa em condutores comestíveis são os corantes alimentares E174 e E175, eles também são ouro e prata. Mas em que reações eletroquímicas esses materiais podem ser usados se estiverem próximos uns dos outros em uma série eletroquímica de tensões? Mas aqui devemos lembrar que ouro e prata têm atividade eletrocatalítica. Onde os catalisadores são usados em fontes de energia eletroquímicas? Nas células de combustível!Como funciona uma célula de combustível? Como outras fontes de energia eletroquímicas, as células de combustível têm dois eletrodos imersos em um eletrólito. Mas, diferentemente das baterias e supercapacitores, esses eletrodos não são materiais ativos, mas catalisadores nos quais ocorre a oxidação do "combustível", que é fornecido do lado de fora, e a redução do oxidante. Por exemplo, no exemplo clássico de uma célula a combustível de hidrogênio, o combustível é hidrogênio e o agente oxidante é o oxigênio. A propósito, em comparação com outras fontes de energia eletroquímica, por exemplo, baterias e supercapacitores, as células de combustível são as que consomem mais energia, pois funcionam enquanto os reagentes são fornecidos aos eletrodos. Mas sua desvantagem é a baixa potência, limitada pela velocidade das reações eletroquímicas e pela velocidade de fornecimento de combustível e oxidante aos eletrodos.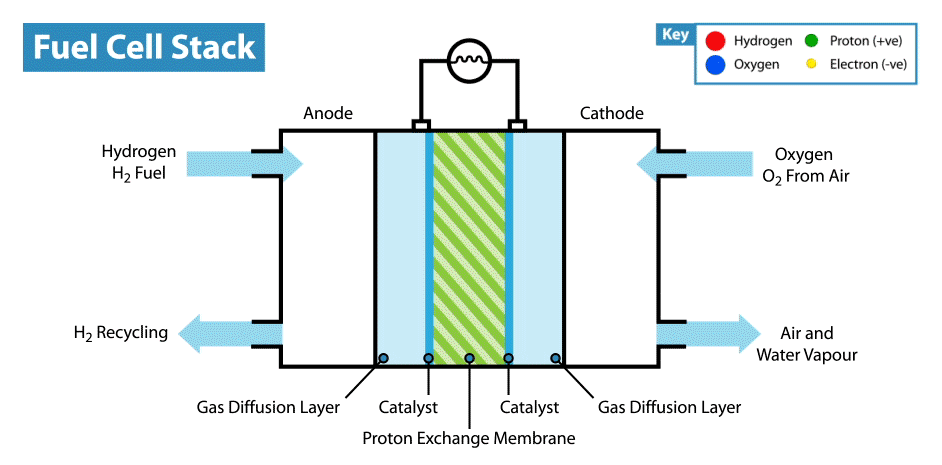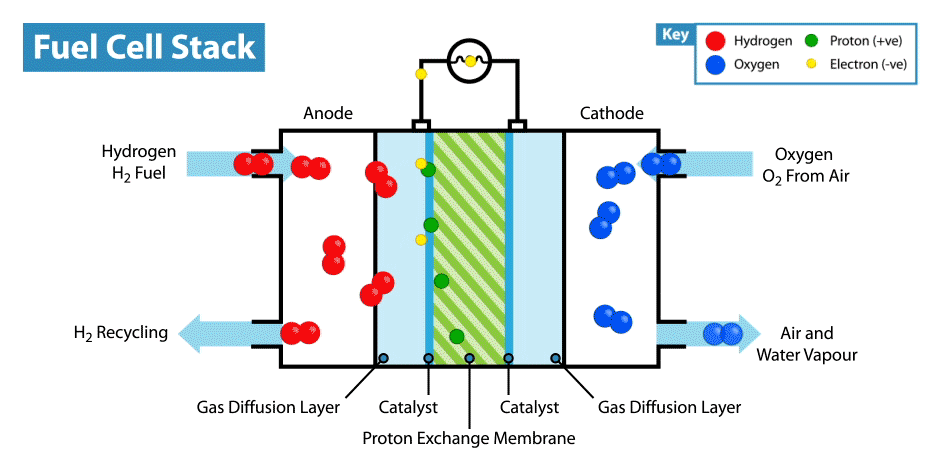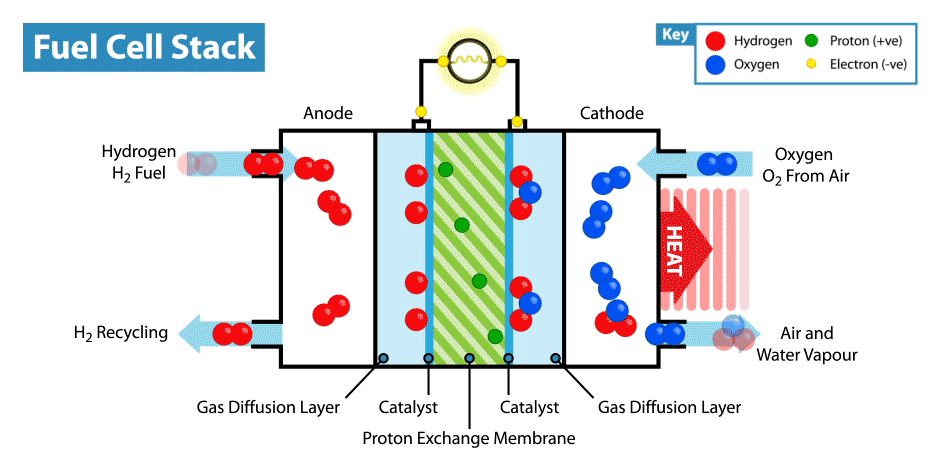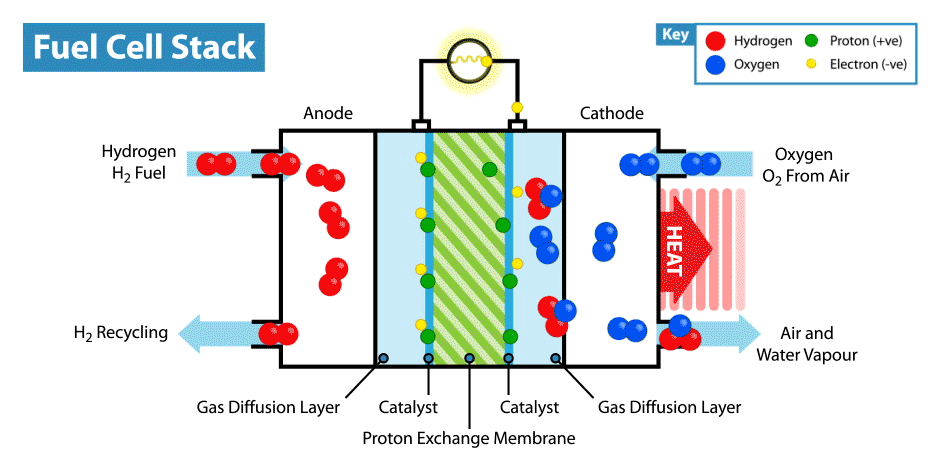

Source: https://habr.com/ru/post/pt398091/
All Articles