Baterias de lítio-enxofre para futuros programas espaciais
Hoje, as baterias nos programas espaciais são usadas principalmente como fontes de energia reserva, quando os dispositivos estão na sombra e não podem receber energia de painéis solares ou em trajes espaciais para sair para o espaço sideral. Mas os tipos de baterias usadas atualmente (íons de lítio, Ni-H 2 ) têm várias limitações. Em primeiro lugar, eles são muito pesados, uma vez que a preferência não é dada à intensidade energética, mas à segurança, como resultado de múltiplos mecanismos de proteção para reduzir o volume, de maneira alguma contribui. Em segundo lugar, as baterias modernas têm limites de temperatura e, em programas futuros, dependendo da localização, as temperaturas podem variar de -150 ° C a +450 ° C.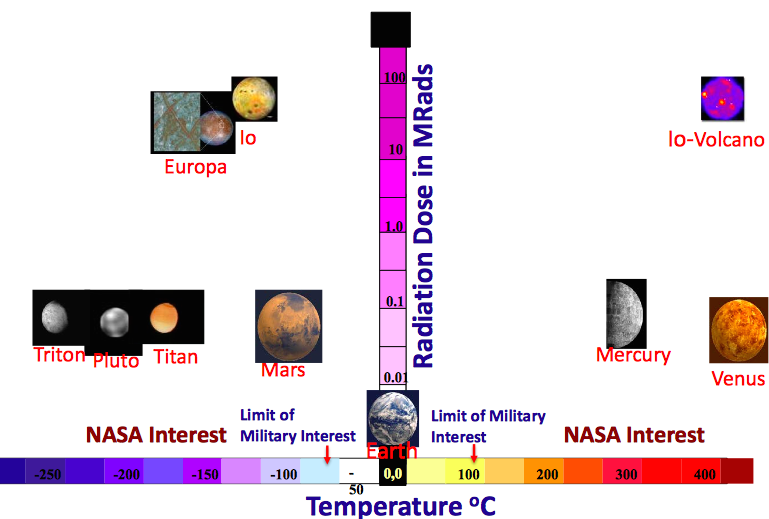 FonteAlém disso, não se esqueça do aumento da radiação de fundo. Em geral, as baterias futuras para a indústria espacial devem não apenas ser compactas, duráveis, seguras e intensivas em energia, mas também operar em altas ou baixas temperaturas, bem como em condições de maior radiação. Hoje, naturalmente, essa tecnologia mágica não existe. No entanto, existem desenvolvimentos científicos promissores que estão tentando se aproximar dos requisitos para programas futuros. Em particular, gostaria de falar sobre uma direção da pesquisa, apoiada pela NASA no âmbito do programa Game Changing Development (GCD).Como combinar todas as especificações acima em uma bateria é uma tarefa difícil, o principal objetivo da NASA hoje é obter baterias mais compactas, com uso intenso de energia e mais seguras. Como alcançar esse objetivo?Para começar, para aumentar significativamente o consumo de energia por unidade de volume, são necessárias baterias com materiais fundamentalmente novos para eletrodos, uma vez que os recursos das baterias de íons de lítio (íon de lítio) são limitados pelas capacidades dos materiais do cátodo (cerca de 250 mAh / g para óxidos) e do ânodo ( 370 mAh / g para grafite), bem como os limites de tensão nos quais o eletrólito é estável. E uma das tecnologias que permite aumentar a capacidade usando reações fundamentalmente novas em vez da intercalação nos eletrodos são as baterias de lítio-enxofre (Li-S), cujo ânodo contém lítio metálico e o enxofre é usado como material ativo para o cátodo. A operação de uma bateria de lítio-enxofre é um pouco semelhante à operação de uma bateria de lítio-íon: os íons de lítio estão envolvidos na transferência de carga para lá e para cá. Mas, ao contrário do íon de lítio, os íons do íon de lítio não se integram na estrutura em camadas do cátodo,e entre na seguinte reação com ele:
FonteAlém disso, não se esqueça do aumento da radiação de fundo. Em geral, as baterias futuras para a indústria espacial devem não apenas ser compactas, duráveis, seguras e intensivas em energia, mas também operar em altas ou baixas temperaturas, bem como em condições de maior radiação. Hoje, naturalmente, essa tecnologia mágica não existe. No entanto, existem desenvolvimentos científicos promissores que estão tentando se aproximar dos requisitos para programas futuros. Em particular, gostaria de falar sobre uma direção da pesquisa, apoiada pela NASA no âmbito do programa Game Changing Development (GCD).Como combinar todas as especificações acima em uma bateria é uma tarefa difícil, o principal objetivo da NASA hoje é obter baterias mais compactas, com uso intenso de energia e mais seguras. Como alcançar esse objetivo?Para começar, para aumentar significativamente o consumo de energia por unidade de volume, são necessárias baterias com materiais fundamentalmente novos para eletrodos, uma vez que os recursos das baterias de íons de lítio (íon de lítio) são limitados pelas capacidades dos materiais do cátodo (cerca de 250 mAh / g para óxidos) e do ânodo ( 370 mAh / g para grafite), bem como os limites de tensão nos quais o eletrólito é estável. E uma das tecnologias que permite aumentar a capacidade usando reações fundamentalmente novas em vez da intercalação nos eletrodos são as baterias de lítio-enxofre (Li-S), cujo ânodo contém lítio metálico e o enxofre é usado como material ativo para o cátodo. A operação de uma bateria de lítio-enxofre é um pouco semelhante à operação de uma bateria de lítio-íon: os íons de lítio estão envolvidos na transferência de carga para lá e para cá. Mas, ao contrário do íon de lítio, os íons do íon de lítio não se integram na estrutura em camadas do cátodo,e entre na seguinte reação com ele:2 Li + S -> Li 2 S
Embora na prática, a reação no cátodo seja mais ou menos assim:S 8 -> Li 2 S 8 -> Li 2 S 6 -> Li 2 S 4 -> Li 2 S 2 -> Li 2 S
FonteA principal vantagem dessa bateria é sua alta capacidade, que é 2-3 vezes maior que a capacidade das baterias de íon-lítio. Mas, na prática, nem tudo é tão róseo. Durante cargas repetidas, os íons de lítio se instalam no ânodo como horríveis, formando correntes metálicas (dendritos), que acabam levando a um curto-circuito. Além disso, as reações entre lítio e enxofre no cátodo levam a grandes mudanças no volume do material (até 80%), de modo que o eletrodo é destruído rapidamente e os próprios compostos de enxofre são maus condutores, portanto, muito material de carbono deve ser adicionado ao cátodo. E por último, e mais importante, os produtos de reação intermediária (polissulfetos) dissolvem-se gradualmente no eletrólito orgânico e "viajam" entre o ânodo e o cátodo, o que leva a uma autodescarga muito forte.Mas todos os problemas acima estão tentando resolver um grupo de cientistas da Universidade de Maryland (UMD), que ganhou uma bolsa da NASA. Então, como os cientistas chegaram à solução de todos esses problemas? Primeiro, eles decidiram “atacar” um dos principais problemas das baterias de lítio-enxofre, a autodescarga. E em vez de um eletrólito orgânico líquido, que, como mencionado acima, dissolve gradualmente os materiais ativos, eles usaram um eletrólito sólido de cerâmica, ou melhor, Li 6 PS 5 Cl, que conduz íons de lítio muito bem através de sua estrutura cristalina.Mas se os eletrólitos sólidos resolverem um problema, eles também criarão dificuldades adicionais. Por exemplo, grandes alterações no volume do cátodo durante a reação podem levar a uma rápida perda de contato entre o eletrodo sólido e o eletrólito e a uma acentuada diminuição na capacidade da bateria. Portanto, os cientistas propuseram uma solução elegante: eles criaram um nanocompósito constituído por nanopartículas do material ativo do cátodo (LI 2 S) e eletrólito (Li 6 PS 5 Cl) envolto em uma matriz de carbono.FonteEste nanocompósito possui as seguintes vantagens: primeiro, a distribuição de nanopartículas de um material que muda de volume durante a reação com lítio em carbono, cujo volume permanece praticamente inalterado, melhora as propriedades mecânicas do nanocompósito (ductilidade e resistência) e reduz o risco de rachaduras. Além disso, o carbono não apenas melhora a condutividade, mas também não interfere no movimento dos íons de lítio, pois também possui boa condutividade iônica. E devido ao fato de os materiais ativos serem nanoestruturados, o lítio não precisa percorrer longas distâncias para reagir, e todo o volume do material é usado com mais eficiência. Por fim, o uso de tal composto melhora o contato entre o eletrólito, o material ativo e o carbono condutor.Como resultado, os cientistas adquiriram uma bateria totalmente sólida com uma capacidade de cerca de 830 mAh / g. Obviamente, é muito cedo para falar sobre o lançamento de uma bateria no espaço, pois ela funciona apenas por 60 ciclos de carga / descarga. Mas, ao mesmo tempo, apesar de uma perda tão rápida de capacidade, 60 ciclos já são uma melhoria significativa em relação aos resultados anteriores, pois antes disso, as baterias sólidas de lítio-enxofre não funcionavam por mais de 20 ciclos. Deve-se notar também que esses eletrólitos sólidos podem funcionar em uma ampla faixa de temperatura (a propósito, funcionam melhor em temperaturas acima de 100 ° C), de modo que os limites de temperatura dessas baterias sejam mais prováveis devido aos materiais ativos do que ao eletrólito, que distingue esses sistemas de baterias usando soluções orgânicas como eletrólito. Source: https://habr.com/ru/post/pt398529/
All Articles