Classificação de Transtornos Depressivos; o papel das monoaminas (dopamina, noradrenalina e serotonina); mecanismos de ação de antidepressivos; depressão, estresse e neuroplasticidade.
Depressão (de lat.
Deprimo - suprimir) - uma doença mental caracterizada por uma
"tríade depressiva" , que inclui os seguintes distúrbios:
1.
Na esfera emocional. Humor deprimido e anedonia - a incapacidade de apreciar coisas naturais: comida, álcool, socialização, sexo, etc.
2. Na esfera cognitiva. Uma auto-imagem negativa, uma experiência mundial negativa, uma visão negativa do futuro - essa é a chamada
"tríade cognitiva" . A tríade dentro da tríade + uma pessoa é incapaz de uma avaliação adequada da situação, não pode aplicar a experiência positiva anterior de resolver o problema.
3.
Na esfera do motor. Como regra geral, a inibição motora, mas também pode haver uma reação inversa - agitação agitada: um paciente em um ambiente calmo pode pular constantemente, balançar os braços, mudar constantemente de postura ou, por exemplo, levantar-se e sair no meio de uma conversa.
 Psiquiatria: Um Guia Nacional. M .: GEOTAR-Media, 2009.1000 s.
Psiquiatria: Um Guia Nacional. M .: GEOTAR-Media, 2009.1000 s.Existem sintomas adicionais: perda ou aumento do apetite (perda ou ganho de peso), distúrbios do sono (sonolência ou insônia), sensação de cansaço, aumento da fadiga etc.
Segundo a OMS (Newsletter nº 369), mais de 300 milhões de pessoas sofrem de depressão, e esse indicador tem tendência a aumentar. A depressão é diferente das mudanças de humor comuns e reações emocionais de curto prazo aos problemas da vida cotidiana. Pode levar a sérios problemas de saúde, má adaptação social, baixo desempenho e aprendizado. Nos piores casos, pode levar ao suicídio.
Anualmente, cerca de 800.000 pessoas morrem como resultado de suicídio - a segunda principal causa de morte entre pessoas de 15 a 29 anos.
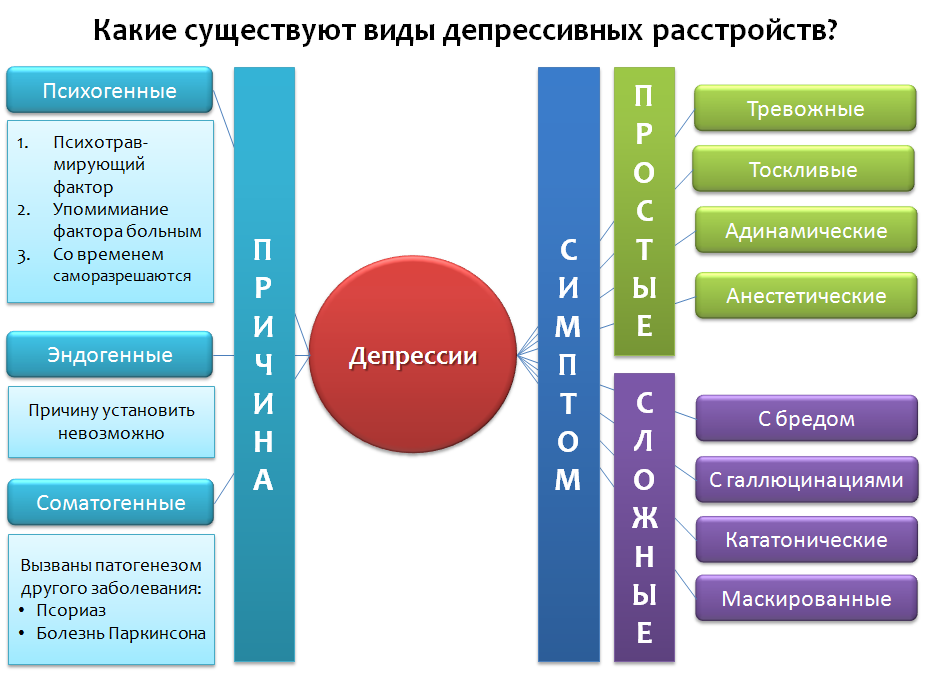 Fig. 1 Depressão: o tratamento e tratamento da depressão em adultos (edição atualizada). Leicester (Reino Unido): Sociedade Psicológica Britânica, 2010.
Fig. 1 Depressão: o tratamento e tratamento da depressão em adultos (edição atualizada). Leicester (Reino Unido): Sociedade Psicológica Britânica, 2010.Vamos dar uma olhada na classificação simplificada de transtornos depressivos (Fig. 1), que não é absoluta, mas inclui exemplos básicos. A depressão pode ser classificada pelo motivo que os causou (etiologia) e a predominância de certos sintomas, bem como suas diversas combinações.
No primeiro caso, três categorias podem ser distinguidas:
1. Depressão
psicogênica (reativa) causada por um fator traumático. Esse fator aparece no discurso do paciente. Como regra, essas depressões podem resolver por conta própria ao longo do tempo, a cessação do fator - “o tempo cura”.
2.
Endógena - depressões causadas por fatores internos que não podem ser estabelecidos.
3.
Somatogenic - causado pela patogênese (mecanismo de desenvolvimento da doença) de várias doenças. É importante não confundi-los com psicogênicos. Por exemplo, se uma pessoa tem depressão devido à
consciência da presença de uma doença, é depressão psicogênica (reativa). Somatogenic são aquelas depressões causadas pelo mecanismo de outra doença. Por exemplo, na doença de Parkinson, as células nervosas que produzem dopamina morrem, o que, por sua vez, desempenha um papel importante na resposta emocional. A deficiência de dopamina nas áreas do cérebro responsáveis pela resposta emocional leva à depressão. Um segundo exemplo é a psoríase, que pode levar a uma diminuição na produção de serotonina (um importante regulador do humor) no sistema nervoso central, aumentando assim o risco de desenvolver distúrbios depressivos.
De acordo com o sintoma predominante da depressão, pode haver: ansioso, triste, adinâmico, anestésico (experimentando falta de emoções - “anestesia emocional”) - esses são exemplos de
“depressão simples” .
As "depressões complexas" combinam os sintomas da depressão e outras psicopatologias: depressão com delírios, alucinações, catatônicas, mascaradas - os sintomas se disfarçam de doenças de órgãos internos ou "somatizam" de outra maneira - dores de cabeça, dores abdominais, coração etc.
A complexidade do tratamento de transtornos depressivos é a falta de recuperação total no caso de formas graves ou complicadas de transtornos depressivos. Mas a auto-resolução dessa doença também é possível; se o curso não for grave, não haverá complicações na forma de sintomas de outras psicopatologias, etc.
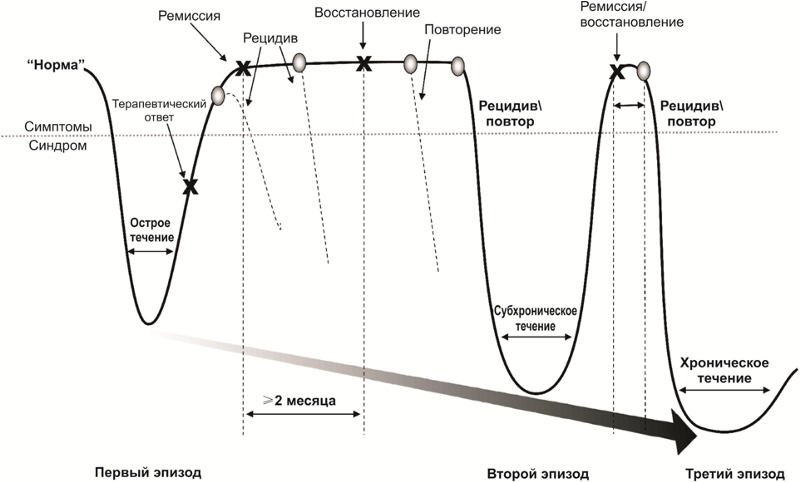 A natureza do curso dos transtornos depressivos
A natureza do curso dos transtornos depressivosApós um curso bem-sucedido de medicamentos e psicoterapia, começa um período de remissão, que é acompanhado por um enfraquecimento (remissão parcial) ou um desaparecimento completo dos sintomas (remissão completa) da doença. Durante o período de tratamento ativo e remissão parcial ou completa, o risco de retornar os sintomas da doença - recaída - permanece.
Além disso, há riscos de episódios repetidos de depressão após uma recuperação completa do primeiro episódio. Episódios repetidos podem ser caracterizados por um conjunto de outros sintomas e um curso mais grave. A doença pode adquirir um curso crônico. Freqüentemente, o primeiro episódio de um distúrbio depressivo é psicogênico (reativo) e repetido (se o problema é insolúvel, o fator traumático era muito forte ou prolongado) - endógeno.
Serotonina, noradrenalina e dopamina
A Figura 2 resume os principais parâmetros da teoria da depressão da monoamina.
As fórmulas de
monoamina são dadas para explicar o nome desse grupo de substâncias - elas contêm apenas um grupo amino (-NH2).
O papel das monoaminas no desenvolvimento de sintomas depressivos
 Fig. 2 Teoria da Depressão Monoamínica* Outro grupo NH de serotonina não é um grupo amino, faz parte do heterociclo indole.
Fig. 2 Teoria da Depressão Monoamínica* Outro grupo NH de serotonina não é um grupo amino, faz parte do heterociclo indole.Acredita-se que o papel das monoaminas na formação de sintomas individuais de depressão seja heterogêneo. Portanto,
para um sentimento de culpa e inutilidade, idéias suicidas e perda de apetite podem ser responsáveis pela
deficiência de serotonina .
A dopamina e a norepinefrina são responsáveis pela
apatia, disfunção executiva e fadiga .
Uma deficiência de
todas as monoaminas no complexo indica
humor deprimido, disfunção psicomotora e distúrbios do sono.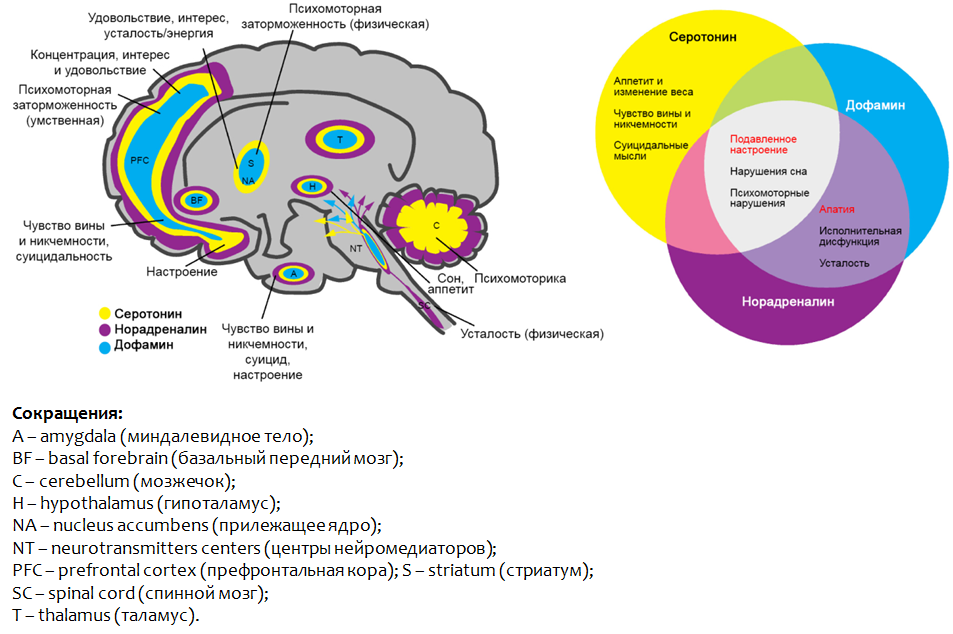 Fig. 3. Saltiel PF, Silvershein DI Transtorno depressivo maior: prescrição baseada em mecanismos para medicina personalizada // Neuropsychiatr Dis Treat. 2015. 11. P. 875-88.
Fig. 3. Saltiel PF, Silvershein DI Transtorno depressivo maior: prescrição baseada em mecanismos para medicina personalizada // Neuropsychiatr Dis Treat. 2015. 11. P. 875-88.A Figura 3 mostra as partes do cérebro em que a disfunção das monoaminas apresentadas leva ao desenvolvimento de sintomas depressivos.
Como já dissemos, todos os antidepressivos clinicamente eficazes modernos são criados dentro da estrutura da teoria da depressão da monoamina.
Antidepressivos
Condicionalmente, o princípio de ação dos antidepressivos pode ser dividido em dois grupos:
1. Meios que
aumentam a concentração de monoaminas (principalmente serotonina e noradrenalina) no cérebro;
2. Meios que
assumem a função de monoaminas (principalmente serotonina), estimulando receptores específicos.
 Fig. 4
Fig. 4Vamos considerar com mais detalhes os principais grupos de mecanismos moleculares dos antidepressivos. A Figura 5 mostra o contato sináptico entre duas células nervosas: acima está a terminação nervosa de um neurônio (
sinapse ); abaixo está outra célula nervosa que recebe um sinal.
Os principais mecanismos moleculares dos antidepressivos no contexto da hipótese de depressão da monoamina
 Fig. 5. Terapia medicamentosa para transtornos de depressão e ansiedade. A base farmacológica da terapêutica de Goodman e Gilman. Décima segunda edição. 2011. Stahl SM Psicofarmacologia básica de antidepressivos. Parte 1: Os antidepressivos têm sete mecanismos distintos de ação // The Journal of Clinical Psychiatry. 1998. 59. Suppl 4. P. 5-14.
Fig. 5. Terapia medicamentosa para transtornos de depressão e ansiedade. A base farmacológica da terapêutica de Goodman e Gilman. Décima segunda edição. 2011. Stahl SM Psicofarmacologia básica de antidepressivos. Parte 1: Os antidepressivos têm sete mecanismos distintos de ação // The Journal of Clinical Psychiatry. 1998. 59. Suppl 4. P. 5-14.A síntese de neurotransmissores (serotonina e noradrenalina) ocorre nas células nervosas, com a ajuda das quais as células transmitem um sinal umas às outras. O material de partida para a síntese são aminoácidos essenciais - L-triptofano e L-fenilalanina. Após a síntese, os neurotransmissores são acondicionados em grânulos -
vesículas especiais, nos quais se movem para as terminações nervosas (
sinapses ) e são depositados ali.
Depois que a célula
recebe um estímulo específico, os
mediadores são liberados da terminação nervosa (sinapse) para a
fenda sináptica - a lacuna entre duas células nervosas. Na superfície da célula sinalizadora "receptora" existem formações especiais de proteínas -
receptores (neste caso, serotonina e receptores adrenérgicos) que se ligam ao mediador. Após a ligação, o mediador ativa (estimula) o receptor correspondente, o que leva a uma alteração nos processos metabólicos dentro da célula e, consequentemente, altera sua função (melhora ou suprime).
Depois de desempenhar com sucesso sua função, 80% do mediador é capturado de volta na célula nervosa, onde parte do mediador é destruída pela enzima
monoamina oxidase tipo A (MAO-A) e parte é novamente acondicionada em vesículas para reutilização. A captura do mediador pode reduzir significativamente os custos de energia para a síntese do mediador a partir de aminoácidos.
 Fig. 6 Os contras superam e justificam a busca de novas hipóteses e metas.
Fig. 6 Os contras superam e justificam a busca de novas hipóteses e metas.Brevemente sobre como os antidepressivos agem

1. Violar a recaptação do neurotransmissor na extremidade nervosa, aumentando assim sua concentração na fenda sináptica e aumentando seu efeito sobre os receptores. É possível uma violação separada da recaptação de serotonina (fluoxetina, fluvoxamina, paroxetina) e noradrenalina (reboxetina, atomoxetina) e uma violação simultânea da captura de ambos os mediadores (amitriptilina).
2. Aumente a liberação de mediadores das terminações nervosas (mirtazapina e tianeptina
atualmente proibida ).
3. Suprima a atividade da enzima MAO-A e, assim, preserve o mediador da destruição (moclobemida).
4. Os receptores de serotonina do 1º subtipo (Vilazodona) são estimulados, cuja ativação está associada ao alívio dos sintomas depressivos ("bons" receptores).
5. Bloqueie os receptores de serotonina do tipo 2 (receptores "ruins"), responsáveis pelo desenvolvimento de sintomas de ansiedade e depressão (trazodona).
Depressão e estresse
Atualmente, é atribuído ao estresse o papel de um dos mecanismos desencadeantes (desencadeantes) dos distúrbios afetivos (distúrbios da esfera emocional, afeto), incluindo os depressivos. Acredita-se que seja perigoso não apenas um evento estressante único e grave, mas um efeito menos intenso e constante do estresse, especialmente eventos estressantes imprevisíveis todos os dias. É impossível se adaptar a esses efeitos estressantes e leva à ativação crônica dos mecanismos de defesa e adaptação com seu subsequente esgotamento.
Um dos componentes mais importantes da resposta fisiológica do corpo ao estresse é o eixo hipotálamo-hipófise-adrenal (Fig. 7).
 Fig. 7. Varghese FP & Brown ES O eixo hipotálamo-hipófise-adrenal no transtorno depressivo maior: uma breve cartilha para médicos de cuidados primários // companheiro de cuidados primários do Journal of Clinical Psychiatry. 2001.3 (4). P. 151-155.
Fig. 7. Varghese FP & Brown ES O eixo hipotálamo-hipófise-adrenal no transtorno depressivo maior: uma breve cartilha para médicos de cuidados primários // companheiro de cuidados primários do Journal of Clinical Psychiatry. 2001.3 (4). P. 151-155.A ativação sucessiva do estresse das estruturas centrais (amígdalas - hipotálamo - hipófise) leva ao desenvolvimento de hormônios do córtex adrenal - glicocorticóides (cortisol) - hormônios do estresse. Estes últimos são capazes de agir sobre a estrutura do cérebro (responsável pela resposta ao estresse emocional (córtex pré-frontal e hipocampo)) e interromper os processos de neuroplasticidade.
Distúrbios da neuroplasticidade *
As violações da neuroplasticidade levam a uma violação da conexão normal entre as estruturas do cérebro (responsável pela resposta emocional).
* Neuroplasticidade é a capacidade do cérebro de se adaptar às mudanças através da reorganização, sob desenvolvimento normal e em condições patológicas.
 Fig. 8 Fuchs E., Flügge G. Neuroplasticidade de adultos: Mais de 40 anos de pesquisa // Plasticidade Neural. 2014. ID do artigo 541870. Doi: 10.1155 / 2014/541870; Joyce Sh. Neuroplasticidade e Prática Clínica: Construindo o Poder Cerebral para a Saúde // Fronteiras em Psicologia. 7 (2016): 1118. PMC. Web 7 de maio de 2017. Zilles K. Plasticidade neuronal como propriedade adaptativa do sistema nervoso central // Annals of Anatomy. 1992. Vol. 174. Não. 5. P. 383-391.
Fig. 8 Fuchs E., Flügge G. Neuroplasticidade de adultos: Mais de 40 anos de pesquisa // Plasticidade Neural. 2014. ID do artigo 541870. Doi: 10.1155 / 2014/541870; Joyce Sh. Neuroplasticidade e Prática Clínica: Construindo o Poder Cerebral para a Saúde // Fronteiras em Psicologia. 7 (2016): 1118. PMC. Web 7 de maio de 2017. Zilles K. Plasticidade neuronal como propriedade adaptativa do sistema nervoso central // Annals of Anatomy. 1992. Vol. 174. Não. 5. P. 383-391.Os mais importantes no contexto dos transtornos depressivos são o córtex pré-frontal, amígdala e hipocampo.
A interação das estruturas cerebrais é normal
 Fig. 9. Gorman JM, Docherty JP Papel Hipotesizado para Remodelação Dendrítica na Etiologia de Transtornos de Humor e Ansiedade // The Journal of Neuropsychiatry and Clinical Neurosciences. 2010.22: 3. P. 256-264
Fig. 9. Gorman JM, Docherty JP Papel Hipotesizado para Remodelação Dendrítica na Etiologia de Transtornos de Humor e Ansiedade // The Journal of Neuropsychiatry and Clinical Neurosciences. 2010.22: 3. P. 256-264Normalmente, quando há uma conexão completa entre os neurônios dessas estruturas, o córtex pré-frontal processa as informações recebidas do hipocampo (memória, coloração emocional de lembranças e eventos). A amígdala é a estrutura responsável pelo sentimento de medo. Normalmente, o córtex pré-frontal suprime a atividade excessiva dessa estrutura.
Fig. 10Sabe-se que, no contexto de distúrbios depressivos, os processos de neuroplasticidade são interrompidos, em particular, o número de contatos entre as células nervosas diminui, a velocidade da transmissão do impulso muda e o número de neurônios diminui. Além disso, no contexto da depressão, observa-se uma diminuição no volume do hipocampo e do córtex pré-frontal. Tais mudanças contribuem para a ruptura do relacionamento funcional normal entre as estruturas apresentadas.
Aparentemente, os sintomas depressivos podem ser mediados por essas alterações: a ansiedade descontrolada que geralmente ocorre em pacientes com depressão pode ser devida à falta de inibição da amígdala pelo córtex pré-frontal.
A interação das estruturas cerebrais na depressão (teoria)
 Fig. 11. Gorman JM, Docherty JP Um papel hipotético para a remodelação dendrítica na etiologia dos transtornos de humor e ansiedade. O Jornal de Neuropsiquiatria e Neurociências Clínicas. 2010.22 (3). P. 256-64. Kudryashov N.V. Um estudo experimental da atividade psicotrópica dos derivados de pirazolo [c] piridina GIZh-72 e pirrolodiazepina GMAL-24 nas condições de estresse moderado crônico imprevisível / dissertação do candidato de Ciências Biológicas. 14/03/06. M., 2016. 198 p.
Fig. 11. Gorman JM, Docherty JP Um papel hipotético para a remodelação dendrítica na etiologia dos transtornos de humor e ansiedade. O Jornal de Neuropsiquiatria e Neurociências Clínicas. 2010.22 (3). P. 256-64. Kudryashov N.V. Um estudo experimental da atividade psicotrópica dos derivados de pirazolo [c] piridina GIZh-72 e pirrolodiazepina GMAL-24 nas condições de estresse moderado crônico imprevisível / dissertação do candidato de Ciências Biológicas. 14/03/06. M., 2016. 198 p.A incapacidade de avaliar adequadamente a situação e usar a experiência positiva anterior é o resultado de uma violação da conexão entre o córtex pré-frontal e o hipocampo. Uma diminuição no volume do hipocampo pode explicar um humor patologicamente reduzido.
Os mecanismos de regulação da neuroplasticidade no cenário de transtornos depressivos
Fig. 12Um importante regulador dos processos de neuroplasticidade é o
fator neurotrófico cerebral (BDNF -
fator neurotrófico derivado do cérebro ), cujos níveis diminuem devido ao estresse e à depressão.
Hormônios do estresse, como o cortisol, um glicocorticosteróide produzido pelo córtex adrenal, também podem atuar como reguladores negativos da neuroplasticidade. É sabido que a maioria dos antidepressivos utilizados (em uso crônico) é capaz de aumentar os níveis de BDNF e, aparentemente, isso faz parte de seu efeito terapêutico.
Propriedades do fator neurotrófico cerebral (BDNF *) e a perspectiva de seu uso como antidepressivo
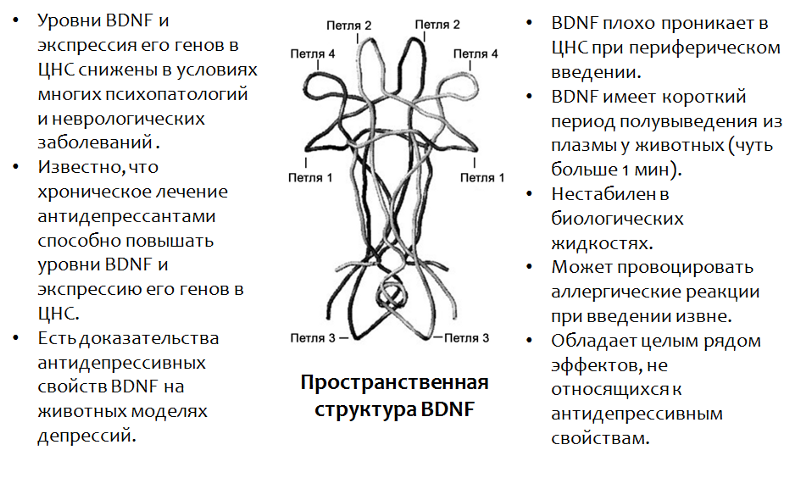 Fig. 13. Castrén E., Rantamäki T. O papel do BDNF e seus receptores na depressão e na ação antidepressiva: Reativação da plasticidade do desenvolvimento // Neurobiologia do Desenvolvimento. 2010.70 (5). P. 289–97.
Fig. 13. Castrén E., Rantamäki T. O papel do BDNF e seus receptores na depressão e na ação antidepressiva: Reativação da plasticidade do desenvolvimento // Neurobiologia do Desenvolvimento. 2010.70 (5). P. 289–97.* O BDNF desempenha um papel importante em muitas psicopatologias, incluindo e depressão. O uso do próprio BDNF não é possível devido a vários motivos (listados na figura).
Além dos antidepressivos, existem outros fatores que contribuem para o aumento dos níveis de BDNF no sistema nervoso central e coincidem com estímulos positivos da neuroplasticidade - treinamento, exercícios, novas experiências, dieta etc. Além disso, freqüentemente esses fatores podem complementar a terapia medicamentosa para transtornos depressivos.
A Figura 14 apresenta dados sobre um estudo das propriedades antidepressivas do próprio BDNF em modelos animais (ratos). Como o próprio BDNF não pode penetrar no cérebro (através da barreira hematoencefálica) durante a administração periférica, nas experiências o BDNF foi injetado diretamente no cérebro.
Estudo das propriedades antidepressivas do fator neurotrófico cerebral (BDNF) em modelos animais
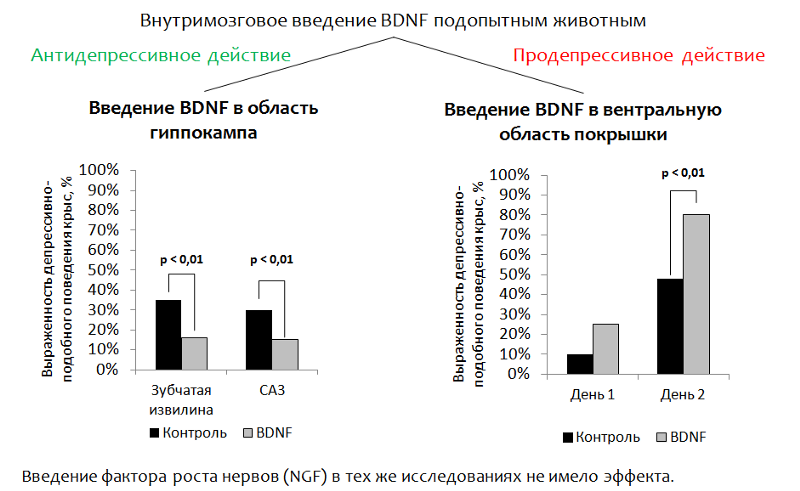 Fig. 14 Eisch AJ, Bolaños CA, de Wit J. et al. Fator neurotrófico derivado do cérebro na via ventral do mesencéfalo-núcleo accumbens: um papel na depressão // Psiquiatria Biológica. 2003.54 (10). P. 994-1005; Shirayama Y., Chen AC, Nakagawa S., Russell DS, Duman RS O fator neurotrófico derivado do cérebro produz efeitos antidepressivos em modelos comportamentais de depressão. Jornal de Neurociência. 2002.22 (8). P. 3251–61.
Fig. 14 Eisch AJ, Bolaños CA, de Wit J. et al. Fator neurotrófico derivado do cérebro na via ventral do mesencéfalo-núcleo accumbens: um papel na depressão // Psiquiatria Biológica. 2003.54 (10). P. 994-1005; Shirayama Y., Chen AC, Nakagawa S., Russell DS, Duman RS O fator neurotrófico derivado do cérebro produz efeitos antidepressivos em modelos comportamentais de depressão. Jornal de Neurociência. 2002.22 (8). P. 3251–61.1.
Introdução ao hipocampo . A idéia principal foi a introdução direcionada de BDNF na região do cérebro responsável pela neurogênese (o giro dentado do hipocampo é um dos chamados
"nichos neurogênicos" ). Após a administração, foi avaliado o comportamento depressivo dos animais.
(O componente disfórico da depressão é avaliado. Os animais (ratos ou camundongos) são colocados em um cilindro com água da qual é impossível sair por conta própria. Após algum tempo, as tentativas ativas do animal de sair do cilindro são substituídas por um "estado de desespero" (o animal está na água praticamente sem movimentos).A redução da imobilidade (imobilização) do animal é considerada um correlato do efeito antidepressivo. O BDNF teve um efeito antidepressivo após a introdução no giro dentado (nicho neurogênico) e na zona CA3 do hipocampo (os neurônios dessa zona fornecem interação do giro dentado com outras áreas do hipocampo).
2.
Quando o BDNF foi introduzido na região ventral do pneu (a zona responsável pela produção de dopamina e que sofre de distúrbios depressivos), o efeito oposto foi registrado - um aumento no comportamento do tipo depressivo.
Miméticos
Como não é possível usar o próprio BDNF como medicamento, está sendo desenvolvido um medicamento baseado nesse fator. Em particular, as regiões ativas da molécula de BDNF foram bem estudadas (cuja estrutura espacial determina o nome do laço. Fig. 15).
Atualmente, os miméticos (substâncias que imitam a atividade) do BDNF estão sendo estudados ativamente.
Desenvolvimento de uma nova geração de medicamentos baseados no fator neurotrófico cerebral (BDNF)
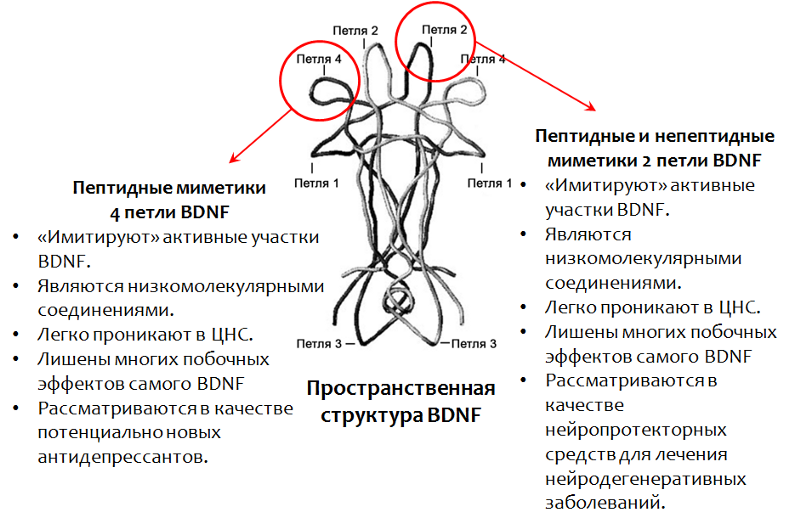 Fig. 15. Fletcher JM, Morton CJ, Zwar RA et al. Projeto de um mimético circular definido de forma conformacional e proteoliticamente estável do fator neurotrófico derivado do cérebro // The Journal of Biological Chemistry. 2008.283 (48). P. 33375-83. Massa SM, Yang T., Xie Y. et al. V Os miméticos de moléculas pequenas de BDNF ativam a sinalização de TrkB e evitam a degeneração neuronal em roedores // The Journal of Clinical Investigation. 20/11/2010 (5). P. 1774–85. .., .., .. . BDNF, -106 // Acta Naturae. 2013. 4(19). P. 116–120.
Fig. 15. Fletcher JM, Morton CJ, Zwar RA et al. Projeto de um mimético circular definido de forma conformacional e proteoliticamente estável do fator neurotrófico derivado do cérebro // The Journal of Biological Chemistry. 2008.283 (48). P. 33375-83. Massa SM, Yang T., Xie Y. et al. V Os miméticos de moléculas pequenas de BDNF ativam a sinalização de TrkB e evitam a degeneração neuronal em roedores // The Journal of Clinical Investigation. 20/11/2010 (5). P. 1774–85. .., .., .. . BDNF, -106 // Acta Naturae. 2013. 4(19). P. 116–120.4 (BDNF) — -106
 Fig. 16. Seredenin S.B., Voronina T.A., Gudasheva T.A. et al. Efeito antidepressivo do mimético BDNF original de baixo peso molecular, dipeptídeo dimérico GSB-106 // Acta Naturae. 2013.4 (19). P. 116-120.GSB-106 - uma substância da estrutura peptídica, é um BDNF mimético de 4 laços (desenvolvimento doméstico). A substância tem um efeito antidepressivo em modelos animais sob vários modos de administração. Atualmente, estudos extensivos das propriedades farmacológicas deste composto estão sendo conduzidos com o objetivo de criar uma nova geração de antidepressivo em sua base.
Fig. 16. Seredenin S.B., Voronina T.A., Gudasheva T.A. et al. Efeito antidepressivo do mimético BDNF original de baixo peso molecular, dipeptídeo dimérico GSB-106 // Acta Naturae. 2013.4 (19). P. 116-120.GSB-106 - uma substância da estrutura peptídica, é um BDNF mimético de 4 laços (desenvolvimento doméstico). A substância tem um efeito antidepressivo em modelos animais sob vários modos de administração. Atualmente, estudos extensivos das propriedades farmacológicas deste composto estão sendo conduzidos com o objetivo de criar uma nova geração de antidepressivo em sua base.Neurogênese * e depressão
* A neurogênese é um processo de vários estágios da formação de novas células nervosas no sistema nervoso central maduro, que é uma função adaptativa do sistema nervoso.
 Fuchs E., Flügge G. Neuroplasticidade de adultos: Mais de 40 anos de pesquisa // Plasticidade Neural. 2014. ID do artigo 541870, doi: 10.1155 / 2014/541870Fig. 17Na Figura 17, mostramos as zonas neurogênicas (nichos) dos mamíferos:1) O giro dentado do hipocampo2) As lâmpadas olfativas3) A zona subventricularAcredita-se que o principal nicho neurogênico em humanos seja o hipocampo (giro dentado).O estresse, considerado um dos principais fatores desencadeantes de transtornos depressivos, leva a uma diminuição nos níveis de BDNF e a um aumento no cortisol, o que, por sua vez, aumenta o efeito do glutamato no sistema nervoso central.
Fuchs E., Flügge G. Neuroplasticidade de adultos: Mais de 40 anos de pesquisa // Plasticidade Neural. 2014. ID do artigo 541870, doi: 10.1155 / 2014/541870Fig. 17Na Figura 17, mostramos as zonas neurogênicas (nichos) dos mamíferos:1) O giro dentado do hipocampo2) As lâmpadas olfativas3) A zona subventricularAcredita-se que o principal nicho neurogênico em humanos seja o hipocampo (giro dentado).O estresse, considerado um dos principais fatores desencadeantes de transtornos depressivos, leva a uma diminuição nos níveis de BDNF e a um aumento no cortisol, o que, por sua vez, aumenta o efeito do glutamato no sistema nervoso central. Fig. 18Essas alterações, em conjunto, suprimem a neurogênese do hipocampo e levam a uma diminuição no volume do hipocampo. Sob a ação do glutamato, a apoptose (morte programada das células nervosas) também é possível. Violando a neurogênese, o cérebro não consegue compensar totalmente a perda e os sintomas depressivos se desenvolvem.O glutamato é um dos principais aminoácidos excitatórios do sistema nervoso central. A violação da neuroplasticidade sob a influência da ação excessiva do glutamato, aparentemente, está associada a uma reação compensatória. Os neurônios “removem” conexões desnecessárias e morrem (apoptose), a fim de proteger o sistema nervoso central da superexcitação e conseqüências prejudiciais subsequentes desse processo.Um fato bem conhecido é a capacidade dos antidepressivos de estimular a neurogênese, no entanto, os mecanismos subjacentes a esse fenômeno ainda não foram totalmente estudados. Sabe-se que todos os grupos de antidepressivos atuam no sistema monoamínico do cérebro e compensam os déficits funcionais ou materiais da serotonina e da noradrenalina. Além disso, as drogas desse grupo farmacológico aumentam os níveis do fator neurotrófico cerebral.
Fig. 18Essas alterações, em conjunto, suprimem a neurogênese do hipocampo e levam a uma diminuição no volume do hipocampo. Sob a ação do glutamato, a apoptose (morte programada das células nervosas) também é possível. Violando a neurogênese, o cérebro não consegue compensar totalmente a perda e os sintomas depressivos se desenvolvem.O glutamato é um dos principais aminoácidos excitatórios do sistema nervoso central. A violação da neuroplasticidade sob a influência da ação excessiva do glutamato, aparentemente, está associada a uma reação compensatória. Os neurônios “removem” conexões desnecessárias e morrem (apoptose), a fim de proteger o sistema nervoso central da superexcitação e conseqüências prejudiciais subsequentes desse processo.Um fato bem conhecido é a capacidade dos antidepressivos de estimular a neurogênese, no entanto, os mecanismos subjacentes a esse fenômeno ainda não foram totalmente estudados. Sabe-se que todos os grupos de antidepressivos atuam no sistema monoamínico do cérebro e compensam os déficits funcionais ou materiais da serotonina e da noradrenalina. Além disso, as drogas desse grupo farmacológico aumentam os níveis do fator neurotrófico cerebral.Antidepressivos podem estimular a neurogênese
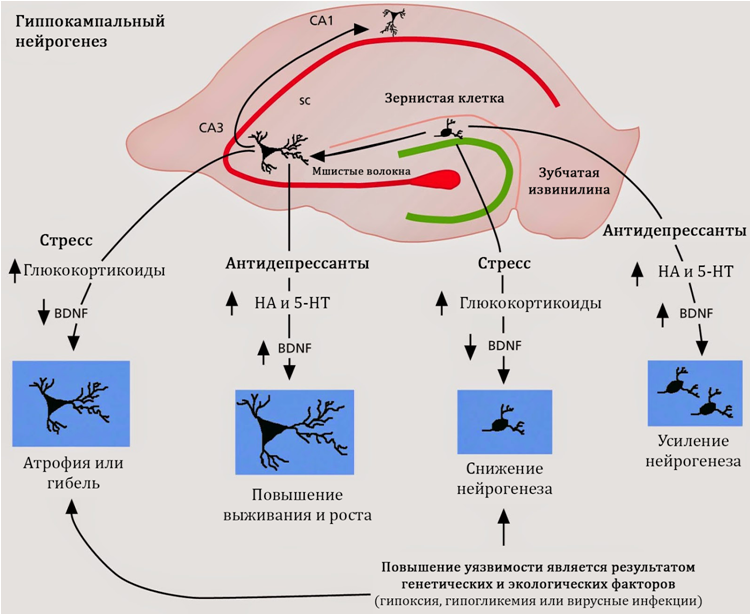 Fig. 19A estimulação da neurogênese é característica dos antidepressivos, independentemente de seu mecanismo de ação, estrutura química ou classe. Portanto, a busca por mecanismos de regulação da neurogênese deve ser realizada em propriedades comuns a todos os antidepressivos. Tais propriedades comuns são a atividade de antidepressivos contra a serotonina e a noradrenalina.Hoje, uma idéia está se formando sobre o papel da serotonina na regulação da neurogênese do hipocampo.
Fig. 19A estimulação da neurogênese é característica dos antidepressivos, independentemente de seu mecanismo de ação, estrutura química ou classe. Portanto, a busca por mecanismos de regulação da neurogênese deve ser realizada em propriedades comuns a todos os antidepressivos. Tais propriedades comuns são a atividade de antidepressivos contra a serotonina e a noradrenalina.Hoje, uma idéia está se formando sobre o papel da serotonina na regulação da neurogênese do hipocampo.Possíveis mecanismos de atividade neurogênica de antidepressivos
 Fig. 20. Alenina N., Klempin F. O papel da serotonina na neurogênese do hipocampo adulto. Pesquisa comportamental do cérebro. 2015. 277. P. 49-57.Em primeiro lugar, o giro dentado do hipocampo recebe regulação da serotonina dos grandes núcleos da sutura (o acúmulo de células nervosas que produzem serotonina; localizadas no tronco cerebral) tanto diretamente quanto através de neurônios intercalares que carregam vários subtipos de receptores de serotonina em sua superfície.Em segundo lugar, nas próprias células-tronco, foram detectados receptores de serotonina do subtipo 1A , o que indica a capacidade potencial da serotonina em regular as células-tronco cerebrais.
Fig. 20. Alenina N., Klempin F. O papel da serotonina na neurogênese do hipocampo adulto. Pesquisa comportamental do cérebro. 2015. 277. P. 49-57.Em primeiro lugar, o giro dentado do hipocampo recebe regulação da serotonina dos grandes núcleos da sutura (o acúmulo de células nervosas que produzem serotonina; localizadas no tronco cerebral) tanto diretamente quanto através de neurônios intercalares que carregam vários subtipos de receptores de serotonina em sua superfície.Em segundo lugar, nas próprias células-tronco, foram detectados receptores de serotonina do subtipo 1A , o que indica a capacidade potencial da serotonina em regular as células-tronco cerebrais.Os mecanismos de atividade neurogênica dos antidepressivos
 Fig. 21Como mostrado em estudos experimentais (em animais e culturas de células), inibidores seletivos da recaptação de serotonina (ISRSs, um medicamento clássico desse grupo - fluoxetina) podem estimular o estágio de proliferação da neurogênese no hipocampo.O mecanismo proposto é um aumento na concentração de serotonina (5-HT - serotonina, também conhecida como 5-hidroxitriptamina) no sistema nervoso central e a subsequente (aprimorada) estimulação da neurogênese da serotonina. Os receptores de serotonina do subtipo 1A (receptores 5HT1A) também podem servir comoalvos potenciais para antidepressivos durante a neurogênese. Essas suposições são consistentes com os dados sobre o efeito positivo (terapêutico) da ativação dos receptores de serotonina 5-HT1A por antidepressivos (por exemplo, Vilazodona) em pacientes com distúrbios depressivos.Outro argumento que nos permite considerar a estimulação da neurogênese como o principal mecanismo de ação dos antidepressivos é a coincidência no tempo entre o tempo médio de início do efeito terapêutico (de 2 a 7 semanas) e o ciclo completo da neurogênese (3 a 7 semanas).Além desses mecanismos, os antidepressivos SSRI também demonstram a capacidade de aumentar os níveis de BDNF, mas os mecanismos desse efeito permanecem desconhecidos.
Fig. 21Como mostrado em estudos experimentais (em animais e culturas de células), inibidores seletivos da recaptação de serotonina (ISRSs, um medicamento clássico desse grupo - fluoxetina) podem estimular o estágio de proliferação da neurogênese no hipocampo.O mecanismo proposto é um aumento na concentração de serotonina (5-HT - serotonina, também conhecida como 5-hidroxitriptamina) no sistema nervoso central e a subsequente (aprimorada) estimulação da neurogênese da serotonina. Os receptores de serotonina do subtipo 1A (receptores 5HT1A) também podem servir comoalvos potenciais para antidepressivos durante a neurogênese. Essas suposições são consistentes com os dados sobre o efeito positivo (terapêutico) da ativação dos receptores de serotonina 5-HT1A por antidepressivos (por exemplo, Vilazodona) em pacientes com distúrbios depressivos.Outro argumento que nos permite considerar a estimulação da neurogênese como o principal mecanismo de ação dos antidepressivos é a coincidência no tempo entre o tempo médio de início do efeito terapêutico (de 2 a 7 semanas) e o ciclo completo da neurogênese (3 a 7 semanas).Além desses mecanismos, os antidepressivos SSRI também demonstram a capacidade de aumentar os níveis de BDNF, mas os mecanismos desse efeito permanecem desconhecidos.O efeito da fluoxetina (Prozac) na neurogênese de primatas não humanos
 Fig. 22. Perera TD, Dwork AJ, Keegan KA, et al. Necessidade da neurogênese hipocampal para a ação terapêutica de antidepressivos em primatas não humanos adultos // PLoS ONE. 2011.6 (4): e17600. doi: 10.1371 / journal.pone.0017600.Estudos em primatas (o modelo animal mais relevante) demonstraram a capacidade da fluoxetina (nome comercial "Prozac") em estimular a neurogênese contra o estresse (neste caso, usamos o modelo de estresse de isolamento). A Figura 22 mostra que a fluoxetina aumentou significativamente (estatisticamente significante) a taxa de proliferação (divisão) de células nervosas-tronco no hipocampo de primatas.
Fig. 22. Perera TD, Dwork AJ, Keegan KA, et al. Necessidade da neurogênese hipocampal para a ação terapêutica de antidepressivos em primatas não humanos adultos // PLoS ONE. 2011.6 (4): e17600. doi: 10.1371 / journal.pone.0017600.Estudos em primatas (o modelo animal mais relevante) demonstraram a capacidade da fluoxetina (nome comercial "Prozac") em estimular a neurogênese contra o estresse (neste caso, usamos o modelo de estresse de isolamento). A Figura 22 mostra que a fluoxetina aumentou significativamente (estatisticamente significante) a taxa de proliferação (divisão) de células nervosas-tronco no hipocampo de primatas.O efeito da fluoxetina na neurogênese de primatas não humanos
 Fig. 23. Perera TD, Dwork AJ, Keegan KA, et al. Necessidade da neurogênese hipocampal para a ação terapêutica de antidepressivos em primatas não humanos adultos // PLoS ONE. 2011.6 (4): e17600. doi: 10.1371 / journal.pone.0017600.O efeito do estresse levou a uma diminuição da camada granular do giro dentado do hipocampo - a principal zona neurogênica do cérebro dos primatas. A administração de fluoxetina em um contexto de exposição estressante impediu essa alteração e manteve o volume dessa estrutura (volume total) normal.
Fig. 23. Perera TD, Dwork AJ, Keegan KA, et al. Necessidade da neurogênese hipocampal para a ação terapêutica de antidepressivos em primatas não humanos adultos // PLoS ONE. 2011.6 (4): e17600. doi: 10.1371 / journal.pone.0017600.O efeito do estresse levou a uma diminuição da camada granular do giro dentado do hipocampo - a principal zona neurogênica do cérebro dos primatas. A administração de fluoxetina em um contexto de exposição estressante impediu essa alteração e manteve o volume dessa estrutura (volume total) normal.O efeito da fluoxetina na neurogênese de primatas não humanos
Correlação entre anedonia (comportamento depressivo) e neurogênese
Perera TD, Dwork AJ, Keegan KA, et al. Necessidade da neurogênese hipocampal para a ação terapêutica de antidepressivos em primatas não humanos adultos. MAIS UM. 2011.6 (4): e17600. doi: 10.1371 / journal.pone.0017600.Verificou-se que existe uma correlação entre o estímulo da neurogênese pela fluoxetina e a prevenção do desenvolvimento de comportamento depressivo (anedonia).
Ao estudar o efeito da fluoxitina na neurogênese de primatas não humanos, foi estabelecida uma correlação significativa entre uma diminuição na neurogênese (causada pelo estresse) e um aumento no comportamento depressivo dos primatas (anedonia, que foi determinado por uma combinação de distúrbios sociais e alimentares), bem como uma correlação entre a estimulação da neurogênese com fluoxetina e a ausência de depressão comportamento semelhante.
A noradrenalina é outra monoamina importante que, juntamente com a serotonina, é capaz de participar da regulação da neurogênese do hipocampo.
Possíveis mecanismos de atividade neurogênica de antidepressivos
 Fig. 25. Jhaveri DJ, Mackay EW, Hamlin AS e outros. A norepinefrina ativa diretamente os precursores do hipocampo adulto via receptores adrenérgicos β3 // The Journal of Neuroscience. 2010.30 (7). Z. 2795-2806. doi: 10.1523 / JNEUROSCI.3780-09-09.
Fig. 25. Jhaveri DJ, Mackay EW, Hamlin AS e outros. A norepinefrina ativa diretamente os precursores do hipocampo adulto via receptores adrenérgicos β3 // The Journal of Neuroscience. 2010.30 (7). Z. 2795-2806. doi: 10.1523 / JNEUROSCI.3780-09-09.Em estudos sobre culturas de neurônios do hipocampo, foi demonstrado que a noradrenalina (ao contrário da serotonina) aumentou o número de células-tronco. A serotonina, como demonstrado anteriormente, não afetou a quantidade, mas a taxa de proliferação.
Além das alterações quantitativas, a norepinefrina também causou alterações qualitativas - aumentou o tamanho das neuroesferas, o que é claramente mostrado na imagem do microscópio eletrônico (ver Fig. 26).
Possíveis mecanismos de atividade neurogênica de antidepressivos
 Fig. 26. Jhaveri DJ, Mackay EW, Hamlin AS e outros. A norepinefrina ativa diretamente os precursores do hipocampo adulto via receptores adrenérgicos β3 // The Journal of Neuroscience. 2010.30 (7). Z. 2795-2806. doi: 10.1523 / JNEUROSCI.3780-09-09.
Fig. 26. Jhaveri DJ, Mackay EW, Hamlin AS e outros. A norepinefrina ativa diretamente os precursores do hipocampo adulto via receptores adrenérgicos β3 // The Journal of Neuroscience. 2010.30 (7). Z. 2795-2806. doi: 10.1523 / JNEUROSCI.3780-09-09.O papel das células gliais na formação de transtornos depressivos
Examinamos previamente alterações nos neurônios, mas ignoramos o papel das células gliais na formação de distúrbios depressivos. No entanto, estudos experimentais e clínicos indicam um possível papel da patologia das células da glia na patogênese da depressão.
O papel da glia na formação de transtornos depressivos
 Fig. 27. Rajkowska G., Miguel-Hidalgo JJ Gliogênese e Patologia Glial em Depressão // CNS e Distúrbios Neurológicos Alvos de Drogas. 2007.6 (3). P. 219-233.
Fig. 27. Rajkowska G., Miguel-Hidalgo JJ Gliogênese e Patologia Glial em Depressão // CNS e Distúrbios Neurológicos Alvos de Drogas. 2007.6 (3). P. 219-233.Os pesquisadores apresentaram um diagrama da patogênese dos distúrbios depressivos envolvendo a glia (Fig. 27).
Uma predisposição genética pode incluir: um fator hereditário (a presença de um distúrbio depressivo em um dos pais aumenta o risco dessa doença na criança); polimorfismo genético: BDNF, um transportador de serotonina (envolvido na recaptação de serotonina nas células nervosas e gliais), receptores de serotonina, enzimas de síntese de serotonina (triptofano hidroxilase tipo 2).
A vulnerabilidade genética, combinada com fatores ambientais e de estresse, cria um ambiente favorável para a formação de transtorno depressivo.Os cientistas descobriram que o papel das células da glia não é o mesmo em pacientes jovens e idosos (Fig. 28). As células da glia podem desempenhar um papel importante na patogênese dos estágios iniciais dos distúrbios depressivos, o que pode causar uma diminuição pronunciada no número de neurônios piramidais na idade adulta.
O papel das células gliais na formação de distúrbios depressivos não é o mesmo em pacientes jovens e idosos.
 Fig. 28. Rajkowska G., Miguel-Hidalgo JJ Gliogênese e Patologia Glial em Depressão // CNS e Distúrbios Neurológicos Alvos de Drogas. 2007.6 (3). P. 219-233.
Fig. 28. Rajkowska G., Miguel-Hidalgo JJ Gliogênese e Patologia Glial em Depressão // CNS e Distúrbios Neurológicos Alvos de Drogas. 2007.6 (3). P. 219-233.Em particular, a perda da função das células da glia em uma idade jovem aumenta o risco de desenvolver episódios repetidos de depressão na velhice, mas a deficiência de neurônios piramidais em vez de células da glia já prevalecerá.
 Fig. 29. Rajkowska G., Miguel-Hidalgo JJ Gliogênese e Patologia Glial em Depressão // CNS e Distúrbios Neurológicos Alvos de Drogas. 2007.6 (3). P. 219-233.
Fig. 29. Rajkowska G., Miguel-Hidalgo JJ Gliogênese e Patologia Glial em Depressão // CNS e Distúrbios Neurológicos Alvos de Drogas. 2007.6 (3). P. 219-233.Essa dinâmica é consistente com uma das funções mais importantes das células da glia - a absorção do excesso de glutamato pela fenda sináptica (contato entre as células nervosas). O glutamato é um dos principais neurotransmissores excitatórios do sistema nervoso central e sua ação excessiva pode levar a neuroplasticidade e excitotoxicidade prejudicadas (neurotoxicidade associada à excitação excessiva; parece ser uma reação protetora das células nervosas devido à superexcitação - o número de neurônios e conexões entre elas diminui).
Nas células gliais, existe uma proteína transportadora envolvida na transferência de glutamato da fenda sináptica para a célula glial, onde o glutamato é metabolizado.
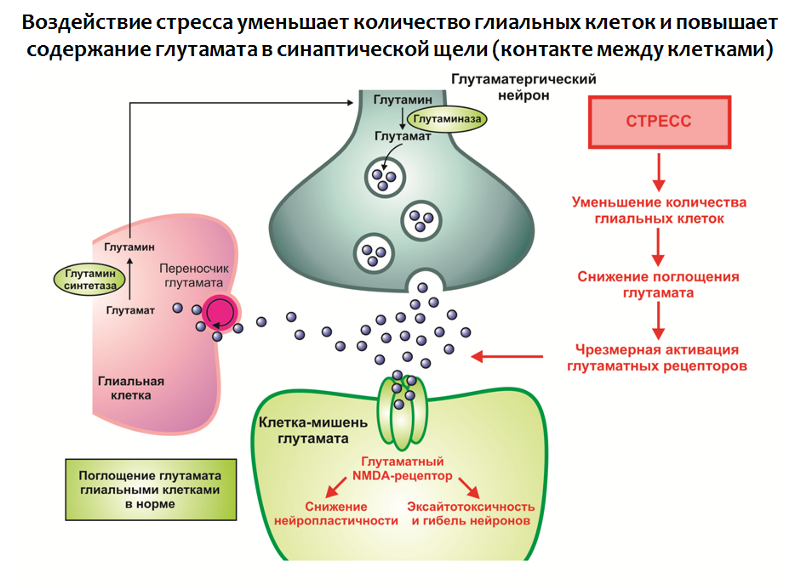 Fig. 30. Rajkowska G., Miguel-Hidalgo JJ Gliogênese e Patologia Glial em Depressão // CNS e Distúrbios Neurológicos Alvos de Drogas. 2007.6 (3). P. 219-233.
Fig. 30. Rajkowska G., Miguel-Hidalgo JJ Gliogênese e Patologia Glial em Depressão // CNS e Distúrbios Neurológicos Alvos de Drogas. 2007.6 (3). P. 219-233.A exposição ao estresse em combinação com outros fatores leva a:
1. Diminuição do número de células gliais nas estruturas do sistema límbico do cérebro;
2. Hiperprodução de glutamato.
Assim, forma-se um excesso desse emocionante neurotransmissor, que é um modulador negativo da neuroplasticidade (acredita-se que isso possa fazer parte de uma reação compensatória que protege o sistema nervoso da superexcitação).
A função das células gliais não se limita à absorção do glutamato, elas também estão envolvidas na produção de neurotrofinas, em particular o BDNF (Fig. 31).
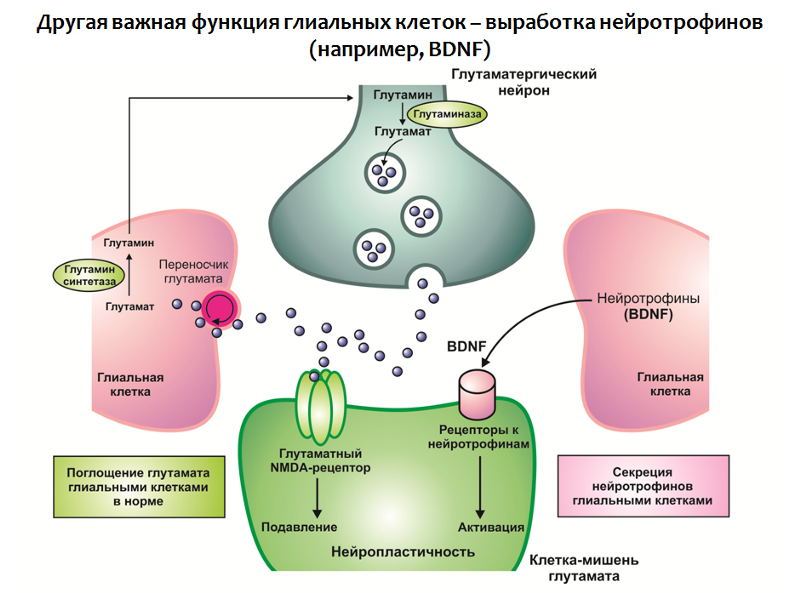 Fig. 31
Fig. 31Em conjunto, um déficit de neurotrofinas e um excesso de glutamato levam a uma violação da neuroplasticidade e alterações depressivas (uma diminuição do volume do hipocampo e do córtex pré-frontal, uma violação da conexão funcional normal entre as estruturas do círculo límbico).
No contexto desse conceito, também é possível encontrar explicações para a eficácia terapêutica dos antidepressivos (Fig. 32):
1. Os antidepressivos são capazes de "mitigar" o efeito do estresse normalizando a atividade do eixo hipotálamo-hipófise-adrenal;
2. Aumentar a concentração de BDNF no sistema nervoso central;
3. Estimular os processos de neuroplasticidade.
 Fig. 32.
Fig. 32.A Figura 33 mostra um esquema de transtorno depressivo generalizado, que se baseia no conceito de neurodegeneração mediada pelo estresse. Observa-se que os antidepressivos ocupam o nicho de "corretores dos efeitos do estresse". Com todas as vantagens e potencial terapêutico, os antidepressivos nem sempre são eficazes na eliminação dos sintomas depressivos.
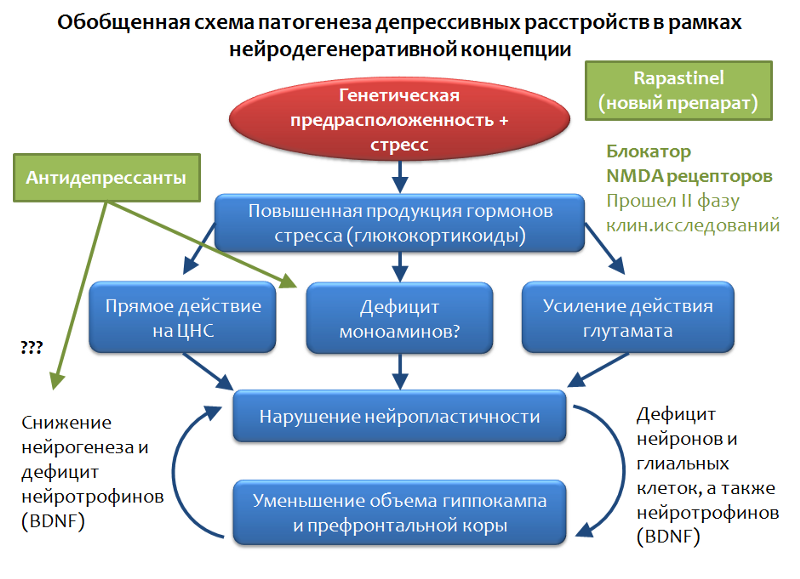 Fig. 33
Fig. 33Existem formas chamadas de distúrbios depressivos resistentes à farmacoterapia. Eles tentam explicar esse fenômeno com uma variedade de fatores de estresse, com diferentes forças e duração da exposição ao estresse e com características individuais (mutação dos alvos antidepressivos). Mas existe apenas uma conclusão a partir dessa situação - é necessária uma busca de alvos fundamentalmente novos para a farmacoterapia dos transtornos depressivos.
Novas tendências na criação de antidepressivos
Uma direção promissora é o efeito no sistema glutamato, se considerarmos esse neurotransmissor como um dos elementos-chave na patogênese dos transtornos depressivos. Sucesso significativo foi alcançado nessa área - um antidepressivo fundamentalmente novo foi criado, que por seu mecanismo é um
bloqueador dos receptores NMDA de glutamato e evita a atividade excessiva desse aminoácido. O antidepressivo Rapasintel passou com sucesso na Fase I e II dos ensaios clínicos, onde demonstrou ser altamente eficaz e é considerado um tratamento para formas persistentes de distúrbios depressivos.
No quadro da teoria glutamatérgica dos transtornos depressivos, pode-se considerar o papel do principal mediador inibitório do sistema nervoso central - ácido gama-aminobutírico (GABA ou GABA).
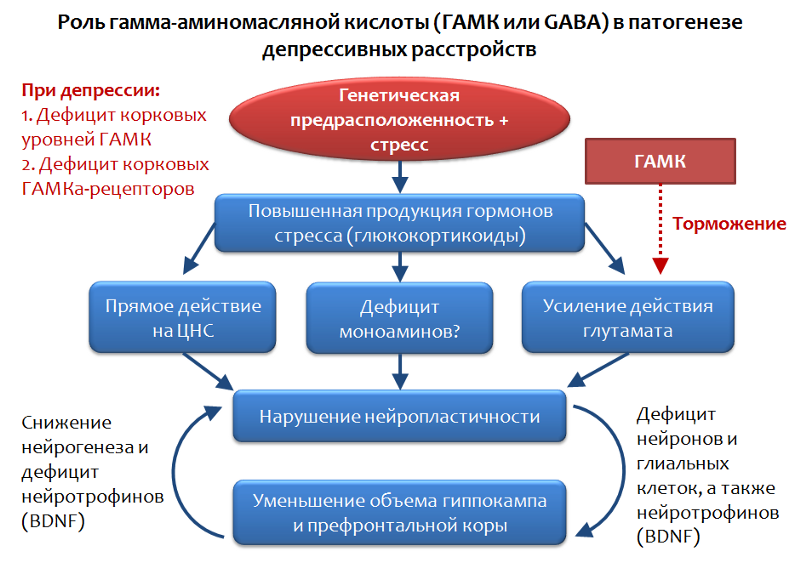 Fig. 34. Möhler H. O sistema GABA em ansiedade e depressão e seu potencial terapêutico // Neuropharmacology. 2012. Jan. 62 (1). P. 42-53.
Fig. 34. Möhler H. O sistema GABA em ansiedade e depressão e seu potencial terapêutico // Neuropharmacology. 2012. Jan. 62 (1). P. 42-53.O GABA é o oposto funcional do glutamato e é capaz de limitar seu efeito estimulante; portanto, a avaliação do papel do GABA nos transtornos depressivos parece bastante lógica.
Foi estabelecido que, no contexto de distúrbios depressivos, é observada uma deficiência dos níveis corticais de GABA e seus receptores. Em particular, os neurônios piramidais que produzem glutamato podem ser inibidos por interneurônios que produzem GABA. O GABA realiza seu efeito inibitório ativando o receptor GABA-A.
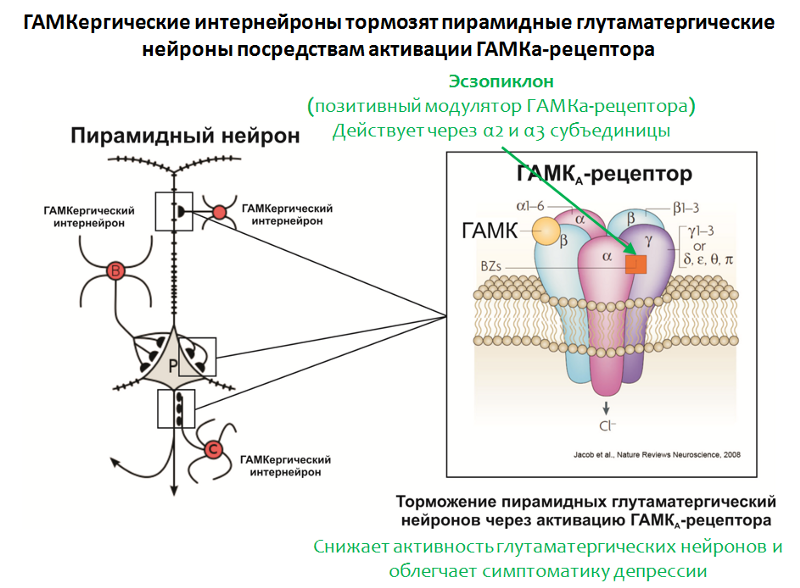 Fig. 35. Möhler H. O sistema GABA em ansiedade e depressão e seu potencial terapêutico // Neuropharmacology. 2012. Jan. 62 (1). P. 42-53.A estrutura do receptor GABA-A
Fig. 35. Möhler H. O sistema GABA em ansiedade e depressão e seu potencial terapêutico // Neuropharmacology. 2012. Jan. 62 (1). P. 42-53.A estrutura do receptor GABA-A é mostrada na Figura 35. O receptor consiste em 5 subunidades (2α, 2β e γ), cada subunidade possui um subtipo, por exemplo, 6 variantes de subunidades α são conhecidas. A combinação de diferentes variantes de subunidades determina o subtipo do receptor GABA-A.
Em apoio ao papel do GABA, a eficácia do modulador positivo do receptor GABA-A, o esopiclon, também fala. O alvo desta droga são os receptores GABA-A que transportam subunidades α2 e α3 em sua composição.
O eszopiklon às vezes
é usado em combinação com antidepressivos e alivia significativamente os sintomas depressivos, mesmo após a retirada do antidepressivo. Acredita-se que seu efeito terapêutico esteja associado a uma diminuição da função do glutamato. Curiosamente, outros moduladores positivos do receptor GABA-A (que requerem a presença de outras variantes das subunidades a, por exemplo,
zolpidem ) não possuem essa atividade.
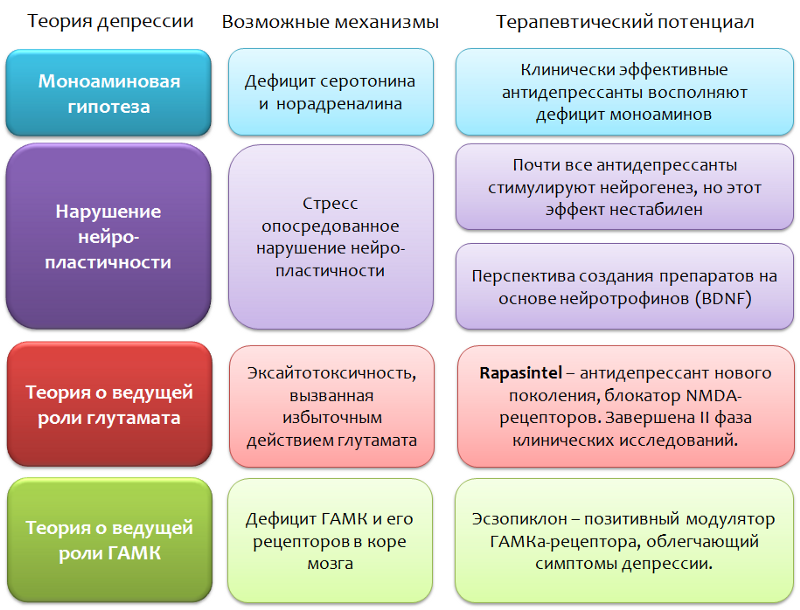 Fig. 36.
Fig. 36.E assim, no esquema apresentado (Fig. 37), resumimos os dados sobre a violação dos processos de neuroplasticidade e o desenvolvimento de sintomas depressivos.
1) A supressão dos processos de neuroplasticidade não é estritamente específica para transtornos depressivos, mas também é observada em outras psicopatologias (esquizofrenia, transtorno afetivo bipolar) e doenças neurológicas (esclerose múltipla, doença de Parkinson, doença de Alzheimer).
2) Em modelos animais, a supressão da proliferação de células-tronco por agentes químicos não bloqueia os efeitos dos antidepressivos (diferentemente dos raios X, onde o efeito oposto é observado).
3) O recurso da neurogênese pode ser limitado e estimulação excessiva pode levar à exaustão.
4) Os efeitos a longo prazo da estimulação artificial prolongada da neurogênese são desconhecidos. Existe o risco de desenvolver um processo tumoral?
5) A violação da neuroplasticidade não é um conceito exaustivo de transtornos depressivos. O conceito não pode explicar completamente a presença de TODOS os sintomas da doença (por exemplo, somatização dos sintomas depressivos, quando os sintomas da depressão são disfarçados como doenças dos órgãos internos - dor de cabeça, dor no coração, abdômen etc.), a natureza do curso (ciclo) e resistência algumas formas de depressão à terapia medicamentosa (apesar do fato de que os antidepressivos ativam a neurogênese e aumentam o BDNF).
Violação dos processos de neuroplasticidade e transtornos depressivos - falhas no conceito
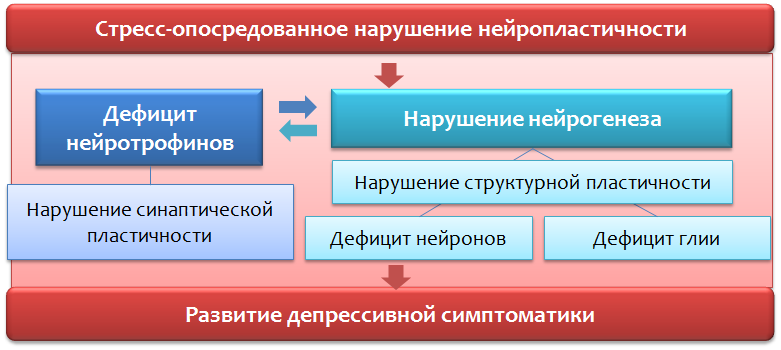 Fig. 37.
Fig. 37.- A supressão dos processos de neuroplasticidade não é específica para transtornos depressivos
- Em modelos animais, a supressão da proliferação de células-tronco nem sempre bloqueia os efeitos dos antidepressivos
- O recurso da neurogênese pode ser limitado e a estimulação excessiva pode levar à exaustão.
- As consequências a longo prazo da estimulação "violenta" prolongada da neurogênese são desconhecidas. Existe o risco de desenvolver um processo tumoral?
- A violação da neuroplasticidade não é um conceito exaustivo de transtornos depressivos.
As teorias sobre o papel dos aminoácidos dos neurotransmissores - glutamato e GABA, não são exaustivas. Primeiramente, os sistemas apresentados (glutamatérgico e GABAérgico) não podem ser considerados isoladamente de outros fatores, porque de fato, eles são um elo intermediário na patogênese de distúrbios depressivos ou sintomas individuais. Em segundo lugar, alterações nos sistemas glutamatérgicos e GABAérgicos do cérebro são observadas não apenas em depressão, mas também em vários outros distúrbios e condições (esquizofrenia, transtornos de ansiedade, ataques de pânico, epilepsia, sensibilidade à dor, doença de Parkinson, doença de Alzheimer).
 Fig. 38.
Fig. 38.Se considerarmos a intervenção farmacológica no sistema glutamatérgico, é sem dúvida promissora e até inovadora, porque anteriormente, todos os antidepressivos agiam exclusivamente no sistema monoaminegico do cérebro. No entanto, uma ampla funcionalidade do glutamato no sistema nervoso central pode levar ao desenvolvimento de efeitos indesejáveis e a várias contra-indicações. Mas é muito cedo para fazer previsões, o bloqueador de receptores de glutamato ainda não passou por testes clínicos de fase III. O medicamento não é considerado um substituto dos antidepressivos modernos, mas como um meio de terapia adjuvante (por exemplo, com formas persistentes de depressão).
Os medicamentos moduladores positivos dos receptores GABAA atualmente não são considerados antidepressivos independentes; são úteis na eliminação de sintomas individuais de transtornos depressivos.
Droga "ideal"
Uma direção promissora para o desenvolvimento de novos antidepressivos eficazes e seguros é o estudo dos mecanismos do estresse propriamente dito, uma vez que é o fator estressante (eventos estressantes) que é considerado o principal gatilho para a formação de transtornos depressivos.
Como deve ser um medicamento promissor?
A busca e criação de um antidepressivo “ideal” deve ser baseada em dois princípios simples (de acordo com Franco Borsini):
1. O medicamento não deve alterar a psique de uma pessoa saudável
2. O medicamento deve agir apenas em condições de psicopatologia
 Fig. 39. Borsini F. Modelos para depressão na triagem de medicamentos e estudos pré-clínicos: Direções futuras // World Journal of Pharmacology. 2012.1 (1). P. 21–29.
Fig. 39. Borsini F. Modelos para depressão na triagem de medicamentos e estudos pré-clínicos: Direções futuras // World Journal of Pharmacology. 2012.1 (1). P. 21–29.A interrupção dos mecanismos de estresse nos estágios iniciais impediria todas as alterações consideradas no contexto de nosso artigo. Tal método de correção, em teoria, parece ser o mais eficaz não apenas para prevenir o desenvolvimento da depressão, mas também para proteção confiável contra recaídas e episódios repetidos e mais graves.
A terapia medicamentosa, por si só, não é o único meio de correção da psicopatologia considerada. Não menos importância deve ser dada à comunicação com os pacientes, identificando a causa da doença. Em alguns casos, a eficácia da psicoterapia também tem alto potencial, pois Ajuda a encontrar soluções para o problema e não combate os sintomas da doença, deixando o problema não resolvido e traduzindo a depressão em formas subcrônicas e crônicas.