"Acho que, a longo prazo, provavelmente podemos usar injeções de RNA para reduzir os efeitos da doença de Alzheimer e de distúrbios pós-traumáticos", diz David Glanzman, principal autor do estudo de cópia de memórias de lebres do mar, uma das quais o biólogo tem em suas mãosÉ geralmente aceito que a memória de longo prazo (LTM) em animais é codificada por alterações na força das conexões sinápticas entre os neurônios. A transmissão de um impulso nervoso entre as células é realizada quimicamente usando mediadores ou eletricamente, através da passagem de íons de uma célula para outra, enquanto a amplitude e a frequência do sinal podem ser reguladas durante a transmissão sináptica.
Mas há uma versão alternativa em que o LTM é codificado por alterações epigenéticas. Nesse caso, os RNAs não codificantes podem servir como mediadores para alterações epigenéticas. Esta versão é considerada uma alternativa, porque até agora pouca evidência empírica foi coletada a seu favor.
Bem, evidências empíricas já foram obtidas.
Um grupo de cientistas da Universidade da Califórnia, Los Angeles, conduziu um
experimento bem -
sucedido na transmissão de memórias de longo prazo da aplisia, um dos maiores representantes do molusco posterior, também chamado de lebres do mar. A memória de longo prazo foi transferida pela injeção de RNA de uma lebre marinha sensibilizada para outras pessoas que nunca haviam experimentado essa experiência antes. Mas, com a ajuda de uma injeção de RNA, eles "sobreviveram" a ela, ou seja, receberam memórias idênticas.
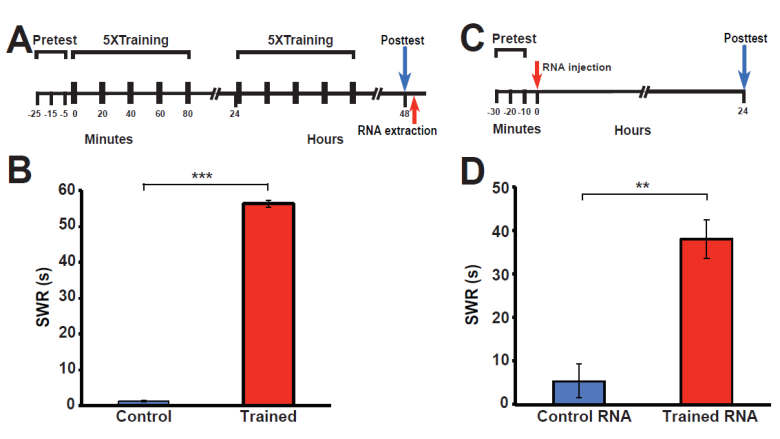
Durante o experimento, lebres do mar foram batidas com fraca corrente elétrica na região da cauda. As lebres receberam cinco descargas elétricas, uma vez a cada 20 minutos, e depois outras cinco com um intervalo de 24 horas. Descargas elétricas reforçavam o reflexo protetor da lebre, que exibe para proteger contra possíveis danos. Quando os caracóis foram batidos mais tarde, os choques elétricos anteriormente experimentados foram reduzidos para proteção em aproximadamente 50 segundos - esse é o tipo de treinamento conhecido como “sensibilização”. Aqueles que não receberam um choque elétrico foram reduzidos em apenas um segundo.
Os biólogos extraíram o RNA do sistema nervoso de lebres marinhas treinadas, bem como daqueles que não receberam golpes. Em seguida, o RNA do primeiro grupo (sensibilizado) foi introduzido em sete aves com uma cajadada, que não recebeu nenhum golpe, e o RNA do segundo grupo foi introduzido nos representantes do grupo controle de sete outros caracóis, que também não receberam nenhum golpe.
Os cientistas descobriram que sete pássaros com uma cajadada, que receberam RNA de caracóis treinados, se comportaram como se tivessem experimentado essa experiência: uma redução protetora durou em média cerca de 40 segundos. Como esperado, nenhuma redução a longo prazo foi encontrada no grupo controle de caracóis.
"Se a memória de longo prazo fosse armazenada nas sinapses, nosso experimento não teria funcionado", explicou Glantzman e acrescentou que a lebre do mar é um excelente modelo para o estudo do cérebro e da memória, porque os cientistas estudaram bem a biologia celular dessa forma animal simples, na qual tradicionalmente colocavam experiências. Os processos celulares e moleculares na lebre marinha são muito semelhantes aos humanos, embora tenha cerca de 20.000 neurônios no sistema nervoso central e cerca de 100 bilhões em seres humanos.
Agora, os cientistas provaram que a mudança celular específica subjacente à sensibilização em lebres do mar (excitabilidade excessiva do neurônio sensorial) pode ser reproduzida expondo os RNAs sensoriais de animais treinados. Esses resultados fornecem evidências para apoiar o modelo epigenético não sináptico de memória em lebres do mar.
Conhecer os mecanismos de formação da memória a longo prazo é muito importante para o desenvolvimento de modelos de aprendizado mais eficazes. Se a memória de longo prazo é realmente programada pela exposição ao RNA de um animal treinado, é possível criar modelos de treinamento mais eficazes.
Em vez de treinar milhares de objetos, você pode treinar um único animal, tirar o RNA e injetar todos os outros animais, que precisam transferir a experiência correspondente para a memória de longo prazo.
Além disso, a técnica abre campo para experimentos em "apagar" memórias traumáticas desnecessárias da memória de longo prazo. Por exemplo, se eles trazem dor e sofrimento a um animal ou causam seu comportamento incorreto, como é o caso do
desamparo aprendido . Assim, você pode efetivamente "reprogramar" o comportamento de um ser vivo para seu próprio bem. Naturalmente, as memórias do fato de reprogramar também podem ser apagadas.
O artigo científico foi
publicado em 14 de maio de 2018 na revista
eNeuro (doi: 10.1523 / ENEURO.0038-18.2018,
pdf ).