Antes de iniciar a apresentação do material, gostaria de dizer algumas palavras sobre mim: um membro das comunidades para combater a negação do HIV (“dissidência de HIV / AIDS”): em 2016-2018 “dissidentes de HIV / AIDS e seus filhos”, de 2018 - “Negação do HIV / AIDS e medicina alternativa.”
Minha opinião - e não apenas a minha - é que a maioria dos casos de recusa ao tratamento do HIV é causada por um mal-entendido banal de que se trata de uma infecção crônica controlada, bem como pela estigmatização de pessoas vivendo com HIV - o uso do clichê comum de que o HIV - uma doença das camadas mais baixas da sociedade ou vice-versa, a "elite cultural". Isso não acontece há muito tempo - na Rússia, aproximadamente 1% da população vive com HIV, e a situação não planeja melhorar.
Há cerca de um ano, vários artigos sobre esse recurso me incentivaram a escrever cinco notas sobre a história da luta contra vírus. O objetivo desses artigos era descrever os princípios de trabalho de vários tipos de medicamentos para o HIV (os consultores eram um microbiologista e um especialista em doenças infecciosas). Espero que você goste de organizar essas anotações.
Sobre vírus
Então, algumas palavras sobre vírus em geral: eles ocupam uma posição intermediária entre o mundo vivo e o não-vivo; são incapazes de reprodução independente e, para isso, são necessárias as células do organismo hospedeiro.
O vírus é organizado de maneira bem simples: possui um código genético, o código é fechado em um capsídeo, o capsídeo às vezes é cercado por uma concha. O código pode ser apresentado de várias maneiras. O transportador de código é DNA ou RNA, isto é, ácido nucleico (NK). As cadeias de código podem ser uma ou duas: NK de cadeia dupla e cadeia simples. A corrente pode ser fechada em um anel ou linear. Em 1971, David Baltimore, de acordo com esses sinais, dividiu o vírus em sete classes. Essa classificação ainda está em uso hoje e será importante para explicar como alguns medicamentos funcionam.
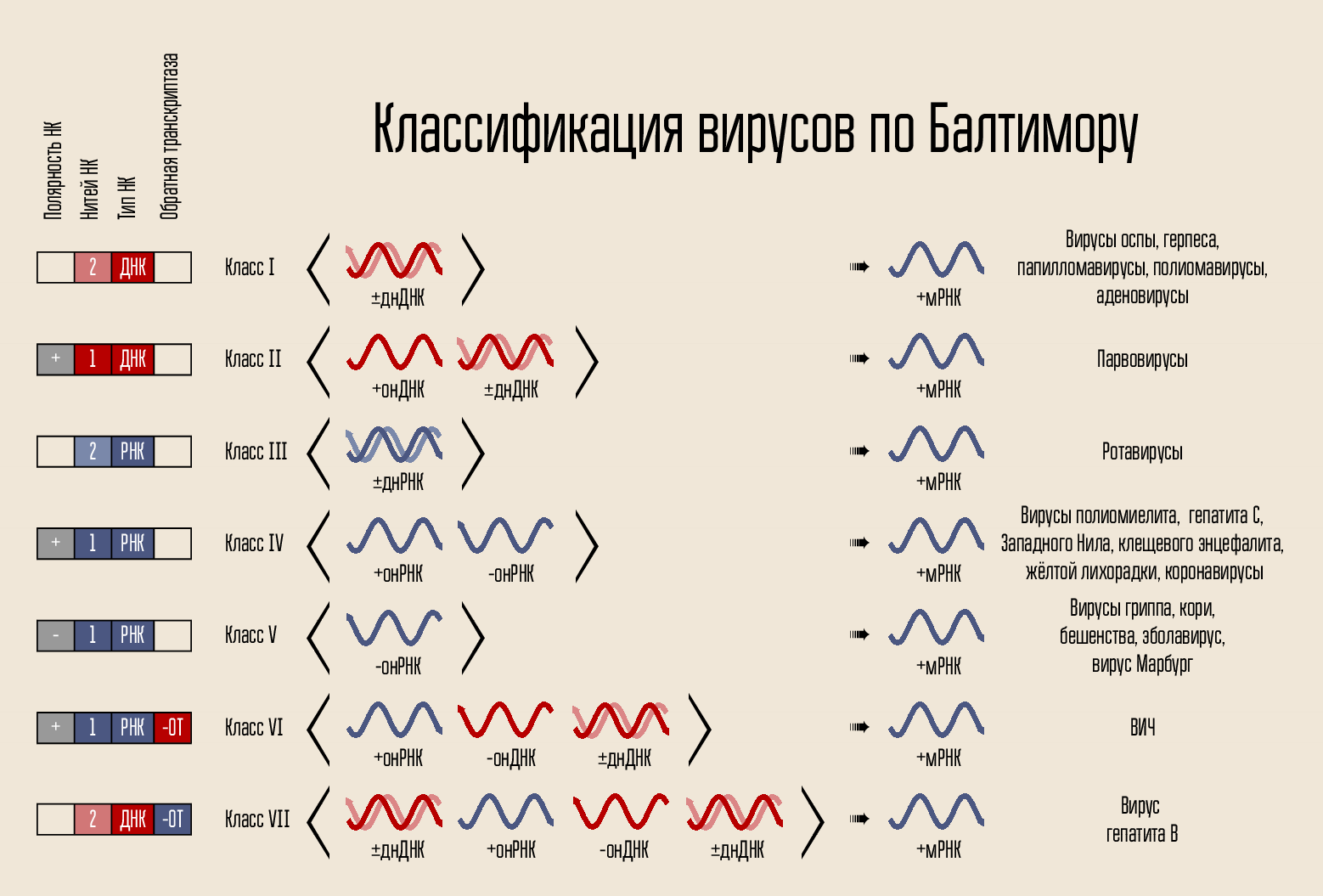
O próprio código para a construção de um novo vírus não pode penetrar na própria célula; ele precisa de algum mecanismo de penetração. Portanto, existe uma concha de proteína - um capsídeo, que protege a NK do vírus e ajuda a penetrar na célula. Em alguns casos, os vírus podem ter membranas lipídicas adicionais.
A penetração do vírus na célula

Para entrar na célula, o vírus deve se conectar à sua membrana. Para fazer isso, existem proteínas na superfície do vírus que se ligam às proteínas receptoras da célula hospedeira - em locais na superfície da parede celular às quais o vírus é capaz de se conectar. E eles devem se encaixar estritamente no vírus, caso contrário ele nem será capaz de se apegar à célula.
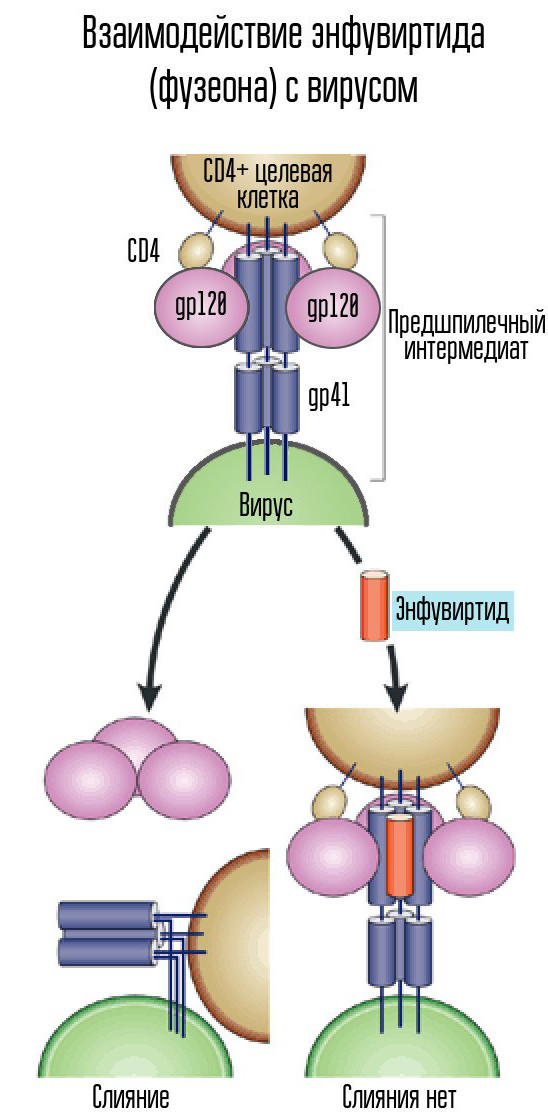
Para isso, o HIV utiliza o receptor CD4 (as células com esse receptor são as células imunológicas do corpo, incluindo linfócitos T, monócitos, macrófagos, etc.). CD4 sozinho não é suficiente - você precisa de outro co-receptor, CCR5 ou CXCR4. O HIV usa a proteína gp120 para aderir. Depois disso, o formato de outra proteína do envelope de vírus, a gp41, muda. Dobra-se para o lado, formando um gancho de cabelo e permitindo que o capsídeo do vírus se funda com a célula.
Enfuvirtida (Fuzeon), um inibidor da proteína gp41, é um dos agentes usados no combate ao vírus. Enfuvirtida combina-se com esta proteína para prevenir a formação de grampos. Assim, o capsídeo do vírus não pode se fundir à célula e a infecção não ocorre. Este medicamento é o único inibidor de fusão desenvolvido e aprovado.
Os retrovírus, dos quais o HIV pertence, são um alvo extremamente inconveniente para os medicamentos devido à sua variabilidade. As células humanas são muito menos voláteis. Sabe-se que cerca de 1% da população do norte da Europa é imune ao HIV: eles são portadores da mutação CCR5-∂32, o que torna o receptor CCR5 inadequado para a combinação com o HIV.
Infelizmente, mudar a forma desse receptor para sempre, inclusive para novas células que continuam aparecendo no corpo humano, é uma tarefa extremamente difícil (embora tenha havido tentativas), mas desenvolver um inibidor de receptor é uma droga que se ligaria ao receptor celular e, assim, impediria a entrada do HIV. para ele - muito possivelmente.
Vários inibidores do receptor CCR5 e CXCR4 estavam em desenvolvimento, mas o único aprovado até o momento é o maraviroc, um inibidor do CCR5.
Transcrição reversa
O que acontece após a fusão do vírus com a célula no caso do HIV?
O HIV é o vírus Classe VI de Baltimore, que armazena seu genoma no RNA. Há DNA no núcleo da célula, então o HIV precisa transformar um ácido nucleico em outro. Essa transcrição (NK → NK) é realizada pelas enzimas correspondentes chamadas polimerases. Para a polimerase de DNA dependente de RNA (isto é, lendo informações do RNA) (isto é, na saída da qual o DNA aparece), existe um nome especial - transcriptase reversa. A transcriptase reversa pega o desoxinucleósido desejado (por uma questão de simplicidade, na verdade envolve trifosfatos desoxinucleósidos) e constrói DNA que é complementar ao RNA viral correspondente.
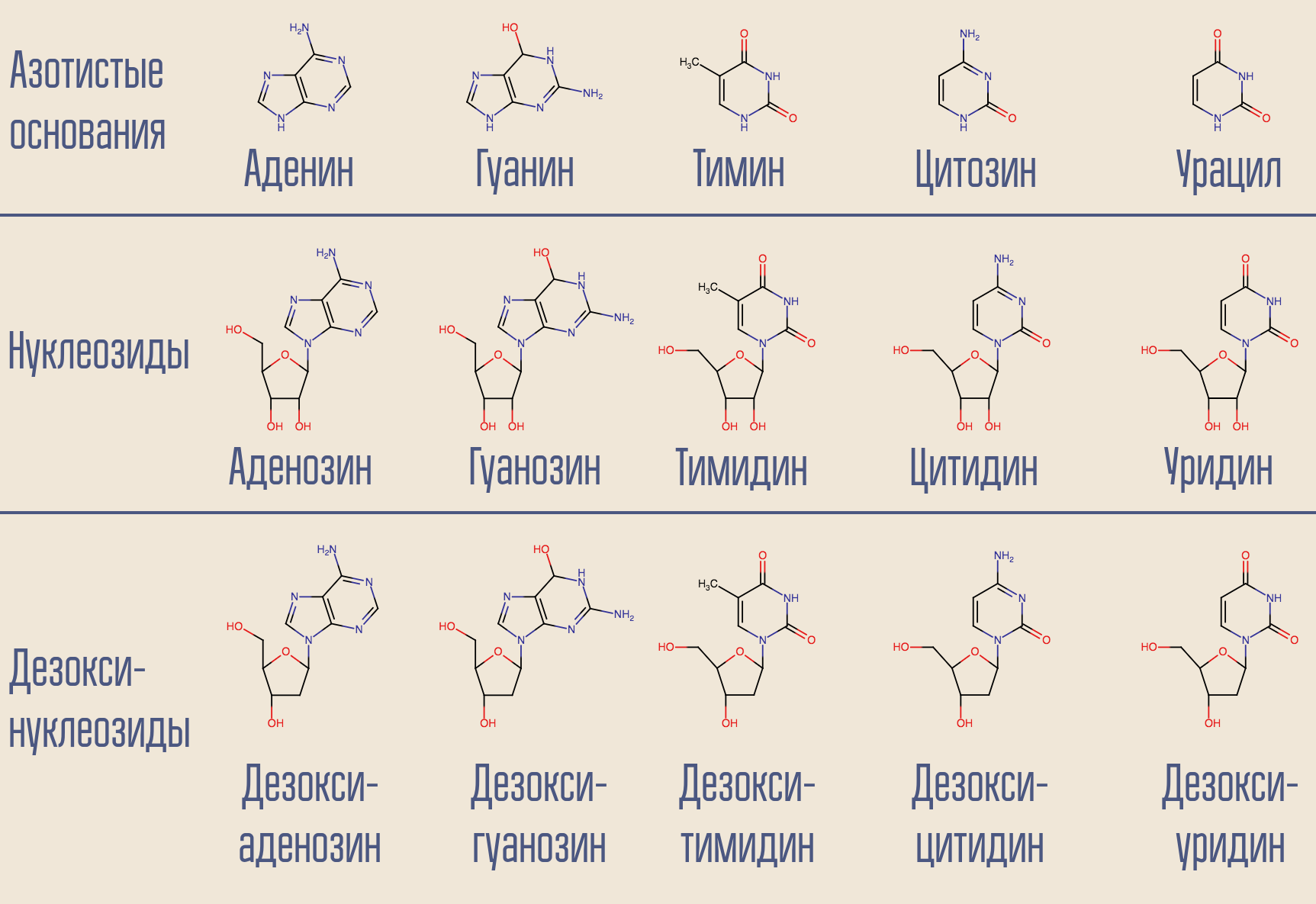
É possível interromper esse processo? Sim, para isso, você só precisa desativar uma transcriptase reversa, algo que se assemelha a um desoxinucleossídeo, mas não é um. Foi assim que o primeiro medicamento para o HIV, a zidovudina (azidotimidina, AZT), agiu. É semelhante à desoxitimidina, mas não é.
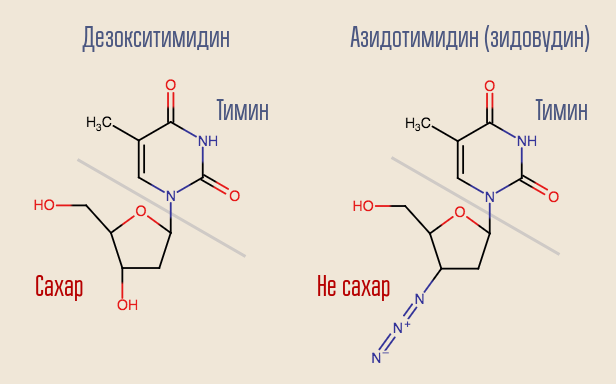
A azidotimidina foi desenvolvida como parte de uma pesquisa por substâncias que poderiam combater tumores. Supunha-se que ele seria incorporado na construção do DNA humano comum, interrompendo-o. Assim, a droga afetaria mais fortemente as células que se dividiam mais rapidamente - células tumorais. Havia certas razões para pensar assim - anteriormente sintetizado outro medicamento desse grupo, a 6-mercaptopurina, foi eficaz no tratamento da leucemia.
Infelizmente, em testes em animais, a droga se mostrou ineficaz e foi esquecida por algum tempo, até que em 1984 o virologista Marty St. Clair, que trabalhava nos laboratórios da Burroughs Wellcome Foundation, iniciou estudos para verificar todas as substâncias disponíveis para opções de tratamento. eles têm uma nova doença - infecção pelo HIV.
A transcriptase reversa “reconheceu” a zidovudina como desoxitimidina e tentou incorporá-la no DNA. A síntese de DNA neste local foi interrompida porque o medicamento era semelhante apenas à desoxitimidina. A zidovudina suprimiu completamente a reprodução do vírus e os testes em humanos foram iniciados quase imediatamente.
Os voluntários infectados pelo HIV foram divididos em dois grupos, um dos quais recebeu placebo e o outro recebeu AZT. A diferença entre os dois grupos foi tão impressionante que mais testes foram considerados desumanos - o medicamento mostrou uma eficácia impressionante.
O sucesso da zidovudina levou a estudos de outros inibidores da transcriptase reversa de nucleosídeos (NRTIs), e muitos outros medicamentos surgiram em pouco tempo. A mais interessante das primeiras drogas é a lamivudina, um análogo de outro desoxinucleosídeo, a desoxicitidina. A desvantagem da lamivudina é que, com a monoterapia com este medicamento, a resistência se desenvolve muito rapidamente, em cerca de um mês. Isto é devido à mutação de ponto único do HIV, M184V. Apesar disso, era desejável deixar a lamivudina no esquema. O fato é que um vírus com essa mutação é hipersensível à zidovudina, e a própria mutação reduz a taxa de replicação do vírus.
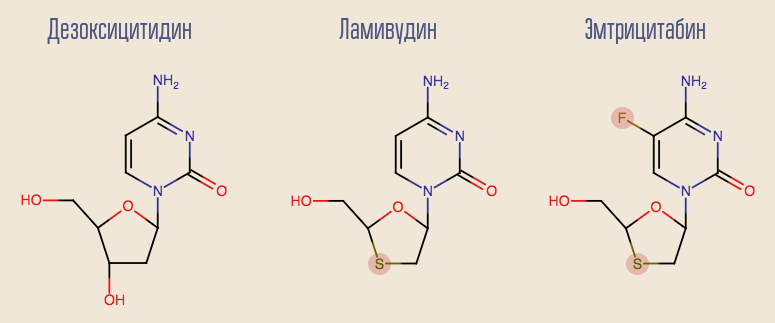
Atualmente, a lamivudina está gradualmente começando a retroceder no passado, dando lugar à sua emtricitabina analógica mais moderna. Tanto a lamivudina como o análogo da desoxiadenosina, adefovir, mostram bons resultados no tratamento da hepatite B. Infelizmente, o adefovir demonstrou ser ineficaz no tratamento do HIV. No entanto, após uma ligeira modificação de sua molécula, uma versão atualizada dela apareceu - tenofovir. Tenofovir e emtricitabina fazem parte de muitas linhas modernas de terapia.
A combinação de dois NRTIs pode prolongar significativamente a vida das pessoas vivendo com HIV, no entanto, ficou claro que, para suprimir totalmente o vírus, era necessário incluir pelo menos um medicamento de um tipo diferente de ação, porque mais cedo ou mais tarde o vírus desenvolveu resistência a qualquer combinação de NRTIs. Uma das primeiras substâncias de um tipo diferente de ação foi outro tipo de inibidor da transcriptase reversa - não nucleósido (NNRTI). Embora a transcriptase reversa (RT) queira trabalhar com algo semelhante a um nucleosídeo (trifosfato de nucleosídeo), você pode tentar criar uma substância que se ligue à RT e mude sua forma para que não possa mais desempenhar suas funções.
Em 1996 e 1998, duas dessas substâncias, nevirapina e efavirenz, respectivamente, foram aprovadas. Cada um deles suprime efetivamente o trabalho do TO e, em combinação com dois NRTIs, cria um esquema completo de terapia anti-retroviral altamente ativa (HAART) - suficiente para uma pessoa que vive com HIV viver uma vida inteira, cuja duração não difere muito da vida de uma pessoa sem HIV .
Em 2006, o primeiro medicamento combinado para uso único por dia foi aprovado: Atripla. O Atripla consiste em dois NRTIs, emtricitabina e tenofovir (na forma de tenofovir disoproxil - um pró-fármaco, uma forma de dosagem quimicamente modificada que se transforma em uma droga diretamente no corpo) e um NNRTI, a efavirenza. Atripla tornou-se um passo qualitativamente novo no sentido de melhorar a qualidade de vida dos pacientes. Até o momento, os medicamentos genéricos da Atripla são um dos medicamentos mais usados no mundo (nos países em desenvolvimento).
No entanto, hoje as NNRTIs estão gradualmente deixando o mercado - medicamentos antigos causam vários efeitos colaterais. Assim, por exemplo, os primeiros dois meses após o início do tratamento com efavirenz podem causar tonturas e outros efeitos semelhantes em alguns pacientes (nem todos!). Claro, isso é muito melhor do que a morte iminente; Essa condição não dura tanto tempo e eles já aprenderam a lidar com ela - no entanto, a tendência atual é a transição para esses medicamentos, o paciente não percebe nenhum efeito colateral deles.
Integração
Se a transcriptase reversa fez seu trabalho, é possível interromper a incorporação do DNA viral no DNA da célula? Uma enzima especial chamada integrase está envolvida nesse processo.
O processo de integração do DNA viral ocorre em várias etapas. Inicialmente, a integrase se liga ao DNA viral, removendo o dinucleotídeo GT da extremidade 3 'de cada fita. Então todo o complexo é transportado para o núcleo, onde a integrase catalisa o estágio da transferência da cadeia. Esse estágio é uma reação de transesterificação (troca de radicais): os nucleotídeos de DNA da célula se conectam não entre si, mas com os nucleotídeos do DNA viral. A integrase ataca ligações internucleotídicas localizadas a uma distância de cinco nucleotídeos. Assim, após a integração, permanecem: o processamento das extremidades 5 'das cadeias virais de DNA, a conclusão de 5 nucleotídeos ausentes e a ligação (a conexão de duas fitas NK com uma enzima ligase), que são realizadas com a participação de proteínas celulares [1].
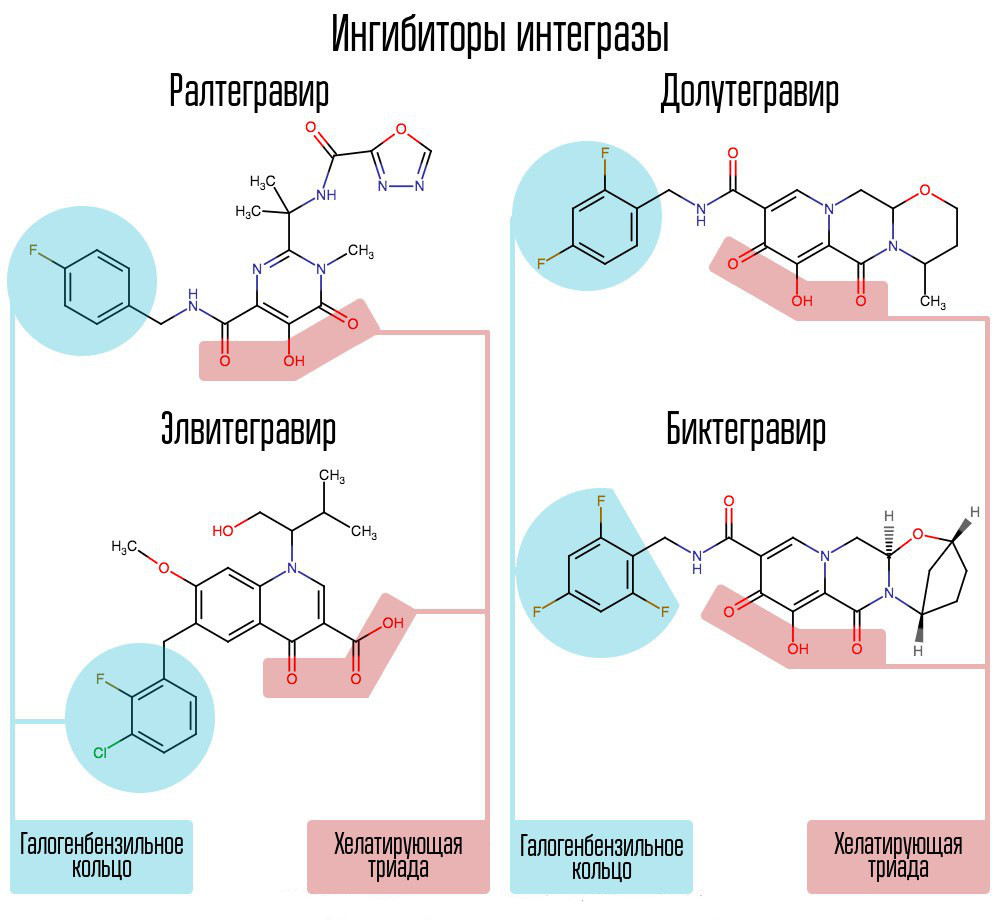
O rastreio de cerca de 250.000 substâncias em bibliotecas de compostos químicos revelou substâncias que inibem a integrase do HIV. Todos eles se mostraram compostos de ácido 2,4-dioxobutanóico. Eles coordenaram íons metálicos no centro ativo da integrase - naquela parte, responsável pela transferência da cadeia. Outras tentativas de desenvolver inibidores da integrase do HIV-1 levaram ao surgimento de um derivado da N-pirimidinona, uma substância MK-0518, chamada raltegravir. [2]
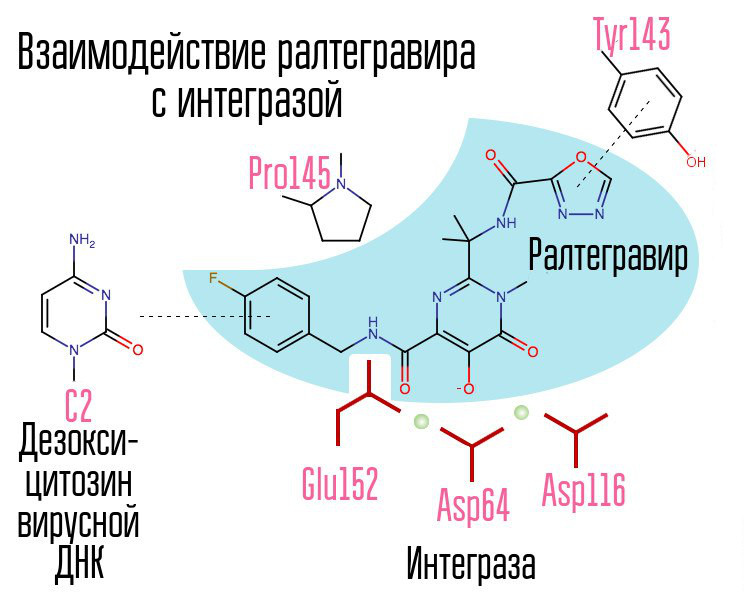
Comum ao raltegravir e aos subsequentes inibidores da integrase são a tríade quelante (íons metálicos coordenadores) e o anel halogênio-benzila que interage com a penitima desoxicitosina na extremidade 3 'do DNA viral ligado à enzima.
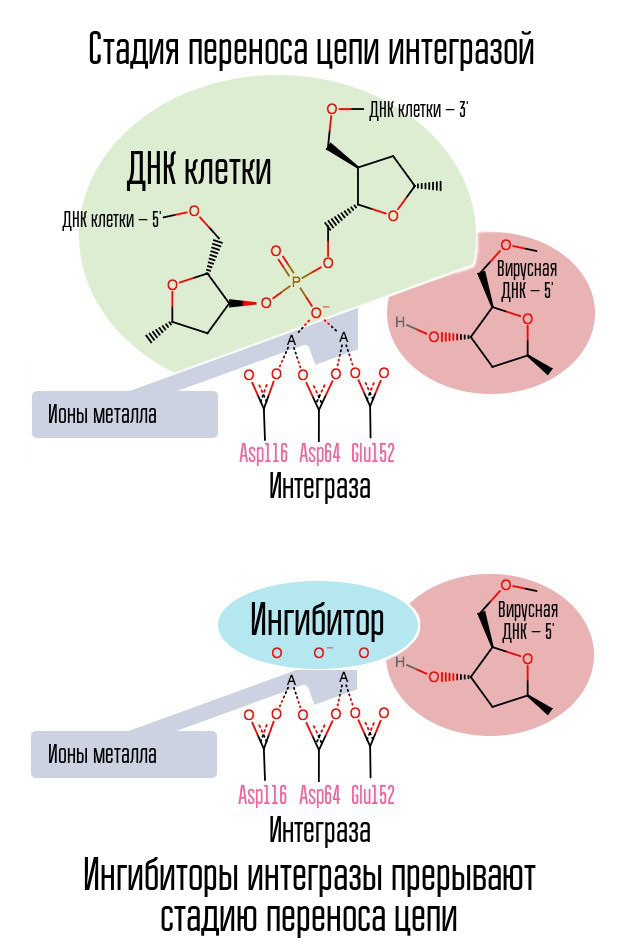
O processo de integração do vírus na célula é o último passo em que a profilaxia pós-exposição é eficaz. Depois disso, as células que transportam o DNA do HIV em seus núcleos aparecem no corpo humano. A janela mais eficaz para a profilaxia pós-exposição é de cerca de 6 a 10 horas.
O anel halogenbenzila na molécula inibidora da integrase interage com o DNA viral e o grupo de átomos de oxigênio interage com dois átomos de metal. A integrase de vírus usa esses átomos de metal para introduzir DNA viral na célula. Como resultado, o processo de integração está bloqueado.
As IAs modernas, como o dolutegravir, conseguiram derrotar as “doenças da infância” do raltegravir associadas à rápida formação de resistência.
Proteólise
Depois que o genoma viral passa pelo estágio de transcrição, os RNAs virais criados são enviados para sair da célula. No processo de criação do virião, está envolvida outra enzima viral chamada protease. A protease corta longas poliproteínas em proteínas funcionais individuais, resultando na formação de enzimas virais e proteínas estruturais do vírus.
A protease é ativa não apenas contra proteínas do HIV, mas também contra proteínas da célula hospedeira, o que pode explicar o efeito citotóxico do HIV (morte celular).
Se a protease estiver bloqueada, o virion não poderá passar pelo estágio de maturação e permanecerá completamente inoperante. A protease do HIV-1 é uma protease aspártica retroviral típica com a sequência de aminoácidos característica Asp25 Thr26 Gly27 (ácido aspártico - treonina - glicina) no centro ativo. O primeiro inibidor de protease, saquinavir, foi aprovado pelo FDA em 6 de dezembro de 1995. Assim, foi após a criação do saquinavir que a terapia antirretroviral altamente ativa ficou disponível pela primeira vez.
Outro representante típico desse grupo de drogas é o lopinavir (usado em conjunto com o ritonavir - kaletra - um dos medicamentos mais comuns para o HIV na Rússia). O ritonavir também é um inibidor da protease, mas é usado como potenciador - graças à sua ação, a concentração da droga principal aumenta.
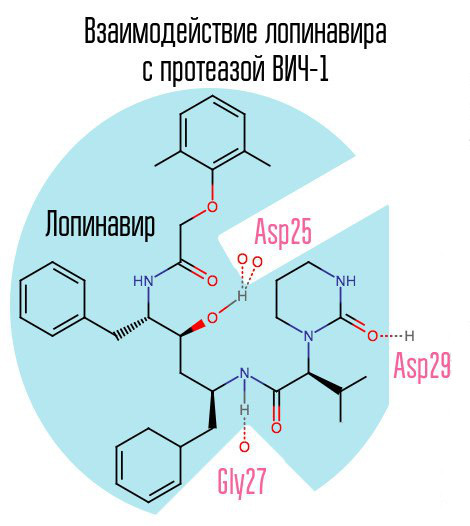
Como o saquinavir e os inibidores subsequentes de protease (IPs) são direcionados especificamente ao centro ativo da enzima, com o desenvolvimento de resistência a um IP, existe uma alta probabilidade de que ocorra resistência a outros IPs. A solução para esse problema pode ser a criação de inibidores direcionados para outras zonas de protease.
O medicamento darunavir (prezista), que apareceu em 2006, atenuou, em certa medida, o problema agudo das cepas resistentes ao HIV-1, pois formava um vínculo anteriormente não utilizado com o ácido aspártico na posição 30.
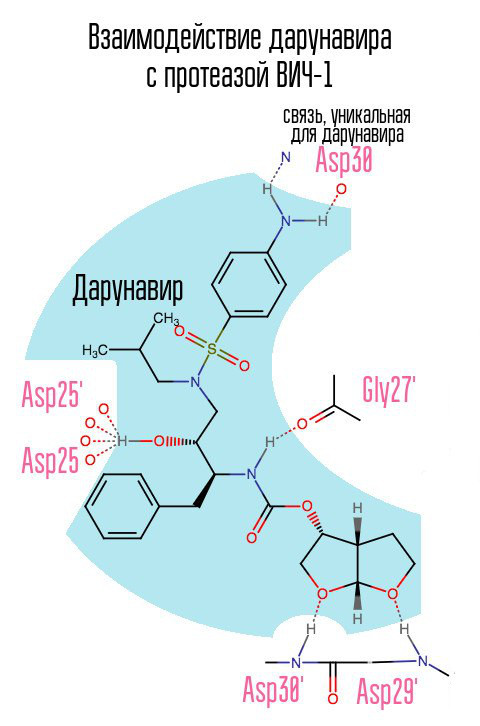
Sem protease, o vírus não pode passar pelo processo de maturação. Os inibidores se ligam ao centro ativo da protease e impedem que ela funcione.
Os inibidores de protease são altamente eficazes em alta carga viral: como neste momento muitos novos virions nascem no corpo, os IPs não permitem que eles amadurecem, reduzindo efetivamente a carga viral em um curto espaço de tempo. No entanto, no momento, os IPs não são utilizados na terapia de primeira linha, dando lugar aos inibidores da integrase (II).
A razão para isso foram os efeitos colaterais: o fato é que, por exemplo, o mesmo kaletra levou à inibição inespecífica da proteólise das proteínas fornecidas com os alimentos, como resultado das quais essas proteínas entraram no intestino delgado e causaram diarréia. Seguir uma dieta específica ou usar novos IPs, como o prezista, pode reduzir esse efeito a quase zero, mas outro efeito associado ao aumento dos níveis de açúcar geralmente impede o uso de inibidores de protease indefinidamente.
Regimes de tratamento modernos
Até o momento, os mais modernos são considerados esquemas que consistem em um inibidor da integrase e um ou dois NRTIs (dolutegravir + abacavir + lamivudina; dolutegravir + lamivudina é um esquema popular de dois componentes, no entanto, não é adequado para todos). Esses esquemas permitem que uma pessoa viva uma vida plena que não diferir em duração da vida de uma pessoa sem HIV.
Apesar de todos os sucessos, uma cura completa para o HIV ainda não é possível (o transplante de células-tronco da medula óssea de um doador com mutação CCR5-∂32 permite alcançar esse resultado, mas, aparentemente, somente se ocorrer uma reação de transplante versus hospedeiro, num grande número de casos que levam à morte do destinatário).
Conclusão
Os métodos de HIV desenvolvidos ajudaram no combate a outras doenças infecciosas: como mencionado acima, lamivudina e tenofovir são eficazes contra o vírus da hepatite B (Baltimore classe VII - polimerase da hepatite B pode transferir RNA para DNA, portanto, alguns NRTIs são eficazes no combate a ele) . O conhecimento adquirido ajudou a desenvolver medicamentos de ação direta contra a hepatite C, que hoje podem curar completamente esta doença (a hepatite C não possui uma fase latente, portanto, ao suprimir a carga viral, novos virions não têm para onde vir - a doença está completamente curada).
[1] Korolev S. P., Agapkina Yu. Yu., Gottikh M. B. Problemas e perspectivas de uso clínico de inibidores da integração do HIV-1
[2] Shahgildyan V.I. Inibidores da integrase do HIV - a base da terapia anti-retroviral eficaz e segura