Os métodos de administração direcionada de medicamentos estão no auge da popularidade - um efeito pontual nos focos da lesão permite combater a doença, quase sem afetar o tecido saudável. No entanto, permanecem questões: como aumentar a eficácia dessa terapia, acelerar o efeito da droga e minimizar seu acúmulo no corpo? Cientistas do Laboratório de Nanomateriais Biológicos da NUST MISiS trabalham nessa direção há vários anos e, entre as últimas descobertas da equipe, houve um aumento de 30% na eficiência da administração de medicamentos a um tumor maligno usando neutrófilos - células do sistema imunológico. Os resultados são publicados na revista científica internacional
ACS Nano .

Os cientistas conduziram um estudo intravital (no tecido vivo) do mecanismo de administração direcionada de medicamentos a tumores malignos usando lipossomas. Descobriu-se que as células imunológicas dos neutrófilos aumentam a eficiência da administração de medicamentos ao tumor em 30%.
Os lipossomas - vesículas de gordura criadas artificialmente - penetram no tumor devido ao chamado efeito de permeabilidade e retenção aprimoradas (EPR). Dentro dos lipossomas, o medicamento é "suturado" e, quando entra no tecido maligno, é liberado.
O efeito da EPR ocorre devido ao crescimento excessivo de vasos sanguíneos, causado pela necessidade anormal do tumor de oxigênio e nutrição.Com o crescimento patológico, grandes poros aparecem nas paredes dos vasos sanguíneos com diâmetro de até 200 nm. Além disso, o crescimento do tumor causa compressão dos vasos linfáticos e impede a saída normal do líquido intercelular. Assim, os lipossomas penetram no tumor e não podem sair devido à drenagem linfática prejudicada.
Acredita-se que, devido ao efeito EPR, os lipossomas possam penetrar apenas no tumor, mas não nos tecidos saudáveis. Mas isso é realmente verdade? E o que acontece no navio?
No decorrer do estudo, os cientistas observaram a entrega do medicamento aos tecidos de camundongos saudáveis e a vários tipos de tumores malignos: câncer de mama, câncer de próstata e melanoma. As observações foram realizadas usando um microscópio intravital, que permite estudar processos diretamente em um organismo vivo.
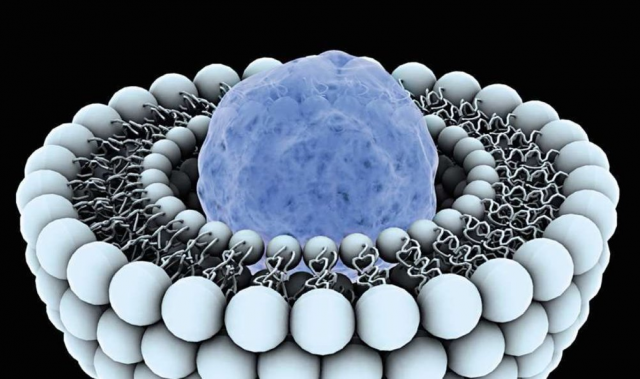 Lipossomas "agarrados" a uma célula cancerígena
Lipossomas "agarrados" a uma célula cancerígena“A primeira conclusão que recebemos como resultado do estudo é que dois tipos de penetração dos lipossomas dos vasos sanguíneos nos tecidos ocorrem nos tecidos vivos. Um microinfiltração é um pequeno acúmulo isolado de lipossomos ao redor de um vaso. Esse processo é inútil para o tratamento de tumores, pois não permite que o medicamento atinja as células tumorais. Além disso, micro-vazamentos foram encontrados em tecidos saudáveis, o que explica a toxicidade dos medicamentos baseados em lipossomos usados em uma clínica moderna ”, diz Viktor Naumenko , autor do trabalho, pesquisador do Laboratório de Nanomateriais Biomédicos do NUST MISiS .
O segundo resultado de observação mais interessante é o neutrófilo, um tipo de glóbulo branco e a célula imune do corpo que vaza para o tecido tumoral. Quando o neutrófilo sai do vaso, junto com ele, através da “porta entreaberta” na parede vascular, os lipossomas conseguem penetrar no tumor. De acordo com os resultados obtidos pela equipe científica, os neutrófilos aumentam em um terço a eficiência da penetração de lipossomas no tumor.
Essa descoberta fornece um padrão claro: os neutrófilos aumentam a permeabilidade vascular do tumor para a administração direcionada de drogas lipossômicas e, portanto, aumentam a chance de cura. Além disso, isso acontece apenas no caso de um macroleak, que é uma grande “nuvem” difusa de lipossomas que penetra profundamente no tumor, garantindo assim a entrega direcionada do medicamento.
“A distinção entre os dois tipos de vazamentos é importante para entender o mecanismo de como os medicamentos baseados em lipossomos funcionam. Nossos resultados indicam que os micro-vazamentos não apenas não contribuem para a entrega de medicamentos às células tumorais, mas também são responsáveis por seu acúmulo indesejável em tecidos saudáveis. O efeito terapêutico é alcançado devido aos macreaklings, e os neutrófilos podem ajudar a fortalecê-lo ” , enfatizou Viktor Naumenko.
Atualmente, a equipe continua estudos laboratoriais para reduzir os efeitos colaterais indesejados da terapia com lipossomas. O desenvolvimento de mecanismos de estimulação artificial para a produção de neutrófilos no corpo do paciente para melhorar a oncoterapia é uma das áreas promissoras de aplicação dos dados obtidos.