Spark Therapeutics开发的基因治疗药物Luxturna可帮助遗传性失明患者恢复视力。
直接注入眼睛的DNA填充病毒剂量是美国允许的第一种基因疗法,用于治疗遗传病。 自从大约三十年前开始进行基因疗法的第一项研究以来,这种药物的拆分对于这个起伏不定的地区来说是一个重要的时刻。
Luxturna是今年第三种获批的基因疗法。 8月,该机构批准了诺华公司的Kymriah(CAR-T细胞免疫疗法,其中,患者的免疫细胞被去除,在体外被修饰,然后回到血液中对抗白血病)。 第二种批准的CAR-T细胞免疫疗法是Gilead Sciences的Yescarta。 与命名相反的是,当充满DNA的病毒直接引入体内时,Luxturna是第一种与基因疗法的“传统”观念相对应的药物。 迄今为止,在美国进行了超过600项使用基因疗法的临床试验。
Luxturna的起源始于1990年代宾夕法尼亚大学的Jean Bennet的研究。 在2000年,她测试了基因疗法治疗狗的视网膜遗传病。 但是,在基因治疗的其他临床试验中广泛报道了患者死亡后,难以获得进一步的资助。 贝内特后来与费城儿童医院合作,后者决定通过在2013年提供5000万美元启动Spark Therapeutics将该技术商业化。
Luxturna可以通过RPE65基因突变来改善人们的视力,该基因编码一种对视力很重要的酶。
暴露于光线下会导致“挤压”的顺式视网膜转变为“减压”的反式视网膜。 这种物理变化会触发向大脑的信号。 为了再次开始循环,RPE65酶使跨视网膜返回顺式视网膜。 但是,具有抑制RPE65产生的基因突变的人不能“循环”。 这导致视力障碍,通常在婴儿期或儿童期开始,并导致几乎完全失明。
用正常工作的RPE65酶再生光敏细胞(反式视黄醇向11-顺式-视网膜的光转导-Wiki):
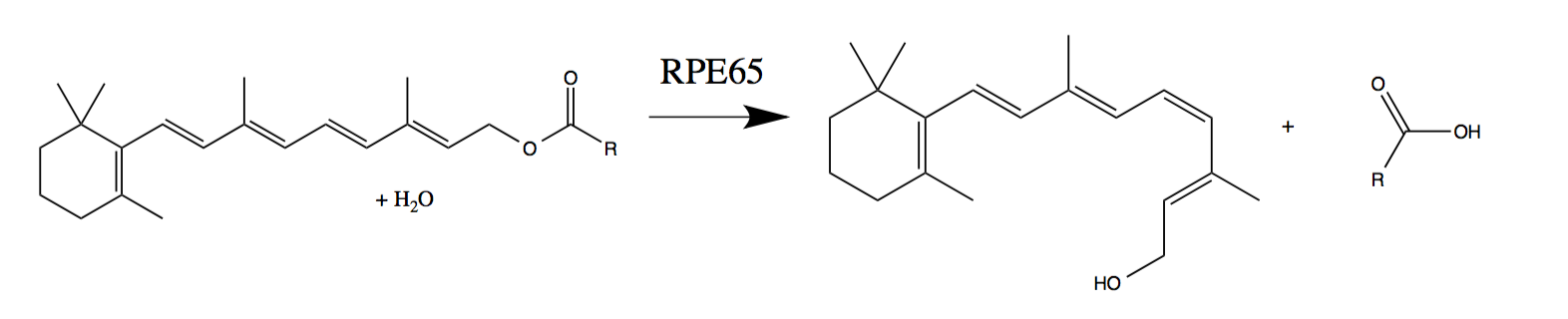
尽管RPE65中的许多突变会导致失明,但从理论上讲,Luxturna应该将它们全部治疗。 该产品包含包装在腺相关病毒中的RPE65的完整副本,这是将DNA转移至视网膜细胞以获得功能齐全的酶所必需的。
当外科医生直接在每只眼睛的视网膜下方注射包含约1500亿个填充DNA病毒颗粒的溶液时,该工具将用于一次性治疗。 对具有不同照明水平的障碍物的测试表明,治疗可以改善患者的视力。
根据FDA的说法,在美国有1,000至2,000名RPE65突变患者可以从Luxturna中受益。 然而,即使是少数患者接受治疗,药物的高昂价格也可能是一个问题。 价格尚未公开,但根据Spark首席执行官的声明,每位患者的治疗费用可能超过100万美元。
另外,带有录像的毒品管理动画的旧视频:
更多患有这种失明症的人可以看到:
让·贝内特(Jean Bennett)以及以RPE65工作问题的儿童为例的治疗成功案例: